Calan 40mg, 80mg, 120mg, 240mg Verapamil Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Calan 240mg, og hvordan bruges det?
Calan 80mg er en receptpligtig medicin, der bruges til at behandle symptomerne på forhøjet blodtryk (hypertension), brystsmerter (angina) og visse hjerterytmeforstyrrelser. Calan kan bruges alene eller sammen med anden medicin.
Calan tilhører en klasse af lægemidler kaldet Antidysrhythmics, IV; Calciumkanalblokkere; Calciumkanalblokkere, ikke-dihydropyridin.
Det vides ikke, om Calan er sikkert og effektivt til børn.
Hvad er de mulige bivirkninger af Calan?
Calan kan forårsage alvorlige bivirkninger, herunder:
- nældefeber,
- åndedrætsbesvær,
- hævelse af dit ansigt, læber, tunge eller hals,
- brystsmerter,
- hurtig eller langsom puls,
- svimmelhed,
- stakåndet,
- hævelse,
- hurtig vægtøgning
- ,
- feber,
- smerter i øvre mave,
- føler sig utilpas,
- angst,
- svedeture,
- bleg hud,
- hvæsen,
- gisper efter vejret, og
- hoste med skummende slim
- kvalme,
- forstoppelse,
- hovedpine,
- svimmelhed, og
- lavt blodtryk
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Calan 80mg omfatter:
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Calan. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
CALAN (verapamil HCl) er en calciumion-influx-hæmmer (langsom-kanalblokker eller calciumion-antagonist) tilgængelig til oral administration i filmovertrukne tabletter indeholdende 40 mg, 80 mg eller 120 mg verapamilhydrochlorid.
Strukturformlen for verapamil HCl er:
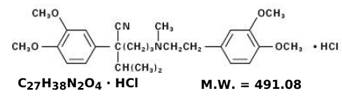 C27H38N2O4 · HCI MW = 491,08
C27H38N2O4 · HCI MW = 491,08 Benzenacetonitril, a-[3-[[2-(3,4-dimethoxyphenyl)ethyl]methylamino]propyl]-3,4dimethoxy-a-(1-methylethyl)hydrochlorid
Verapamil HCl er et næsten hvidt, krystallinsk pulver, praktisk talt fri for lugt, med en bitter smag. Det er opløseligt i vand, chloroform og methanol. Verapamil HCl er ikke kemisk relateret til andre kardioaktive lægemidler.
Inaktive ingredienser omfatter mikrokrystallinsk cellulose, majsstivelse, gelatine, hydroxypropylcellulose, hypromellose, jernoxidfarvestof, laktose, magnesiumstearat, polyethylenglycol, talkum og titaniumdioxid.
INDIKATIONER
CALAN tabletter er indiceret til behandling af følgende:
Angina
- Vasospastisk (Prinzmetals variant) angina
- Ustabil (crescendo, præ-infarkt) angina
Arytmier
Essentiel hypertension
CALAN 120mg er indiceret til behandling af hypertension for at sænke blodtrykket. Sænkning af blodtrykket reducerer risikoen for fatale og ikke-dødelige kardiovaskulære hændelser, primært slagtilfælde og myokardieinfarkter. Disse fordele er blevet set i kontrollerede forsøg med antihypertensiva fra en lang række farmakologiske klasser, herunder dette lægemiddel.
Kontrol af forhøjet blodtryk bør være en del af omfattende kardiovaskulær risikostyring, herunder, hvor det er relevant, lipidkontrol, diabetesbehandling, antitrombotisk behandling, rygestop, motion og begrænset natriumindtag. Mange patienter vil kræve mere end ét lægemiddel for at nå blodtryksmålene. For specifik rådgivning om mål og ledelse, se offentliggjorte retningslinjer, såsom dem fra National High Blood Pressure Education Program's Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure (JNC).
Talrige antihypertensiva, fra en række farmakologiske klasser og med forskellige virkningsmekanismer, er i randomiserede kontrollerede forsøg blevet vist at reducere kardiovaskulær morbiditet og dødelighed, og det kan konkluderes, at det er blodtryksreduktion og ikke en anden farmakologisk egenskab ved stofferne, der i høj grad er ansvarlige for disse fordele. Den største og mest konsistente kardiovaskulære udfaldsfordel har været en reduktion i risikoen for slagtilfælde, men reduktioner i myokardieinfarkt og kardiovaskulær dødelighed er også set regelmæssigt.
Forhøjet systolisk eller diastolisk tryk forårsager øget kardiovaskulær risiko, og den absolutte risikostigning pr. mmHg er større ved højere blodtryk, så selv beskedne reduktioner af svær hypertension kan give væsentlige fordele. Relativ risikoreduktion fra blodtryksreduktion er ens på tværs af populationer med varierende absolut risiko, så den absolutte fordel er større hos patienter, der er i højere risiko uafhængigt af deres hypertension (f.eks. patienter med diabetes eller hyperlipidæmi), og sådanne patienter kan forventes at drage fordel af mere aggressiv behandling til et lavere blodtryksmål.
Nogle antihypertensiva har mindre blodtrykseffekter (som monoterapi) hos sorte patienter, og mange antihypertensiva har yderligere godkendte indikationer og virkninger (f.eks. på angina, hjertesvigt eller diabetisk nyresygdom). Disse overvejelser kan styre valg af terapi.
DOSERING OG ADMINISTRATION
Dosis af verapamil skal individualiseres ved titrering. Nytten og sikkerheden af doser over 480 mg/dag er ikke blevet fastlagt; derfor bør denne daglige dosis ikke overskrides. Da halveringstiden for verapamil øges under kronisk dosering, kan maksimal respons være forsinket.
Angina
Kliniske forsøg viser, at den sædvanlige dosis er 80 mg til 120 mg tre gange dagligt. Dog kan 40 mg tre gange dagligt være berettiget hos patienter, som kan have en øget respons på verapamil (f.eks. nedsat leverfunktion, ældre osv.). Opadgående titrering bør baseres på terapeutisk effekt og sikkerhed vurderet ca. otte timer efter dosering. Dosis kan øges dagligt (f.eks. patienter med ustabil angina) eller ugentlige intervaller, indtil optimal klinisk respons opnås.
Arytmier
Doseringen til digitaliserede patienter med kronisk atrieflimren (se FORHOLDSREGLER ) varierer fra 240 til 320 mg/dag i opdelte (tid eller qid) doser. Doseringen til profylakse af PSVT (ikke-digitaliserede patienter) varierer fra 240 til 480 mg/dag i opdelte (tid eller qid) doser. Generelt vil maksimal effekt for enhver given dosis være synlig i løbet af de første 48 timers behandling.
Essentiel hypertension
Dosis skal individualiseres ved titrering. Den sædvanlige initiale monoterapidosis i kliniske forsøg var 80 mg tre gange dagligt (240 mg/dag). Daglige doser på 360 og 480 mg er blevet brugt, men der er ingen beviser for, at doser ud over 360 mg gav ekstra effekt. Det bør overvejes at påbegynde titrering med 40 mg tre gange dagligt hos patienter, som kan reagere på lavere doser, såsom ældre eller personer af lille statur. Den antihypertensive virkning af CALAN er tydelig inden for den første uge af behandlingen. Opadgående titrering bør baseres på terapeutisk effekt, vurderet ved slutningen af doseringsintervallet.
HVORDAN LEVERET
CALAN 40 mg tabletterne er runde, lyserøde, filmovertrukne, med CALAN præget på den ene side og 40 på den anden, leveret som:
CALAN 80 mg tabletterne er ovale, ferskenfarvede, delekærv, filmovertrukne, med CALAN præget på den ene side og 80 på den anden, leveret som:
CALAN 120 mg tabletterne er ovale, brune, delekærv, filmovertrukne, med CALAN 120 præget på den ene side, leveret som:
Opbevares ved 59° til 77°F (15° til 25°C) og beskyt mod lys. Dispenser i tætte, lysbestandige beholdere.
Distribueret af: GD Searle LLC, Division Pfizer Inc ,NY 10017. Revideret: sep 2017
BIVIRKNINGER
Alvorlige bivirkninger er ualmindelige, når CALAN 40 mg-behandling påbegyndes med opadgående dosistitrering inden for den anbefalede enkelt- og samlede daglige dosis. Se ADVARSLER til diskussion af hjertesvigt, hypotension, forhøjede leverenzymer, AV-blokering og hurtig ventrikulær respons. Reversibel (ved seponering af verapamil) ikke-obstruktiv, paralytisk ileus er sjældent blevet rapporteret i forbindelse med brugen af verapamil. Følgende reaktioner på oralt administreret verapamil forekom med hastigheder på mere end 1,0 % eller forekom i lavere frekvenser, men viste sig klart lægemiddelrelaterede i kliniske forsøg hos 4.954 patienter:
kliniske undersøgelser relateret til kontrol af ventrikulært respons hos digitaliserede patienter, som havde atrieflimren eller -flimmer, forekom ventrikulære rater under 50 i hvile hos 15 % af patienterne, og asymptomatisk hypotension forekom hos 5 % af patienterne.
Følgende reaktioner, rapporteret hos 1,0 % eller mindre af patienterne, opstod under forhold (åbne forsøg, markedsføringserfaring), hvor en årsagssammenhæng er usikker; de er opført for at advare lægen om et muligt forhold:
Kardiovaskulær: angina pectoris, atrioventrikulær dissociation, brystsmerter, claudicatio, myokardieinfarkt, hjertebanken, purpura (vaskulitis), synkope.
Fordøjelsessystemet: diarré, mundtørhed, mave-tarmbesvær, gingival hyperplasi.
Hemisk og lymfatisk: ekkymose eller blå mærker.
Nervesystem: cerebrovaskulær ulykke, forvirring, ligevægtsforstyrrelser, søvnløshed, muskelkramper, paræstesi, psykotiske symptomer, rysten, somnolens, ekstrapyramidale symptomer.
Hud: artralgi og udslæt, eksantem, hårtab, hyperkeratose, makuler, svedtendens, nældefeber, Stevens-Johnsons syndrom, erythema multiforme.
Særlige sanser: sløret syn, tinnitus.
Urogenital: gynækomasti, galaktoré/hyperprolaktinæmi, øget vandladning, plettet menstruation, impotens.
Behandling af akutte kardiovaskulære bivirkninger
Hyppigheden af kardiovaskulære bivirkninger, der kræver behandling, er sjælden; derfor er erfaring med deres behandling begrænset. Når der opstår alvorlig hypotension eller fuldstændig AV-blokering efter oral administration af verapamil, skal passende nødforanstaltninger træffes omgående. f.eks. intravenøst administreret noradrenalinbitartrat, atropinsulfat, isoproterenol HCl (alle i de sædvanlige doser) eller calciumgluconat (10 % opløsning). Hos patienter med hypertrofisk kardiomyopati (IHSS) bør alfa-adrenerge midler (phenylephrin-HCl, metaraminolbitartrat eller methoxamin-HCl) anvendes til at opretholde blodtrykket, og isoproterenol og norepinephrin bør undgås. Hvis yderligere støtte er nødvendig, kan dopamin HCl eller dobutamin HCl administreres. Faktisk behandling og dosering bør afhænge af sværhedsgraden af den kliniske situation og den behandlende læges vurdering og erfaring.
DRUGSINTERAKTIONER
Cytokrominducere/hæmmere
In vitro metaboliske undersøgelser indikerer, at verapamil metaboliseres af cytochrom P450 CYP3A4, CYP1A2, CYP2C8, CYP2C9 og CYP2C18. Der er rapporteret klinisk signifikante interaktioner med hæmmere af CYP3A4 (f.eks. erythromycin, ritonavir), der forårsager forhøjede plasmaniveauer af verapamil, mens inducere af CYP3A4 (f.eks. rifampin) har forårsaget en sænkning af plasmaniveauer af verapamil.
HMG-CoA-reduktasehæmmere
Brugen af HMG-CoA-reduktasehæmmere, som er CYP3A4-substrater i kombination med verapamil, er blevet forbundet med rapporter om myopati/rhabdomyolyse.
Samtidig administration af flere doser på 10 mg verapamil og 80 mg simvastatin resulterede i eksponering for simvastatin 2,5 gange så stor som efter simvastatin alene. Begræns dosis af simvastatin til patienter på verapamil til 10 mg dagligt. Begræns den daglige dosis af lovastatin til 40 mg. Lavere start- og vedligeholdelsesdoser af andre CYP3A4-substrater (f.eks. atorvastatin) kan være påkrævet, da verapamil kan øge plasmakoncentrationen af disse lægemidler.
Ivabradin
Samtidig brug af verapamil øger eksponeringen for ivabradin og kan forværre bradykardi og ledningsforstyrrelser. Undgå samtidig administration af verapamil og ivabradin.
Aspirin
I nogle få rapporterede tilfælde har samtidig administration af verapamil med aspirin ført til øgede blødningstider, der er længere end observeret med aspirin alene.
Grapefrugtjuice
Grapefrugtjuice kan øge plasmaniveauerne af verapamil.
Alkohol
Verapamil kan øge alkoholkoncentrationen i blodet og forlænge dets virkning.
Beta-blokkere
Kontrollerede undersøgelser med et lille antal patienter tyder på, at samtidig brug af CALAN 120mg og orale beta-adrenerge blokerende midler kan være gavnligt hos visse patienter med kronisk stabil angina eller hypertension, men tilgængelig information er ikke tilstrækkelig til med sikkerhed at forudsige virkningerne af samtidig behandling hos patienter med venstre ventrikulær dysfunktion eller hjerteledningsabnormiteter. Samtidig behandling med beta-adrenerge blokkere og verapamil kan resultere i additive negative effekter på hjertefrekvens, atrioventrikulær ledning og/eller hjertekontraktilitet.
en undersøgelse, der involverede 15 patienter behandlet med høje doser propranolol (median dosis: 480 mg/dag; interval: 160 til 1.280 mg/dag) for svær angina, med bevaret venstre ventrikelfunktion (ejektionsfraktion større end 35%), hæmodynamisk effekter af yderligere behandling med verapamil HCl blev vurderet ved hjælp af invasive metoder. Tilføjelsen af verapamil til højdosis betablokkere inducerede beskedne negative inotrope og kronotrope virkninger, som ikke var alvorlige nok til at begrænse kortvarig (48 timer) kombinationsbehandling i denne undersøgelse. Disse beskedne kardiodepressive virkninger varede i mere end 6 men mindre end 30 timer efter pludselig ophør med betablokkere og var tæt forbundet med plasmaniveauer af propranolol. Den primære verapamil/betablokker-interaktion i denne undersøgelse så ud til at være hæmodynamisk snarere end elektrofysiologisk.
andre undersøgelser inducerede verapamil generelt ikke signifikante negative inotrope, kronotrope eller dromotrope virkninger hos patienter med bevaret venstre ventrikelfunktion, der fik lave eller moderate doser af propranolol (mindre end eller lig med 320 mg/dag); hos nogle patienter fremkaldte kombineret terapi dog sådanne virkninger. Hvis kombineret behandling anvendes, bør der derfor udføres tæt overvågning af den kliniske status. Kombineret behandling bør sædvanligvis undgås hos patienter med atrioventrikulære ledningsabnormiteter og patienter med deprimeret venstre ventrikelfunktion.
Asymptomatisk bradykardi (36 slag/min) med en vandrende atriel pacemaker er blevet observeret hos en patient, der samtidig fik timolol (en beta-adrenerg blokker) øjendråber og oral verapamil.
Et fald i metoprolol og propranolol clearance er blevet observeret, når begge lægemidler administreres samtidig med verapamil. Der er set en variabel effekt, når verapamil og atenolol blev givet sammen.
Digitalis
Klinisk brug af verapamil hos digitaliserede patienter har vist, at kombinationen tolereres godt, hvis digoxindoserne er korrekt justeret. Kronisk verapamilbehandling kan dog øge serumdigoxinniveauet med 50 % til 75 % i løbet af den første uge af behandlingen, og dette kan resultere i digitalis-toksicitet. Hos patienter med levercirrhose er verapamils indflydelse på digoxin-kinetikken forstørret. Verapamil kan reducere total kropsclearance og ekstrarenal clearance af digitoxin med henholdsvis 27 % og 29 %. Vedligeholdelses- og digitaliseringsdoser bør reduceres, når verapamil administreres, og patienten bør revurderes for at undgå over- eller underdigitalisering. Når der er mistanke om overdigitalisering, bør den daglige dosis af digitalis reduceres eller midlertidigt seponeres. Ved ophør med brugen af CALAN 80 mg skal patienten revurderes for at undgå underdigitalisering.
Antihypertensive midler
Verapamil administreret samtidig med orale antihypertensiva (f.eks. vasodilatorer, angiotensin-konverterende enzymhæmmere, diuretika, betablokkere) vil sædvanligvis have en additiv effekt på at sænke blodtrykket. Patienter, der får disse kombinationer, bør overvåges passende. Samtidig brug af midler, der svækker alfa-adrenerg funktion, med verapamil kan resultere i en for høj blodtryksreduktion hos nogle patienter. En sådan effekt blev observeret i et studie efter samtidig administration af verapamil og prazosin.
Antiarytmiske midler
Disopyramid
Indtil der er opnået data om mulige interaktioner mellem verapamil og disopyramid, bør disopyramid ikke administreres inden for 48 timer før eller 24 timer efter verapamil administration.
Flecainid
En undersøgelse med raske frivillige viste, at samtidig administration af flecainid og verapamil kan have additive virkninger på myokardiekontraktilitet, AV-ledning og repolarisering. Samtidig behandling med flecainid og verapamil kan resultere i additiv negativ inotrop effekt og forlængelse af atrioventrikulær ledning.
Quinidin
Hos et lille antal patienter med hypertrofisk kardiomyopati (IHSS) resulterede samtidig brug af verapamil og quinidin i signifikant hypotension. Indtil yderligere data er opnået, bør kombineret behandling med verapamil og quinidin til patienter med hypertrofisk kardiomyopati sandsynligvis undgås.
De elektrofysiologiske virkninger af quinidin og verapamil på AV-ledning blev undersøgt hos 8 patienter. Verapamil modvirkede signifikant virkningerne af quinidin på AV-ledning. Der har været en rapport om øgede quinidinniveauer under verapamilbehandling.

Andre agenter
Nitrater
Verapamil er blevet givet samtidig med kort- og langtidsvirkende nitrater uden nogen uønskede lægemiddelinteraktioner. Den farmakologiske profil af begge lægemidler og den kliniske erfaring tyder på gavnlige interaktioner.
Cimetidin
Interaktionen mellem cimetidin og kronisk administreret verapamil er ikke blevet undersøgt. Variable resultater om clearance er opnået i akutte undersøgelser af raske frivillige; clearance af verapamil var enten reduceret eller uændret.
Lithium
Øget følsomhed over for virkningerne af lithium (neurotoksicitet) er blevet rapporteret under samtidig verapamil-lithium-behandling; lithium niveauer er blevet observeret nogle gange at stige, nogle gange at falde og nogle gange at være uændret. Patienter, der får begge lægemidler, skal overvåges omhyggeligt.
Carbamazepin
Verapamilbehandling kan øge carbamazepinkoncentrationerne under kombineret behandling. Dette kan give carbamazepin bivirkninger såsom diplopi, hovedpine, ataksi eller svimmelhed.
Rifampin
Behandling med rifampin kan markant reducere oral verapamils biotilgængelighed.
Fenobarbital
Fenobarbitalbehandling kan øge verapamil-clearance.
Cyclosporin
Verapamilbehandling kan øge serumniveauet af ciclosporin.
Theophyllin
Verapamil kan hæmme clearance og øge plasmaniveauerne af theophyllin.
Indåndingsbedøvelsesmidler
Dyreforsøg har vist, at inhalationsanæstetika sænker kardiovaskulær aktivitet ved at mindske den indadgående bevægelse af calciumioner. Ved samtidig brug bør inhalationsanæstetika og calciumantagonister, såsom verapamil, titreres omhyggeligt for at undgå overdreven kardiovaskulær depression.
Neuromuskulære blokerende midler
Kliniske data og dyreforsøg tyder på, at verapamil kan forstærke aktiviteten af neuromuskulære blokerende midler (curare-lignende og depolariserende). Det kan være nødvendigt at nedsætte dosis af verapamil og/eller dosis af det neuromuskulære blokerende middel, når lægemidlerne anvendes samtidig.
telithromycin
Hypotension og bradyarytmier er blevet observeret hos patienter, der samtidig får telithromycin, et antibiotikum i ketolidklassen.
Clonidin
Sinusbradykardi, der resulterer i hospitalsindlæggelse og pacemakerindsættelse, er blevet rapporteret i forbindelse med brug af clonidin samtidig med verapamil. Overvåg hjertefrekvens hos patienter, der samtidig får verapamil og clonidin.
Pattedyrsmål for Rapamycin (mTOR)-hæmmere
I et studie med 25 raske frivillige med samtidig administration af verapamil og sirolimus, blev Cmax og AUC for sirolimus i fuldblod øget med henholdsvis 130 % og 120 %. Plasma S-(-) verapamil Cmax og AUC var begge øget med 50 %. Samtidig administration af verapamil og everolimus hos 16 raske frivillige øgede Cmax og AUC for everolimus med henholdsvis 130 % og 250 %. Ved samtidig brug af mTOR-hæmmere (f.eks. sirolimus, temsirolimus og everolimus) og verapamil, overveje passende dosisreduktioner af begge lægemidler.
ADVARSLER
Hjertefejl
Verapamil har en negativ inotrop effekt, som hos de fleste patienter kompenseres af dens afterload-reduktion (nedsat systemisk vaskulær modstand) egenskaber uden en nettoforringelse af ventrikulær ydeevne. I klinisk erfaring med 4.954 patienter udviklede 87 (1,8%) kongestivt hjertesvigt eller lungeødem. Verapamil bør undgås hos patienter med svær venstre ventrikulær dysfunktion (f.eks. ejektionsfraktion mindre end 30 %) eller moderate til svære symptomer på hjertesvigt og hos patienter med enhver grad af ventrikulær dysfunktion, hvis de får en beta-adrenerg blokker (se DRUGSINTERAKTIONER ). Patienter med mildere ventrikulær dysfunktion bør om muligt kontrolleres med optimale doser digitalis og/eller diuretika før verapamilbehandling. ( Bemærk interaktioner med digoxin under FORHOLDSREGLER )
Hypotension
Lejlighedsvis kan den farmakologiske virkning af verapamil forårsage et fald i blodtrykket under normale niveauer, hvilket kan resultere i svimmelhed eller symptomatisk hypotension. Hyppigheden af hypotension observeret hos 4.954 patienter inkluderet i kliniske forsøg var 2,5 %. Hos hypertensive patienter er fald i blodtrykket under det normale usædvanlige. Tilt-table test (60 grader) var ikke i stand til at inducere ortostatisk hypotension.
Forhøjede leverenzymer
Forhøjelser af transaminaser med og uden samtidige stigninger i alkalisk fosfatase og bilirubin er blevet rapporteret. Sådanne stigninger har nogle gange været forbigående og kan forsvinde selv ved fortsat verapamilbehandling. Adskillige tilfælde af hepatocellulær skade relateret til verapamil er blevet påvist ved genudsættelse; halvdelen af disse havde kliniske symptomer (utilpashed, feber og/eller smerter i højre øvre kvadrant) ud over forhøjelse af SGOT, SGPT og alkalisk fosfatase. Periodisk monitorering af leverfunktionen hos patienter, der får verapamil, er derfor fornuftig.
Tilbehørs bypass-kanal (Wolff-Parkinson-White eller Lown-Ganong-Levine)
Nogle patienter med paroxysmal og/eller kronisk atrieflimren eller atrieflimren og en sideløbende tilbehørs-AV-bane har udviklet øget antegrad ledning på tværs af den tilbehørsvej, der passerer AV-knuden, hvilket producerer en meget hurtig ventrikulær respons eller ventrikulær fibrillering efter at have fået intravenøs verapamil (eller digitalis) . Selvom en risiko for, at dette sker med oral verapamil ikke er blevet fastlagt, kan sådanne patienter, der får oral verapamil, være i fare, og dets brug hos disse patienter er kontraindiceret (se KONTRAINDIKATIONER ). Behandling er normalt DC-kardioversion. Cardioversion er blevet brugt sikkert og effektivt efter oral CALAN.
Atrioventrikulær blokering
Virkningen af verapamil på AV-ledning og SA-knuden kan forårsage asymptomatisk førstegrads AV-blokering og forbigående bradykardi, nogle gange ledsaget af nodale escape-rytmer. PR-intervalforlængelse er korreleret med verapamil plasmakoncentrationer, især i den tidlige titreringsfase af behandlingen. Højere grader af AV-blok blev dog sjældent (0,8%) observeret. Markeret førstegradsblokering eller progressiv udvikling til anden- eller tredjegrads AV-blokering kræver en reduktion i dosis eller i sjældne tilfælde seponering af verapamil HCl og indførelse af passende behandling, afhængigt af den kliniske situation.
Patienter med hypertrofisk kardiomyopati (IHSS)
-enHos 120 patienter med hypertrofisk kardiomyopati (de fleste af dem refraktære eller intolerante over for propranolol), som fik behandling med verapamil i doser op til 720 mg/dag, blev der set en række alvorlige bivirkninger. Tre patienter døde i lungeødem; alle havde alvorlig venstre ventrikulær udstrømningsobstruktion og en tidligere historie med venstre ventrikulær dysfunktion. Otte andre patienter havde lungeødem og/eller svær hypotension; unormalt højt (større end 20 mm Hg) pulmonært kiletryk og en markant venstre ventrikulær udstrømningsobstruktion var til stede hos de fleste af disse patienter. Samtidig administration af quinidin (se FORHOLDSREGLER , DRUGSINTERAKTIONER gik forud for den alvorlige hypotension hos 3 af de 8 patienter (hvoraf 2 udviklede lungeødem). Sinusbradykardi forekom hos 11 % af patienterne, andengrads AV-blokering hos 4 % og sinusstop hos 2 %. Det skal forstås, at denne gruppe patienter havde en alvorlig sygdom med høj dødelighed. De fleste bivirkninger reagerede godt på dosisreduktion, og kun sjældent måtte brugen af verapamil afbrydes.
FORHOLDSREGLER
Generel
Anvendelse hos patienter med nedsat leverfunktion
Da verapamil i høj grad metaboliseres af leveren, bør det administreres med forsigtighed til patienter med nedsat leverfunktion. Alvorlig leverdysfunktion forlænger eliminationshalveringstiden for verapamil til omkring 14 til 16 timer; derfor bør ca. 30 % af den dosis, der gives til patienter med normal leverfunktion, administreres til disse patienter. Omhyggelig overvågning for unormal forlængelse af PR-intervallet eller andre tegn på overdreven farmakologisk effekt (se OVERDOSIS ) skal udføres.
Anvendelse hos patienter med svækket (nedsat) neuromuskulær transmission
Det er blevet rapporteret, at verapamil nedsætter neuromuskulær transmission hos patienter med Duchennes muskeldystrofi, forlænger restitutionen fra det neuromuskulære blokerende middel vecuronium og forårsager en forværring af myasthenia gravis. Det kan være nødvendigt at reducere dosis af verapamil, når det administreres til patienter med svækket neuromuskulær transmission.
Anvendelse hos patienter med nedsat nyrefunktion
Ca. 70 % af en administreret dosis verapamil udskilles som metabolitter i urinen. Verapamil fjernes ikke ved hæmodialyse. Indtil yderligere data er tilgængelige, bør verapamil administreres med forsigtighed til patienter med nedsat nyrefunktion. Disse patienter skal overvåges omhyggeligt for unormal forlængelse af PR-intervallet eller andre tegn på overdosering (se OVERDOSIS ).
Karcinogenese, mutagenese, svækkelse af fertilitet
Et 18-måneders toksicitetsstudie i rotter med et lavt multiplum (6 gange) af den maksimalt anbefalede humane dosis og ikke den maksimalt tolererede dosis, antydede ikke et tumorigent potentiale. Der var ingen tegn på et kræftfremkaldende potentiale af verapamil indgivet i foderet til rotter i to år i doser på 10, 35 og 120 mg/kg/dag eller henholdsvis ca. 1, 3,5 og 12 gange den maksimalt anbefalede daglige humane dosis dosis (480 mg/dag eller 9,6 mg/kg/dag).
Verapamil var ikke mutagent i Ames-testen i 5 teststammer med 3 mg pr. plade med eller uden metabolisk aktivering.
Undersøgelser med hunrotter med daglige diætdoser op til 5,5 gange (55 mg/kg/dag) den maksimalt anbefalede humane dosis viste ikke nedsat fertilitet. Effekter på mandlig fertilitet er ikke blevet bestemt.
Graviditet
Reproduktionsundersøgelser er blevet udført på kaniner og rotter ved orale doser op til henholdsvis 1,5 (15 mg/kg/dag) og 6 (60 mg/kg/dag) gange den humane orale daglige dosis, og har ikke afsløret tegn på teratogenicitet. Hos rotter var dette multiplum af den humane dosis imidlertid embryocidal og forsinket fostervækst og -udvikling, sandsynligvis på grund af uønskede maternelle virkninger afspejlet i reducerede vægtforøgelser hos moderdyrene. Denne orale dosis har også vist sig at forårsage hypotension hos rotter. Der er ingen tilstrækkelige og velkontrollerede undersøgelser af gravide kvinder. Da reproduktionsstudier på dyr ikke altid forudsiger human respons, bør dette lægemiddel kun anvendes under graviditet, hvis det er klart nødvendigt. Verapamil krydser placentabarrieren og kan påvises i navleblod ved fødslen.
Arbejde og levering
Det vides ikke, om brugen af verapamil under fødslen eller fødslen har umiddelbare eller forsinkede bivirkninger på fosteret, eller om det forlænger fødslens varighed eller øger behovet for fødslen med tang eller anden obstetrisk intervention. Sådanne uønskede oplevelser er ikke blevet rapporteret i litteraturen på trods af en lang historie med brug af verapamil i Europa til behandling af hjertebivirkninger af beta-adrenerge agonister, der anvendes til behandling af for tidlig fødsel.
Ammende mødre
Verapamil udskilles i modermælk. På grund af risikoen for bivirkninger hos ammende spædbørn fra verapamil, bør amningen seponeres, mens verapamil administreres.
Pædiatrisk brug
Sikkerhed og effektivitet hos pædiatriske patienter er ikke blevet fastslået.
OVERDOSIS
Behandl alle verapamil-overdoser som alvorlige og oprethold observation i mindst 48 timer (især CALAN 120mg SR), helst under kontinuerlig hospitalsbehandling. Forsinkede farmakodynamiske konsekvenser kan forekomme med formuleringen med langvarig frigivelse. Verapamil er kendt for at reducere gastrointestinal transittid.
Behandling af overdosering bør være støttende. Beta-adrenerg stimulering eller parenteral administration af calciumopløsninger kan øge calciumionflux over den langsomme kanal og er blevet brugt effektivt til behandling af bevidst overdosering med verapamil. I nogle få rapporterede tilfælde er overdosering med calciumkanalblokkere blevet forbundet med hypotension og bradykardi, som oprindeligt var modstandsdygtig overfor atropin, men blev mere lydhør over for denne behandling, når patienterne fik store doser (tæt på 1 gram/time i mere end 24 timer) Kalcium Klorid. Verapamil kan ikke fjernes ved hæmodialyse. Klinisk signifikante hypotensive reaktioner eller høj grad af AV-blok bør behandles med henholdsvis vasopressorer eller hjertestimulering. Asystoli bør håndteres med de sædvanlige foranstaltninger, herunder hjerte-lunge-redning.
KONTRAINDIKATIONER
Verapamil HCl tabletter er kontraindiceret i:
KLINISK FARMAKOLOGI
CALAN 80mg er en calciumion-influx-hæmmer (langsom-kanalblokker eller calciumion-antagonist), der udøver sine farmakologiske virkninger ved at modulere tilstrømningen af ionisk calcium gennem cellemembranen i den arterielle glatte muskel samt i konduktive og kontraktile myokardieceller.
Handlingsmekanisme
Angina
Den præcise virkningsmekanisme af CALAN 40mg som et antianginal middel er endnu ikke helt bestemt, men inkluderer følgende to mekanismer:
Hvorvidt denne effekt spiller nogen rolle i klassisk anstrengelsesangina er ikke klart, men undersøgelser af træningstolerance har ikke vist en stigning i det maksimale træningshastighed-tryk-produkt, et bredt accepteret mål for iltudnyttelse. Dette tyder på, at lindring af spasmer eller udvidelse af kranspulsårer generelt ikke er en vigtig faktor ved klassisk angina.
Arytmi
Elektrisk aktivitet gennem AV-knuden afhænger i væsentlig grad af calciumtilstrømning gennem den langsomme kanal. Ved at reducere tilstrømningen af calcium forlænger CALAN 120mg den effektive refraktære periode i AV-knuden og sænker AV-ledning på en hastighedsrelateret måde. Denne egenskab forklarer CALAN 240mg's evne til at sænke ventrikelfrekvensen hos patienter med kronisk atrieflimren eller atrieflimren.
Normal sinusrytme påvirkes sædvanligvis ikke, men hos patienter med sick sinus syndrome kan CALAN forstyrre sinus-knudeimpulsgenerering og kan inducere sinusstop eller sinoatrial blokering. Atrioventrikulær blokering kan forekomme hos patienter uden eksisterende ledningsdefekter (se ADVARSLER ). CALAN 240mg reducerer hyppigheden af episoder med paroxysmal supraventrikulær takykardi.
CALAN 240mg ændrer ikke det normale atrielle aktionspotentiale eller intraventrikulære ledningstid, men i deprimerede atrielle fibre reducerer det amplitude, depolarisationshastighed og ledningshastighed. CALAN kan forkorte den antegrade effektive refraktære periode for tilbehørsbypasskanalen. Acceleration af ventrikulær frekvens og/eller ventrikulær fibrillation er blevet rapporteret hos patienter med atrieflimren eller atrieflimren og en sideløbende ekstra AV-vej efter administration af verapamil (se ADVARSLER ).
CALAN har en lokalbedøvelse, der er 1,6 gange procain på ækvimolær basis. Det vides ikke, om denne virkning er vigtig ved de doser, der anvendes til mennesker.
Essentiel hypertension
CALAN 120mg udøver antihypertensiv effekt ved at reducere systemisk vaskulær modstand, normalt uden ortostatiske fald i blodtryk eller reflekstakykardi; bradykardi (hastighed mindre end 50 slag/min) er ualmindelig (1,4%). Under isometrisk eller dynamisk træning ændrer CALAN ikke den systoliske hjertefunktion hos patienter med normal ventrikulær funktion.
CALAN ændrer ikke det samlede serumkalciumniveau. En rapport antydede imidlertid, at calciumniveauer over det normale område kan ændre den terapeutiske virkning af CALAN.
Farmakokinetik og metabolisme
Mere end 90 % af den oralt indgivne dosis af CALAN absorberes. På grund af den hurtige biotransformation af verapamil under dets første passage gennem portalcirkulationen varierer biotilgængeligheden fra 20 % til 35 %. Maksimal plasmakoncentration nås mellem 1 og 2 timer efter oral administration. Kronisk oral administration af 120 mg verapamil HCl hver 6. time resulterede i plasmaniveauer af verapamil varierende fra 125 til 400 ng/ml, med højere værdier rapporteret lejlighedsvis. Der eksisterer en ikke-lineær sammenhæng mellem den administrerede dosis verapamil og plasmaniveauer af verapamil. Der er ikke påvist nogen sammenhæng mellem plasmakoncentrationen af verapamil og en reduktion i blodtrykket. Ved tidlig dosistitrering med verapamil eksisterer der en sammenhæng mellem plasmakoncentration af verapamil og forlængelse af PR-intervallet. Men under kronisk administration kan dette forhold forsvinde. Den gennemsnitlige eliminationshalveringstid i enkeltdosisundersøgelser varierede fra 2,8 til 7,4 timer. I disse samme undersøgelser, efter gentagen dosering, steg halveringstiden til et område fra 4,5 til 12,0 timer (efter mindre end 10 på hinanden følgende doser givet med 6 timers mellemrum). Halveringstid af verapamil kan øges under titrering. Aldring kan påvirke farmakokinetikken af verapamil. Eliminationshalveringstid kan være forlænget hos ældre. Hos raske mænd gennemgår oralt administreret CALAN 240mg omfattende metabolisme i leveren. Tolv metabolitter er blevet identificeret i plasma; alle undtagen norverapamil er kun til stede i spormængder. Norverapamil kan nå steady-state plasmakoncentrationer, der er omtrent lig med verapamil selv. Den kardiovaskulære aktivitet af norverapamil ser ud til at være ca. 20 % af verapamils. Ca. 70 % af en administreret dosis udskilles som metabolitter i urinen og 16 % eller mere i fæces inden for 5 dage. Omkring 3% til 4% udskilles i urinen som uændret lægemiddel. Cirka 90% er bundet til plasmaproteiner. Hos patienter med leverinsufficiens er metabolismen forsinket, og eliminationshalveringstiden forlænges med op til 14 til 16 timer (se FORHOLDSREGLER ); fordelingsvolumenet øges, og plasmaclearance reduceres til ca. 30 % af det normale. Verapamil-clearance-værdier tyder på, at patienter med leverdysfunktion kan opnå terapeutiske plasmakoncentrationer af verapamil med en tredjedel af den orale daglige dosis, der kræves til patienter med normal leverfunktion.
Efter fire ugers oral dosering (120 mg qid) blev niveauer af verapamil og norverapamil noteret i cerebrospinalvæsken med en estimeret fordelingskoefficient på 0,06 for verapamil og 0,04 for norverapamil.
Hæmodynamik og myokardiemetabolisme
CALAN 120mg reducerer afterload og myokardiekontraktilitet. Forbedret venstre ventrikulær diastolisk funktion hos patienter med idiopatisk hypertrofisk subaortisk stenose (IHSS) og patienter med koronar hjertesygdom er også blevet observeret med CALAN-behandling. Hos de fleste patienter, inklusive dem med organisk hjertesygdom, modvirkes den negative inotrope virkning af CALAN 240mg af reduktion af afterload, og hjerteindeks reduceres normalt ikke. Hos patienter med alvorlig venstre ventrikulær dysfunktion (f.eks. pulmonal kiletryk over 20 mm Hg eller ejektionsfraktion mindre end 30 %) eller hos patienter, der tager beta-adrenerge blokerende midler eller andre kardiodepressive lægemidler, kan der dog forekomme forringelse af ventrikulær funktion (se DRUGSINTERAKTIONER ).
Lungefunktion
CALAN 120mg inducerer ikke bronkokonstriktion og forringer derfor ikke ventilationsfunktionen.
Dyrefarmakologi og/eller dyretoksikologi
kroniske dyretoksikologiske undersøgelser forårsagede verapamil linse- og/eller suturlinjeændringer ved 30 mg/kg/dag eller mere, og åbenlyse grå stær ved 62,5 mg/kg/dag eller mere hos beaglehunden, men ikke hos rotter. Udvikling af grå stær på grund af verapamil er ikke blevet rapporteret hos mennesker.
PATIENTOPLYSNINGER
Ingen oplysninger angivet. Der henvises til ADVARSLER og FORHOLDSREGLER sektioner.
