Adalat 10mg, 20mg, 30mg Nifedipine Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Adalat, og hvordan bruges det?
Adalat er en receptpligtig medicin, der bruges til at behandle symptomerne på brystsmerter (angina), forhøjet blodtryk (hypertension) og pulmonal hypertension. Adalat 30mg kan bruges alene eller sammen med anden medicin.
Adalat 20mg tilhører en klasse af lægemidler kaldet Calcium Channel Blockers; Calciumkanalblokkere, dihydropyridin.
Det vides ikke, om Adalat 30mg er sikkert og effektivt til børn under 6 år.
Hvad er de mulige bivirkninger af Adalat 10mg?
Adalat kan forårsage alvorlige bivirkninger, herunder:
- nældefeber,
- åndedrætsbesvær,
- hævelse i dit ansigt eller hals,
- feber,
- ondt i halsen,
- brændende øjne,
- hudsmerter,
- rødt eller lilla hududslæt med blærer og afskalning,
- forværrede brystsmerter,
- bankende hjerteslag,
- flagrende i dit bryst,
- svimmelhed,
- hævelse i dine hænder eller underben,
- smerter i øvre mave, og
- gulfarvning af huden eller øjnene (gulsot)
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Adalat omfatter:
- hævelse,
- rødmen (varme, rødme eller prikkende følelse),
- hovedpine,
- svimmelhed,
- kvalme,
- halsbrand, og
- føler sig svag eller træt
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Adalat. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Adalat® CC er en tablet-dosisform med forlænget frigivelse af calciumkanalblokkeren nifedipin. Nifedipin er 3,5-pyridindicarboxylsyre, 1,4-dihydro-2,6-dimethyl-4-(2-nitrophenyl)-dimethylester, C17H18N2O6, og har strukturformlen:
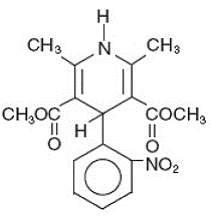
Nifedipin er et gult krystallinsk stof, praktisk talt uopløseligt i vand, men opløseligt i ethanol. Det har en molekylvægt på 346,3. Adalat CC tabletter består af et eksternt lag og en indvendig kerne. Begge indeholder nifedipin, pelsen som en slow release-formulering og kernen som en fast release-formulering. Adalat CC tabletter indeholder enten: 30, 60 eller 90 mg nifedipin til oral administration én gang dagligt.
Inerte ingredienser i formuleringen er: hydroxypropylcellulose, lactose, majsstivelse, crospovidon, mikrokrystallinsk cellulose, siliciumdioxid og magnesiumstearat. De inaktive ingredienser i filmcoatingen til Adalat 30mg CC 30 og 60 er: hypromellose, polyethylenglycol, ferrioxid og titaniumdioxid. De inaktive ingredienser i filmcoatingen til Adalat 20mg CC 90 er: hypromellose, polyethylenglycol og ferrioxid
INDIKATIONER
Adalat 10mg CC er indiceret til behandling af hypertension. Det kan anvendes alene eller i kombination med andre antihypertensiva.
DOSERING OG ADMINISTRATION
Dosis bør justeres efter hver patients behov. Det anbefales, at Adalat 20 mg CC administreres oralt én gang dagligt på tom mave. Adalat 10mg CC er en doseringsform med forlænget frigivelse, og tabletterne skal sluges hele, ikke bides eller deles. Generelt bør titreringen forløbe over en 7-14 dages periode begyndende med 30 mg én gang dagligt. Opadgående titrering bør baseres på terapeutisk effekt og sikkerhed. Den sædvanlige vedligeholdelsesdosis er 30 mg til 60 mg én gang dagligt. Titrering til doser over 90 mg dagligt anbefales ikke.
Hvis seponering af Adalat 30mg CC er nødvendig, tyder god klinisk praksis på, at dosis bør nedsættes gradvist under nøje overvågning af lægen.
Samtidig administration af nifedipin og grapefrugtjuice skal undgås (se KLINISK FARMAKOLOGI og FORHOLDSREGLER ).
Der skal udvises forsigtighed ved dispensering af Adalat CC for at sikre, at doseringsformen med forlænget frigivelse er blevet ordineret.
HVORDAN LEVERET
Adalat CC tabletter med forlænget frigivelse leveres som 30 mg, 60 mg og 90 mg runde filmovertrukne tabletter. De forskellige styrker kan identificeres som følger:
Adalat® CC tabletter leveres i:
Tabletterne skal beskyttes mod lys og fugt og opbevares under 86°F (30°C). Dispenser i tætte, lysbestandige beholdere.
Fremstillet for: Bayer HealthCare Pharmaceuticals Inc., Wayne, NJ 07470. Fremstillet i Tyskland. Revideret: december 2015
BIVIRKNINGER
Uønskede oplevelser
Hyppigheden af uønskede hændelser under behandling med Adalat CC i doser op til 90 mg dagligt blev afledt af multicenter placebo-kontrollerede kliniske forsøg med 370 hypertensive patienter. Atenolol 50 mg én gang dagligt blev brugt samtidigt hos 187 af de 370 patienter på Adalat CC og hos 64 af de 126 patienter på placebo. Alle bivirkninger rapporteret under Adalat 30 mg CC-behandling blev opstillet i tabulering uafhængigt af deres årsagssammenhæng til medicin.
Den mest almindelige bivirkninger rapporteret med Adalat 10 mg CC var perifert ødem. Dette var dosisrelateret, og frekvensen var 18 % på Adalat 30 mg CC 30 mg dagligt, 22 % på Adalat 30 mg CC 60 mg dagligt og 29 % på Adalat 10 mg CC 90 mg dagligt versus 10 % på placebo.
Andre almindelige bivirkninger rapporteret i ovenstående placebokontrollerede forsøg omfatter:
Hvor hyppigheden af bivirkninger med Adalat 20 mg CC og placebo er ens, kan årsagssammenhæng ikke fastslås.
Følgende bivirkninger blev rapporteret med en forekomst på 3 % eller mindre i daglige doser op til 90 mg:
Kroppen som helhed/systemisk: brystsmerter, smerter i benene
Centralnervesystemet: paræstesi, svimmelhed
Dermatologisk: udslæt
Gastrointestinale: forstoppelse
Muskuloskeletale: kramper i benene
Åndedræt: næseblødning, rhinitis
Urogenital: impotens, vandladningsfrekvens
Andre bivirkninger rapporteret med en incidens på mindre end 1,0 % var:
Kroppen som helhed/systemisk: allergisk reaktion, asteni, cellulitis, substernale brystsmerter, kulderystelser, ansigtsødem, unormale laboratorieprøver, utilpashed, nakkesmerter, bækkensmerter, smerter, lysfølsomhedsreaktion Hjerte-kar: atrieflimren, bradykardi, hjertestop, ekstrasystoli, hypotension, migræne, hjertebanken , flebitis, postural hypotension, takykardi, kutane angiectaser
Centralnervesystemet: angst, forvirring, nedsat libido, depression, hypertoni, hypestesi, søvnløshed, somnolens
Dermatologisk: angioødem, petechialt udslæt, kløe, svedtendens
Gastrointestinale: mavesmerter, diarré, mundtørhed, dysfagi, dyspepsi, eruktion, esophagitis, flatulens, mave-tarmlidelse, gastrointestinal blødning, GGT øget, tandkødssygdom, tandkødsblødning, opkastning
Hæmatologisk: eosinofili, lymfadenopati
Metabolisk: gigt, vægttab
Muskuloskeletale: artralgi, gigt, ledlidelse, myalgi, myasteni
Åndedræt: dyspnø, øget hoste, raser, pharyngitis, stridor
Særlige sanser: unormalt syn, amblyopi, conjunctivitis, diplopi, øjenlidelse, øjenblødning, tinnitus
Urogenital/reproduktiv: dysuri, nyresten, nocturi, brystoversvømmelse, polyuri, urogenital lidelse, erektil dysfunktion (ED)
Følgende bivirkninger er sjældent blevet rapporteret hos patienter, der fik nifedipin i pelskerne eller andre formuleringer: allergifremkaldende hepatitis, alopeci, anafylaktisk reaktion, anæmi, arthritis med ANA (+), depression, erythromelalgi, eksfoliativ dermatitis, feber, gingival hyperplasi, gynækomasti, hyperglykæmi, gulsot, leukopeni, humørsvingninger, muskelkramper, nervøsitet, paranoid syndrom, purpura, rysten, søvnforstyrrelser, Stevens-Johnsons syndrom, synkope, smagsforstyrrelser, trombocytopeni, toksisk epidermal nekrolyse, forbigående blindhed ved toppen af plasmaniveauet, tremor og nældefeber.
DRUGSINTERAKTIONER
Nifedipin elimineres hovedsageligt ved metabolisme og er et substrat for CYP3A. Hæmmere og inducere af CYP3A kan påvirke eksponeringen for nifedipin og følgelig dets ønskelige og uønskede virkninger. In vitro og in vivo data indikerer, at nifedipin kan hæmme metabolismen af lægemidler, der er substrater for CYP3A, og derved øge eksponeringen for andre lægemidler. Nifedipin er en vasodilator, og samtidig administration af andre lægemidler, der påvirker blodtrykket, kan resultere i farmakodynamiske interaktioner.
CYP3A-hæmmere
CYP3A-hæmmere såsom ketoconazol, fluconazol, itraconazol, clarithromycin, erythromycin (Azithromycin, selvom strukturelt beslægtet med klassen af makrolidantibiotikum er uden klinisk relevant CYP3A4-hæmning), grapefrugt, nefazodon, fluquinavirnel, ind-, saviron, ind-, saviron, ind- og savira i øget eksponering for nifedipin ved samtidig administration. Omhyggelig overvågning og dosisjustering kan være nødvendig; overveje at starte nifedipin ved den laveste tilgængelige dosis, hvis det gives samtidig med disse lægemidler.
Stærke CYP3A-inducere
Stærke CYP3A-inducere, såsom rifampin, rifabutin, phenobarbital, phenytoin, carbamazepin og perikon reducerer biotilgængeligheden og effektiviteten af nifedipin; derfor bør nifedipin ikke anvendes i kombination med stærke CYP3A-inducere såsom rifampin (se KONTRAINDIKATIONER ).
Kardiovaskulære lægemidler
Antiarytmika
Quinidin: Quinidin er et substrat for CYP3A og har vist sig at hæmme CYP3A in vitro. Samtidig administration af flere doser quinidinsulfat, 200 mg tid, og nifedipin, 20 mg tid, øgede Cmax og AUC for nifedipin hos raske frivillige med faktorer på henholdsvis 2,30 og 1,37. Hjertefrekvensen i det indledende interval efter lægemiddeladministration blev øget med op til 17,9 slag/minut. Eksponeringen for quinidin blev ikke ændret væsentligt i nærvær af nifedipin. Monitorering af hjertefrekvens og justering af nifedipin-dosis, om nødvendigt, anbefales, når quinidin tilsættes en behandling med nifedipin.
Flecainid: Der har været for lidt erfaring med samtidig administration af Tambocor og nifedipin til at anbefale samtidig brug.
Calciumkanalblokkere
Diltiazem: Forbehandling af raske frivillige med 30 mg eller 90 mg tid diltiazem po øgede AUC for nifedipin efter en enkelt dosis på 20 mg nifedipin med faktorer på henholdsvis 2,2 og 3,1. De tilsvarende Cmax-værdier for nifedipin steg med faktorer på henholdsvis 2,0 og 1,7. Der bør udvises forsigtighed ved samtidig administration af diltiazem og nifedipin, og en reduktion af dosis af nifedipin bør overvejes.
Verapamil: Verapamil, en CYP3A-hæmmer, kan hæmme metabolismen af nifedipin og øge eksponeringen for nifedipin under samtidig behandling. Blodtrykket bør overvåges, og reduktion af nifedipindosis bør overvejes.
ACE-hæmmere
Benazepril: Hos raske frivillige, der fik en enkeltdosis på 20 mg nifedipin ER og benazepril 10 mg, var plasmakoncentrationerne af benazeprilat og nifedipin i nærvær og fravær af hinanden ikke statistisk signifikant forskellige. En hypotensiv effekt sås kun efter samtidig administration af de to lægemidler. Den takykardiske virkning af nifedipin blev svækket i nærvær af benazepril.
Angiotensin-II-blokkere
Irbesartan: In vitro undersøgelser viser signifikant hæmning af nifedipins dannelse af oxiderede irbesartan-metabolitter. I kliniske undersøgelser havde samtidig nifedipin imidlertid ingen effekt på irbesartans farmakokinetik.
Candesartan: Der er ikke rapporteret nogen signifikant lægemiddelinteraktion i studier med candesartan cilexitil givet sammen med nifedipin. Da candesartan ikke metaboliseres signifikant af cytokrom P450-systemet og i terapeutiske koncentrationer ikke har nogen effekt på cytokrom P450-enzymer, ville interaktioner med lægemidler, der hæmmer eller metaboliseres af disse enzymer, ikke forventes.
Beta-blokkere
Adalat 10 mg CC blev godt tolereret, når det blev administreret i kombination med betablokkere til 187 hypertensive patienter i et placebokontrolleret klinisk forsøg. Der har dog været lejlighedsvise litteraturrapporter, der tyder på, at kombinationen nifedipin og beta-adrenerge blokerende lægemidler kan øge sandsynligheden for kongestiv hjertesvigt, alvorlig hypotension eller forværring af angina hos patienter med kardiovaskulær sygdom. Klinisk monitorering anbefales, og en dosisjustering af nifedipin bør overvejes.
Timolol: Hypotension er mere sandsynligt, hvis dihydropryridin-calciumantagonister såsom nifedipin administreres sammen med timolol.
Central Alpha1-blokering
Doxazosin: Raske frivillige, der deltog i et doxazosin-nifedipin interaktionsstudie med flere doser, fik 2 mg doxazosin dagligt alene eller kombineret med 20 mg nifedipin ER bid. Samtidig administration af nifedipin resulterede i et fald i AUC og Cmax for doxazosin til 83 % og 86 % af værdierne i fravær af nifedipin hhv. I nærvær af doxazosin blev AUC og Cmax for nifedipin øget med faktorer på henholdsvis 1,13 og 1,23. Sammenlignet med nifedipin monoterapi var blodtrykket lavere ved tilstedeværelse af doxazosin. Blodtrykket bør overvåges, når doxazosin administreres sammen med nifedipin, og dosisreduktion af nifedipin bør overvejes.
Digitalis
Digoxin: Samtidig administration af nifedipin og digoxin kan føre til reduceret clearance, hvilket resulterer i en stigning i plasmakoncentrationen af digoxin. Da der har været isolerede rapporter om patienter med forhøjede digoxinniveauer, og der er en mulig interaktion mellem digoxin og Adalat CC, anbefales det, at digoxinniveauer overvåges ved påbegyndelse, justering og seponering af Adalat 10mg CC for at undgå mulig over- eller under- digitalisering.
Antitrombotika
Kumariner: Der har været sjældne rapporter om øget protrombintid hos patienter, der tager coumarinantikoagulantia, til hvem nifedipin blev administreret. Forholdet til nifedipinbehandling er dog usikkert.
Blodpladeaggregationshæmmere
Clopidogrel: Der blev ikke observeret nogen klinisk signifikante farmakodynamiske interaktioner, når clopidrogrel blev administreret sammen med nifedipin.
Tirofiban: Samtidig administration af nifedipin ændrede ikke eksponeringen for tirofiban væsentligt.
Andet
Diuretika, PDE5-hæmmere, alfa-methyldopa: Nifedipin kan øge den blodtrykssænkende effekt af disse samtidig administrerede midler.
Ikke-kardiovaskulære lægemidler
Antifungale lægemidler
Ketoconazol, itraconazol og fluconazol er CYP3A-hæmmere og kan hæmme metabolismen af nifedipin og øge eksponeringen for nifedipin under samtidig behandling. Blodtrykket bør overvåges, og en dosisreduktion af nifedipin bør overvejes.
Antisekretoriske stoffer
Omeprazol: Hos raske frivillige, der fik en enkeltdosis på 10 mg nifedipin, var AUC og Cmax for nifedipin efter forbehandling med omeprazol 20 mg dagligt i 8 dage 1,26 og 0,87 gange højere end efter forbehandling med placebo. Forbehandling med eller samtidig administration af omeprazol påvirkede ikke virkningen af nifedipin på blodtryk eller hjertefrekvens. Omeprazols indvirkning på nifedipin er sandsynligvis ikke af klinisk relevans.
Pantoprazol: Hos raske frivillige blev eksponeringen for ingen af lægemidlerne ændret væsentligt i nærvær af det andet lægemiddel.
Ranitidin: Fem undersøgelser med raske frivillige undersøgte virkningen af multiple ranitidindoser på enkelt- eller multiple-dosis-farmakokinetikken af nifedipin. To undersøgelser undersøgte virkningen af samtidig administreret ranitidin på blodtrykket hos hypertensive personer på nifedipin. Samtidig administration af ranitidin havde ingen relevante virkninger på eksponeringen for nifedipin, som påvirkede blodtrykket eller hjertefrekvensen hos normotensive eller hypertensive personer.
Cimetidin: Fem undersøgelser med raske frivillige undersøgte virkningen af multiple cimetidindoser på enkelt- eller multiple-dosis-farmakokinetikken af nifedipin. To undersøgelser undersøgte virkningen af samtidig administreret cimetidin på blodtrykket hos hypertensive personer på nifedipin. Hos normotensive forsøgspersoner, der fik enkeltdoser på 10 mg eller flere doser på op til 20 mg nifedipin tid alene eller sammen med cimetidin op til 1000 mg/dag, var AUC-værdierne for nifedipin i nærvær af cimetidin mellem 1,52 og 2,01 gange dem i fravær af cimetidin. Cmax-værdierne for nifedipin i nærvær af cimetidin blev øget af faktorer, der lå mellem 1,60 og 2,02. Stigningen i eksponering for nifedipin med cimetidin blev ledsaget af relevante ændringer i blodtryk eller hjertefrekvens hos normotensive personer. Hypertensive personer, der fik 10 mg qd nifedipin alene eller i kombination med cimetidin 1000 mg qd, oplevede også relevante ændringer i blodtrykket, når cimetidin blev tilføjet til nifedipin. Interaktionen mellem cimetidin og nifedipin er af klinisk relevans, og blodtrykket bør overvåges, og en reduktion af dosis af nifedipin bør overvejes.
Cisaprid: Samtidig administration af cisaprid og nifedipin kan føre til øgede plasmakoncentrationer af nifedipin.
Antibakterielle lægemidler
Quinupristin/Dalfopristin: In vitro lægemiddelinteraktionsstudier har vist, at quinupristin/dalfopristin signifikant hæmmer CYP3A-metabolismen af nifedipin. Samtidig administration af quinupristin/dalfopristin og nifedipin (gentagen oral dosis) hos raske frivillige øgede AUC og Cmax for nifedipin med faktorer på henholdsvis 1,44 og 1,18 sammenlignet med nifedipin monoterapi. Ved samtidig administration af quinupristin/dalfopristin og nifedipin bør blodtrykket overvåges, og en reduktion af nifedipindosis bør overvejes.
Erythromycin: Erythromycin, en CYP3A-hæmmer, kan hæmme metabolismen af nifedipin og øge eksponeringen for nifedipin under samtidig behandling. Blodtrykket bør overvåges, og reduktion af nifedipindosis bør overvejes.
Antituberkulære lægemidler
Rifampin: Stærke CYP3A-inducere, såsom rifampin, rifapentin og rifabutin reducerer biotilgængeligheden af nifedipin, hvilket kan reducere effektiviteten af nifedipin; derfor bør nifedipin ikke anvendes i kombination med stærke CYP3A-inducere såsom rifampin (se KONTRAINDIKATIONER ). Virkningen af flere orale doser på 600 mg rifampin på nifedipins farmakokinetik efter en enkelt oral dosis på 20 mg nifedipinkapsel blev evalueret i et klinisk studie. Tolv raske mandlige frivillige modtog en enkelt oral dosis på 20 mg nifedipinkapsel på undersøgelsesdag 1. Fra undersøgelsesdag 2 modtog forsøgspersonerne 600 mg rifampin én gang dagligt i 14 dage. På undersøgelsesdag 15 blev en anden enkelt oral dosis på 20 mg nifedipinkapsel administreret sammen med den sidste dosis rifampin. Sammenlignet med undersøgelsesdag 1 reducerede 14 dages forbehandling med rifampin Cmax og AUC for samtidig administreret nifedipin i gennemsnit med henholdsvis 95 % og 97 %.

Antivirale lægemidler
Amprenavir, atanazavir, delavirin, fosamprinavir, indinavir, nelfinavir og ritonavir, som CYP3A-hæmmere, kan hæmme metabolismen af nifedipin og øge eksponeringen for nifedipin. Forsigtighed er berettiget, og klinisk monitorering af patienter anbefales.
CNS-lægemidler
Nefazodon, en CYP3A-hæmmer, kan hæmme metabolismen af nifedipin og øge eksponeringen for nifedipin under samtidig behandling. Blodtrykket bør overvåges, og en reduktion af dosis af nifedipin bør overvejes.
Fluoxetin, en CYP3A-hæmmer, kan hæmme metabolismen af nifedipin og øge eksponeringen for nifedipin under samtidig behandling. Blodtrykket bør overvåges, og en reduktion af dosis af nifedipin bør overvejes.
Valproinsyre kan øge eksponeringen for nifedipin under samtidig behandling. Blodtrykket bør overvåges, og en dosisreduktion af nifedipin bør overvejes.
Phenytoin, Phenobarbital og Carbamazepin: Nifedipin metaboliseres af CYP3A. Samtidig administration af nifedipin 10 mg kapsel og 60 mg nifedipin kappe-tablet med phenytoin, en inducer af CYP3A, sænkede AUC og Cmax for nifedipin med ca. 70 %. Phenobarbital og carbamazepin er også inducere af CYP3A. Alternativ antihypertensiv behandling bør overvejes hos patienter, der tager phenytoin, phenobarbital og carbamazepin.
Antiemetiske lægemidler
Dolasetron: Hos patienter, der fik dolasetron oralt eller intravenøst og nifedipin, blev der ikke vist nogen effekt på clearance af hydrodolasetron.
Immunsuppressive lægemidler
Tacrolimus: Tacrolimus har vist sig at blive metaboliseret via CYP3A-systemet. Nifedipin har vist sig at hæmme metabolismen af tacrolimus in vitro. Transplanterede patienter på tacrolimus og nifedipin krævede fra 26 % til 38 % mindre doser end patienter, der ikke fik nifedipin. Nifedipin kan øge eksponeringen for tacrolimus. Når nifedipin administreres sammen med tacrolimus, bør blodkoncentrationerne af tacrolimus overvåges, og en reduktion af dosis af tacrolimus bør overvejes.
Sirolimus: En enkelt dosis på 60 mg nifedipin og en enkelt dosis på 10 mg sirolimus oral opløsning blev givet til 24 raske frivillige. Der blev ikke observeret klinisk signifikante farmakokinetiske lægemiddelinteraktioner.
Glukosesænkende lægemidler
Pioglitazon: Samtidig administration af pioglitazon i 7 dage med 30 mg nifedipin ER administreret oralt dagligt i 4 dage til mandlige og kvindelige frivillige, resulterede i mindste kvadratiske middelværdier (90 % CI) for uændret nifedipin på 0,83 (0,73-0,95) for Cmax og 0,88 ( 0,80-0,96) for AUC i forhold til nifedipin monoterapi. I lyset af den høje variation af nifedipins farmakokinetik er den kliniske betydning af dette fund ukendt.
Rosiglitazon: Samtidig administration af rosiglitazon (4 mg to gange dagligt) har ikke vist sig at have nogen klinisk relevant effekt på nifedipins farmakokinetik.
Metformin: En enkeltdosis metformin-nifedipin interaktionsundersøgelse hos normale raske frivillige viste, at samtidig administration af nifedipin øgede plasmametformin Cmax og AUC med henholdsvis 20 % og 9 % og øgede mængden af metformin udskilt i urinen. Tmax og halveringstid var upåvirket. Nifedipin ser ud til at øge absorptionen af metformin.
Miglitol: Der blev ikke observeret nogen effekt af miglitol på nifedipins farmakokinetik og farmakodynamik.
Repaglinid: Samtidig administration af 10 mg nifedipin med en enkelt dosis på 2 mg repaglinid (efter 4 dage nifedipin 10 mg tid og repaglinid 2 mg tid) resulterede i uændrede AUC- og Cmax-værdier for begge lægemidler.
Acarbose: Nifedipin har en tendens til at producere hyperglykæmi og kan føre til tab af glukosekontrol. Hvis nifedipin administreres sammen med acarbose, bør blodsukkerniveauet overvåges omhyggeligt, og en dosisjustering af nifedipin bør overvejes.
Lægemidler, der forstyrrer fødevareoptagelsen
Orlistat: Hos 17 normalvægtige forsøgspersoner, der fik orlistat 120 mg dagligt i 6 dage, ændrede orlistat ikke biotilgængeligheden af 60 mg nifedipin (tabletter med forlænget frigivelse).
Kosttilskud
Grapefrugtjuice: Hos raske frivillige øgede en enkelt dosis samtidig administration af 250 ml dobbeltstyrke grapefrugtjuice med 10 mg nifedipin AUC og Cmax med faktorer på henholdsvis 1,35 og 1,13. Indtagelse af gentagne doser grapefrugtjuice (5 x 200 ml på 12 timer) efter administration af 20 mg nifedipin ER øgede AUC og Cmax for nifedipin med en faktor 2. Grapefrugtjuice bør undgås af patienter på nifedipin. Indtagelsen af grapefrugtjuice bør stoppes mindst 3 dage før påbegyndelse af patienter med nifedipin.
Urter
St. John's Wort: Perikon er en inducer af CYP3A og kan nedsætte eksponeringen for nifedipin. Alternativ antihypertensiv behandling bør overvejes hos patienter, hvor behandling med perikon er nødvendig.
CYP2D6 Probe Drug
Debrisokin: Hos raske frivillige ændrede forbehandling med nifedipin 20 mg tid i 5 dage ikke det metaboliske forhold mellem hydroxydebrisoquin og debrisoquin målt i urin efter en enkelt dosis på 10 mg debrisoquin. Det er således usandsynligt, at nifedipin in vivo hæmmer metabolismen af andre lægemidler, der er substrater for CYP2D6.
ADVARSLER
Overdreven hypotension
Selvom den hypotensive effekt af nifedipin hos de fleste patienter er beskeden og veltolereret, har lejlighedsvise patienter haft overdreven og dårligt tolereret hypotension. Disse responser er sædvanligvis forekommet under initial titrering eller på tidspunktet for efterfølgende opjustering af dosis og kan være mere sandsynlige hos patienter, der samtidig bruger betablokkere.
Alvorlig hypotension og/eller øget behov for væskevolumen er blevet rapporteret hos patienter, som fik kapsler med øjeblikkelig frigivelse sammen med et beta-blokerende middel, og som har gennemgået en koronararterie-bypass-operation med højdosis fentanylanæstesi. Interaktionen med højdosis fentanyl synes at skyldes kombinationen af nifedipin og en betablokker, men muligheden for, at den kan forekomme med nifedipin alene, med lave doser af fentanyl, ved andre kirurgiske indgreb eller med andre narkotiske analgetika kan ikke udelukket. Hos nifedipin-behandlede patienter, hvor kirurgi med højdosis fentanylanæstesi påtænkes, bør lægen være opmærksom på disse potentielle problemer, og hvis patientens tilstand tillader det, skal der gives tilstrækkelig tid (mindst 36 timer) til at nifedipin kan vaskes ud af kroppen før operationen.
Øget angina og/eller myokardieinfarkt
Sjældent har patienter, især dem, der har svær obstruktiv koronararteriesygdom, udviklet veldokumenteret øget hyppighed, varighed og/eller sværhedsgrad af angina eller akut myokardieinfarkt ved start af nifedipin eller på tidspunktet for dosisstigning. Mekanismen for denne effekt er ikke etableret.
Beta-blokering tilbagetrækning
Når du seponerer en betablokker, er det vigtigt at nedtrappe dosis, hvis det er muligt, i stedet for at stoppe pludseligt, før du begynder med nifedipin. Patienter, der for nylig er seponeret fra betablokkere, kan udvikle et abstinenssyndrom med øget angina, sandsynligvis relateret til øget følsomhed over for katekolaminer. Påbegyndelse af nifedipin-behandling vil ikke forhindre denne forekomst og er nogle gange blevet rapporteret at øge den.
Kongestiv hjertesvigt
Sjældent har patienter (normalt mens de får en betablokker) udviklet hjertesvigt efter påbegyndelse af nifedipin. Patienter med stram aortastenose kan have større risiko for en sådan hændelse, da aflastningseffekten af nifedipin forventes at være til mindre gavn for disse patienter på grund af deres faste impedans til at strømme hen over aortaklappen.
FORHOLDSREGLER
Generel
Hypotension
Fordi nifedipin nedsætter perifer vaskulær modstand, foreslås omhyggelig overvågning af blodtrykket under den indledende administration og titrering af Adalat CC. Tæt observation anbefales især til patienter, der allerede tager medicin, der vides at sænke blodtrykket (se ADVARSLER ).
Perifert ødem
Mildt til moderat perifert ødem opstår på en dosisafhængig måde med Adalat CC. Den placebo-subtraherede rate er ca. 8 % ved 30 mg, 12 % ved 60 mg og 19 % ved 90 mg daglig. Dette ødem er et lokaliseret fænomen, der menes at være forbundet med vasodilatation af afhængige arterioler og små blodkar og ikke på grund af venstre ventrikulær dysfunktion eller generaliseret væskeretention. Hos patienter, hvis hypertension er kompliceret af kongestiv hjerteinsufficiens, bør der udvises forsigtighed for at differentiere dette perifere ødem fra virkningerne af øget venstre ventrikulær dysfunktion.
Anvendelse hos cirrosepatienter
Clearance af nifedipin reduceres, og systemisk eksponering øges hos patienter med cirrhose. Det er ukendt, hvordan systemisk eksponering kan ændres hos patienter med moderat eller svær leverinsufficiens. Omhyggelig overvågning og dosisreduktion kan være nødvendig; overveje at starte behandlingen med den laveste tilgængelige dosis.
Laboratorieprøver
Sjældne, sædvanligvis forbigående, men lejlighedsvis signifikante forhøjelser af enzymer såsom alkalisk fosfatase, CPK, LDH, SGOT og SGPT er blevet noteret. Forholdet til nifedipinbehandling er i de fleste tilfælde usikkert, men sandsynligt i nogle tilfælde. Disse laboratorieabnormiteter er sjældent blevet forbundet med kliniske symptomer; der er dog rapporteret kolestase med eller uden gulsot. En lille stigning (
Nifedipin nedsætter ligesom andre calciumkanalblokkere blodpladeaggregation in vitro. Begrænsede kliniske undersøgelser har vist et moderat, men statistisk signifikant fald i blodpladeaggregation og øget blødningstid hos nogle nifedipinpatienter. Dette menes at være en funktion af hæmning af calciumtransport over blodplademembranen. Ingen klinisk betydning for disse fund er blevet påvist.
Positiv direkte Coombs' test med eller uden hæmolytisk anæmi er blevet rapporteret, men en årsagssammenhæng mellem administration af nifedipin og positiviteten af denne laboratorietest, inklusive hæmolyse, kunne ikke bestemmes.
Selvom nifedipin er blevet brugt sikkert til patienter med nyreinsufficiens og er blevet rapporteret at have en gavnlig effekt i visse tilfælde, er sjældne reversible stigninger i BUN og serumkreatinin blevet rapporteret hos patienter med allerede eksisterende kronisk nyreinsufficiens. Forholdet til nifedipinbehandling er usikkert i de fleste tilfælde, men sandsynligt i nogle tilfælde.
Karcinogenese, mutagenese, svækkelse af fertilitet
Nifedipin blev indgivet oralt til rotter i to år og viste sig ikke at være kræftfremkaldende. Når det blev givet til rotter før parring, forårsagede nifedipin nedsat fertilitet ved en dosis på ca. 30 gange den maksimalt anbefalede humane dosis. Der er en litteraturrapport om reversibel reduktion i evnen hos menneskelig sæd opnået fra et begrænset antal infertile mænd, der tager anbefalede doser af nifedipin til at binde sig til og befrugte et æg in vitro. In vivo mutagenicitetsundersøgelser var negative.
Graviditet
Graviditetskategori C
Hos gnavere, kaniner og aber har nifedipin vist sig at have en række embryotoksiske, placentotoksiske, teratogene og føtotoksiske virkninger, herunder forkrøplede fostre (rotter, mus og kaniner), digitale anomalier (rotter og kaniner), ribbensdeformiteter (mus), ganespalte (mus), små moderkager og underudviklede chorionvilli (aber), embryonale og føtale dødsfald (rotter, mus og kaniner), forlænget graviditet (rotter; ikke vurderet hos andre arter) og nedsat neonatal overlevelse (rotter; ikke evalueret i andre arter). På mg/kg- eller mg/m²-basis er nogle af de doser, der er forbundet med disse forskellige virkninger, højere end den maksimalt anbefalede humane dosis, og nogle er lavere, men alle er inden for en størrelsesorden af den.
De digitale anomalier, der ses hos nifedipin-eksponerede kaninunger, ligner slående dem, der ses hos unger, der er udsat for phenytoin, og disse ligner igen de phalangeale deformiteter, der er den mest almindelige misdannelse, der ses hos menneskebørn med in utero eksponering for phenytoin.
Ud fra den tilgængelige kliniske dokumentation er en specifik prænatal risiko ikke blevet identificeret. Der er dog rapporteret en stigning i perinatal asfyksi, kejsersnit, præmaturitet og intrauterin væksthæmning.
Omhyggelig overvågning af blodtrykket skal udføres hos gravide kvinder, når nifedipin administreres i kombination med IV magnesiumsulfat på grund af muligheden for et for stort blodtryksfald, som kan skade moderen og fosteret.
Der er ingen tilstrækkelige og velkontrollerede undersøgelser af gravide kvinder.
Ammende mødre
Nifedipin udskilles i modermælk. Ammende mødre rådes til ikke at amme deres babyer, når de tager stoffet.
Pædiatrisk brug
Sikkerheden og effektiviteten af Adalat 30mg CC hos pædiatriske patienter er ikke blevet fastslået.
Geriatrisk brug
Selvom små farmakokinetiske undersøgelser har identificeret en øget halveringstid og øget Cmax og AUC (se KLINISK FARMAKOLOGI : Farmakokinetik og metabolisme ), omfattede kliniske undersøgelser af nifedipin ikke et tilstrækkeligt antal forsøgspersoner på 65 år og derover til at afgøre, om de reagerer anderledes end yngre forsøgspersoner. Andre rapporterede kliniske erfaringer har ikke identificeret forskelle i respons mellem ældre og yngre patienter. Generelt bør dosisvalg for en ældre patient være forsigtigt, sædvanligvis begyndende i den lave ende af doseringsområdet, hvilket afspejler den større hyppighed af nedsat lever-, nyre- eller hjertefunktion og af samtidig sygdom eller anden lægemiddelbehandling.
Patienter med galaktoseintolerance
Da dette lægemiddel indeholder lactose, bør patienter med sjældne arvelige problemer med galactoseintolerance, Lapp lactase-mangel eller glucose-galactosemalabsorption ikke tage dette lægemiddel.
OVERDOSIS
Erfaring med overdosering af nifedipin er begrænset. Symptomer forbundet med alvorlig overdosering af nifedipin omfatter bevidsthedstab, blodtryksfald, hjerterytmeforstyrrelser, metabolisk acidose, hypoxi, kardiogent shock med lungeødem. Generelt kræver overdosering med nifedipin, der fører til udtalt hypotension, aktiv kardiovaskulær støtte, herunder monitorering af kardiovaskulær og respiratorisk funktion, hævede ekstremiteter, fornuftig brug af calciuminfusion, pressormidler og væsker. Efter oral indtagelse er grundig maveskylning indiceret, om nødvendigt i kombination med skylning af tyndtarmen. I tilfælde, der involverer overdosering af et slowrelease-produkt som nifedipin, skal eliminationen være så fuldstændig som muligt, også fra tyndtarmen, for at forhindre efterfølgende absorption af det aktive stof. Yderligere væske eller volumen skal administreres med forsigtighed på grund af risikoen for væskeoverbelastning.
Clearance af nifedipin forventes at blive forlænget hos patienter med nedsat leverfunktion. Da nifedipin er stærkt proteinbundet, vil dialyse sandsynligvis ikke være til gavn; plasmaferese kan dog være gavnlig.
Der har været et rapporteret tilfælde af massiv overdosering med tabletter af en anden depotformulering af nifedipin. De vigtigste virkninger af indtagelse af ca. 4800 mg nifedipin hos en ung mand, der forsøgte selvmord som følge af kokain-induceret depression, var indledende svimmelhed, hjertebanken, rødmen og nervøsitet. Inden for flere timer efter indtagelse udviklede der sig kvalme, opkastning og generaliseret ødem. Ingen signifikant hypotension var synlig ved præsentationen 18 timer efter indtagelse. Blodkemiske abnormiteter bestod af en mild, forbigående forhøjelse af serumkreatinin og beskedne forhøjelser af LDH og CPK, men normal SGOT. Vitale tegn forblev stabile, ingen elektrokardiografiske abnormiteter blev noteret, og nyrefunktionen vendte tilbage til normal inden for 24 til 48 timer med rutinemæssige støtteforanstaltninger alene. Der blev ikke observeret længerevarende følgesygdomme.
Effekten af en enkelt 900 mg indtagelse af nifedipinkapsler hos en deprimeret anginapatient på tricykliske antidepressiva var bevidsthedstab inden for 30 minutter efter indtagelse og dyb hypotension, som reagerede på calciuminfusion, pressormidler og væskeerstatning. En række EKG-abnormaliteter blev set hos denne patient med en historie med bundtgrenblok, herunder sinusbradykardi og varierende grader af AV-blok. Disse dikterede den profylaktiske placering af en midlertidig ventrikulær pacemaker, men forsvandt ellers spontant. Betydelig hyperglykæmi blev indledningsvis set hos denne patient, men plasmaglukoseniveauer normaliseredes hurtigt uden yderligere behandling.
En ung hypertensiv patient med fremskreden nyresvigt indtog 280 mg nifedipinkapsler på én gang, med deraf følgende markant hypotension, der reagerede på calciuminfusion og væsker. Ingen AV-ledningsabnormiteter, arytmier eller udtalte ændringer i hjertefrekvens blev noteret, og der var heller ingen yderligere forringelse af nyrefunktionen.
Bradykardiale hjerterytmeforstyrrelser kan behandles symptomatisk med ß-sympathomimetika, og ved livstruende bradykardiale forstyrrelser af hjerterytmen kan midlertidig pacemakerbehandling tilrådes.
KONTRAINDIKATIONER
Samtidig administration med stærke P450-inducere, såsom rifampin, er kontraindiceret, da virkningen af nifedipin-tabletter kan reduceres væsentligt. (Se DRUGSINTERAKTIONER )
Nifedipin må ikke anvendes i tilfælde af kardiogent shock.
Adalat er kontraindiceret til patienter med kendt overfølsomhed over for enhver komponent i tabletten.
KLINISK FARMAKOLOGI
Nifedipin er en calciumion-influx-hæmmer (langsom-kanalblokker eller calciumion-antagonist), som hæmmer den transmembrane tilstrømning af calciumioner i vaskulær glat muskulatur og hjertemuskulatur. De kontraktile processer i vaskulær glat muskulatur og hjertemuskulatur er afhængige af bevægelsen af ekstracellulære calciumioner ind i disse celler gennem specifikke ionkanaler. Nifedipin hæmmer selektivt calciumiontilstrømning gennem cellemembranen i vaskulær glat muskulatur og hjertemuskel uden at ændre serumcalciumkoncentrationen.
Handlingsmekanisme
Den mekanisme, hvorved nifedipin reducerer det arterielle blodtryk, involverer perifer arteriel vasodilatation og som følge heraf en reduktion i perifer vaskulær modstand. Den øgede perifere vaskulære modstand, en underliggende årsag til hypertension, skyldes en stigning i aktiv spænding i den vaskulære glatte muskel. Undersøgelser har vist, at stigningen i aktiv spænding afspejler en stigning i cytosolisk frit calcium.
Nifedipin er en perifer arteriel vasodilator, som virker direkte på vaskulær glat muskulatur. Bindingen af nifedipin til spændingsafhængige og muligvis receptor-opererede kanaler i vaskulær glat muskulatur resulterer i en hæmning af calciumtilstrømning gennem disse kanaler. Depoter af intracellulært calcium i vaskulær glat muskulatur er begrænsede og er således afhængige af tilstrømningen af ekstracellulært calcium for, at kontraktion kan forekomme. Reduktionen i calciumtilstrømning af nifedipin forårsager arteriel vasodilatation og nedsat perifer vaskulær modstand, hvilket resulterer i reduceret arterielt blodtryk.
Farmakokinetik og metabolisme
Nifedipin absorberes fuldstændigt efter oral administration. Biotilgængeligheden af nifedipin som Adalat CC i forhold til nifedipin med øjeblikkelig frigivelse er i intervallet 84%-89%. Efter indtagelse af Adalat CC-tabletter under fastende forhold topper plasmakoncentrationen ved ca. 2,5-5 timer med en anden lille top eller skulder, der er tydelig ca. 6-12 timer efter dosis. Eliminationshalveringstiden for nifedipin administreret som Adalat CC er ca. 7 timer i modsætning til den kendte 2 timers eliminationshalveringstid for nifedipin administreret som en kapsel med øjeblikkelig frigivelse.
Når Adalat CC administreres som multipla af 30 mg tabletter over et dosisområde på 30 mg til 90 mg, er arealet under kurven (AUC) dosisproportionalt; den maksimale plasmakoncentration for 90 mg dosis givet som 3 x 30 mg er dog 29 % større end forudsagt ud fra 30 mg og 60 mg doser.
To 30 mg Adalat CC tabletter kan udskiftes med en 60 mg Adalat CC tablet. Tre 30 mg Adalat CC-tabletter resulterer imidlertid i væsentligt højere Cmax-værdier end dem efter en enkelt 90 mg Adalat 20 mg CC-tablet. Tre 30 mg tabletter bør derfor ikke betragtes som udskiftelige med en 90 mg tablet.
En gang daglig dosering af Adalat CC under fastende forhold resulterer i nedsatte fluktuationer i plasmakoncentrationen af nifedipin sammenlignet med tiddosering med nifedipinkapsler med øjeblikkelig frigivelse. Den gennemsnitlige maksimale plasmakoncentration af nifedipin efter en 90 mg Adalat 30 mg CC-tablet, indgivet under fastende forhold, er ca. 115 ng/ml. Når Adalat CC gives umiddelbart efter et fedtrigt måltid til raske frivillige, er der en gennemsnitlig stigning på 60 % i peak plasma nifedipin koncentrationen, en forlængelse af tiden til peak koncentration, men ingen signifikant ændring i AUC. Plasmakoncentrationer af nifedipin, når Adalat 20 mg CC tages efter et fedtholdigt måltid, resulterer i lidt lavere toppe sammenlignet med den samme daglige dosis af formuleringen med øjeblikkelig frigivelse administreret i tre opdelte doser. Dette kan til dels skyldes, at Adalat CC er mindre biotilgængelig end formuleringen med øjeblikkelig frigivelse.
Nifedipin metaboliseres i vid udstrækning til meget vandopløselige, inaktive metabolitter, der tegner sig for 60 % til 80 % af den dosis, der udskilles i urinen. Kun spor (mindre end 0,1 % af dosis) af den uændrede form kan påvises i urinen. Resten udskilles i fæces i metaboliseret form, højst sandsynligt som følge af galdeudskillelse.
Nifedipin metaboliseres via cytochrom P450 3A4-systemet. Lægemidler, der vides at enten hæmme eller inducere dette enzymsystem, kan ændre den første passage eller clearance af nifedipin.
Der er ikke udført undersøgelser med Adalat 30 mg CC hos patienter med nyresvigt; der er dog ikke rapporteret signifikante ændringer i farmakokinetikken af nifedipin kapsler med øjeblikkelig frigivelse hos patienter, der gennemgår hæmodialyse eller kronisk ambulatorisk peritonealdialyse. Da absorptionen af nifedipin fra Adalat CC kan modificeres af nyresygdom, bør der udvises forsigtighed ved behandling af sådanne patienter.
Fordi nifedipin metaboliseres via cytochrom P450 3A4-systemet, kan dets farmakokinetik blive ændret hos patienter med kronisk leversygdom. Adalat 20 mg CC er ikke blevet undersøgt hos patienter med leversygdom; Hos patienter med nedsat leverfunktion (levercirrhose) har nifedipin imidlertid en længere eliminationshalveringstid og højere biotilgængelighed end hos raske frivillige.
Nifedipins proteinbindingsgrad er høj (92%-98%). Proteinbinding kan være stærkt reduceret hos patienter med nedsat nyre- eller leverfunktion.
Efter administration af Adalat 30 mg CC til raske ældre mænd og kvinder (alder > 60 år) er den gennemsnitlige Cmax 36 % højere, og den gennemsnitlige plasmakoncentration er 70 % højere end hos yngre patienter.
Hos raske forsøgspersoner var eliminationshalveringstiden for en anden nifedipin-formulering med vedvarende frigivelse længere hos ældre forsøgspersoner (6,7 timer) sammenlignet med unge forsøgspersoner (3,8 timer) efter oral administration. En nedsat clearance blev også observeret hos ældre (348 ml/min) sammenlignet med unge forsøgspersoner (519 ml/min) efter intravenøs administration.
Samtidig administration af nifedipin og grapefrugtjuice resulterer i op til en 2-fold stigning i AUC og Cmax på grund af hæmning af CYP3A-relateret first-pass metabolisme. Indtagelse af grapefrugt og grapefrugtjuice bør undgås, mens du tager nifedipin.
Kliniske Studier
Adalat 10 mg CC gav dosisrelaterede fald i systolisk og diastolisk blodtryk som vist i to dobbeltblindede, randomiserede, placebokontrollerede forsøg, hvor over 350 patienter blev behandlet med Adalat CC 30, 60 eller 90 mg én gang dagligt i 6 uger. I den første undersøgelse blev Adalat 10 mg CC givet som monoterapi, og i den anden undersøgelse blev Adalat 20 mg CC tilføjet til en betablokker hos patienter, der ikke var kontrolleret med en betablokker alene. Det gennemsnitlige laveste (24 timer efter dosis) blodtryksresultater fra disse undersøgelser er vist nedenfor:
GENNEMFØRELSE AF REDUKTIONER I BLODTRYK PÅ LIGGENDE SUPINE (mmHg) SYSTOLISK/DIASTOLISK
Lav-/peak-forholdet estimeret ud fra 24-timers blodtryksmonitorering varierede fra 41%-78% for diastolisk og 46%-91% for systolisk blodtryk.
Hæmodynamik
Som andre langsomme-kanalblokkere udøver nifedipin en negativ inotrop effekt på isoleret myokardievæv. Dette ses sjældent eller aldrig hos intakte dyr eller mennesker, sandsynligvis på grund af refleksreaktioner på dets vasodilaterende virkninger. Hos mennesker nedsætter nifedipin perifer vaskulær modstand, hvilket fører til et fald i systolisk og diastolisk tryk, normalt minimalt hos normotensive frivillige (mindre end 5-10 mm Hg systolisk), men nogle gange større. Med Adalat 30mg CC er disse fald i blodtrykket ikke ledsaget af nogen signifikant ændring i hjertefrekvensen. Hæmodynamiske undersøgelser af formuleringen af nifedipin med øjeblikkelig frigivelse hos patienter med normal ventrikulær funktion har generelt fundet en lille stigning i hjerteindekset uden større effekter på ejektionsfraktion, venstre ventrikel end-diastolisk tryk (LVEDP) eller volumen (LVEDV). Hos patienter med nedsat ventrikelfunktion har de fleste akutte undersøgelser vist en vis stigning i ejektionsfraktion og reduktion i venstre ventrikelfyldningstryk.
Elektrofysiologiske effekter
Selvom nifedipin, ligesom andre medlemmer af sin klasse, forårsager en let sænkning af sinoatrial nodefunktion og atrioventrikulær ledning i isolerede myokardiepræparater, er sådanne virkninger ikke set i studier med intakte dyr eller hos mennesker. I formelle elektrofysiologiske undersøgelser, hovedsageligt hos patienter med normale ledningssystemer, har nifedipin administreret som kapsel med øjeblikkelig frigivelse ikke haft en tendens til at forlænge atrioventrikulær lednings- eller sinusknudegendannelsestid eller at sænke sinushastigheden.
PATIENTOPLYSNINGER
Adalat CC er en forlænget frigivelsestablet og skal sluges hel og tages på tom mave. Det bør ikke indgives sammen med mad. Tabletter må ikke tygges, deles eller knuses.
