Trecator-SC 250mg Ethionamide Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Trecator, og hvordan bruges det?
Trecator er en receptpligtig medicin, der bruges til at behandle symptomerne på aktiv tuberkulose. Trecator kan bruges alene eller sammen med anden medicin.
Trecator tilhører en klasse af lægemidler kaldet antituberkulære midler.
Hvad er de mulige bivirkninger af Trecator?
Trecator kan forårsage alvorlige bivirkninger, herunder:
- nældefeber,
- åndedrætsbesvær,
- hævelse af dit ansigt, læber, tunge eller hals,
- følelsesløshed, prikken eller brænden i dine hænder eller fødder,
- forvirring,
- usædvanlige tanker eller adfærd,
- øjensmerter,
- sløret syn,
- Dobbelt syn,
- svimmelhed,
- anfald,
- smerter i øvre mave,
- mørk urin,
- lerfarvede afføring, og
- gulfarvning af huden eller øjnene (gulsot)
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Trecator omfatter:
- kvalme,
- opkastning,
- diarré,
- mavesmerter,
- mistet appetiten,
- øget spytudskillelse,
- metallisk smag i munden,
- vabler eller sår i munden,
- rødt eller hævet tandkød,
- synkebesvær,
- hovedpine,
- svimmelhed,
- døsighed,
- nedtrykt humør, og
- rastløs følelse
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Trecator. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Trecator® (ethionamidtabletter, USP) bruges til behandling af tuberkulose. Det kemiske navn for ethionamid er 2-ethylthioisonicotinamid med følgende strukturformel:
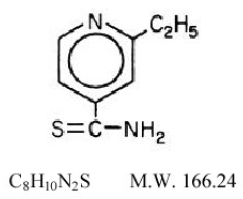
Ethionamid er en gul krystallinsk, ikke-hygroskopisk forbindelse med en svag til moderat sulfidlugt og et smeltepunkt på 162°C. Det er praktisk talt uopløseligt i vand og ether, men opløseligt i methanol og ethanol. Den har en fordelingskoefficient (oktanol/vand) Log P-værdi på 0,3699. Trecator-tabletter indeholder 250 mg ethionamid. De tilstedeværende inaktive ingredienser er croscarmellosenatrium, FD&C Yellow #6, magnesiumstearat, mikrokrystallinsk cellulose, polyethylenglycol, polyvinylalkohol, povidon, siliciumdioxid, talkum og titaniumdioxid.
INDIKATIONER
Trecator er primært indiceret til behandling af aktiv tuberkulose hos patienter med M. tuberculosis resistente over for isoniazid eller rifampin, eller når der er intolerance hos patienten over for andre lægemidler. Dets anvendelse alene i behandlingen af tuberkulose resulterer i den hurtige udvikling af resistens. Det er derfor vigtigt at give et eller flere passende ledsagende lægemidler, idet valget er baseret på resultaterne af følsomhedstests. Hvis følsomhedstestene indikerer, at patientens organisme er resistent over for et af de første-line antituberkuloselægemidler (dvs. isoniazid eller rifampin), men alligevel er modtagelig over for ethionamid, skal ethionamid ledsages af mindst ét lægemiddel, som M. tuberkuloseisolat er kendt for at være modtageligt.3 Hvis tuberkulosen er resistent over for både isoniazid og rifampin, men alligevel modtagelig over for ethionamid, bør ethionamid ledsages af mindst to andre lægemidler, som M. tuberculosis isolatet vides at være modtagelige for.3
For at reducere udviklingen af lægemiddelresistente bakterier og bevare effektiviteten af Trecator og andre antibakterielle lægemidler, bør Trecator kun bruges til at behandle infektioner, der er bevist eller stærkt mistænkt for at være forårsaget af modtagelige bakterier. Når kultur- og modtagelighedsoplysninger er tilgængelige, bør de overvejes ved udvælgelse eller ændring af antibakteriel behandling. I mangel af sådanne data kan lokal epidemiologi og modtagelighedsmønstre bidrage til den empiriske udvælgelse af terapi.
Patienters manglende overholdelse af ordineret behandling kan resultere i behandlingssvigt og i udvikling af lægemiddelresistent tuberkulose, som kan være livstruende og føre til andre alvorlige sundhedsrisici. Det er derfor vigtigt, at patienterne overholder lægemiddelregimet i hele behandlingens varighed. Direkte observeret terapi anbefales til alle patienter, der modtager behandling for tuberkulose. Patienter, hvor lægemiddelresistente M. tuberculosis-organismer er isoleret, bør behandles i samråd med en ekspert i behandling af lægemiddelresistent tuberkulose.
DOSERING OG ADMINISTRATION
Ved behandling af tuberkulose er en væsentlig årsag til fremkomsten af lægemiddelresistente organismer, og dermed behandlingssvigt, patientens manglende overholdelse af den foreskrevne behandling. Behandlingssvigt og lægemiddelresistente organismer kan være livstruende og kan resultere i andre alvorlige sundhedsrisici. Det er derfor vigtigt, at patienterne overholder lægemiddelregimet i hele behandlingens varighed. Direkte observeret terapi anbefales, når patienter er i behandling for tuberkulose. Konsultation med en ekspert i behandling af lægemiddelresistent tuberkulose tilrådes til patienter, hvor der er mistanke om lægemiddelresistent tuberkulose eller sandsynligt. Ethionamid bør administreres sammen med mindst et, nogle gange to, andre lægemidler, som organismen vides at være modtagelig for (se INDIKATIONER ).
Trecator administreres oralt. Den sædvanlige voksendosis er 15 til 20 mg/kg/dag, administreret én gang dagligt eller, hvis patienten udviser dårlig gastrointestinal tolerance, i opdelte doser med en maksimal daglig dosis på 1 gram.
Trecator-tabletter er blevet omformuleret fra en sukkerovertrukket tablet til en filmovertrukket tablet. Patienterne skal overvåges og få deres dosis genreguleret, når de skifter fra den sukkerovertrukne tablet til den filmovertrukne tablet (se KLINISK FARMAKOLOGI ).
Behandlingen bør påbegyndes med en dosis på 250 mg dagligt med gradvis titrering til optimale doser, som patienten tolererer. Et regime på 250 mg dagligt i 1 eller 2 dage efterfulgt af 250 mg to gange dagligt i 1 eller 2 dage med en efterfølgende stigning til 1 g i 3 eller 4 opdelte doser er blevet rapporteret.4,5 Indtil videre er der ikke tilstrækkelig evidens. for at angive de laveste effektive dosisniveauer. For at minimere risikoen for udvikling af resistens over for lægemidlet eller det ledsagende lægemiddel er princippet om at give den højeste tolererede dosis (baseret på gastrointestinal intolerance) derfor fulgt. Hos voksne ser det ud til at være mellem 0,5 og 1,0 g dagligt, med et gennemsnit på 0,75 g dagligt.
Den optimale dosis til pædiatriske patienter er ikke fastlagt. Dog er pædiatriske doser på 10 til 20 mg/kg po dagligt i 2 eller 3 opdelte doser givet efter måltider eller 15 mg/kg/24 timer som en enkelt daglig dosis blevet anbefalet.1,2 Som for voksne kan ethionamid administreres. til pædiatriske patienter én gang dagligt. Det skal bemærkes, at der kan forekomme malabsorptionssyndrom hos patienter med samtidig tuberkulose og HIV-infektion. Lægemiddelmalabsorption bør mistænkes hos patienter, som følger behandlingen, men som ikke reagerer korrekt. I sådanne tilfælde bør terapeutisk lægemiddelovervågning overvejes (se KLINISK FARMAKOLOGI ).
De bedste indgivelsestider er dem, som den enkelte patient finder bedst egnede for at undgå eller minimere gastrointestinal intolerance, som normalt er ved måltiderne. Der bør gøres alt for at tilskynde patienter til at fortsætte behandlingen, når der opstår gastrointestinale bivirkninger, da de kan aftage i sværhedsgrad, efterhånden som behandlingen skrider frem.
Samtidig administration af pyridoxin anbefales.
Behandlingsvarigheden bør baseres på individuel klinisk respons. Generelt skal du fortsætte med behandlingen, indtil den bakteriologiske omdannelse er blevet permanent, og der er opnået maksimal klinisk forbedring.
HVORDAN LEVERET
Trecator (ethionamidtabletter, USP) leveres i flasker med 100 tabletter som følger:
250 mg, orange filmovertrukken tablet mærket "W" på den ene side og "4117" på bagsiden, NDC 0008-4117-01.
Opbevares ved kontrolleret stuetemperatur 20° til 25°C (68° til 77°F). Dispenser i en tæt beholder.
REFERENCER
1. Feigin, RD, og Cherry, JD: Lærebog i pædiatriske infektionssygdomme, 2. udgave. Philadelphia, WB Saunders Co., 1987, s. 1371-1372.
2. Nelson, WE, Behrman, RE, Vaughan, VC (red.): Nelson Textbook of Pediatrics, 13. udgave. Philadelphia, WB Saunders Co., 1987, s.636.
3. Behandling af tuberkulose og tuberkuloseinfektion hos voksne og børn, Am J Respiratory and Critical Care Medicine, 149:1359-1374, 1994.
4. Peloquin, CA: Pharmacology of the Antimycobacterial Drugs, Med Clin North Am 77(6): 1230-1262, 1993.
5. American Thoracic Society. Am J Respir Crit Care Med 1997;156:S1-S25.
Distribueret af: Pfizer, Wyeth Pharmaceuticals LLC, Et datterselskab af Pfizer Inc, Philadelphia, PA 19101. Revideret: Jan 2020
BIVIRKNINGER
Gastrointestinale
De mest almindelige bivirkninger af ethionamid er gastrointestinale forstyrrelser, herunder kvalme, opkastning, diarré, mavesmerter, overdreven savlen, metallisk smag, stomatitis, anoreksi og vægttab. Uønskede gastrointestinale virkninger ser ud til at være dosisrelaterede, hvor ca. 50 % af patienterne ikke er i stand til at tolerere 1 g som en enkelt dosis. Gastrointestinale virkninger kan minimeres ved at reducere dosis, ved at ændre tidspunktet for lægemiddeladministration eller ved samtidig administration af et antiemetikum.
Nervesystem
Psykotiske forstyrrelser (herunder mental depression), døsighed, svimmelhed, rastløshed, hovedpine og postural hypotension er blevet rapporteret med ethionamid. Sjældne rapporter om perifer neuritis, optisk neuritis, diplopi, sløret syn og et pellagra-lignende syndrom er også blevet rapporteret. Samtidig administration af pyridoxin er blevet anbefalet for at forebygge eller lindre neurotoksiske virkninger.
Hepatisk
Forbigående stigninger i serumbilirubin, SGOT, SGPT; Hepatitis (med eller uden gulsot).
Andet
Overfølsomhedsreaktioner inklusive udslæt, lysfølsomhed, trombocytopeni og purpura er sjældent blevet rapporteret. Hypoglykæmi, hypothyroidisme, gynækomasti, impotens og acne er også forekommet. Håndteringen af patienter med diabetes mellitus kan blive vanskeligere hos dem, der får ethionamid.
DRUGSINTERAKTIONER
Trecator har vist sig midlertidigt at øge serumkoncentrationen af isoniazid. Trecator kan forstærke de negative virkninger af andre antituberkuløse lægemidler, der administreres samtidigt. Der er især rapporteret om kramper, når ethionamid administreres sammen med cycloserin, og der skal udvises særlig forsigtighed, når behandlingsregimet omfatter begge disse lægemidler. Overdreven indtagelse af ethanol bør undgås, fordi en psykotisk reaktion er blevet rapporteret.
ADVARSLER
Anvendelse af Trecator alene til behandling af tuberkulose resulterer i hurtig udvikling af resistens. Det er derfor vigtigt at give et eller flere passende ledsagende lægemidler, idet valget er baseret på resultaterne af følsomhedstest. Behandlingen kan dog påbegyndes før modtagelse af resultaterne af følsomhedstests, som lægen skønner passende. Ethionamid bør administreres sammen med mindst et, nogle gange to, andre lægemidler, som organismen vides at være modtagelig for (se INDIKATIONER ). Lægemidler, der er blevet brugt som ledsagende midler, er rifampin, ethambutol, pyrazinamid, cycloserin, kanamycin, streptomycin og isoniazid. De sædvanlige advarsler, forholdsregler og doseringsregimer for disse ledsagende lægemidler skal overholdes.
Patientcompliance er afgørende for succesen med antituberkuloseterapien og for at forhindre fremkomsten af lægemiddelresistente organismer. Patienter bør derfor følge lægemiddelregimet i hele behandlingens varighed. Det anbefales, at direkte observeret terapi praktiseres, når patienter får antituberkuløs medicin. Yderligere konsultation fra eksperter i behandling af lægemiddelresistent tuberkulose anbefales, når patienter udvikler lægemiddelresistente organismer.
FORHOLDSREGLER
Generel
Det er usandsynligt, at ordination af Trecator i fravær af en påvist eller stærkt mistænkt bakteriel infektionsindikation vil gavne patienten og øger risikoen for udvikling af lægemiddelresistente bakterier.
Ethionamid kan forstærke bivirkningerne af de andre antituberkuløse lægemidler, der administreres samtidigt (se DRUGSINTERAKTIONER ). Oftalmologiske undersøgelser (inklusive oftalmoskopi) bør udføres før og periodisk under behandling med Trecator.
Laboratorieprøver
Bestemmelse af serumtransaminaser (SGOT, SGPT) bør foretages før påbegyndelse af behandlingen og bør monitoreres månedligt. Hvis serumtransaminaserne bliver forhøjede under behandlingen, kan ethionamid og det ledsagende antituberkuloselægemiddel eller lægemidler midlertidigt seponeres, indtil laboratorieabnormiteterne er løst. Ethionamid og ledsagende antituberkulosemedicin(er) bør derefter genindføres sekventielt for at bestemme, hvilket lægemiddel (eller hvilke lægemidler) der er ansvarlige for hepatotoksiciteten.
Blodsukkerbestemmelser bør foretages før og periodisk under behandlingen med Trecator. Diabetikere bør være særligt opmærksomme på episoder med hypoglykæmi.
Periodisk monitorering af thyreoideafunktionstest anbefales, da hypothyroidisme, med eller uden struma, er blevet rapporteret ved ethionamidbehandling.
Karcinogenese, mutagenese, svækkelse af fertilitet
Teratogene virkninger
Dyreforsøg udført med Trecator indikerer, at lægemidlet har teratogent potentiale hos kaniner og rotter. De doser, der blev anvendt i disse undersøgelser på mg/kg-basis, var betydeligt højere end dem, der blev anbefalet til mennesker. Der er ingen tilstrækkelige og velkontrollerede undersøgelser af gravide kvinder. På grund af disse dyreforsøg skal det dog anbefales, at Trecator udelukkes fra kvinder, der er gravide, eller som sandsynligvis vil blive gravide under behandling, medmindre den ordinerende læge anser det for at være en væsentlig del af behandlingen.
Arbejde og levering
Effekten af Trecator på fødsel og fødsel hos gravide kvinder er ukendt.
Ammende mødre
Da der ikke er tilgængelig information om udskillelse af ethionamid i modermælk, bør Trecator kun administreres til ammende mødre, hvis fordelene opvejer risiciene. Nyfødte, der ammes af mødre, der tager Trecator, bør overvåges for bivirkninger.
Pædiatrisk brug
På grund af det faktum, at lungetuberkulose, der er resistent over for primær terapi, sjældent findes hos nyfødte, spædbørn og børn, har undersøgelser været begrænsede i disse aldersgrupper. På nuværende tidspunkt bør lægemidlet ikke anvendes til pædiatriske patienter under 12 år, undtagen når organismerne er definitivt resistente over for primær terapi og systemisk spredning af sygdommen eller andre livstruende komplikationer af tuberkulose vurderes at være nært forestående.
OVERDOSIS
Der er ingen specifik information tilgængelig om behandling af overdosering med Trecator. Hvis det skulle opstå, skal der anvendes standardprocedurer til at evakuere maveindholdet og til at understøtte vitale funktioner.
KONTRAINDIKATIONER
Ethionamid er kontraindiceret hos patienter med svært nedsat leverfunktion og hos patienter, der er overfølsomme over for lægemidlet.
KLINISK FARMAKOLOGI
Absorption
Ethionamid absorberes i det væsentlige fuldstændigt efter oral administration og udsættes ikke for nogen nævneværdig first pass-metabolisme. Ethionamidtabletter kan indgives uden hensyntagen til tidspunktet for måltider.
De farmakokinetiske parametre for ethionamid efter en enkelt oral dosisadministration af 250 mg Trecator filmovertrukne tabletter under fastende forhold til 40 raske voksne frivillige er angivet i tabel 1.
Trecator-tabletter er blevet omformuleret fra en sukkerovertrukket tablet til en filmovertrukket tablet. Cmax for de filmovertrukne tabletter (2,16 μg/ml) var signifikant højere end for sukkerovertrukne tabletter (1,48 μg/mL) (se DOSERING OG ADMINISTRATION ).
Fordeling
Ethionamid distribueres hurtigt og bredt i kropsvæv og væsker efter administration af en sukkerovertrukket tablet, med koncentrationer i plasma og forskellige organer, der er omtrent lige store. Signifikante koncentrationer er også til stede i cerebrospinalvæsken efter administration af en sukkerovertrukket tablet. Fordeling af ethionamid i det samme kropsvæv og -væsker, inklusive cerebrospinalvæske efter administration af den filmovertrukne tablet, er ikke blevet undersøgt, men forventes ikke at adskille sig væsentligt fra den sukkerovertrukne tablet. Lægemidlet er cirka 30 % bundet til proteiner. Det gennemsnitlige (SD) tilsyneladende orale distributionsvolumen observeret hos 40 raske frivillige efter en 250 mg oral dosis af filmovertrukne tabletter var 93,5 (19,2) L.
Metabolisme
Ethionamid metaboliseres i vid udstrækning til aktive og inaktive metabolitter. Metabolisme formodes at forekomme i leveren, og indtil videre er 6 metabolitter blevet isoleret: 2-ethylisonicotinamid, carbonyl-dihydropyridin, thiocarbonyl-dihydropyridin, S-oxocarbamoyl dihydropyridin, 2-ethylthioiso-nicotinamid og ethionamid sulfoxid. Sulphoxidmetabolitten har vist sig at have antimikrobiel aktivitet mod Mycobacterium tuberculosis.
Elimination
Den gennemsnitlige (SD) halveringstid observeret hos 40 raske frivillige efter en 250 mg oral dosis filmovertrukne tabletter var 1,92 (0,27) timer. Mindre end 1 % af den orale dosis udskilles som ethionamid i urinen.
Handlingsmekanisme
Ethionamid kan virke bakteriostatisk eller bakteriedræbende, afhængigt af koncentrationen af lægemidlet opnået på infektionsstedet og den inficerende organismes modtagelighed. Den nøjagtige virkningsmekanisme af ethionamid er ikke blevet fuldstændig belyst, men lægemidlet ser ud til at hæmme peptidsyntese i modtagelige organismer.
Mikrobiologi
In vitro aktivitet
Ethionamid udviser bakteriostatisk aktivitet mod ekstracellulære og intracellulære Mycobacterium tuberculosis-organismer. Udviklingen af ethionamid-resistente M. tuberculosis-isolater kan opnås ved gentagen subkultur i flydende eller på faste medier indeholdende stigende koncentrationer af ethionamid. Multi-drug-resistente stammer af M. tuberculosis kan have erhvervet resistens over for både isoniazid og ethionamid. Imidlertid er størstedelen af M. tuberculosisisolater, der er resistente over for den ene, sædvanligvis modtagelige for den anden. Der er ingen tegn på krydsresistens mellem ethionamid og para-aminosalicylsyre (PAS), streptomycin eller cycloserin. Begrænsede data tyder dog på, at der kan eksistere krydsresistens mellem ethionamid og thiosemicarbazoner (dvs. thiacetazon) samt isoniazid.
In vivo aktivitet
Ethionamid administreret oralt reducerede oprindeligt antallet af dyrkbare Mycobacterium tuberculosis-organismer fra lungerne af H37Rv-inficerede mus. Lægemiddelresistens udviklede sig ved fortsat ethionamid monoterapi, men forekom ikke, når mus fik ethionamid i kombination med streptomycin eller isoniazid.
Modtagelighedstest
For specifik information om fortolkningskriterier for følsomhedstest og tilhørende testmetoder og kvalitetskontrolstandarder, der er anerkendt af FDA for dette lægemiddel, se venligst: https://www.fda.gov/STIC.
PATIENTOPLYSNINGER
Patienter bør rådes til at konsultere deres læge, hvis der opstår sløret syn eller tab af syn, med eller uden øjensmerter, under behandlingen.
Overdreven indtagelse af ethanol bør undgås, fordi en psykotisk reaktion er blevet rapporteret.
Patienter bør rådgives om, at antibakterielle lægemidler inklusive Trecator kun bør anvendes til behandling af bakterielle infektioner. De behandler ikke virusinfektioner (f.eks. forkølelse). Når Trecator ordineres til behandling af en bakteriel infektion, skal patienterne fortælles, at selvom det er almindeligt at føle sig bedre tidligt i behandlingsforløbet, skal medicinen tages nøjagtigt som anvist. At springe doser over eller ikke fuldføre hele behandlingsforløbet kan (1) mindske effektiviteten af den øjeblikkelige behandling og (2) øge sandsynligheden for, at bakterier udvikler resistens og ikke vil kunne behandles med Trecator eller andre antibakterielle lægemidler i fremtiden.
