Duricef 250mg, 500mg Cefadroxil Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Duricef, og hvordan bruges det?
Duricef (cefadroxil) er et cephalosporin-antibiotikum, der bruges til at behandle mange forskellige typer infektioner forårsaget af bakterier. Varemærket Duricef er udgået, og cefadroxil er tilgængelig i generisk form.
Hvad er bivirkninger af Duricef?
Almindelige bivirkninger af Duricef (cefadroxil) omfatter:
- mavebesvær eller smerter,
- kvalme,
- opkastning,
- diarré,
- stive eller stramme muskler,
- ledsmerter,
- følelse rastløs eller hyperaktiv,
- usædvanlig eller ubehagelig smag i munden,
- kløe eller hududslæt, eller
- vaginal kløe eller udflåd.
Fortæl det til din læge, hvis du har usandsynlige, men meget alvorlige bivirkninger af Duricef (cefadroxil), herunder:
- vedvarende kvalme eller opkastning,
- gulne øjne eller hud,
- mørk urin,
- nye tegn på infektion (f.eks. vedvarende ondt i halsen eller feber),
- let blå mærker eller blødning,
- ændringer i mængden af urin, eller
- mentale/humørændringer (såsom forvirring).
BESKRIVELSE
DURICEF (cefadroxil) er et semisyntetisk cephalosporin-antibiotikum beregnet til oral administration. Det er et hvidt til gulligt-hvidt krystallinsk pulver. Det er opløseligt i vand og er syrestabilt. Det er kemisk betegnet som 5-Thia-l-azabicyclo[4.2.0]oct-2-en-2-carboxylsyre, 7-[[amino(4-hydroxyphenyl)acetyl]amino]-3-methyl-8-oxo -, monohydrat[6R-[6a,7β(R*)]]-. Det har formlen C16H17N3O5S•H20 og molekylvægten på 381,40. Den har følgende strukturformel:
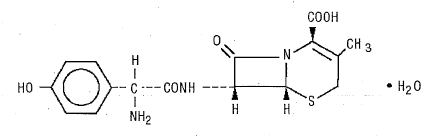
DURICEF (cefadroxil) filmovertrukne tabletter, 1 g, indeholder følgende inaktive ingredienser: mikrokrystallinsk cellulose, hydroxypropylmethylcellulose, magnesiumstearat, polyethylenglycol, polysorbat 80, simeticonemulsion og titaniumdioxid.
DURICEF (cefadroxil) til oral suspension indeholder følgende inaktive ingredienser: FD&C Yellow No. 6, smagsstoffer (naturlige og kunstige), polysorbat 80, natriumbenzoat, saccharose og xanthangummi.
DURICEF (cefadroxil) kapsler indeholder følgende inaktive ingredienser: D&C Red No. 28, FD&C Blue No. 1, FD&C Red No. 40, gelatine, magnesiumstearat og titaniumdioxid.
INDIKATIONER
DURICEF (cefadroxil) er indiceret til behandling af patienter med infektion forårsaget af modtagelige stammer af de udpegede organismer i følgende sygdomme:
Urinvejsinfektioner forårsaget af E. coli; P. mirabilis og Klebsiella arter.
Hud- og hudstrukturinfektioner forårsaget af stafylokokker og/eller streptokokker.
Pharyngitis og/eller tonsillitis forårsaget af Streptococcus pyogenes (gruppe A beta-hæmolytiske streptokokker).
Bemærk: Kun penicillin ad intramuskulær indgivelsesvej har vist sig at være effektiv til profylakse af gigtfeber. DURICEF (cefadroxil) er generelt effektiv til udryddelse af streptokokker fra oropharynx. Data, der fastslår effektiviteten af DURICEF (cefadroxil) til profylakse af efterfølgende gigtfeber, er dog ikke tilgængelige.
Bemærk: Dyrknings- og modtagelighedstest bør påbegyndes før og under behandlingen. Nyrefunktionsundersøgelser bør udføres, når det er indiceret.
For at reducere udviklingen af lægemiddelresistente bakterier og bevare effektiviteten af DURICEF (cefadroxil) og andre antibakterielle lægemidler, bør DURICEF (cefadroxil) kun bruges til at behandle eller forebygge infektioner, der er bevist eller stærkt mistænkt for at være forårsaget af modtagelige bakterier. Når kultur- og modtagelighedsoplysninger er tilgængelige, bør de overvejes ved udvælgelse eller ændring af antibakteriel behandling. I mangel af sådanne data kan lokal epidemiologi og modtagelighedsmønstre bidrage til den empiriske udvælgelse af terapi.
DOSERING OG ADMINISTRATION
DURICEF (cefadroxil) er syrestabilt og kan indgives oralt uden hensyntagen til måltider. Administration sammen med mad kan være nyttig til at mindske potentielle gastrointestinale lidelser, der lejlighedsvis er forbundet med oral cephalosporinbehandling.
Voksne
Urinvejsinfektioner: For ukomplicerede nedre urinvejsinfektioner (dvs. blærebetændelse) er den sædvanlige dosis 1 eller 2 g dagligt i en enkelt (qd) eller opdelte doser (bid).
For alle andre urinvejsinfektioner er den sædvanlige dosis 2 g pr. dag i opdelte doser (bid).
Hud- og hudstrukturinfektioner: For hud- og hudstrukturinfektioner er den sædvanlige dosis 1 g pr. dag i enkelt (qd) eller opdelte doser (bid).
Pharyngitis og tonsillitis: Behandling af gruppe A beta-hæmolytisk streptokok pharyngitis og tonsillitis-1 g daglig i enkelt (qd) eller opdelte doser (bid) i 10 dage.
Børn
Ved urinvejsinfektioner er den anbefalede daglige dosis til børn 30 mg/kg/dag i opdelte doser hver 12. time. For pharyngitis, tonsillitis og impetigo er den anbefalede daglige dosis til børn 30 mg/kg/dag i en enkelt dosis eller i ligeligt opdelte doser hver 12. time. For andre hud- og hudstrukturinfektioner er den anbefalede daglige dosis 30 mg/kg/dag i ligeligt opdelte doser hver 12. time. Ved behandling af beta-hæmolytiske streptokokinfektioner bør en terapeutisk dosis af DURICEF (cefadroxil) administreres i mindst 10 dage.
Se skemaet for den samlede daglige dosis til børn.
Nedsat nyrefunktion
Hos patienter med nedsat nyrefunktion bør dosis af cefadroxilmonohydrat justeres i overensstemmelse med kreatininclearance-hastigheder for at forhindre lægemiddelakkumulering. Følgende tidsplan foreslås. Hos voksne er startdosis 1000 mg DURICEF (cefadroxil), og vedligeholdelsesdosis (baseret på kreatininclearance rate [ml/min/1,73 M2]) er 500 mg med de tidsintervaller, der er angivet nedenfor.
Patienter med kreatininclearance-hastigheder over 50 ml/min kan behandles, som om de var patienter med normal nyrefunktion.
HVORDAN LEVERET
DURICEF® (cefadroxil monohydrat, USP) 500 mg kapsler: uigennemsigtige, rødbrune og hvide hårde gelatinekapsler, præget med "PPP" og "784" i den ene ende og med "DURICEF (cefadroxil) " og "500 mg" i den anden ende .
Kapslerne leveres som følger:
N 0430-0780-19...................flaske med 50 stk
Opbevares ved kontrolleret stuetemperatur 15° - 30° C (59° - 86° F).
DURICEF® (cefadroxil) 1 gram tabletter: hvide til råhvide, overskåret i top, oval, præget med "PPP" på den ene side af halveringsstykket og "785" på den anden side af halveringsstykket. Tabletterne leveres som følger:
N 0430-0781-19....................... Flaske med 50 stk
Opbevares ved kontrolleret stuetemperatur 15° - 30° C (59° - 86° F).
DURICEF® (cefadroxil) til oral suspension er appelsin-ananas-smag og leveres som følger:
250mg/5mL................................N 0430-2782-15 50 mL flaske
Før rekonstitution: Opbevares ved kontrolleret stuetemperatur 15° - 30° C (59° - 86° F).
Fremstillet af Bristol-Myers Squibb Co. Princeton, NJ 08543. For Warner Chilcott Company, Inc. Fajardo, PR 00738. Markedsført af Warner Chilcott (US), Inc. Rockaway, NJ 07866. Revideret april 2007. FDA rev.dato: 6/ 5/2007
BIVIRKNINGER
Gastrointestinale
Debut af pseudomembranøs colitis-symptomer kan forekomme under eller efter antibiotikabehandling (se ADVARSLER ). Dyspepsi, kvalme og opkastning er sjældent blevet rapporteret. Diarré er også forekommet.
Overfølsomhed
Allergier (i form af udslæt, nældefeber, angioødem og pruritus) er blevet observeret. Disse reaktioner forsvandt normalt ved seponering af lægemidlet. Anafylaksi er også blevet rapporteret.
Andet
Andre reaktioner har inkluderet leverdysfunktion, herunder kolestase og forhøjede serumtransaminase, genital pruritus, genital moniliasis, vaginitis, moderat forbigående neutropeni, feber. Agranulocytose, trombocytopeni, idiosynkratisk leversvigt, erythema multiforme, Stevens-Johnsons syndrom, serumsyge og artralgi er sjældent rapporteret.
Ud over de ovennævnte bivirkninger, som er blevet observeret hos patienter behandlet med cefadroxil, er følgende bivirkninger og ændrede laboratorietests blevet rapporteret for antibiotika af cephalosporinklassen:
Toksisk epidermal nekrolyse, mavesmerter, superinfektion, nyreinsufficiens, toksisk nefropati, aplastisk anæmi, hæmolytisk anæmi, blødning, forlænget protrombintid, positiv Coombs' test, øget BUN, øget kreatinin, forhøjet alkalisk fosfatase (AST), forhøjet aminofosfatase, forhøjet alaninaminotransferase (ALT), forhøjet bilirubin, forhøjet LDH, eosinofili, pancytopeni, neutropeni.
Adskillige cephalosporiner har været impliceret i at udløse anfald, især hos patienter med nedsat nyrefunktion, når dosis ikke blev reduceret (se DOSERING OG ADMINISTRATION og OVERDOSERING ). Hvis der opstår anfald i forbindelse med lægemiddelbehandling, skal lægemidlet seponeres. Antikonvulsiv behandling kan gives, hvis det er klinisk indiceret.
DRUGSINTERAKTIONER
Interaktioner med lægemiddel/laboratorietest
Positive direkte Coombs' test er blevet rapporteret under behandling med cephalosporin-antibiotika. I hæmatologiske undersøgelser eller i transfusions-krydsmatchende procedurer, når antiglobulintest udføres på den mindre side eller i Coombs' test af nyfødte, hvis mødre har fået cephalosporin-antibiotika før fødslen, skal det erkendes, at en positiv Coombs' test kan skyldes medicin.
ADVARSLER
FØR BEHANDLING MED DURICEF (cefadroxil) INDLEDES, SKAL DER UNDERSØGES FOR AT BESTEMME, OM PATIENTEN HAR HAVET TIDLIGERE OVERfølsomhedsreaktioner på CEFADROXTL, CEFALOSPORINER, PENICILLINER. HVIS DETTE PRODUKT SKAL GIVES TIL PENICILLIN-SENSITIVE PATIENTER, SKAL VÆRE FORSIGTIG, FORDI KRYDS-SENSITIVITET BLANDT BETA-LACTAM ANTIBIOTIKA ER VÆRET KLART DOKUMENTET OG KAN FOREKOMME I OP TIL 10% PÅ 10 %.
HVIS EN ALLERGISK REAKTION PÅ DURICEF (cefadroxil) OPtræder, SKAL DU AFBINDE MED MEDICINEN. ALVORLIGE AKUTTE OVERfølsomhedsreaktioner KAN KRÆVE BEHANDLING MED EPINEFRIN OG ANDRE NØDFORANSTALTNINGER, HERUNDER ILT, INTRAVENØSE VÆSKER, INTRAVENØSE ANTIHISTAMINER, CORTICOSTEROIDER, PRESSOR-AMINATE, PRESSOR AMINAT.
Clostridium difficile associeret diarré (CDAD) er blevet rapporteret ved brug af næsten alle antibakterielle midler, inklusive DURICEF (cefadroxil), og kan variere i sværhedsgrad fra mild diarré til fatal colitis. Behandling med antibakterielle midler ændrer den normale flora i tyktarmen, hvilket fører til overvækst af C. difficile.
C. difficile producerer toksinerne A og B, som bidrager til udviklingen af CD AD. Hypertoksinproducerende stammer af C. difficile forårsager øget morbiditet og dødelighed, da disse infektioner kan være modstandsdygtige over for antimikrobiel behandling og kan kræve kolektomi. CD AD skal overvejes hos alle patienter, som får diarré efter brug af antibiotika. Omhyggelig sygehistorie er nødvendig, da CD AD er blevet rapporteret at forekomme over to måneder efter administration af antibakterielle midler.
Hvis der er mistanke om eller bekræftet CD AD, kan det være nødvendigt at afbryde igangværende antibiotikabrug, der ikke er rettet mod C. difficile. Passende væske- og elektrolytbehandling, proteintilskud, antibiotikabehandling af C. difficile og kirurgisk evaluering bør iværksættes som klinisk indiceret.
FORHOLDSREGLER
Generel
DURICEF (cefadroxil) bør anvendes med forsigtighed ved markant nedsat nyrefunktion (kreatinin-clearance-hastighed på mindre end 50 ml/min/1,73 M2). (Se DOSERING OG ADMINISTRATION .) Hos patienter med kendt eller mistænkt nyreinsufficiens bør der foretages omhyggelig klinisk observation og passende laboratorieundersøgelser før og under behandlingen.
Udskrivning af DURICEF (cefadroxil) i fravær af en påvist eller stærkt mistænkt bakteriel infektion eller en profylaktisk indikation vil sandsynligvis ikke give patienten fordel og øger risikoen for udvikling af lægemiddelresistente bakterier.
Langvarig brug af DURICEF (cefadroxil) kan resultere i overvækst af følsomme organismer. Omhyggelig observation af patienten er afgørende. Hvis der opstår superinfektion under behandlingen, skal der træffes passende foranstaltninger.
DURICEF (cefadroxil) bør ordineres med forsigtighed til personer med anamnese med gastrointestinale sygdomme, især colitis.
Karcinogenese, mutagenese og svækkelse af fertilitet
Der er ikke udført langtidsundersøgelser for at bestemme kræftfremkaldende potentiale. Der er ikke udført genetiske toksicitetstests.
Graviditet: Graviditetskategori B
Reproduktionsundersøgelser er blevet udført på mus og rotter i doser op til 11 gange den humane dosis og har ikke afsløret tegn på nedsat fertilitet eller skade på fosteret på grund af cefadroxilmonohydrat. Der er dog ingen tilstrækkelige og velkontrollerede undersøgelser af gravide kvinder. Da reproduktionsstudier på dyr ikke altid forudsiger human respons, bør dette lægemiddel kun anvendes under graviditet, hvis det er klart nødvendigt.
Arbejde og levering
DURICEF (cefadroxil) er ikke blevet undersøgt til brug under veer og fødsel. Behandling bør kun gives, hvis det er klart nødvendigt.
Ammende mødre
Der skal udvises forsigtighed, når cefadroxilmonohydrat administreres til en ammende mor.
Pædiatrisk brug
(Se DOSERING OG ADMINISTRATION. )
Geriatrisk brug
Ud af cirka 650 patienter, der fik cefadroxil til behandling af urinvejsinfektioner i tre kliniske forsøg, var 28 % 60 år og ældre, mens 16 % var 70 år og ældre. Ud af cirka 1.000 patienter, der fik cefadroxil til behandling af hud- og hudstrukturinfektioner i 14 kliniske forsøg, var 12 % 60 år og ældre, mens 4 % var 70 år og derover. Der blev ikke observeret nogen overordnede forskelle i sikkerhed mellem de ældre patienter i disse undersøgelser og yngre patienter. Kliniske undersøgelser af cefadroxil til. behandling af pharyngitis eller tonsillitis omfattede ikke et tilstrækkeligt antal patienter på 65 år og ældre til at afgøre, om de reagerer anderledes end yngre patienter. Andre rapporterede kliniske erfaringer med cefadroxil har ikke identificeret forskelle i respons mellem ældre og yngre patienter, men større følsomhed hos nogle ældre individer kan ikke udelukkes.
Cefadroxil udskilles i det væsentlige via nyrerne, og dosisjustering er indiceret til patienter med nedsat nyrefunktion (se DOSERING OG ADMINISTRATION: Nedsat nyrefunktion ). Da ældre patienter er mere tilbøjelige til at have nedsat nyrefunktion, bør der udvises forsigtighed ved dosisvalg, og det kan være nyttigt at overvåge nyrefunktionen.
OVERDOSIS
En undersøgelse af børn under seks år antydede, at indtagelse af mindre end 250 mg/kg cephalosporiner ikke er forbundet med signifikante resultater. Der kræves ingen handling udover generel støtte og observation. For mængder større end 250 mg/kg, inducer mavetømning.
Hos fem anuriske patienter blev det påvist, at gennemsnitligt 63 % af en 1 g oral dosis ekstraheres fra kroppen under en 6-8 timers hæmodialysesession.
KONTRAINDIKATIONER
DURICEF (cefadroxil) er kontraindiceret til patienter med kendt allergi over for cephalosporingruppen af antibiotika.
KLINISK FARMAKOLOGI
DURICEF (cefadroxil) absorberes hurtigt efter oral administration. Efter enkeltdoser på 500 mg og 1000 mg var de gennemsnitlige maksimale serumkoncentrationer henholdsvis ca. 16 og 28 |ag/ml. Målbare niveauer var til stede 12 timer efter administration. Over 90 % af lægemidlet udskilles uændret i urinen inden for 24 timer. Maksimal urinkoncentration er ca. 1800 pg/ml i perioden efter en enkelt 500 mg oral dosis. Forøgelser i dosis giver generelt en proportional stigning i DURICEF (cefadroxil monohydrat, USP) urinkoncentration. Antibiotikumkoncentrationen i urinen efter en dosis på 1 g blev holdt et godt stykke over MIC for modtagelige urinpatogener i 20 til 22 timer.
Mikrobiologi
In vitro-tests viser, at cephalosporinerne er bakteriedræbende på grund af deres hæmning af cellevægssyntese. Cefadroxil har vist sig at være aktiv mod følgende organismer både in vitro og ved kliniske infektioner (se INDIKATIONER ):
Beta-hæmolytiske streptokokker Stafylokokker, herunder penicillinase-producerende stammer Streptococcus (Diplococcus) pneumoniae Escherichia coli Proteus mirabilis Klebsiella arter Moraxella (Branhamella) catarrhalis
Bemærk: De fleste stammer af Entervcoccus faecalis (tidligere Streptococcus faecalis) og Enterococcus faecium (tidligere Streptococcus faecium) er resistente over for DURICEF (cefadroxil). Det er ikke aktivt mod de fleste stammer af Enterobacter-arter, Morganella morganii (tidligere Proteus morganii) og P. vulgaris. Det har ingen aktivitet mod Pseudomonas-arter og Acinetobacter calcoaceticus (tidligere Mima- og Herellea-arter).
Modtagelighedstest: Diffusionsteknikker
Brugen af antibiotiske diskfølsomhedstestmetoder, som måler zonediameter, giver et nøjagtigt estimat af antibiotikafølsomhed. En sådan standardprocedure1, som er blevet anbefalet til brug med diske til at teste organismers modtagelighed for cefadroxil, bruger cephalosporin-klassen (cephalothin) disken. Fortolkning involverer korrelationen af diametrene opnået i disktesten med den minimale hæmmende koncentration (MIC) for cefadroxil.
Rapporter fra laboratoriet, der giver resultater af standard single-disk følsomhedstesten med en 30 µg cephalothin disk skal fortolkes i henhold til følgende kriterier:
En rapport om "følsom" indikerer, at patogenet sandsynligvis vil blive hæmmet af generelt opnåelige blodniveauer. En rapport om "mellem følsomhed" antyder, at organismen ville være modtagelig, hvis høje doser anvendes, eller hvis infektionen er begrænset til væv og væsker (f.eks. urin), hvori høje antibiotikaniveauer opnås. En rapport om "Resistent" indikerer, at opnåelige koncentrationer af antibiotika er usandsynligt at være 'hæmmende, og anden terapi bør vælges.
Standardiserede procedurer kræver brug af laboratoriekontrolorganismer. 30 µg cephalothin-skiven skal give følgende zonediametre:
Fortyndingsteknikker
Ved brug af NCCLS agarfortynding eller bouillonfortynding (inklusive mikrofortynding) metode2 eller tilsvarende, kan et bakterieisolat anses for modtageligt, hvis MIC-værdien (minimum inhibitorisk koncentration) for cephalothin er 8 µg/ml eller mindre. Organismer anses for at være resistente, hvis MIC er 32 µg/mL eller mere. Organismer med en MIC-værdi på mindre end 32 µg/mL, men større end 8 µg/mL, er mellemliggende.
Som med standarddiffusionsmetoder kræver fortyndingsprocedurer brug af laboratoriekontrolorganismer. Standard cephalothinpulver skal give MIC-værdier i intervallet 0,12 µg/mL og 0,5 µg/ml for Staphylococcus aureus ATCC 29213. Vox Escherichia coli ATCC 25922, MIC-intervallet skal være mellem 4,0 µg/mL og µ1,0 µg/mL. For Streptococcus faecalis ATCC 29212 bør MIC-området være mellem 8,0 og 32,0 µg/ml.
REFERENCER
1. National Committee for Clinical Laboratory Standards, Approved Standard, Performance Standards for Antimicrobial Disk Suceptibility Test, 4th Edition, Vol. 10 (7): M2-A4, Villanova, PA, april, 1990.
2. National Committee for Clinical Laboratory Standards, Approved Standard: Methods for Dilution Antimicrobial Susceptibility Tests for Bacteria that Grow Aerobically, 2nd Edition, Vol. 10 (8): M7-A2, Villanova, PA, april, 1990.
PATIENTOPLYSNINGER
Patienter bør rådgives om, at antibakterielle lægemidler inklusive DURICEF (cefadroxil) kun bør anvendes til behandling af bakterielle infektioner. De behandler ikke virusinfektioner (f.eks. forkølelse). Når DURICEF (cefadroxil) ordineres til behandling af en bakteriel infektion, skal patienterne fortælles, at selvom det er almindeligt at føle sig bedre tidligt i behandlingsforløbet, skal medicinen tages nøjagtigt som anvist. At springe doser over eller ikke fuldføre hele behandlingsforløbet kan (1) mindske effektiviteten af den øjeblikkelige behandling og (2) øge sandsynligheden for, at bakterier udvikler resistens og ikke vil kunne behandles med DURICEF (cefadroxil) eller andre antibakterielle lægemidler i fremtiden .
Diarré er et almindeligt problem forårsaget af antibiotika, som normalt ophører, når antibiotikaen seponeres. Nogle gange kan patienter efter start af behandling med antibiotika udvikle vandig og blodig afføring (med eller uden mavekramper og feber) selv så sent som to eller flere måneder efter at have taget den sidste dosis af antibiotika. Hvis dette sker, skal patienter kontakte deres læge hurtigst muligt.
