Amoxil 250mg, 500mg, 625mg, 1000mg Amoxicillin Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Amoxicillin, og hvordan bruges det?
Hvad er Amoxil 1000mg?
Amoxil er en receptpligtig medicin, der bruges til at behandle symptomerne på mange forskellige typer af bakterielle infektioner såsom tonsillitis, bronkitis, lungebetændelse og infektioner i øre, næse, hals, hud eller urinveje. Amoxil 1000mg kan bruges alene eller sammen med anden medicin.
Amoxil tilhører en klasse af lægemidler kaldet Penicilliner, Amino.
Hvad er de mulige bivirkninger af Amoxil?
Amoxil kan forårsage alvorlige bivirkninger, herunder:
- nældefeber,
- åndedrætsbesvær,
- hævelse af dit ansigt, læber, tunge eller hals,
- feber,
- ondt i halsen,
- brændende øjne,
- hudsmerter,
- rødt eller lilla hududslæt med blærer og afskalning,
- stærke mavesmerter, og
- diarré, der er vandig eller blodig (selvom den opstår måneder efter din sidste dosis)
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Amoxil omfatter:
- kvalme,
- opkastning,
- diarré, og
- udslæt
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Amoxil. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Formuleringer af AMOXIL indeholder amoxicillin, et semisyntetisk antibiotikum, en analog af ampicillin, med et bredt spektrum af bakteriedræbende aktivitet mod mange Gram-positive og Gram-negative mikroorganismer. Kemisk er det (2S,5,R,6,R)-6-[(,R)-(-)-2-amino-2-(p-hydroxyphenyl)acetamido]-3,3-dimethyl-7- oxo-4-thia-1-azabicyclo[3.2.0]heptan-2-carboxylsyretrihydrat. Det kan være repræsenteret strukturelt som:
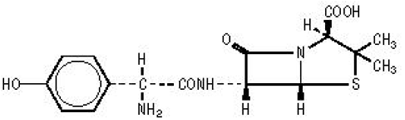
Amoxicillin-molekylformlen er C16H19N3O5S•3H2O, og molekylvægten er 419,45.
Kapsler : Hver kapsel af AMOXIL, med kongeblå uigennemsigtig hætte og lyserød uigennemsigtig krop, indeholder 250 mg eller 500 mg amoxicillin som trihydrat. Hætten og hoveddelen af 250 mg-kapslen er præget med produktnavnet AMOXIL 1000mg og 250; hætten og kroppen på 500 mg-kapslen er præget med AMOXIL 1000mg og 500. Inaktive ingredienser: D&C Red No. 28, FD&C Blue No. 1, FD&C Red No. 40, gelatine, magnesiumstearat og titaniumdioxid.
Hver tablet indeholder 500 mg eller 875 mg amoxicillin som trihydrat. Hver filmovertrukket, kapselformet, pink tablet er præget med AMOXIL 500 mg centreret over henholdsvis 500 eller 875. Tabletten på 875 mg har delekærv på bagsiden. Inaktive ingredienser: Kolloid siliciumdioxid, crospovidon, FD&C Red No. 30 aluminium lake, hypromellose, magnesiumstearat, mikrokrystallinsk cellulose, polyethylenglycol, natriumstivelsesglycolat og titaniumdioxid.
Pulver til oral suspension Hver 5 ml rekonstitueret suspension indeholder 125 mg, 200 mg, 250 mg eller 400 mg amoxicillin som trihydrat. Hver 5 ml af den 125 mg rekonstituerede suspension indeholder 0,11 mEq (2,51 mg) natrium. Hver 5 ml af den 200 mg rekonstituerede suspension indeholder 0,15 mEq (3,39 mg) natrium. Hver 5 ml af den 250 mg rekonstituerede suspension indeholder 0,15 mEq (3,36 mg) natrium; hver 5 ml af den 400 mg rekonstituerede suspension indeholder 0,19 mEq (4,33 mg) natrium. Inaktive ingredienser: FD&C Red No. 3, smagsstoffer, silicagel, natriumbenzoat, natriumcitrat, saccharose og xanthangummi.
INDIKATIONER
Infektioner i øre, næse og hals
AMOXIL® er indiceret til behandling af infektioner på grund af modtagelige (KUN β-lactamase-negative) isolater af Streptococcus arter. (kun a- og β-hæmolytiske isolater), Streptococcus pneumoniae, Staphylococcus spp. eller Haemophilus influenzae.
Infektioner i genitourinary tract
AMOXIL® er indiceret til behandling af infektioner på grund af modtagelige (KUN β-lactamase-negative) isolater af Escherichia coli, Proteus mirabilis eller Enterococcus faecalis.
Infektioner af hud og hudstruktur
AMOXIL® er indiceret til behandling af infektioner på grund af modtagelige (KUN β-lactamase-negative) isolater af Streptococcus spp. (kun a- og β-hæmolytiske isolater), Staphylococcus spp. eller E. coli.
Infektioner i de nedre luftveje
AMOXIL® er indiceret til behandling af infektioner på grund af modtagelige (KUN β-lactamase-negative) isolater af Streptococcus spp. (kun a- og β-hæmolytiske isolater), S. pneumoniae, Staphylococcus spp. eller H. influenzae.
Helicobacter pylori infektion
Triple Therapy for Helicobacter Pylori med Clarithromycin og Lansoprazol
AMOXIL, i kombination med clarithromycin plus lansoprazol som tredobbelt behandling, er indiceret til behandling af patienter med H. pylori-infektion og duodenalsårsygdom (aktiv eller 1-årig historie med duodenalsår) for at udrydde H. pylori. Udryddelse af H. pylori har vist sig at reducere risikoen for tilbagefald af duodenalsår.
Dobbeltterapi for H. Pylori med Lansoprazol
AMOXIL, i kombination med lansoprazol-kapsler med forsinket frigivelse som dobbeltterapi, er indiceret til behandling af patienter med H. pylori-infektion og duodenalsårsygdom (aktiv eller 1-årig historie med duodenalsår) som enten er allergiske eller intolerante over for clarithromycin, eller hvor resistens over for clarithromycin er kendt eller mistænkt. (Se indlægssedlen for clarithromycin , Mikrobiologi .) Udryddelse af H. pylori har vist sig at reducere risikoen for tilbagefald af duodenalsår.
Brug
For at reducere udviklingen af lægemiddelresistente bakterier og bevare effektiviteten af AMOXIL (amoxicillin) og andre antibakterielle lægemidler, bør AMOXIL 250mg kun bruges til at behandle infektioner, der er bevist eller stærkt mistænkt for at være forårsaget af bakterier. Når kultur- og modtagelighedsoplysninger er tilgængelige, bør de overvejes ved udvælgelse eller ændring af antibakteriel behandling. I mangel af sådanne data kan lokal epidemiologi og modtagelighedsmønstre bidrage til den empiriske udvælgelse af terapi.
DOSERING OG ADMINISTRATION
Dosering til voksne og pædiatriske patienter > 3 måneders alderen
Behandlingen bør fortsættes i minimum 48 til 72 timer efter det tidspunkt, hvor patienten bliver asymptomatisk, eller der er opnået tegn på bakteriel udryddelse. Det anbefales, at der er mindst 10 dages behandling for enhver infektion forårsaget af Streptococcus pyogenes for at forhindre forekomsten af akut gigtfeber. I nogle infektioner kan behandling være nødvendig i flere uger. Det kan være nødvendigt at fortsætte klinisk og/eller bakteriologisk opfølgning i flere måneder efter behandlingens ophør.
Dosering til nyfødte og spædbørn i alderen ≤ 12 uger (≤ 3 måneder)
Behandlingen bør fortsættes i minimum 48 til 72 timer efter det tidspunkt, hvor patienten bliver asymptomatisk, eller der er opnået tegn på bakteriel udryddelse. Det anbefales, at der er mindst 10 dages behandling for enhver infektion forårsaget af Streptococcus pyogenes for at forhindre forekomsten af akut gigtfeber. På grund af ufuldstændigt udviklet nyrefunktion, der påvirker eliminationen af amoxicillin i denne aldersgruppe, er den anbefalede øvre dosis af AMOXIL 30 mg/kg/dag fordelt hver 12. time. Der er i øjeblikket ingen doseringsanbefalinger til pædiatriske patienter med nedsat nyrefunktion.
Dosering til H. Pylori-infektion
Tredobbelt terapi
Den anbefalede orale dosis til voksne er 1 gram AMOXIL 1000 mg, 500 mg clarithromycin og 30 mg lansoprazol, alle givet to gange dagligt (hver 12. time) i 14 dage.
Dobbelt terapi
Den anbefalede orale dosis til voksne er 1 gram AMOXIL 625 mg og 30 mg lansoprazol, hver givet tre gange dagligt (hver 8. time) i 14 dage. Se venligst den fulde ordinationsinformation for clarithromycin og lansoprazol.
Dosering ved nedsat nyrefunktion
- Patienter med nedsat nyrefunktion behøver generelt ikke en dosisreduktion, medmindre svækkelsen er alvorlig.
- Svært svækkede patienter med en glomerulær filtrationshastighed på
- Patienter med en glomerulær filtrationshastighed på 10 til 30 ml/min bør modtage 500 mg eller 250 mg hver 12. time, afhængigt af infektionens sværhedsgrad.
- Patienter med en glomerulær filtrationshastighed på mindre end 10 ml/min bør modtage 500 mg eller 250 mg hver 24. time, afhængigt af infektionens sværhedsgrad.
- Hæmodialysepatienter bør modtage 500 mg eller 250 mg hver 24. time, afhængigt af infektionens sværhedsgrad. De skal have en ekstra dosis både under og ved afslutningen af dialysen.
Vejledning til blanding af oral suspension
Tryk på flasken, indtil alt pulver flyder frit. Tilsæt ca. 1/3 af den samlede mængde vand til rekonstitution (se tabel 2) og ryst kraftigt til vådt pulver. Tilsæt resten af vandet og ryst igen kraftigt.
Efter rekonstitution skal den påkrævede mængde suspension placeres direkte på barnets tunge for at synke. Alternative indgivelsesmåder er at tilsætte den nødvendige mængde suspension til formel, mælk, frugtjuice, vand, ingefærøl eller kolde drikke. Disse præparater skal derefter tages med det samme.
BEMÆRK: RYST ORAL SUSPENSION GODT FØR BRUG. Hold flasken tæt lukket. Enhver ubrugt del af den rekonstituerede suspension skal kasseres efter 14 dage. Køling er at foretrække, men ikke påkrævet.
HVORDAN LEVERET
Doseringsformer og styrker
Kapsler
250 mg, 500 mg. Hver kapsel af AMOXIL 625 mg, med kongeblå uigennemsigtig hætte og lyserød uigennemsigtig krop, indeholder 250 mg eller 500 mg amoxicillin som trihydrat. Hætten og hoveddelen af 250 mg kapslen er præget med produktnavnet AMOXIL og 250; hætten og kroppen på 500 mg kapslen er præget med AMOXIL og 500.
Tabletter
500 mg, 875 mg. Hver tablet indeholder 500 mg eller 875 mg amoxicillin som trihydrat. Hver filmovertrukken, kapselformet, pink tablet er præget med AMOXIL centreret over henholdsvis 500 eller 875. Tabletten på 875 mg har delekærv på bagsiden.
Pulver til oral suspension
125 mg/5 mL, 200 mg/5 mL, 250 mg/5 mL, 400 mg/5 mL. Hver 5 ml rekonstitueret suspension med jordbærsmag indeholder 125 mg amoxicillin som trihydrat. Hver 5 ml rekonstitueret suspension med boblegummi-smag indeholder 200 mg, 250 mg eller 400 mg amoxicillin som trihydrat.
Opbevaring og håndtering
Kapsler: Hver kapsel af AMOXIL, med kongeblå uigennemsigtig hætte og lyserød uigennemsigtig krop, indeholder 250 mg eller 500 mg amoxicillin som trihydrat. Hætten og hoveddelen af 250 mg kapslen er præget med produktnavnet AMOXIL og 250; hætten og kroppen på 500 mg kapslen er præget med AMOXIL og 500.
250 mg kapsel
NDC 43598-025-01 Flasker á 100 stk NDC 43598-025-05 Flasker á 500 stk
500 mg kapsel
NDC 43598-005-01 Flasker á 100 stk NDC 43598-005-05 Flasker á 500 stk
Hver tablet indeholder 500 mg eller 875 mg amoxicillin som trihydrat. Hver filmovertrukken, kapselformet, pink tablet er præget med AMOXIL centreret over henholdsvis 500 eller 875. Tabletten på 875 mg har delekærv på bagsiden.
500 mg tablet
NDC 43598-024-01 Flasker á 100 stk NDC 43598-024-05 Flasker á 500 stk
875 mg tablet
NDC 43598-019-01 Flasker á 100 stk NDC 43598-019-14 Flasker á 20 stk
Pulver til oral suspension: Hver 5 ml rekonstitueret suspension med jordbærsmag indeholder 125 mg amoxicillin som trihydrat. Hver 5 ml rekonstitueret suspension med boblegummi-smag indeholder 200 mg, 250 mg eller 400 mg amoxicillin som trihydrat.
125 mg/5 ml
NDC 43598-022-80 80 ml flaske NDC 43598-022-52 100 ml flaske NDC 43598-022-53 150 ml flaske
200 mg/5 ml
NDC 43598-023-50 50 ml flaske NDC 43598-023-51 75 ml flaske NDC 43598-023-52 100 ml flaske
250 mg/5 ml
NDC 43598-009-80 80 ml flaske NDC 43598-009-52 100 ml flaske NDC 43598-009-53 150 ml flaske
400 mg/5 ml
NDC 43598-007-50 50 ml flaske NDC 43598-007-51 75 ml flaske NDC 43598-007-52 100 ml flaske
Opbevares ved eller under 20°C (68°F) -250 mg og 500 mg kapsler og 125 mg og 250 mg ikke-rekonstitueret pulver.
Opbevares ved eller under 25°C (77°F) -500 mg og 875 mg tabletter og 200 mg og 400 mg ikke-rekonstitueret pulver.
Dispenser i en tæt beholder.
Fremstillet. Af: Dr. Reddy's Laboratories Tennessee, LLC. Bristol, TN 37620. Revideret: sep. 2015
BIVIRKNINGER
Følgende diskuteres mere detaljeret i andre afsnit af mærkningen:
- Anafylaktiske reaktioner [se ADVARSLER OG FORHOLDSREGLER ]
- CDAD [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring med kliniske forsøg
Fordi kliniske forsøg udføres under vidt forskellige forhold, kan bivirkningsrater observeret i de kliniske forsøg med et lægemiddel ikke direkte sammenlignes med hastigheder i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de frekvenser, der observeres i praksis.
De mest almindelige bivirkninger (> 1%) observeret i kliniske forsøg med AMOXIL kapsler, tabletter eller oral suspension var diarré, udslæt, opkastning og kvalme.
Tredobbelt terapi : De hyppigst rapporterede bivirkninger for patienter, der fik tripelbehandling (amoxicillin/clarithromycin/lansoprazol) var diarré (7 %), hovedpine (6 %) og smagsforstyrrelser (5 %).
Dobbelt terapi : De hyppigst rapporterede bivirkninger for patienter, der fik dobbeltbehandling med amoxicillin/lansoprazol, var diarré (8%) og hovedpine (7%). For mere information om bivirkninger med clarithromycin eller lansoprazol henvises til afsnittet Bivirkninger i deres indlægssedler.
Postmarketing eller anden erfaring
Ud over bivirkninger rapporteret fra kliniske forsøg, er følgende hændelser blevet identificeret under postmarketing brug af penicilliner. Da de rapporteres frivilligt fra en population af ukendt størrelse, kan der ikke foretages skøn over hyppigheden. Disse hændelser er blevet valgt til inklusion på grund af en kombination af deres alvor, hyppighed af rapportering eller potentielle årsagssammenhænge til AMOXIL.
- Infektioner og angreb : Mukokutan candidiasis.
- Gastrointestinale : Sort behåret tunge og hæmoragisk/pseudomembranøs colitis. Debut af pseudomembranøs colitis symptomer kan forekomme under eller efter antibakteriel behandling [se ADVARSLER OG FORHOLDSREGLER ].
- Overfølsomhedsreaktioner : Anafylaksi [se ADVARSLER OG FORHOLDSREGLER ]. Serumsygelignende reaktioner, erytematøst makulopapulært udslæt, erythema multiforme, Stevens-Johnsons syndrom, eksfoliativ dermatitis, toksisk epidermal nekrolyse, akut generaliseret eksantematøs pustulose, hypersensitiv vaskulitis og nældefeber er blevet rapporteret.
- Lever Der er observeret en moderat stigning i ASAT og/eller ALAT, men betydningen af dette fund er ukendt. Leverdysfunktion inklusive kolestatisk gulsot, hepatisk kolestase og akut cytolytisk hepatitis er blevet rapporteret.
- Renal : Krystalluri er blevet rapporteret [se OVERDOSERING ].
- Hemiske og lymfatiske systemer : Anæmi, herunder hæmolytisk anæmi, trombocytopeni, trombocytopenisk purpura, eosinofili, leukopeni og agranulocytose er blevet rapporteret. Disse reaktioner er normalt reversible ved seponering af behandlingen og menes at være overfølsomhedsfænomener.
- Centralnervesystemet : Reversibel hyperaktivitet, agitation, angst, søvnløshed, forvirring, kramper, adfærdsændringer og/eller svimmelhed er blevet rapporteret
- Diverse : Tandmisfarvning (brun, gul eller grå farvning) er blevet rapporteret. De fleste rapporter forekom hos pædiatriske patienter. Misfarvning blev reduceret eller elimineret med børstning eller tandrensning i de fleste tilfælde.
DRUGSINTERAKTIONER
Probenecid
Probenecid nedsætter den renale tubulære sekretion af amoxicillin. Samtidig brug af amoxicillin og probenecid kan resultere i øgede og forlængede niveauer af amoxicillin i blodet.
Orale antikoagulantia
Unormal forlængelse af protrombintid (øget internationalt normaliseret ratio [INR]) er blevet rapporteret hos patienter, der får amoxicillin og orale antikoagulantia. Passende overvågning bør udføres, når antikoagulantia ordineres samtidigt. Det kan være nødvendigt at justere dosis af orale antikoagulantia for at opretholde det ønskede niveau af antikoagulering.
Allopurinol
Samtidig administration af allopurinol og amoxicillin øger forekomsten af udslæt hos patienter, der får begge lægemidler, sammenlignet med patienter, der får amoxicillin alene. Det vides ikke, om denne forstærkning af amoxicillin-udslæt skyldes allopurinol eller den hyperurikæmi, der er til stede hos disse patienter.
Orale præventionsmidler
AMOXIL kan påvirke tarmfloraen, hvilket fører til lavere østrogenreabsorption og reduceret effektivitet af kombinerede orale østrogen/progesteron-præventionsmidler.

Andre antibakterielle midler
Chloramphenicol, makrolider, sulfonamider og tetracykliner kan interferere med penicillins bakteriedræbende virkning. Dette er blevet påvist in vitro; dog er den kliniske betydning af denne interaktion ikke veldokumenteret.
Effekter på laboratorietests
Høje urinkoncentrationer af ampicillin kan resultere i falsk-positive reaktioner, når der testes for tilstedeværelsen af glukose i urinen med CLINITEST®, Benedict's Solution eller Fehling's Solution. Da denne effekt også kan forekomme med amoxicillin, anbefales det, at der anvendes glukosetest baseret på enzymatiske glucoseoxidasereaktioner (såsom CLINISTIX®).
Efter administration af ampicillin eller amoxicillin til gravide kvinder er der observeret et forbigående fald i plasmakoncentrationen af total konjugeret østriol, østriol-glucuronid, konjugeret østron og østradiol.
ADVARSLER
Inkluderet som en del af FORHOLDSREGLER afsnit.
FORHOLDSREGLER
Anafylaktiske reaktioner
Alvorlige og lejlighedsvis fatale overfølsomhedsreaktioner (anafylaktiske) er blevet rapporteret hos patienter i penicillinbehandling inklusive amoxicillin. Selvom anafylaksi er hyppigere efter parenteral behandling, er det forekommet hos patienter på orale penicilliner. Disse reaktioner er mere tilbøjelige til at forekomme hos personer med en historie med penicillin-overfølsomhed og/eller en historie med følsomhed over for flere allergener. Der har været rapporter om personer med en historie med overfølsomhed over for penicillin, som har oplevet alvorlige reaktioner ved behandling med cephalosporiner. Inden behandling med AMOXIL påbegyndes, bør der foretages omhyggelig undersøgelse vedrørende tidligere overfølsomhedsreaktioner over for penicilliner, cephalosporiner eller andre allergener.
Clostridium Difficile Associeret Diarré
Clostridium difficile-associeret diarré (CDAD) er blevet rapporteret ved brug af næsten alle antibakterielle midler, inklusive AMOXIL, og kan variere i sværhedsgrad fra mild diarré til fatal colitis. Behandling med antibakterielle midler ændrer den normale flora i tyktarmen, hvilket fører til overvækst af C. difficile.
C. difficile producerer toksinerne A og B, som bidrager til udviklingen af CDAD. Hypertoksin-producerende stammer af C. difficile forårsager øget morbiditet og dødelighed, da disse infektioner kan være modstandsdygtige over for antimikrobiel behandling og kan kræve kolektomi. CDAD skal overvejes hos alle patienter, som får diarré efter antibakteriel brug. Omhyggelig sygehistorie er nødvendig, da CDAD er blevet rapporteret at forekomme over 2 måneder efter administration af antibakterielle midler.
Hvis CDAD er mistænkt eller bekræftet, kan det være nødvendigt at afbryde igangværende antibiotikabrug, der ikke er rettet mod C. difficile. Passende væske- og elektrolytbehandling, proteintilskud, antibiotikabehandling af C. difficile og kirurgisk evaluering bør iværksættes som klinisk indiceret.
Udvikling af lægemiddelresistente bakterier
Ordinering af AMOXIL i fravær af en påvist eller stærkt mistænkt bakteriel infektion vil sandsynligvis ikke give gavn for patienten og øger risikoen for udvikling af lægemiddelresistente bakterier
Anvendelse hos patienter med mononukleose
En høj procentdel af patienter med mononukleose, som får amoxicillin, udvikler erytematøst hududslæt. Amoxicillin bør derfor ikke administreres til patienter med mononukleose.
Fenylketonurik
Amoxil 250mg tyggetabletter indeholder aspartam, som indeholder phenylalanin. Hver 200 mg tyggetablet indeholder 1,82 mg phenylalanin; hver 400 mg tyggetablet indeholder 3,64 mg phenylalanin. De orale suspensioner af Amoxil indeholder ikke phenylalanin og kan bruges af phenylketonurika.
Ikke-klinisk toksikologi
Karcinogenese, mutagenese, svækkelse af fertilitet
Langtidsundersøgelser på dyr er ikke blevet udført for at vurdere kræftfremkaldende potentiale. Undersøgelser til påvisning af mutagent potentiale af amoxicillin alene er ikke blevet udført; dog er følgende information tilgængelig fra tests på en 4:1 blanding af amoxicillin og kaliumclavulanat (AUGMENTIN). AUGMENTIN var ikke-mutagen i Ames bakterielle mutationsassay og gærgenkonverteringsassay. AUGMENTIN var svagt positiv i muse-lymfom-assayet, men tendensen mod øgede mutationsfrekvenser i dette assay forekom ved doser, der også var forbundet med nedsat celleoverlevelse. AUGMENTIN var negativ i mikronukleustesten hos mus og i den dominerende letale analyse hos mus. Kaliumclavulanat alene blev testet i Ames bakterielle mutationsassay og i muse mikronucleus test og var negativ i hver af disse assays. I et multi-generations reproduktionsstudie med rotter blev der ikke set nogen svækkelse af fertiliteten eller andre uønskede reproduktionseffekter ved doser op til 500 mg/kg (ca. 2 gange den humane dosis på 3 g baseret på kropsoverfladeareal).
Brug i specifikke populationer
Graviditet
Teratogene virkninger
Graviditet Kategori B. Reproduktionsundersøgelser er blevet udført på mus og rotter i doser op til 2000 mg/kg (3 og 6 gange 3 g human dosis, baseret på kropsoverfladeareal). Der var ingen tegn på skade på fosteret på grund af amoxicillin. Der er dog ingen tilstrækkelige og velkontrollerede undersøgelser af gravide kvinder. Da reproduktionsstudier på dyr ikke altid forudsiger human respons, bør amoxicillin kun anvendes under graviditet, hvis det er klart nødvendigt.
Arbejde og levering
Oral ampicillin absorberes dårligt under fødslen. Det vides ikke, om brug af amoxicillin hos mennesker under fødslen eller fødslen har umiddelbare eller forsinkede bivirkninger på fosteret, forlænger fødslens varighed eller øger sandsynligheden for nødvendigheden af en obstetrisk intervention.
Ammende mødre
Penicilliner har vist sig at blive udskilt i modermælk. Amoxicillinbrug af ammende mødre kan føre til sensibilisering af spædbørn. Der skal udvises forsigtighed, når amoxicillin administreres til en ammende kvinde.
Pædiatrisk brug
På grund af ufuldstændigt udviklet nyrefunktion hos nyfødte og spædbørn kan eliminationen af amoxicillin forsinkes. Dosering af AMOXIL 625 mg bør ændres hos pædiatriske patienter 12 uger eller yngre (≤ 3 måneder). [Se DOSERING OG ADMINISTRATION ]
Geriatrisk brug
En analyse af kliniske undersøgelser af AMOXIL 250 mg blev udført for at bestemme, om forsøgspersoner på 65 år og derover reagerer anderledes end yngre forsøgspersoner. Disse analyser har ikke identificeret forskelle i respons mellem ældre og yngre patienter, men en større følsomhed hos nogle ældre individer kan ikke udelukkes.
Dette lægemiddel vides at udskilles væsentligt af nyrerne, og risikoen for toksiske reaktioner på dette lægemiddel kan være større hos patienter med nedsat nyrefunktion. Da ældre patienter er mere tilbøjelige til at have nedsat nyrefunktion, bør der udvises forsigtighed ved dosisvalg, og det kan være nyttigt at overvåge nyrefunktionen.
Dosering ved nedsat nyrefunktion
Amoxicillin elimineres primært via nyrerne, og dosisjustering er normalt påkrævet hos patienter med svært nedsat nyrefunktion (GFR Dosering ved nedsat nyrefunktion for specifikke anbefalinger til patienter med nedsat nyrefunktion.
OVERDOSIS
I tilfælde af overdosering skal du afbryde medicinen, behandle symptomatisk og iværksætte støttende foranstaltninger efter behov. En prospektiv undersøgelse af 51 pædiatriske patienter på et giftkontrolcenter antydede, at overdosering på mindre end 250 mg/kg amoxicillin ikke er forbundet med signifikante kliniske symptomer.
Interstitiel nefritis, der resulterer i oligurisk nyresvigt, er blevet rapporteret hos et lille antal patienter efter overdosering med amoxicillin1.
Krystalluri, som i nogle tilfælde fører til nyresvigt, er også blevet rapporteret efter overdosering af amoxicillin hos voksne og pædiatriske patienter. I tilfælde af overdosering bør tilstrækkelig væskeindtagelse og diurese opretholdes for at reducere risikoen for amoxicillinkrystalluri.
Nedsat nyrefunktion ser ud til at være reversibel med ophør af lægemiddeladministration. Høje blodniveauer kan lettere forekomme hos patienter med nedsat nyrefunktion på grund af nedsat renal clearance af amoxicillin. Amoxicillin kan fjernes fra kredsløbet ved hæmodialyse.
KONTRAINDIKATIONER
AMOXIL 625mg er kontraindiceret hos patienter, der har oplevet en alvorlig overfølsomhedsreaktion (f.eks. anafylaksi eller Stevens-Johnsons syndrom) over for AMOXIL eller andre β-lactamantibiotika (f.eks. penicilliner og cephalosporiner).
KLINISK FARMAKOLOGI
Handlingsmekanisme
Amoxicillin er et antibakterielt lægemiddel. [se Mikrobiologi ].
Farmakokinetik
Absorption
Amoxicillin er stabilt i nærvær af mavesyre og absorberes hurtigt efter oral administration. Effekten af mad på absorptionen af amoxicillin fra tabletterne og suspensionen af AMOXIL er blevet delvist undersøgt; 400 mg og 875 mg formuleringer er kun blevet undersøgt, når de blev administreret i starten af et let måltid.
Oralt administrerede doser på 250 mg og 500 mg amoxicillinkapsler resulterer i gennemsnitlige maksimale blodniveauer 1 til 2 timer efter administration i området fra henholdsvis 3,5 mcg/ml til 5,0 mcg/ml og 5,5 mcg/ml til 7,5 mcg/ml. .
Gennemsnitlige farmakokinetiske parametre for amoxicillin fra et åbent, todelt, enkeltdosis crossover bioækvivalensstudie hos 27 voksne, der sammenlignede 875 mg AMOXIL med 875 mg AUGMENTIN® (amoxicillin/clavulanatkalium) viste, at 875 mg tabletten AMOXIL producerer 500mOXIL AUC0-∞ på 35,4 ± 8,1 mcg•time/mL og en Cmax på 13,8 ± 4,1 mcg/mL. Dosering var i starten af et let måltid efter en nats faste.
Oralt administrerede doser af amoxicillin-suspension, 125 mg/5 ml og 250 mg/5 ml, resulterer i gennemsnitlige maksimale blodniveauer 1 til 2 timer efter administration i området fra 1,5 mcg/ml til 3,0 mcg/ml og 3,5 mcg/ml til 5,0 mcg/ml, hhv.
Oral administration af enkeltdoser på 400 mg tyggetabletter og 400 mg/5 ml suspension af AMOXIL 625 mg til 24 voksne frivillige gav sammenlignelige farmakokinetiske data:
Fordeling
Amoxicillin diffunderer let ind i de fleste kropsvæv og -væsker, med undtagelse af hjerne- og rygmarvsvæske, undtagen når meninges er betændt. I blodserum er amoxicillin cirka 20 % proteinbundet. Efter en dosis på 1 gram og ved anvendelse af en speciel hudvindueteknik til at bestemme niveauer af antibiotika, blev det bemærket, at terapeutiske niveauer blev fundet i den interstitielle væske.
Metabolisme og udskillelse
Halveringstiden for amoxicillin er 61,3 minutter. Ca. 60 % af en oralt administreret dosis af amoxicillin udskilles i urinen inden for 6 til 8 timer. Påviselige serumniveauer observeres op til 8 timer efter en oralt administreret dosis af amoxicillin. Da det meste af amoxicillin udskilles uændret i urinen, kan dets udskillelse forsinkes ved samtidig administration af probenecid [se DRUGSINTERAKTIONER ].
Mikrobiologi
Virkningsmekanisme
Amoxicillin ligner penicillin i dets bakteriedræbende virkning mod modtagelige bakterier under aktiv multiplikationsstadiet. Det virker gennem hæmning af cellevægsbiosyntese, der fører til bakteriens død.
Modstandsmekanisme
Resistens over for amoxicillin medieres primært gennem enzymer kaldet beta-lactamaser, der spalter amoxicillins beta-lactamring, hvilket gør den inaktiv.
Amoxicillin har vist sig at være aktivt mod de fleste isolater af de bakterier, der er anført nedenfor, både in vitro og ved kliniske infektioner som beskrevet i INDIKATIONER OG BRUG afsnit.
Gram-positive bakterier
Enterococcus faecalis Staphylococcus spp. Streptococcus pneumoniae Streptococcus spp. (alfa og beta-hæmolytisk)
Gram-negative bakterier
Escherichia coli Haemophilus influenzae Helicobacter pylori Proteus mirabilis
Modtagelighedstestmetoder
Når det er tilgængeligt, bør det kliniske mikrobiologiske laboratorium levere kumulative in vitro-følsomhedstestresultater for antimikrobielle lægemidler, der anvendes på lokale hospitaler og praksisområder, til lægen som periodiske rapporter, der beskriver følsomhedsprofilen for nosokomiale og samfundserhvervede patogener. Disse rapporter skal hjælpe lægen med at vælge det mest effektive antimikrobielle middel.
Fortyndingsteknikker: Kvantitative metoder bruges til at bestemme antimikrobielle minimumshæmmende koncentrationer (MIC'er). Disse MIC'er giver estimater af bakteriers modtagelighed over for antimikrobielle forbindelser. MIC'erne skal bestemmes ved hjælp af en standardiseret testmetode -(bouillon eller agar)2,4. MIC-værdierne skal fortolkes i henhold til kriterierne i tabel 4.
Diffusionsteknikker: Kvantitative metoder, der kræver måling af zonediametre, kan også give reproducerbare estimater af bakteriers modtagelighed over for antimikrobielle forbindelser3,4. Zonestørrelsen bør bestemmes ved hjælp af en standardiseret testmetode3.
Følsomhed over for amoxicillin hos Enterococcus spp., Enterobacteriaceae og H. influenzae kan udledes ved at teste ampicillin4. Følsomhed over for amoxicillin af Staphylococcus spp. og beta-hæmolytiske Streptococcus spp. kan udledes ved at teste penicillin4. Størstedelen af isolater af Enterococcus spp. som er resistente over for ampicillin eller amoxicillin, producerer en TEM-type beta-lactamase. En beta-lactamase-test kan give et hurtigt middel til at bestemme resistens over for ampicillin og amoxicillin4.
Følsomhed over for amoxicillin af Streptococcus pneumoniae (non-meningitis-isolater) kan udledes ved at teste penicillin eller oxacillin4. Fortolkningskriterierne for S. pneumoniae til amoxicillin er angivet i tabel 44.
En rapport om "følsom" indikerer, at det antimikrobielle middel sandsynligvis vil hæmme væksten af patogenet, hvis den antimikrobielle forbindelse når en koncentration på infektionsstedet, der er nødvendig for at hæmme væksten af patogenet. En rapport med "Mellem" angiver, at resultatet skal betragtes som tvetydigt, og hvis mikroorganismen ikke er fuldt modtagelig for alternative, klinisk mulige lægemidler, bør testen gentages. Denne kategori indebærer mulig klinisk anvendelighed på kropssteder, hvor lægemidlet er fysiologisk koncentreret. Denne kategori giver også en bufferzone, der forhindrer små ukontrollerede tekniske faktorer i at forårsage store uoverensstemmelser i fortolkningen. En rapport om "Resistent" indikerer, at det antimikrobielle middel sandsynligvis ikke vil hæmme væksten af patogenet, hvis den antimikrobielle forbindelse når den koncentration, der normalt kan opnås på infektionsstedet; anden terapi bør vælges.
Modtagelighedstest for Helicobacter pylori
Amoxicillin in vitro-følsomhedstestmetoder til bestemmelse af minimale hæmmende koncentrationer (MIC'er) og zonestørrelser er ikke blevet standardiseret, valideret eller godkendt til testning af H. pylori. Prøver for H. pylori- og clarithromycin-følsomhedstestresultater bør indhentes på isolater fra patienter, som mislykkes med tripelbehandling. Hvis der konstateres clarithromycinresistens, bør et ikke-clarithromycinholdigt regime anvendes.
Kvalitetskontrol
Standardiserede følsomhedstestprocedurer2,3,4 kræver brug af laboratoriekontroller til at overvåge og sikre nøjagtigheden og præcisionen af de forsyninger og reagenser, der anvendes i analysen, og teknikkerne for de personer, der udfører testkontrollen. Standard amoxicillinpulver bør give følgende interval af MIC-værdier angivet i Tabel 54. For diffusionsteknikken skal kriterierne i Tabel 5 være opfyldt.
Kliniske Studier
H. pylori-udryddelse for at reducere risikoen for tilbagefald af duodenalsår
Randomiserede, dobbeltblindede kliniske undersøgelser udført i USA hos patienter med H. pylori og duodenalsår (defineret som et aktivt sår eller historie med et sår inden for 1 år) evaluerede effektiviteten af lansoprazol i kombination med amoxicillinkapsler og clarithromycintabletter som tredobbelt 14-dages behandling eller i kombination med amoxicillinkapsler som dobbelt 14-dages behandling til udryddelse af H. pylori. Baseret på resultaterne af disse undersøgelser blev sikkerheden og effekten af 2 forskellige udryddelsesregimer fastlagt: Tredobbelt behandling: Amoxicillin 1 gram to gange dagligt/clarithromycin 500 mg to gange dagligt/lansoprazol 30 mg to gange dagligt (se tabel 6). Dobbeltbehandling: Amoxicillin 1 gram tre gange dagligt/lansoprazol 30 mg tre gange dagligt (se tabel 7. Alle behandlinger var i 14 dage. H. pylori-udryddelse blev defineret som 2 negative tests (kultur og histologi) 4 til 6 uger efter afslutning af behandlingen. Tredobbelt terapi viste sig at være mere effektiv end alle mulige kombinationer af dobbeltterapi. Dobbeltbehandling viste sig at være mere effektiv end begge monoterapier. Udryddelse af H. pylori har vist sig at reducere risikoen for tilbagefald af duodenalsår.
REFERENCER
1. Swanson-Biearman B, Dean BS, Lopez G, Krenzelok EP. Virkningerne af indtagelse af penicillin og cephalosporin hos børn under seks år. Dyrlæge Hum Toxicol. 1988; 30: 66-67.
2. Clinical and Laboratory Standards Institute (CLSI). Metoder til fortynding Antimikrobielle følsomhedstests for bakterier, der vokser aerobt; Godkendt standard – tiende udgave. CLSI-dokument M07-A10, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania 19087, USA, 2015.
3. Clinical and Laboratory Standards Institute (CLSI). Ydeevnestandarder for antimikrobielle diskdiffusionsfølsomhedstests; Godkendt standard – tolvte udgave. CLSI-dokument M02-A12, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania 19087, USA, 2015.
4. Clinical and Laboratory Standards Institute (CLSI). Ydeevnestandarder for antimikrobiel følsomhedstestning; Femogtyvende informationstillæg, CLSI-dokument M100-S25. CLSI-dokument M100-S25, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania 19087, USA, 2015.
PATIENTOPLYSNINGER
- Patienter bør informeres om, at AMOXIL kan tages hver 8. time eller hver 12. time, afhængigt af den ordinerede dosis.
- Patienter bør rådgives om, at antibakterielle lægemidler, inklusive AMOXIL, kun bør anvendes til behandling af bakterielle infektioner. De behandler ikke virusinfektioner (f.eks. forkølelse). Når AMOXIL 250 mg er ordineret til behandling af en bakteriel infektion, skal patienterne fortælles, at selvom det er almindeligt at føle sig bedre tidligt i behandlingsforløbet, skal medicinen tages nøjagtigt som anvist. At springe doser over eller ikke fuldføre hele behandlingsforløbet kan: (1) mindske effektiviteten af den øjeblikkelige behandling og (2) øge sandsynligheden for, at bakterier udvikler resistens og ikke vil kunne behandles med AMOXIL 625mg eller andre antibakterielle lægemidler i fremtiden .
- Patienter bør rådgives om, at diarré er et almindeligt problem forårsaget af antibiotika, og det slutter normalt, når antibiotikaen seponeres. Nogle gange efter påbegyndelse af behandling med antibiotika kan patienter udvikle vandig og blodig afføring (med eller uden mavekramper og feber) selv så sent som 2 eller flere måneder efter at have taget deres sidste dosis af antibiotika. Hvis dette sker, skal patienter kontakte deres læge hurtigst muligt.
- Patienter skal være opmærksomme på, at AMOXIL indeholder et lægemiddel i penicillinklassen, som kan forårsage allergiske reaktioner hos nogle individer.
