Wellbutrin 150mg, 300mg Bupropion Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Wellbutrin 150mg, og hvordan bruges det?
Wellbutrin 150mg er en receptpligtig medicin, der bruges til at behandle symptomerne på svær depression og sæsonbestemt affektiv lidelse. Wellbutrin 150mg kan bruges alene eller sammen med anden medicin.
Wellbutrin 150mg tilhører en klasse af lægemidler kaldet antidepressiva, dopamingenoptagelseshæmmere, antidepressiva, andre hjælpemidler til rygestop.
Hvad er de mulige bivirkninger af Wellbutrin 150mg?
Wellbutrin kan forårsage alvorlige bivirkninger, herunder:
- krampeanfald (kramper),
- forvirring,
- usædvanlige ændringer i humør eller adfærd,
- sløret syn,
- tunnelsyn,
- øjensmerter eller hævelse,
- ser glorier omkring lys,
- hurtig eller uregelmæssig hjerterytme,
- race tanker,
- øget energi,
- hensynsløs opførsel,
- føler dig ekstrem glad eller irritabel,
- taler mere end normalt, og
- alvorlige søvnproblemer
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Wellbutrin omfatter:
- tør mund,
- tilstoppet næse,
- synsproblemer,
- høreproblemer,
- kvalme,
- opkastning,
- forstoppelse,
- søvnproblemer (søvnløshed),
- rystelser,
- svedeture,
- føler sig angst eller nervøs,
- hurtige hjerteslag,
- forvirring,
- agitation,
- fjendtlighed,
- udslæt,
- hovedpine,
- svimmelhed, og
- ledsmerter
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Wellbutrin. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088
ADVARSEL
SELVmordstanker og -adfærd
SUICIDALITET OG ANTIDEPRESSIVE stoffer
Antidepressiva øgede risikoen for selvmordstanker og -adfærd hos børn, unge og unge voksne i kortvarige forsøg. Disse forsøg viste ikke en stigning i risikoen for selvmordstanker og -adfærd ved brug af antidepressiva hos forsøgspersoner over 24 år; der var en reduktion i risikoen ved brug af antidepressiva hos forsøgspersoner på 65 år og ældre [se ADVARSLER OG FORHOLDSREGLER].
Hos patienter i alle aldre, som er startet på antidepressiv behandling, skal du nøje overvåge for forværring og for fremkomsten af selvmordstanker og -adfærd. Rådgiv familier og pårørende om behovet for tæt observation og kommunikation med den ordinerende læge [se ADVARSLER OG FORHOLDSREGLER].
BESKRIVELSE
WELLBUTRIN (bupropionhydrochlorid), et antidepressivt middel af aminoketonklassen, er kemisk ikke relateret til tricykliske, tetracykliske, selektive serotonin-genoptagelseshæmmere eller andre kendte antidepressive midler. Dens struktur minder meget om diethylpropions; det er relateret til phenylethylaminer. Det er betegnet som (±)-1-(3-chlorphenyl)-2-[(1,1-dimethylethyl)amino]-1-propanonhydrochlorid. Molekylvægten er 276,2. Molekylformlen er C13H18ClNO•HCl. Bupropionhydrochloridpulver er hvidt, krystallinsk og meget opløseligt i vand. Det har en bitter smag og fremkalder fornemmelsen af lokalbedøvelse på mundslimhinden. Strukturformlen er:
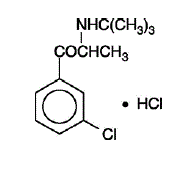
WELLBUTRIN leveres til oral administration som 75 mg (gul-guld) og 100 mg (rød) filmovertrukne tabletter. Hver tablet indeholder den mærkede mængde bupropionhydrochlorid og de inaktive ingredienser: 75 mg tablet – D&C Yellow No. 10 Lake, FD&C Yellow No. 6 Lake, hydroxypropylcellulose, hypromellose, mikrokrystallinsk cellulose, polyethylenglycol, talkum og titaniumdioxid; 100 mg tablet – FD&C Red No. 40 Lake, FD&C Yellow No. 6 Lake, hydroxypropylcellulose, hypromellose, mikrokrystallinsk cellulose, polyethylenglycol, talkum og titaniumdioxid.
INDIKATIONER
WELLBUTRIN (bupropionhydrochlorid) er indiceret til behandling af svær depressiv lidelse (MDD), som defineret i Diagnostic and Statistical Manual (DSM).
Effekten af WELLBUTRIN 300 mg til behandling af en svær depressiv episode blev fastslået i to 4-ugers kontrollerede indlæggelsesforsøg og et 6-ugers kontrolleret ambulant forsøg med voksne forsøgspersoner med MDD [se Kliniske Studier ].
DOSERING OG ADMINISTRATION
Generel brugsanvisning
For at minimere risikoen for anfald øges dosis gradvist [se ADVARSLER OG FORHOLDSREGLER ]. Forøgelser i dosis bør ikke overstige 100 mg/dag i en 3-dages periode. WELLBUTRIN tabletter bør sluges hele og må ikke knuses, deles eller tygges. WELLBUTRIN 300 mg kan tages med eller uden mad.
Den anbefalede startdosis er 200 mg/dag, givet som 100 mg to gange dagligt. Efter 3 dages dosering kan dosis øges til 300 mg/dag, givet som 100 mg 3 gange dagligt, med mindst 6 timer mellem på hinanden følgende doser. Dosering over 300 mg/dag kan opnås ved brug af 75 eller 100 mg tabletter.
Et maksimum på 450 mg/dag, givet i opdelte doser på ikke mere end 150 mg hver, kan overvejes til patienter, som ikke viser nogen klinisk forbedring efter flere ugers behandling med 300 mg/dag. Administrer 100 mg tabletten 4 gange dagligt for ikke at overskride grænsen på 150 mg i en enkelt dosis.
Der er generelt enighed om, at akutte episoder med depression kræver flere måneder eller længere antidepressiv behandling ud over responsen i den akutte episode. Det vides ikke, om den dosis WELLBUTRIN, der er nødvendig til vedligeholdelsesbehandling, er identisk med den dosis, der gav et indledende respons. Vurder med jævne mellemrum behovet for vedligeholdelsesbehandling og den passende dosis til en sådan behandling.
Dosisjustering hos patienter med nedsat leverfunktion
Hos patienter med moderat til svært nedsat leverfunktion (Child-Pugh-score: 7 til 15) er den maksimale dosis af WELLBUTRIN 150 mg 75 mg/dag. Hos patienter med let nedsat leverfunktion (Child-Pugh-score: 5 til 6), skal du overveje at reducere dosis og/eller doseringshyppighed [se Brug i specifikke populationer , KLINISK FARMAKOLOGI ].
Dosisjustering hos patienter med nedsat nyrefunktion
Overvej at reducere dosis og/eller hyppighed af WELLBUTRIN 150 mg hos patienter med nedsat nyrefunktion (glomerulær filtrationshastighed mindre end 90 ml/min) [se Brug i specifikke populationer , KLINISK FARMAKOLOGI ].
At skifte en patient til eller fra et monoaminoxidasehæmmer (MAOI) antidepressivt middel
Der bør gå mindst 14 dage mellem seponering af en MAO-hæmmer beregnet til behandling af depression og påbegyndelse af behandling med WELLBUTRIN. Omvendt bør der gå mindst 14 dage efter ophør med WELLBUTRIN, før man starter et MAO-antidepressivum [se KONTRAINDIKATIONER , DRUGSINTERAKTIONER ].
Brug af WELLBUTRIN med reversible MAO-hæmmere såsom linezolid eller methylenblåt
Start ikke med WELLBUTRIN 300 mg hos en patient, der behandles med en reversibel MAO-hæmmer, såsom linezolid eller intravenøs methylenblåt. Lægemiddelinteraktioner kan øge risikoen for hypertensive reaktioner. Hos en patient, som kræver mere akut behandling af en psykiatrisk tilstand, bør ikke-farmakologiske indgreb, herunder hospitalsindlæggelse, overvejes [se KONTRAINDIKATIONER , DRUGSINTERAKTIONER ].
nogle tilfælde kan en patient, der allerede modtager behandling med WELLBUTRIN, have behov for akut behandling med linezolid eller intravenøs methylenblåt. Hvis acceptable alternativer til linezolid eller intravenøs behandling med methylenblåt ikke er tilgængelige, og de potentielle fordele ved behandling med linezolid eller intravenøs methylenblåt vurderes at opveje risikoen for hypertensive reaktioner hos en bestemt patient, bør WELLBUTRIN 300 mg stoppes omgående, og linezolid eller intravenøs methylen blå kan administreres. Patienten skal overvåges i 2 uger eller indtil 24 timer efter den sidste dosis linezolid eller intravenøs methylenblåt, alt efter hvad der kommer først. Behandling med WELLBUTRIN 300 mg kan genoptages 24 timer efter den sidste dosis linezolid eller intravenøs methylenblåt.
Risikoen ved at administrere methylenblåt ad ikke-intravenøse veje (såsom orale tabletter eller ved lokal injektion) eller i intravenøse doser meget lavere end 1 mg/kg med WELLBUTRIN 300 mg er uklar. Klinikeren bør ikke desto mindre være opmærksom på muligheden for en lægemiddelinteraktion ved en sådan brug [se KONTRAINDIKATIONER , DRUGSINTERAKTIONER ].
HVORDAN LEVERET
Doseringsformer og styrker
- 75 mg - gul-guld, runde, bikonvekse tabletter påtrykt "WELLBUTRIN 75".
- 100 mg - røde, runde, bikonvekse tabletter påtrykt "WELLBUTRIN 100".
Opbevaring og håndtering
WELLBUTRIN 150 mg tabletter, 75 mg bupropionhydrochlorid, er gul-guld, runde, bikonvekse tabletter påtrykt "WELLBUTRIN 75" i flasker med 100 stk. NDC 0173-0177-55).
WELLBUTRIN tabletter, 100 mg bupropionhydrochlorid, er røde, runde, bikonvekse tabletter påtrykt "WELLBUTRIN 100" i flasker med 100 stk. NDC 0173-0178-55).
Opbevares ved stuetemperatur, 20° til 25°C (68° til 77°F); udflugter tilladt mellem 15°C og 30°C (59°F og 86°F) [Se USP kontrolleret rumtemperatur ]. Beskyt mod lys og fugt.
Fremstillet til: GlaxoSmithKline, Research Triangle Park,. Revideret: november 2019
BIVIRKNINGER
Følgende bivirkninger er beskrevet mere detaljeret i andre afsnit af mærkningen:
- Selvmordstanker og -adfærd hos unge og unge voksne [se KASSET ADVARSEL , ADVARSLER OG FORHOLDSREGLER ]
- Neuropsykiatriske symptomer og selvmordsrisiko ved rygestopbehandling [se ADVARSLER OG FORHOLDSREGLER ]
- Anfald [se ADVARSLER OG FORHOLDSREGLER ]
- Hypertension [se ADVARSLER OG FORHOLDSREGLER ]
- Aktivering af mani eller hypomani [se ADVARSLER OG FORHOLDSREGLER ]
- Psykose og andre neuropsykiatriske reaktioner [se ADVARSLER OG FORHOLDSREGLER ]
- Vinkel-lukkende glaukom [se ADVARSLER OG FORHOLDSREGLER ]
- Overfølsomhedsreaktioner [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring med kliniske forsøg
Fordi kliniske forsøg udføres under vidt forskellige forhold, kan bivirkningsrater observeret i de kliniske forsøg med et lægemiddel ikke direkte sammenlignes med frekvenser i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke frekvenserne observeret i klinisk praksis.
Bivirkninger, der fører til seponering af behandling
Bivirkninger var tilstrækkeligt besværlige til at forårsage seponering af behandling med WELLBUTRIN hos ca. 10 % af de 2.400 forsøgspersoner og raske frivillige, som deltog i kliniske forsøg under produktets indledende udvikling. De mere almindelige hændelser, der forårsager seponering, omfatter neuropsykiatriske forstyrrelser (3,0 %), primært agitation og abnormiteter i mental status; gastrointestinale forstyrrelser (2,1%), primært kvalme og opkastning; neurologiske forstyrrelser (1,7%), primært anfald, hovedpine og søvnforstyrrelser; og dermatologiske problemer (1,4%), primært udslæt. Det er dog vigtigt at bemærke, at mange af disse hændelser opstod ved doser, der overstiger den anbefalede daglige dosis.
Almindelig observerede bivirkninger
Almindelige bivirkninger hos patienter behandlet med WELLBUTRIN er agitation, mundtørhed, søvnløshed, hovedpine/migræne, kvalme/opkastning, forstoppelse, tremor, svimmelhed, overdreven svedtendens, sløret syn, takykardi, forvirring, udslæt, fjendtlighed, hjertearrytmi og auditivitet. forstyrrelse.
Tabel 2 opsummerer de bivirkninger, der opstod i placebokontrollerede forsøg med en incidens på mindst 1 % af forsøgspersonerne, der fik WELLBUTRIN 150 mg og hyppigere hos disse forsøgspersoner end i placebogruppen.
Andre bivirkninger observeret under den kliniske udvikling af WELLBUTRIN
Betingelserne og varigheden af eksponeringen for WELLBUTRIN varierede meget, og en betydelig del af erfaringerne blev opnået i åbne og ukontrollerede kliniske omgivelser. I løbet af denne oplevelse blev der rapporteret adskillige bivirkninger; uden passende kontrol er det dog umuligt at fastslå med sikkerhed, hvilke hændelser der var eller ikke var forårsaget af WELLBUTRIN. Følgende opregning er organiseret efter organsystem og beskriver begivenheder i forhold til deres relative hyppighed af rapportering i databasen.
Følgende definitioner af hyppighed anvendes: Hyppige bivirkninger defineres som dem, der forekommer hos mindst 1/100 forsøgspersoner. Sjældne bivirkninger er dem, der forekommer hos 1/100 til 1/1.000 forsøgspersoner, mens sjældne hændelser er dem, der forekommer hos mindre end 1/1.000 forsøgspersoner.
Kardiovaskulær Hyppigt var ødem; sjældne var brystsmerter, elektrokardiogram (EKG) abnormiteter (for tidlige slag og uspecifikke ST-T ændringer) og åndenød/dyspnø; sjældne var rødmen og myokardieinfarkt.
Dermatologisk: Sjældent var alopeci.
Endokrine: Sjældent var gynækomasti; sjældent var glykosuri.
Gastrointestinale: Sjældne var dysfagi, tørstforstyrrelse og leverskade/gulsot; sjældent var tarmperforation.
Genitourinære: Hyppig var nocturia; sjældne var vaginal irritation, testikelhævelse, urinvejsinfektion, smertefuld erektion og retarderet ejakulation; sjældne var enurese og urininkontinens.
Neurologisk: Hyppige var ataksi/inkoordination, krampeanfald, myoklonus, dyskinesi og dystoni; sjældne var mydriasis, vertigo og dysartri; sjældne var elektroencefalogram (EEG) abnormitet og nedsat opmærksomhed.
Neuropsykiatrisk: Hyppige var mani/hypomani, øget libido, hallucinationer, nedsat seksuel funktion og depression; sjældne var hukommelsessvækkelse, depersonalisering, psykose, dysfori, humørstabilitet, paranoia og formel tankeforstyrrelse; sjældent var selvmordstanker.
Mundtlige klager: Hyppig var stomatitis; sjældne var tandpine, bruxisme, tandkødsirritation og oral ødem.
Åndedræt: Sjældne var bronkitis og åndenød/dyspnø; sjælden var lungeemboli.
Særlige sanser: Sjældent var synsforstyrrelser; sjældent var diplopi.
Uspecifik: Hyppige var influenzalignende symptomer; sjældent var uspecifik smerte; sjælden var overdosis.
Ændret appetit og vægt
Et vægttab på mere end 5 lbs. forekom hos 28 % af forsøgspersonerne, der fik WELLBUTRIN. Denne forekomst er omtrent det dobbelte af, hvad der ses hos sammenlignelige forsøgspersoner, der er behandlet med tricykliske eller placebo. Ydermere, mens 35 % af forsøgspersonerne, der fik tricykliske antidepressiva, tog på i vægt, var det kun 9,4 % af forsøgspersonerne, der blev behandlet med WELLBUTRIN, der gjorde det. Hvis vægttab er et væsentligt tegn på en patients depressive sygdom, bør det anorektiske og/eller vægtreducerende potentiale af WELLBUTRIN derfor overvejes.
Postmarketing oplevelse
Følgende bivirkninger er blevet identificeret under brug af WELLBUTRIN efter godkendelse og er ikke beskrevet andetsteds på etiketten. Fordi disse reaktioner rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt pålideligt at estimere deres hyppighed eller etablere en årsagssammenhæng til lægemiddeleksponering.
Krop (generelt)
Artralgi, myalgi og feber med udslæt og andre symptomer, der tyder på forsinket overfølsomhed. Disse symptomer kan ligne serumsyge [se ADVARSLER OG FORHOLDSREGLER ].
Kardiovaskulær
Hypertension (i nogle tilfælde alvorlig), ortostatisk hypotension, tredje grads hjerteblok.
Endokrine
Hyponatriæmi, syndrom af uhensigtsmæssig antidiuretisk hormonsekretion, hyperglykæmi, hypoglykæmi.
Gastrointestinale
Esofagitis, hepatitis.
Hemisk og lymfatisk
Ekkymose, leukocytose, leukopeni, trombocytopeni. Ændret PT og/eller INR, sjældent forbundet med hæmoragiske eller trombotiske komplikationer, blev observeret, når bupropion blev administreret samtidigt med warfarin.
Muskuloskeletale
Muskelstivhed/feber/rhabdomyolyse, muskelsvaghed.
Nervesystem
Aggression, koma, fuldført selvmord, delirium, drømmeabnormiteter, paranoide forestillinger, paræstesi, parkinsonisme, rastløshed, selvmordsforsøg, afsløring af tardiv dyskinesi.
Hud og vedhæng
Stevens-Johnsons syndrom, angioødem, eksfoliativ dermatitis, urticaria.
Særlige sanser
Tinnitus, øget intraokulært tryk.
DRUGSINTERAKTIONER
Potentiale for andre lægemidler til at påvirke WELLBUTRIN
Bupropion metaboliseres primært til hydroxybupropion af CYP2B6. Derfor er der potentiale for lægemiddelinteraktioner mellem WELLBUTRIN og lægemidler, der er hæmmere eller inducere af CYP2B6.
Hæmmere af CYP2B6
Ticlopidin og Clopidogrel
Samtidig behandling med disse lægemidler kan øge eksponeringen for bupropion, men reducere eksponeringen for hydroxybupropion. Baseret på klinisk respons kan dosisjustering af WELLBUTRIN være nødvendig, når det administreres sammen med CYP2B6-hæmmere (f.eks. ticlopidin eller clopidogrel) [se KLINISK FARMAKOLOGI ].
Inducere af CYP2B6
Ritonavir, Lopinavir og Efavirenz
Samtidig behandling med disse lægemidler kan mindske eksponeringen for bupropion og hydroxybupropion. Dosisforøgelse af WELLBUTRIN kan være nødvendig, når det administreres sammen med ritonavir, lopinavir eller efavirenz [se KLINISK FARMAKOLOGI ] men bør ikke overstige den maksimalt anbefalede dosis.
Carbamazepin, Phenobarbital, Phenytoin
Selvom de ikke er systematisk undersøgt, kan disse lægemidler inducere metabolismen af bupropion og kan reducere eksponeringen for bupropion [se KLINISK FARMAKOLOGI ]. Hvis bupropion anvendes samtidig med en CYP-inducer, kan det være nødvendigt at øge dosis af bupropion, men den maksimalt anbefalede dosis bør ikke overskrides.
Potentiale for WELLBUTRIN 300mg til at påvirke andre lægemidler
Lægemidler metaboliseret af CYP2D6
Bupropion og dets metabolitter (erythrohydrobupropion, threohydrobupropion, hydroxybupropion) er CYP2D6-hæmmere. Derfor kan samtidig administration af WELLBUTRIN med lægemidler, der metaboliseres af CYP2D6, øge eksponeringen af lægemidler, der er substrater for CYP2D6. Sådanne lægemidler omfatter visse antidepressiva (f.eks. venlafaxin, nortriptylin, imipramin, desipramin, paroxetin, fluoxetin og sertralin), antipsykotika (f.eks. haloperidol, risperidon, thioridazin), betablokkere (f.eks. metoprolol) og type 1C-antiarytmika (f.eks. , propafenon og flecainid). Når det bruges samtidig med WELLBUTRIN, kan det være nødvendigt at reducere dosis af disse CYP2D6-substrater, især for lægemidler med et snævert terapeutisk indeks.
Lægemidler, der kræver metabolisk aktivering af CYP2D6 for at være effektive (f.eks. tamoxifen), kan teoretisk have reduceret virkning, når de administreres samtidig med CYP2D6-hæmmere, såsom bupropion. Patienter, der behandles samtidig med WELLBUTRIN og sådanne lægemidler, kan kræve øgede doser af lægemidlet [se KLINISK FARMAKOLOGI ].
Digoxin
Samtidig administration af WELLBUTRIN og digoxin kan nedsætte digoxinniveauet i plasma. Overvåg plasmadigoxinniveauer hos patienter, der behandles samtidig med WELLBUTRIN og digoxin [se KLINISK FARMAKOLOGI ].
Lægemidler, der sænker anfaldstærsklen
Vær yderst forsigtig, når du administrerer WELLBUTRIN sammen med andre lægemidler, der sænker krampetærsklen (f.eks. andre bupropionprodukter, antipsykotika, antidepressiva, theophyllin eller systemiske kortikosteroider). Brug lave startdoser og øg dosis gradvist [se KONTRAINDIKATIONER , ADVARSLER OG FORHOLDSREGLER ].
Dopaminerge lægemidler (levodopa og amantadin)
Bupropion, levodopa og amantadin har dopaminagonisteffekter. CNS-toksicitet er blevet rapporteret, når bupropion blev administreret sammen med levodopa eller amantadin. Bivirkninger har omfattet rastløshed, agitation, tremor, ataksi, gangforstyrrelser, vertigo og svimmelhed. Det formodes, at toksiciteten skyldes kumulative dopaminagonisteffekter. Vær forsigtig, når du administrerer WELLBUTRIN 150mg samtidig med disse lægemidler.
Brug med alkohol
Efter markedsføringserfaring har der været sjældne rapporter om uønskede neuropsykiatriske hændelser eller nedsat alkoholtolerance hos patienter, der drak alkohol under behandling med WELLBUTRIN. Indtagelse af alkohol under behandling med WELLBUTRIN bør minimeres eller undgås.
MAO-hæmmere
Bupropion hæmmer genoptagelsen af dopamin og noradrenalin. Samtidig brug af MAO-hæmmere og bupropion er kontraindiceret, fordi der er en øget risiko for hypertensive reaktioner, hvis bupropion anvendes samtidig med MAO-hæmmere. Dyreundersøgelser viser, at den akutte toksicitet af bupropion forstærkes af MAO-hæmmeren phenelzin. Der bør gå mindst 14 dage mellem seponering af en MAO-hæmmer beregnet til behandling af depression og påbegyndelse af behandling med WELLBUTRIN. Omvendt bør der tillades mindst 14 dage efter ophør med WELLBUTRIN 150 mg, før man starter et MAO-antidepressivum [se DOSERING OG ADMINISTRATION , KONTRAINDIKATIONER ].
Interaktioner med lægemiddel-laboratorietest
Falsk-positive urinimmunoassay-screeningstest for amfetamin er blevet rapporteret hos patienter, der tager bupropion. Dette skyldes manglende specificitet af nogle screeningstests. Falsk-positive testresultater kan forekomme, selv efter seponering af bupropionbehandling. Bekræftende test, såsom gaskromatografi/massespektrometri, vil skelne bupropion fra amfetamin.
Stofmisbrug og afhængighed
kontrolleret stof
Bupropion er ikke et kontrolleret stof.
Misbrug
Mennesker
Kontrollerede kliniske forsøg udført med normale frivillige, i forsøgspersoner med en historie med flere stofmisbrug og i deprimerede forsøgspersoner viste en vis stigning i motorisk aktivitet og agitation/spænding, ofte typisk for centralstimulerende aktivitet.
I en population af individer, der har oplevet misbrug af stoffer, frembragte en enkelt oral dosis på 400 mg bupropion mild amfetaminlignende aktivitet sammenlignet med placebo på Morphine-Benzedrine Subscale of the Addiction Research Center Inventories (ARCI) og en score højere end placebo, men mindre end 15 mg af det Schedule II-stimulerende middel dextroamphetamin på ARCI-skalaen. Disse skalaer måler generelle følelser af eufori og stoffer, som ofte er forbundet med misbrugspotentiale.
Resultater i kliniske forsøg vides dog ikke at kunne forudsige misbrugspotentialet af stoffer. Ikke desto mindre tyder beviser fra enkeltdosisforsøg på, at den anbefalede daglige dosis af bupropion, når den administreres oralt i opdelte doser, sandsynligvis ikke vil være væsentligt forstærkende for misbrugere af amfetamin eller CNS-stimulerende midler. Imidlertid kan højere doser (som ikke kunne testes på grund af risikoen for anfald) være beskedent attraktive for dem, der misbruger CNS-stimulerende stoffer.
WELLBUTRIN er kun beregnet til oral brug. Inhalation af knuste tabletter eller injektion af opløst bupropion er blevet rapporteret. Anfald og/eller dødsfald er blevet rapporteret, når bupropion er blevet administreret intranasalt eller ved parenteral injektion.
Dyr
Undersøgelser af gnavere og primater viste, at bupropion udviser nogle farmakologiske virkninger, der er fælles for psykostimulerende midler. Hos gnavere har det vist sig at øge lokomotorisk aktivitet, fremkalde en mild stereotyp adfærdsrespons og øge reaktionshastigheden i flere skema-kontrollerede adfærdsparadigmer. I primatmodeller, der vurderede de positive forstærkende virkninger af psykoaktive stoffer, blev bupropion selvadministreret intravenøst. Hos rotter producerede bupropion amfetaminlignende og kokainlignende diskriminerende stimuluseffekter i narkotikadiskriminationsparadigmer, der blev brugt til at karakterisere de subjektive virkninger af psykoaktive stoffer.
ADVARSLER
Inkluderet som en del af FORHOLDSREGLER afsnit.
FORHOLDSREGLER
Selvmordstanker og -adfærd hos børn, unge og unge voksne
Patienter med MDD, både voksne og pædiatriske, kan opleve forværring af deres depression og/eller fremkomsten af selvmordstanker og -adfærd (suicidalitet) eller usædvanlige ændringer i adfærd, uanset om de tager antidepressiv medicin eller ej, og denne risiko kan vare ved indtil betydelig remission opstår. Selvmord er en kendt risiko for depression og visse andre psykiatriske lidelser, og disse lidelser er i sig selv de stærkeste forudsigere for selvmord. Der har længe været en bekymring for, at antidepressiva kan have en rolle i at inducere forværring af depression og fremkomsten af suicidalitet hos visse patienter i de tidlige faser af behandlingen.
Samlede analyser af kortvarige placebokontrollerede forsøg med antidepressiva (selektive serotoningenoptagelseshæmmere [SSRI] og andre) viser, at disse lægemidler øger risikoen for selvmordstanker og -adfærd (suicidalitet) hos børn, unge og unge voksne (18 år) til 24) med MDD og andre psykiatriske lidelser. Kortvarige kliniske forsøg viste ikke en stigning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne efter 24 år; der var en reduktion med antidepressiva sammenlignet med placebo hos voksne på 65 år og derover.
De samlede analyser af placebokontrollerede forsøg med børn og unge med MDD, obsessiv-kompulsiv lidelse (OCD) eller andre psykiatriske lidelser omfattede i alt 24 korttidsforsøg med 9 antidepressive lægemidler i over 4.400 forsøgspersoner. De samlede analyser af placebokontrollerede forsøg med voksne med MDD eller andre psykiatriske lidelser omfattede i alt 295 korttidsforsøg (median varighed på 2 måneder) af 11 antidepressive lægemidler i over 77.000 forsøgspersoner. Der var betydelig variation i risikoen for suicidalitet blandt stoffer, men en tendens til en stigning i de yngre forsøgspersoner for næsten alle undersøgte stoffer. Der var forskelle i den absolutte risiko for suicidalitet på tværs af de forskellige indikationer, med den højeste forekomst af MDD. Risikoforskellene (lægemiddel vs. placebo) var dog relativt stabile inden for aldersgrupper og på tværs af indikationer. Disse risikoforskelle (lægemiddel-placebo-forskel i antallet af tilfælde af suicidalitet pr. 1.000 behandlede forsøgspersoner) er angivet i tabel 1.
Der forekom ingen selvmord i nogen af de pædiatriske forsøg. Der var selvmord i voksenforsøgene, men antallet var ikke tilstrækkeligt til at nå frem til nogen konklusion om lægemiddeleffekt på selvmord.
Det er uvist, om suicidalitetsrisikoen strækker sig til længerevarende brug, dvs. ud over flere måneder. Der er dog væsentlige beviser fra placebokontrollerede vedligeholdelsesforsøg hos voksne med depression, at brugen af antidepressiva kan forsinke tilbagefald af depression.
Alle patienter, der behandles med antidepressiva for enhver indikation, bør overvåges passende og observeres nøje for klinisk forværring, suicidalitet og usædvanlige ændringer i adfærd, især i løbet af de første par måneder af et lægemiddelbehandlingsforløb, eller i tidspunkter med dosisændringer, enten stigninger eller formindsker [se ADVARSEL MED INDSAT].
Følgende symptomer, angst, agitation, panikanfald, søvnløshed, irritabilitet, fjendtlighed, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshed), hypomani og mani er blevet rapporteret hos voksne og pædiatriske patienter, der også behandles med antidepressiva mod svær depressiv lidelse. som for andre indikationer, både psykiatriske og ikke-psykiatriske. Selvom der ikke er etableret en årsagssammenhæng mellem fremkomsten af sådanne symptomer og enten forværring af depression og/eller fremkomsten af selvmordsimpulser, er der bekymring for, at sådanne symptomer kan repræsentere forløbere for ny suicidalitet.
Det bør overvejes at ændre det terapeutiske regime, herunder eventuelt seponering af medicinen, hos patienter, hvis depression er vedvarende værre, eller som oplever ny suicidalitet eller symptomer, der kan være forløbere for forværring af depression eller suicidalitet, især hvis disse symptomer er alvorlige, pludselige i debut, eller var ikke en del af patientens fremviste symptomer.
Familier og pårørende til patienter, der behandles med antidepressiva for MDD eller andre indikationer, både psykiatriske og ikke-psykiatriske, bør advares om behovet for at overvåge patienter for fremkomsten af agitation, irritabilitet, usædvanlige ændringer i adfærd og de andre symptomer beskrevet ovenfor, som f. samt fremkomsten af suicidalitet, og at rapportere sådanne symptomer straks til sundhedsudbydere. Sådan overvågning bør omfatte daglig observation af familier og omsorgspersoner. Recepter for WELLBUTRIN 150mg bør udskrives for den mindste mængde tabletter i overensstemmelse med god patientbehandling for at reducere risikoen for overdosering.
Neuropsykiatriske bivirkninger og selvmordsrisiko ved rygestopbehandling
WELLBUTRIN er ikke godkendt til rygestopbehandling; det indeholder dog det samme aktive stof som rygestopmedicinen ZYBAN. Alvorlige neuropsykiatriske bivirkninger er blevet rapporteret hos patienter, der tager bupropion for at stoppe med at ryge. Disse postmarketing-rapporter har inkluderet ændringer i humør (herunder depression og mani), psykose, hallucinationer, paranoia, vrangforestillinger, mordforestillinger, aggression, fjendtlighed, agitation, angst og panik, såvel som selvmordstanker, selvmordsforsøg og fuldført selvmord [ se BIVIRKNINGER ]. Nogle patienter, der holdt op med at ryge, kan have oplevet symptomer på nikotinabstinens, herunder nedtrykthed. Depression, som sjældent inkluderer selvmordstanker, er blevet rapporteret hos rygere, der har gennemgået et forsøg på at stoppe med at ryge uden medicin. Nogle af disse bivirkninger forekom dog hos patienter, der tog bupropion, som fortsatte med at ryge.
Neuropsykiatriske bivirkninger forekom hos patienter uden og med allerede eksisterende psykiatrisk sygdom; nogle patienter oplevede forværring af deres psykiatriske sygdomme. Observer patienter for forekomsten af neuropsykiatriske bivirkninger. Rådgiv patienter og pårørende om, at patienten skal stoppe med at tage WELLBUTRIN 300 mg og straks kontakte en sundhedsplejerske, hvis der observeres agitation, deprimeret stemning eller ændringer i adfærd eller tænkning, som ikke er typiske for patienten, eller hvis patienten udvikler selvmordstanker eller selvmordsadfærd. . I mange tilfælde efter markedsføring blev symptomerne forsvundet efter seponering af bupropion rapporteret. Symptomerne vedblev dog i nogle tilfælde; derfor bør der ydes løbende overvågning og støttende behandling, indtil symptomerne forsvinder.
Anfald
WELLBUTRIN 300mg kan forårsage anfald. Risikoen for anfald er dosisrelateret. Dosis bør ikke overstige 450 mg/dag. Forøg dosis gradvist. Afbryd WELLBUTRIN 150mg og genstart ikke behandlingen, hvis patienten oplever et anfald.
Risikoen for anfald er også relateret til patientfaktorer, kliniske situationer og samtidig medicin, der sænker anfaldstærsklen. Overvej disse risici, før du påbegynder behandling med WELLBUTRIN. WELLBUTRIN 300mg er kontraindiceret til patienter med anfaldssygdomme, nuværende eller tidligere diagnose anorexia nervosa eller bulimi, eller som gennemgår brat seponering af alkohol, benzodiazepiner, barbiturater og antiepileptika [se KONTRAINDIKATIONER , DRUGSINTERAKTIONER ]. Følgende tilstande kan også øge risikoen for anfald: alvorlig hovedskade; arteriovenøs misdannelse; CNS-tumor eller CNS-infektion; alvorligt slagtilfælde; samtidig brug af anden medicin, der sænker krampetærsklen (f.eks. andre bupropionprodukter, antipsykotika, tricykliske antidepressiva, teophyllin og systemiske kortikosteroider); metaboliske lidelser (f.eks. hypoglykæmi, hyponatriæmi, alvorlig leverinsufficiens og hypoxi); brug af ulovlige stoffer (f.eks. kokain); eller misbrug eller misbrug af receptpligtig medicin såsom CNS-stimulerende midler. Yderligere disponerende tilstande omfatter diabetes mellitus behandlet med orale hypoglykæmiske lægemidler eller insulin; brug af anorektiske lægemidler; og overdreven brug af alkohol, benzodiazepiner, beroligende/hypnotika eller opiater.
Forekomst af anfald ved brug af bupropion
Bupropion er forbundet med anfald hos ca. 0,4 % (4/1.000) af patienter, der behandles med doser op til 450 mg/dag. Den estimerede forekomst af anfald for WELLBUTRIN stiger næsten 10 gange mellem 450 og 600 mg/dag.
Risikoen for anfald kan reduceres, hvis dosis af WELLBUTRIN 300 mg ikke overstiger 450 mg/dag, givet som 150 mg 3 gange dagligt, og titreringshastigheden er gradvis.
Forhøjet blodtryk
Behandling med WELLBUTRIN kan resultere i forhøjet blodtryk og hypertension. Vurder blodtrykket før påbegyndelse af behandling med WELLBUTRIN 150mg og overvåg regelmæssigt under behandlingen. Risikoen for hypertension er øget, hvis WELLBUTRIN 150 mg anvendes samtidig med MAO-hæmmere eller andre lægemidler, der øger den dopaminerge eller noradrenerge aktivitet [se KONTRAINDIKATIONER ].
Data fra et sammenlignende forsøg med formuleringen med forlænget frigivelse af bupropion HCl, nikotin transdermalt system (NTS), kombinationen af forlænget frigivelse af bupropion plus NTS og placebo som en hjælp til rygestop tyder på en højere forekomst af behandlingsfremkaldt hypertension i patienter behandlet med kombinationen af forlænget frigivelse bupropion og NTS. I dette forsøg havde 6,1 % af forsøgspersonerne behandlet med kombinationen af bupropion med forlænget frigivelse og NTS behandlingsudløst hypertension sammenlignet med henholdsvis 2,5 %, 1,6 % og 3,1 % af forsøgspersonerne behandlet med bupropion med forlænget frigivelse, NTS og placebo. . Størstedelen af disse forsøgspersoner havde tegn på allerede eksisterende hypertension. Tre forsøgspersoner (1,2 %) behandlet med kombinationen af forlænget frigivelse af bupropion og NTS og 1 forsøgsperson (0,4 %) behandlet med NTS fik seponeret undersøgelsesmedicin på grund af hypertension sammenlignet med ingen af forsøgspersonerne behandlet med bupropion eller placebo med forlænget frigivelse. Overvågning af blodtryk anbefales hos patienter, som får kombinationen af bupropion og nikotinerstatning.
et klinisk forsøg med øjeblikkelig frigivelse af bupropion hos MDD-personer med stabil kongestiv hjerteinsufficiens (N = 36), var bupropion forbundet med en forværring af allerede eksisterende hypertension hos 2 forsøgspersoner, hvilket førte til seponering af bupropionbehandling. Der er ingen kontrollerede forsøg, der vurderer sikkerheden af bupropion hos patienter med en nylig historie med myokardieinfarkt eller ustabil hjertesygdom.
Aktivering af mani/hypomani
Antidepressiv behandling kan udløse en manisk, blandet eller hypoman manisk episode. Risikoen ser ud til at være øget hos patienter med bipolar lidelse, eller som har risikofaktorer for bipolar lidelse. Inden påbegyndelse af WELLBUTRIN skal patienter screenes for en historie med bipolar lidelse og tilstedeværelsen af risikofaktorer for bipolar lidelse (f.eks. familiehistorie med bipolar lidelse, selvmord eller depression). WELLBUTRIN 150mg er ikke godkendt til behandling af bipolar depression.
Psykose og andre neuropsykiatriske reaktioner
Deprimerede patienter behandlet med WELLBUTRIN har haft en række neuropsykiatriske tegn og symptomer, herunder vrangforestillinger, hallucinationer, psykoser, koncentrationsforstyrrelser, paranoia og forvirring. Nogle af disse patienter havde diagnosen bipolar lidelse. I nogle tilfælde aftog disse symptomer ved dosisreduktion og/eller seponering af behandlingen. Instruer patienterne i at kontakte en sundhedspersonale, hvis sådanne reaktioner opstår.
Vinkel-lukkende glaukom
Pupilleudvidelsen, der opstår efter brug af mange antidepressive lægemidler, herunder WELLBUTRIN 300 mg, kan udløse et vinkel-lukningsanfald hos en patient med anatomisk snævre vinkler, som ikke har en patenteret iridektomi.
Overfølsomhedsreaktioner
Anafylaktoide/anafylaktiske reaktioner er opstået under kliniske forsøg med bupropion. Reaktioner er blevet karakteriseret ved pruritus, nældefeber, angioødem og dyspnø, der kræver medicinsk behandling. Derudover har der været sjældne, spontane postmarketingrapporter om erythema multiforme, Stevens-Johnsons syndrom og anafylaktisk shock forbundet med bupropion. Instruer patienterne i at seponere WELLBUTRIN 150mg og konsultere en læge, hvis de udvikler en allergisk eller anafylaktoid/anafylaktisk reaktion (f.eks. hududslæt, kløe, nældefeber, brystsmerter, ødem og åndenød) under behandlingen.
Der er rapporter om artralgi, myalgi, feber med udslæt og andre serumsygelignende symptomer, der tyder på forsinket overfølsomhed.
Patientrådgivningsinformation
Råd patienten til at læse den FDA-godkendte patientmærkning ( Medicinvejledning ).
Selvmordstanker og -adfærd
Instruer patienterne, deres familier og/eller deres pårørende om at være opmærksomme på forekomsten af angst, agitation, panikanfald, søvnløshed, irritabilitet, fjendtlighed, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshed), hypomani, mani, andre usædvanlige ændringer i adfærd , forværring af depression og selvmordstanker, især tidligt under antidepressiv behandling, og når dosis justeres op eller ned. Rådgive familier og plejere til patienter om at observere forekomsten af sådanne symptomer på daglig basis, da ændringer kan være pludselige. Sådanne symptomer bør indberettes til patientens ordinerende læge eller sundhedspersonale, især hvis de er alvorlige, pludseligt opstået eller ikke var en del af patientens symptomer. Symptomer som disse kan være forbundet med en øget risiko for selvmordstanker og -adfærd og indikerer behov for meget tæt overvågning og muligvis ændringer i medicinen.
Neuropsykiatriske bivirkninger og selvmordsrisiko ved rygestopbehandling
Selvom WELLBUTRIN 150mg ikke er indiceret til rygestopbehandling, indeholder det den samme aktive ingrediens som ZYBAN, som er godkendt til denne brug. Informer patienterne om, at nogle patienter har oplevet ændringer i humør (herunder depression og mani), psykose, hallucinationer, paranoia, vrangforestillinger, mordforestillinger, aggression, fjendtlighed, agitation, angst og panik, samt selvmordstanker og selvmord, når de forsøger at holde op rygning, mens du tager bupropion. Instruer patienterne i at seponere bupropion og kontakte en sundhedspersonale, hvis de oplever sådanne symptomer [se ADVARSLER OG FORHOLDSREGLER , BIVIRKNINGER ].
Alvorlige allergiske reaktioner
Oplys patienter om symptomer på overfølsomhed og om at seponere WELLBUTRIN 300 mg, hvis de får en alvorlig allergisk reaktion.
Anfald
Instruer patienterne i at afbryde behandlingen og ikke genstarte WELLBUTRIN, hvis de oplever et anfald under behandling. Rådgiv patienterne om, at overdreven brug eller brat seponering af alkohol, benzodiazepiner, antiepileptika eller beroligende midler/hypnotika kan øge risikoen for anfald. Rådgive patienter om at minimere eller undgå brug af alkohol.
Vinkel-lukkende glaukom
Patienter bør informeres om, at indtagelse af WELLBUTRIN 150 mg kan forårsage mild pupiludvidelse, som hos følsomme personer kan føre til en episode med vinkel-lukkende glaukom. Eksisterende glaukom er næsten altid åbenvinklet glaukom, fordi vinkel-lukkende glaukom, når det diagnosticeres, kan behandles definitivt med iridektomi. Åbenvinklet glaukom er ikke en risikofaktor for lukkevinklet glaukom. Patienter kan ønske at blive undersøgt for at afgøre, om de er modtagelige for vinkellukning, og have en profylaktisk procedure (f.eks. iridektomi), hvis de er modtagelige [se ADVARSLER OG FORHOLDSREGLER ].
Bupropion-holdige produkter
Lær patienterne, at WELLBUTRIN 150mg indeholder den samme aktive ingrediens (bupropionhydrochlorid), som findes i ZYBAN, som bruges som en hjælp til rygestopbehandling, og at WELLBUTRIN 150mg ikke bør bruges i kombination med ZYBAN eller andre lægemidler, der indeholder bupropion (f.eks. som WELLBUTRIN 150mg SR, formuleringen med forlænget frigivelse og WELLBUTRIN XL eller FORFIVO XL, formuleringerne med forlænget frigivelse og APLENZIN, formuleringen med forlænget frigivelse af bupropionhydrobromid). Derudover er der en række generiske bupropion HCl-produkter til formuleringerne med øjeblikkelig, vedvarende og forlænget frigivelse.
Potentiale for kognitiv og motorisk svækkelse
Rådgiv patienterne om, at ethvert CNS-aktivt lægemiddel som WELLBUTRIN kan svække deres evne til at udføre opgaver, der kræver dømmekraft eller motoriske og kognitive færdigheder. Rådgiv patienterne, at indtil de er rimeligt sikre på, at WELLBUTRIN 300mg ikke påvirker deres ydeevne negativt, bør de undlade at køre bil eller betjene komplekse, farlige maskiner. WELLBUTRIN 150mg kan føre til nedsat alkoholtolerance.
Samtidig medicinering
Rådgiv patienterne om at underrette deres læge, hvis de tager eller planlægger at tage receptpligtig eller håndkøbsmedicin, fordi WELLBUTRIN 150mg og andre lægemidler kan påvirke hinandens stofskifte.
Graviditet
Rådgive patienter om at underrette deres læge, hvis de bliver gravide eller har til hensigt at blive gravide under behandling med WELLBUTRIN. Rådgiv patienterne om, at der findes et graviditetseksponeringsregister, der overvåger graviditetsresultater hos kvinder, der er eksponeret for WELLBUTRIN 150 mg under graviditeten [se Brug i specifikke populationer ].
Opbevaringsoplysninger
Instruer patienterne i at opbevare WELLBUTRIN ved stuetemperatur, mellem 68°F og 77°F (20°C til 25°C), og hold tabletterne tørre og ude af lys.
Administrationsoplysninger
Instruer patienterne i at tage WELLBUTRIN i ligeligt opdelte doser 3 eller 4 gange dagligt, med doser adskilt med mindst 6 timer for at minimere risikoen for anfald. Instruer patienterne, hvis de glemmer en dosis, om ikke at tage en ekstra tablet for at kompensere for den glemte dosis og at tage den næste tablet på det normale tidspunkt på grund af den dosisrelaterede risiko for anfald. Instruer patienterne i, at WELLBUTRIN tabletter skal sluges hele og ikke knuses, deles eller tygges. WELLBUTRIN kan tages med eller uden mad.
WELLBUTRIN, WELLBUTRIN SR, WELLBUTRIN 150mg XL og ZYBAN er varemærker ejet af eller licenseret til GSK-gruppen af virksomheder. De andre anførte mærker er varemærker ejet af eller licenseret til deres respektive ejere og er ikke ejet af eller licenseret til GSK-gruppen af virksomheder. Producenterne af disse mærker er ikke tilknyttet og støtter ikke GSK-gruppen af virksomheder eller dens produkter.
Ikke-klinisk toksikologi
Karcinogenese, mutagenese, svækkelse af fertilitet
Livsvarige carcinogenicitetsundersøgelser blev udført på rotter og mus ved bupropiondoser på op til henholdsvis 300 og 150 mg/kg/dag. Disse doser er henholdsvis ca. 6 og 2 gange MRHD på mg/m2-basis. I rottestudiet var der en stigning i nodulær proliferative læsioner i leveren ved doser på 100 til 300 mg/kg/dag (ca. 2 til 6 gange MRHD på mg/m2 basis); lavere doser blev ikke testet. Spørgsmålet om, hvorvidt sådanne læsioner kan være forstadier til neoplasmer i leveren, er i øjeblikket uløst. Lignende leverlæsioner blev ikke set i museundersøgelsen, og ingen stigning i maligne tumorer i leveren og andre organer blev set i nogen af undersøgelserne.
Bupropion producerede et positivt respons (2 til 3 gange kontrolmutationshastigheden) i 2 af 5 stammer i Ames bakterielle mutagenicitetsassay. Bupropion gav en stigning i kromosomafvigelser i 1 ud af 3 in vivo cytogenetiske undersøgelser af rotteknoglemarv.
Der var ingen virkninger på han- og hunfrugtbarheden, når rotter fik orale doser bupropion op til 300 mg/kg/dag (ca. 6 gange MRHD på mg/m2-basis) til hunner før parring og enten gennem dag 13 af drægtighed eller gennem laktation og til hanner i 60 dage før og gennem parring. Doser på 200 mg/kg/dag (ca. 4 gange MRHD på mg/m2-basis) eller mere forårsagede imidlertid forbigående ataksi eller adfærdsændringer hos voksne hunrotter. Der var heller ingen negative virkninger på fertilitet, reproduktion eller vækst og udvikling af mandlige eller kvindelige afkom.
Brug i specifikke populationer
Graviditet
Graviditetseksponeringsregister
Der er et uafhængigt graviditetseksponeringsregister, der overvåger graviditetsresultater hos kvinder, der er udsat for antidepressiva under graviditeten. Sundhedsudbydere opfordres til at registrere patienter ved at ringe til National Pregnancy Registry for Antidepressants på 1-844-4056185 eller besøge online på https://womensmentalhealth.org/clinical-and-researchprograms/pregnancyregistry/antidepressants.
Risikooversigt
Data fra epidemiologiske undersøgelser af gravide kvinder udsat for bupropion i første trimester har ikke identificeret en samlet øget risiko for medfødte misdannelser (se Data ). Der er risici for moderen forbundet med ubehandlet depression under graviditeten (se Kliniske overvejelser ). Når bupropion blev administreret til gravide rotter under organogenese, var der ingen tegn på føtale misdannelser ved doser op til ca. 10 gange den maksimalt anbefalede humane dosis (MRHD) på 450 mg/dag. Når det blev givet til drægtige kaniner under organogenese, blev ikke-dosisrelaterede stigninger i forekomsten af føtale misdannelser og skeletvariationer observeret ved doser, der var omtrent lig med MRHD og derover. Nedsat fostervægt blev set ved doser to gange MRHD og højere (se Dyredata ).
Den estimerede baggrundsrisiko for alvorlige fødselsdefekter og abort er ukendt for den angivne population. Alle graviditeter har en baggrundsrisiko for fødselsdefekter, tab eller andre ugunstige udfald. I den generelle befolkning i USA er den estimerede baggrundsrisiko for alvorlige fødselsdefekter og abort i klinisk anerkendte graviditeter henholdsvis 2 % til 4 % og 15 % til 20 %.
Kliniske overvejelser
Sygdomsassocieret moder- og/eller embryo-/fosterrisiko
En prospektiv, longitudinel undersøgelse fulgte 201 gravide kvinder med en historie med svær depressiv lidelse, som var euthymic og tog antidepressiva under graviditeten i begyndelsen af graviditeten. De kvinder, der ophørte med antidepressiva under graviditeten, var mere tilbøjelige til at opleve tilbagefald af svær depression end kvinder, der fortsatte med antidepressiva. Overvej risiciene for moderen ved ubehandlet depression og potentielle virkninger på fosteret, når behandlingen med antidepressiv medicin afbrydes eller ændres under graviditet og efter fødslen.
Data
Menneskelige data
Data fra det internationale bupropion-graviditetsregister (675 eksponeringer i første trimester) og et retrospektivt kohortestudie ved brug af United Healthcare-databasen (1.213 eksponeringer i første trimester) viste ikke en samlet øget risiko for misdannelser. Registret var ikke designet eller drevet til at evaluere specifikke defekter, men foreslog en mulig stigning i hjertemisdannelser.
Der er ikke observeret en samlet øget risiko for kardiovaskulære misdannelser efter bupropioneksponering i første trimester. Den prospektivt observerede frekvens af kardiovaskulære misdannelser i graviditeter med eksponering for bupropion i første trimester fra det internationale graviditetsregister var 1,3 % (9 kardiovaskulære misdannelser/675 eksponeringer for moderbupropion i første trimester), hvilket svarer til baggrundsraten for kardiovaskulære misdannelser (ca. 1 %). Data fra United Healthcare-databasen, som havde et begrænset antal eksponerede tilfælde med kardiovaskulære misdannelser, og et case-kontrolstudie (6.853 spædbørn med kardiovaskulære misdannelser og 5.763 med ikke-kardiovaskulære misdannelser) af selvrapporteret brug af bupropion fra National Birth Defects Forebyggelsesstudie (NBDPS) viste ikke en samlet øget risiko for kardiovaskulære misdannelser efter bupropioneksponering i første trimester.
Undersøgelsesresultater vedrørende bupropioneksponering i første trimester og risiko for obstruktion af venstre ventrikulær udstrømningskanal (LVOTO) er inkonsekvente og tillader ikke konklusioner vedrørende en mulig sammenhæng. United Healthcare-databasen manglede tilstrækkelig magt til at evaluere denne sammenhæng; NBDPS fandt øget risiko for LVOTO (n = 10; justeret OR = 2,6; 95 % CI: 1,2, 5,7), og casekontrolstudiet med Slone Epidemiology fandt ikke øget risiko for LVOTO.
Undersøgelsesresultater vedrørende bupropioneksponering i første trimester og risiko for ventrikulær septumdefekt (VSD) er inkonsistente og tillader ikke konklusioner vedrørende en mulig sammenhæng. Slone Epidemiology Study fandt en øget risiko for VSD efter første trimester maternel bupropion eksponering (n = 17; justeret OR = 2,5; 95 % CI: 1,3, 5,0), men fandt ikke øget risiko for andre undersøgte kardiovaskulære misdannelser (inklusive LVOTO som over). NBDPS- og United Healthcare-databaseundersøgelsen fandt ikke en sammenhæng mellem eksponering for moderens bupropion i første trimester og VSD.
Hvad angår resultaterne af LVOTO og VSD, var undersøgelserne begrænset af det lille antal eksponerede tilfælde, inkonsistente resultater blandt studier og potentialet for tilfældige fund fra flere sammenligninger i case-kontrolstudier.
Dyredata
undersøgelser udført på gravide rotter og kaniner blev bupropion administreret oralt i løbet af organogeneseperioden i doser på henholdsvis op til 450 og 150 mg/kg/dag (henholdsvis ca. 10 og 6 gange MRHD på mg/m2-basis). ). Der var ingen tegn på føtale misdannelser hos rotter. Når det blev givet til drægtige kaniner under organogenese, blev ikke-dosisrelaterede stigninger i forekomsten af føtale misdannelser og skeletvariationer observeret ved den laveste testede dosis (25 mg/kg/dag, omtrent lig med MRHD på mg/m2-basis). og større. Nedsat fostervægt blev observeret ved doser på 50 mg/kg/dag (ca. 2 gange MRHD på mg/m2-basis) og mere. Ingen maternel toksicitet var tydelig ved doser på 50 mg/kg/dag eller mindre.
et præ- og postnatalt udviklingsstudie havde bupropion indgivet oralt til gravide rotter i doser på op til 150 mg/kg/dag (ca. 3 gange MRHD på mg/m2-basis) fra embryonal implantation til laktation ingen effekt på hvalpenes vækst eller udvikling.
Amning
Risikooversigt
Data fra publiceret litteratur rapporterer tilstedeværelsen af bupropion og dets metabolitter i modermælk (se Data ). Der er ingen data om virkningen af bupropion eller dets metabolitter på mælkeproduktionen. Begrænsede data fra postmarketing-rapporter har ikke identificeret en klar sammenhæng mellem bivirkninger hos det ammede spædbarn. De udviklingsmæssige og sundhedsmæssige fordele ved amning bør overvejes sammen med moderens kliniske behov for WELLBUTRIN og eventuelle negative virkninger på det ammede barn fra WELLBUTRIN eller fra den underliggende moderens tilstand.
Data
et amningsstudie med 10 kvinder blev niveauer af oralt doseret bupropion og dets aktive metabolitter målt i udmalket mælk. Den gennemsnitlige daglige spædbørns eksponering (forudsat 150 ml/kg dagligt forbrug) for bupropion og dets aktive metabolitter var 2 % af moderens vægtjusterede dosis. Postmarketing rapporter har beskrevet anfald hos ammede spædbørn. Forholdet mellem bupropioneksponering og disse anfald er uklart.
Pædiatrisk brug
Sikkerhed og effektivitet i den pædiatriske population er ikke blevet fastslået [se KASSET ADVARSEL , ADVARSLER OG FORHOLDSREGLER ].
Geriatrisk brug
Af de ca. 6.000 forsøgspersoner, der deltog i kliniske forsøg med bupropion-tabletter med forlænget frigivelse (forsøg med depression og rygestop), var 275 i alderen ≥65 år og 47 i alderen ≥75 år. Derudover deltog flere hundrede forsøgspersoner i alderen ≥65 år i kliniske forsøg med formuleringen af bupropion med øjeblikkelig frigivelse (depressionsforsøg). Der blev ikke observeret nogen overordnede forskelle i sikkerhed eller effektivitet mellem disse forsøgspersoner og yngre forsøgspersoner. Rapporteret klinisk erfaring har ikke identificeret forskelle i respons mellem ældre og yngre patienter, men større følsomhed hos nogle ældre individer kan ikke udelukkes.
Bupropion metaboliseres i vidt omfang i leveren til aktive metabolitter, som metaboliseres yderligere og udskilles af nyrerne. Risikoen for bivirkninger kan være større hos patienter med nedsat nyrefunktion. Da ældre patienter er mere tilbøjelige til at have nedsat nyrefunktion, kan det være nødvendigt at overveje denne faktor ved dosisvalg; det kan være nyttigt at overvåge nyrefunktionen [se DOSERING OG ADMINISTRATION , Brug i specifikke populationer , KLINISK FARMAKOLOGI ].
Nedsat nyrefunktion
Overvej en reduceret dosis og/eller doseringshyppighed af WELLBUTRIN til patienter med nedsat nyrefunktion (glomerulær filtrationshastighed: mindre end 90 ml/min). Bupropion og dets metabolitter udskilles renalt og kan akkumuleres hos sådanne patienter i højere grad end normalt. Overvåg nøje for bivirkninger, der kunne indikere høj eksponering for bupropion eller metabolitter [se DOSERING OG ADMINISTRATION , KLINISK FARMAKOLOGI ].
Nedsat leverfunktion
Hos patienter med moderat til svært nedsat leverfunktion (Child-Pugh-score: 7 til 15), er den maksimale dosis af WELLBUTRIN 150 mg 75 mg dagligt. Hos patienter med let nedsat leverfunktion (Child-Pugh-score: 5 til 6), skal du overveje at reducere dosis og/eller doseringshyppighed [se DOSERING OG ADMINISTRATION , KLINISK FARMAKOLOGI ].
OVERDOSIS
Menneskelig overdosisoplevelse
Overdoser på op til 30 gram eller mere bupropion er blevet rapporteret. Anfald blev rapporteret i cirka en tredjedel af alle tilfælde. Andre alvorlige reaktioner rapporteret med overdoser af bupropion alene omfattede hallucinationer, bevidsthedstab, sinustakykardi og EKG-forandringer såsom ledningsforstyrrelser (inklusive QRS-forlængelse) eller arytmier. Feber, muskelstivhed, rabdomyolyse, hypotension, stupor, koma og respirationssvigt er primært blevet rapporteret, når bupropion var en del af flere lægemiddeloverdoser.
Selvom de fleste patienter kom sig uden følgesygdomme, er dødsfald forbundet med overdosering af bupropion alene blevet rapporteret hos patienter, der indtog store doser af lægemidlet. Flere ukontrollerede anfald, bradykardi, hjertesvigt og hjertestop før døden blev rapporteret hos disse patienter.
Overdoseringshåndtering
Kontakt et certificeret giftkontrolcenter for at få opdateret vejledning og rådgivning. Telefonnumre til certificerede giftkontrolcentre er angivet i Physician's Desk Reference (PDR). Ring på 1-800-222-1222 eller se www.poison.org.
Der er ingen kendte modgift mod bupropion. I tilfælde af en overdosis, yde støttende pleje, herunder tæt medicinsk overvågning og overvågning. Overvej muligheden for overdosering af flere lægemidler. Sørg for en tilstrækkelig luftvej, iltning og ventilation. Overvåg hjerterytmen og vitale tegn. Induktion af emesis anbefales ikke.
KONTRAINDIKATIONER
- WELLBUTRIN 150mg er kontraindiceret til patienter med anfald.
- WELLBUTRIN er kontraindiceret hos patienter med en aktuel eller tidligere diagnose af bulimi eller anorexia nervosa, da en højere forekomst af anfald blev observeret hos sådanne patienter behandlet med WELLBUTRIN [se ADVARSLER OG FORHOLDSREGLER ].
- WELLBUTRIN 300mg er kontraindiceret til patienter, der gennemgår brat seponering af alkohol, benzodiazepiner, barbiturater og antiepileptika [se ADVARSLER OG FORHOLDSREGLER , DRUGSINTERAKTIONER ].
- Brug af MAO-hæmmere (beregnet til behandling af psykiatriske lidelser) samtidig med WELLBUTRIN 300 mg eller inden for 14 dage efter seponering af behandling med WELLBUTRIN 150 mg er kontraindiceret. Der er en øget risiko for hypertensive reaktioner, når WELLBUTRIN anvendes samtidig med MAO-hæmmere. Brug af WELLBUTRIN inden for 14 dage efter seponering af behandling med en MAO-hæmmer er også kontraindiceret. Start med WELLBUTRIN 150 mg hos en patient behandlet med reversible MAO-hæmmere såsom linezolid eller intravenøs methylenblåt er kontraindiceret [se DOSERING OG ADMINISTRATION , ADVARSLER OG FORHOLDSREGLER , DRUGSINTERAKTIONER ].
- WELLBUTRIN er kontraindiceret til patienter med kendt overfølsomhed over for bupropion eller andre indholdsstoffer i WELLBUTRIN. Anafylaktoide/anafylaktiske reaktioner og Stevens-Johnsons syndrom er blevet rapporteret [se ADVARSLER OG FORHOLDSREGLER ].
KLINISK FARMAKOLOGI
Handlingsmekanisme
Den nøjagtige mekanisme for den antidepressive virkning af bupropion er ikke kendt, men formodes at være relateret til noradrenerge og/eller dopaminerge mekanismer. Bupropion er en relativt svag hæmmer af den neuronale genoptagelse af noradrenalin og dopamin og hæmmer ikke genoptagelsen af serotonin. Bupropion hæmmer ikke monoaminoxidase.
Farmakokinetik
Bupropion er en racemisk blanding. Den farmakologiske aktivitet og farmakokinetik af de individuelle enantiomerer er ikke blevet undersøgt. Den gennemsnitlige eliminationshalveringstid (±SD) for bupropion efter kronisk dosering er 21 (±9) timer, og steady-state plasmakoncentrationer af bupropion nås inden for 8 dage.
Absorption
Den absolutte biotilgængelighed af WELLBUTRIN hos mennesker er ikke blevet bestemt, fordi en intravenøs formulering til human brug ikke er tilgængelig. Det forekommer imidlertid sandsynligt, at kun en lille del af enhver oralt administreret dosis når det systemiske kredsløb intakt. I rotte- og hundeundersøgelser varierede biotilgængeligheden af bupropion fra 5 % til 20 %.
Hos mennesker opnås maksimale plasmakoncentrationer af bupropion normalt inden for 2 timer efter oral administration af WELLBUTRIN 300 mg. Plasma-bupropionkoncentrationer er dosisproportionale efter enkeltdoser på 100 til 250 mg; det vides dog ikke, om proportionaliteten mellem dosis og plasmaniveau opretholdes ved kronisk brug.
Fordeling
In vitro-tests viser, at bupropion er 84 % bundet til humane plasmaproteiner i koncentrationer op til 200 mcg/ml. Omfanget af proteinbinding af hydroxybupropionmetabolitten svarer til det for bupropion, hvorimod omfanget af proteinbinding af threohydrobupropionmetabolitten er omkring halvdelen af det, der ses med bupropion.
Metabolisme
Bupropion metaboliseres i vid udstrækning hos mennesker. Tre metabolitter er aktive: hydroxybupropion, som dannes ved hydroxylering af tert-butylgruppen i bupropion, og aminoalkoholisomererne threohydrobupropion og erythrohydrobupropion, som dannes ved reduktion af carbonylgruppen. In vitro-fund tyder på, at CYP2B6 er det vigtigste isoenzym involveret i dannelsen af hydroxybupropion, mens cytochrom P450-enzymer ikke er involveret i dannelsen af threohydrobupropion. Oxidation af bupropion-sidekæden resulterer i dannelsen af et glycinkonjugat af meta-chlorbenzoesyre, som derefter udskilles som den vigtigste urinmetabolit. Styrken og toksiciteten af metabolitterne i forhold til bupropion er ikke blevet fuldstændigt karakteriseret. Det er dog blevet påvist i en antidepressiv screeningstest hos mus, at hydroxybupropion er halvt så potent som bupropion, mens threohydrobupropion og erythrohydrobupropion er 5 gange mindre potente end bupropion. Dette kan være af klinisk betydning, fordi plasmakoncentrationerne af metabolitterne er lige så høje som eller højere end bupropions.
Efter en enkelt dosis til mennesker opstår maksimale plasmakoncentrationer af hydroxybupropion ca. 3 timer efter administration af WELLBUTRIN og er ca. 10 gange peak-niveauet for moderlægemidlet ved steady state. Eliminationshalveringstiden for hydroxybupropion er ca. 20 (±5) timer, og dens AUC ved steady state er ca. 17 gange større end for bupropion. Tiderne til maksimale koncentrationer for erythrohydrobupropion- og threohydrobupropion-metabolitterne er de samme som for hydroxybupropion-metabolitten. Deres eliminationshalveringstid er dog længere, henholdsvis 33 (±10) og 37 (±13) timer, og steady-state AUC'er er henholdsvis 1,5 og 7 gange større end for bupropion.
Bupropion og dets metabolitter udviser lineær kinetik efter kronisk administration af 300 til 450 mg/dag.
Elimination
Efter oral administration af 200 mg 14C-bupropion til mennesker blev 87 % og 10 % af den radioaktive dosis genfundet i henholdsvis urin og fæces. Kun 0,5 % af den orale dosis blev udskilt som uændret bupropion.
Specifikke populationer
Faktorer eller tilstande, der ændrer metabolisk kapacitet (f.eks. leversygdom, kongestiv hjertesvigt [CHF], alder, samtidig medicin osv.) eller eliminering kan forventes at påvirke graden og omfanget af akkumulering af de aktive metabolitter af bupropion. Elimineringen af hovedmetabolitterne af bupropion kan blive påvirket af nedsat nyre- eller leverfunktion, fordi de er moderat polære forbindelser og sandsynligvis vil gennemgå yderligere metabolisme eller konjugering i leveren før urinudskillelse.
Patienter med nedsat nyrefunktion
Der er begrænset information om bupropions farmakokinetik hos patienter med nedsat nyrefunktion. En sammenligning mellem undersøgelser mellem normale forsøgspersoner og forsøgspersoner med nyresvigt i slutstadiet viste, at Cmax- og AUC-værdierne for moderlægemidlet var sammenlignelige i de 2 grupper, hvorimod hydroxybupropion- og threohydrobupropion-metabolitterne havde en stigning på henholdsvis 2,3 og 2,8 gange. i AUC for forsøgspersoner med nyresvigt i slutstadiet. Et andet forsøg, der sammenlignede normale forsøgspersoner og forsøgspersoner med moderat til svær nyreinsufficiens (GFR 30,9 ± 10,8 ml/min) viste, at eksponeringen for bupropion var ca. 2 gange højere efter en enkelt dosis på 150 mg bupropion med langvarig frigivelse. hos forsøgspersoner med nedsat nyrefunktion, mens niveauerne af hydroxybupropion og threo/erythrohydrobupropion (kombineret) metabolitter var ens i de 2 grupper. Bupropion metaboliseres omfattende i leveren til aktive metabolitter, som metaboliseres yderligere og efterfølgende udskilles af nyrerne. Elimineringen af de vigtigste metabolitter af bupropion kan reduceres ved nedsat nyrefunktion. WELLBUTRIN bør anvendes med forsigtighed til patienter med nedsat nyrefunktion, og en reduceret frekvens og/eller dosis bør overvejes [se Brug i specifikke populationer ].
Patienter med nedsat leverfunktion
Virkningen af nedsat leverfunktion på farmakokinetikken af bupropion blev karakteriseret i 2 enkeltdosisforsøg, et hos forsøgspersoner med alkoholisk leversygdom og et hos forsøgspersoner med mild til svær cirrhose. Det første forsøg viste, at halveringstiden for hydroxybupropion var signifikant længere hos 8 forsøgspersoner med alkoholisk leversygdom end hos 8 raske frivillige (henholdsvis 32 ± 14 timer versus 21 ± 5 timer). Selvom det ikke er statistisk signifikant, var AUC'erne for bupropion og hydroxybupropion mere variable og havde en tendens til at være større (med 53 % til 57 %) hos frivillige med alkoholisk leversygdom. Forskellene i halveringstid for bupropion og de andre metabolitter i de 2 grupper var minimale.
Det andet forsøg viste ingen statistisk signifikante forskelle i farmakokinetikken af bupropion og dets aktive metabolitter hos 9 forsøgspersoner med mild til moderat levercirrhose sammenlignet med 8 raske frivillige. Der blev dog observeret mere variabilitet i nogle af de farmakokinetiske parametre for bupropion (AUC, Cmax og Tmax) og dets aktive metabolitter (t½) hos personer med mild til moderat levercirrhose. Hos personer med svær levercirrhose blev der set signifikante ændringer i farmakokinetikken af bupropion og dets metabolitter (tabel 3).
Patienter med venstre ventrikel dysfunktion
Under et kronisk doseringsforsøg med bupropion hos 14 deprimerede forsøgspersoner med venstre ventrikulær dysfunktion (historie med CHF eller et forstørret hjerte på røntgen), var der ingen synlig effekt på farmakokinetikken af bupropion eller dets metabolitter sammenlignet med raske frivillige.
Alder
Effekten af alder på farmakokinetikken af bupropion og dets metabolitter er ikke blevet fuldstændigt karakteriseret, men en undersøgelse af steady-state bupropionkoncentrationer fra adskillige depressionseffektivitetsforsøg, der involverede forsøgspersoner doseret i et interval på 300 til 750 mg/dag på en 3- tidsplan, viste ingen sammenhæng mellem alder (18 til 83 år) og plasmakoncentrationen af bupropion. Et enkeltdosis farmakokinetisk forsøg viste, at disponeringen af bupropion og dets metabolitter hos ældre forsøgspersoner svarede til den hos yngre forsøgspersoner. Disse data tyder på, at der ikke er nogen fremtrædende effekt af alder på bupropionkoncentrationen; et andet enkelt- og flerdosis farmakokinetisk forsøg antydede imidlertid, at ældre har øget risiko for ophobning af bupropion og dets metabolitter [se Brug i specifikke populationer ].
Mandlige og kvindelige patienter
Samlet analyse af bupropions farmakokinetiske data fra 90 raske mandlige og 90 raske kvindelige frivillige viste ingen kønsrelaterede forskelle i de maksimale plasmakoncentrationer af bupropion. Den gennemsnitlige systemiske eksponering (AUC) var ca. 13 % højere hos mandlige frivillige sammenlignet med kvindelige frivillige. Den kliniske betydning af dette fund er ukendt.
Rygere
Virkningerne af cigaretrygning på farmakokinetikken af bupropion blev undersøgt hos 34 raske mandlige og kvindelige frivillige; 17 var kroniske cigaretrygere og 17 var ikke-rygere. Efter oral administration af en enkelt dosis på 150 mg bupropion var der ingen statistisk signifikante forskelle i Cmax, halveringstid, Tmax, AUC eller clearance af bupropion eller dets aktive metabolitter mellem rygere og ikke-rygere.
Lægemiddelinteraktionsstudier
Potentiale for andre lægemidler til at påvirke WELLBUTRIN
In vitro undersøgelser indikerer, at bupropion primært metaboliseres til hydroxybupropion af CYP2B6. Derfor er der potentiale for lægemiddelinteraktioner mellem WELLBUTRIN og lægemidler, der er hæmmere eller inducere af CYP2B6. Derudover tyder in vitro undersøgelser på, at paroxetin, sertralin, norfluoxetin, fluvoxamin og nelfinavir hæmmer hydroxyleringen af bupropion.
Hæmmere af CYP2B6
Ticlopidin, Clopidogrel: I et forsøg med raske mandlige frivillige øgede clopidogrel 75 mg én gang dagligt eller ticlopidin 250 mg to gange dagligt eksponeringen (Cmax og AUC) af bupropion med 40 % og 60 % for clopidogrel og med 38 % og 85 % for ticlopidin. , henholdsvis. Eksponeringerne (Cmax og AUC) af hydroxybupropion blev reduceret med henholdsvis 50 % og 52 % af clopidogrel og 78 % og 84 %, henholdsvis med ticlopidin. Denne effekt menes at skyldes hæmningen af den CYP2B6-katalyserede bupropion-hydroxylering.
Prasugrel: Prasugrel er en svag hæmmer af CYP2B6. Hos raske forsøgspersoner øgede prasugrel bupropions Cmax og AUC værdier med henholdsvis 14 % og 18 % og reducerede Cmax og AUC værdierne for hydroxybupropion, en aktiv metabolit af bupropion, med henholdsvis 32 % og 24 %.
Cimetidin: Threohydrobupropion-metabolitten af bupropion synes ikke at blive produceret af cytokrom P450-enzymer. Effekten af samtidig administration af cimetidin på farmakokinetikken af bupropion og dets aktive metabolitter blev undersøgt hos 24 raske unge mandlige frivillige. Efter oral administration af bupropion 300 mg med og uden cimetidin 800 mg, var farmakokinetikken af bupropion og hydroxybupropion upåvirket. Der var dog 16 % og 32 % stigninger i henholdsvis AUC og Cmax for de kombinerede dele af threohydrobupropion og erythrohydrobupropion.
Citalopram: Citalopram påvirkede ikke farmakokinetikken af bupropion og dets tre metabolitter.
Inducere af CYP2B6
Ritonavir og Lopinavir: I et forsøg med raske frivillige reducerede ritonavir 100 mg to gange dagligt AUC og Cmax for bupropion med henholdsvis 22 % og 21 %. Eksponeringen af hydroxybupropionmetabolitten blev reduceret med 23 %, threohydrobupropion faldt med 38 %, og erythrohydrobupropion faldt med 48 %.
I et andet forsøg med raske frivillige reducerede ritonavir i en dosis på 600 mg to gange dagligt AUC og Cmax for bupropion med henholdsvis 66 % og 62 %. Eksponeringen af hydroxybupropionmetabolitten blev reduceret med 78 %, threohydrobupropion faldt med 50 %, og erythrohydrobupropion faldt med 68 %.
I et andet forsøg med raske frivillige reducerede lopinavir 400 mg/ritonavir 100 mg to gange dagligt bupropion AUC og Cmax med 57 %. AUC og Cmax for hydroxybupropion blev reduceret med henholdsvis 50 % og 31 %.
Efavirenz: I et forsøg med raske frivillige reducerede efavirenz 600 mg én gang dagligt i 2 uger AUC og Cmax for bupropion med henholdsvis ca. 55 % og 34 %. AUC for hydroxybupropion var uændret, hvorimod Cmax for hydroxybupropion var øget med 50 %.
Carbamazepin, Phenobarbital, Phenytoin: Selvom de ikke er systematisk undersøgt, kan disse lægemidler inducere metabolismen af bupropion.
Potentiale for WELLBUTRIN til at påvirke andre lægemidler
Dyredata indikerede, at bupropion kan være en inducer af lægemiddelmetaboliserende enzymer hos mennesker. I et forsøg, efter kronisk administration af bupropion 100 mg tre gange dagligt til 8 raske mandlige frivillige i 14 dage, var der ingen tegn på induktion af dets eget stofskifte. Ikke desto mindre kan der være potentiale for klinisk vigtige ændringer af blodniveauer af samtidig administrerede lægemidler.
Lægemidler metaboliseret af CYP2D6
In vitro er bupropion og dets metabolitter (erythrohydrobupropion, threohydrobupropion, hydroxybupropion) CYP2D6-hæmmere. I et klinisk forsøg med 15 mandlige forsøgspersoner (i alderen 19 til 35 år), som var omfattende metabolisatorer af CYP2D6, øgede bupropion 300 mg/dag efterfulgt af en enkelt dosis på 50 mg desipramin Cmax, AUC og t½ af desipramin med et gennemsnit på henholdsvis ca. 2-, 5- og 2-fold. Effekten var til stede i mindst 7 dage efter den sidste dosis bupropion. Samtidig brug af bupropion og andre lægemidler metaboliseret af CYP2D6 er ikke blevet formelt undersøgt.
Citalopram: Selvom citalopram ikke primært metaboliseres af CYP2D6, øgede bupropion i et forsøg Cmax og AUC for citalopram med henholdsvis 30 % og 40 %.
Lamotrigin: Flere orale doser af bupropion havde ingen statistisk signifikant effekt på enkeltdosis-farmakokinetikken af lamotrigin hos 12 raske frivillige.
Digoxin: Litteraturdata viste, at digoxineksponeringen blev reduceret, når en enkelt oral dosis på 0,5 mg digoxin blev administreret 24 timer efter en enkelt oral dosis af 150 mg bupropion med forlænget frigivelse hos raske frivillige.
Kliniske Studier
Effekten af WELLBUTRIN 150 mg til behandling af svær depressiv lidelse blev fastslået i to 4-ugers placebokontrollerede forsøg med voksne indlagte patienter med MDD (forsøg 1 og 2 i tabel 4) og i et 6-ugers placebokontrolleret forsøg i voksne ambulante patienter med MDD (forsøg 3 i tabel 4). I det første forsøg var dosisområdet for WELLBUTRIN 300 mg 300 mg til 600 mg/dag indgivet i 3 opdelte doser; 78 % af forsøgspersonerne blev behandlet med doser på 300 mg til 450 mg/dag. Forsøget demonstrerede effektiviteten af WELLBUTRIN 300 mg målt ved Hamilton Depression Rating Scale (HDRS) totalscore, HDRS-deprimeret stemningspunkt (punkt 1) og Clinical Global Impressions-severity-score (CGI-S). Det andet forsøg omfattede 2 doser WELLBUTRIN (300 og 450 mg/dag) og placebo. Dette forsøg viste effektiviteten af WELLBUTRIN 150 mg kun for dosis på 450 mg/dag. Effektresultaterne var statistisk signifikante for HDRS total score og CGI-S score, men ikke for HDRS punkt 1. I det tredje forsøg blev ambulante patienter behandlet med 300 mg/dag WELLBUTRIN. Dette forsøg demonstrerede effektiviteten af WELLBUTRIN 150 mg målt ved HDRS totalscore, HDRS Item 1, Montgomery-Asberg Depression Rating Scale (MADRS), CGI-S score og CGI-Improvement Scale (CGI-I) score . Effektiviteten af WELLBUTRIN 300 mg ved langtidsbrug, det vil sige i mere end 6 uger, er ikke blevet systematisk evalueret i kontrollerede forsøg.
PATIENTOPLYSNINGER
WELLBUTRIN (GOD byu-trin) (bupropion hydrochlorid) Tabletter
VIGTIGT: Sørg for at læse de tre afsnit i denne medicinvejledning. Det første afsnit handler om risikoen for selvmordstanker og -handlinger med antidepressiv medicin; det andet afsnit handler om risikoen for ændringer i tænkning og adfærd, depression og selvmordstanker eller handlinger med medicin, der bruges til at holde op med at ryge; og det tredje afsnit har titlen "Hvilke andre vigtige oplysninger skal jeg vide om WELLBUTRIN 150mg?"
Antidepressiv medicin, depression og andre alvorlige psykiske sygdomme og selvmordstanker eller -handlinger
Dette afsnit af Medicinvejledningen handler kun om risikoen for selvmordstanker og -handlinger med antidepressiv medicin.
Hvad er den vigtigste information, jeg bør vide om antidepressiv medicin, depression og andre alvorlige psykiske sygdomme og selvmordstanker eller -handlinger?
1. Antidepressiv medicin kan øge risikoen for selvmordstanker eller -handlinger hos nogle børn, teenagere eller unge voksne inden for de første måneder af behandlingen.
2. Depression eller andre alvorlige psykiske sygdomme er de vigtigste årsager til selvmordstanker og -handlinger. Nogle mennesker kan have en særlig høj risiko for at få selvmordstanker eller -handlinger. Disse omfatter personer, der har (eller har en familiehistorie med) bipolar sygdom (også kaldet maniodepressiv sygdom) eller selvmordstanker eller -handlinger.
3. Hvordan kan jeg holde øje med og forsøge at forhindre selvmordstanker og -handlinger hos mig selv eller et familiemedlem?
- Vær meget opmærksom på ændringer, især pludselige ændringer, i humør, adfærd, tanker eller følelser. Dette er meget vigtigt, når en antidepressiv medicin startes, eller når dosis ændres.
- Ring til din læge med det samme for at rapportere nye eller pludselige ændringer i humør, adfærd, tanker eller følelser.
- Hold alle opfølgende besøg hos din sundhedsplejerske som planlagt. Ring til lægen mellem besøgene efter behov, især hvis du har bekymringer om symptomer.
Ring til din læge med det samme, hvis du eller dit familiemedlem har nogle af følgende symptomer, især hvis de er nye, værre eller bekymrer dig:
- tanker om selvmord eller døende
- forsøg på at begå selvmord
- ny eller værre depression
- ny eller værre angst
- føler sig meget ophidset eller rastløs
- Angstanfald
- søvnbesvær (søvnløshed)
- ny eller værre irritabilitet
- opfører sig aggressivt, er vred eller voldelig
- handler på farlige impulser
- en ekstrem stigning i aktivitet og tale (mani)
- andre usædvanlige ændringer i adfærd eller humør
Hvad skal jeg ellers vide om antidepressiv medicin?
- Stop aldrig en antidepressiv medicin uden først at tale med en læge. Hvis du pludselig stopper en antidepressiv medicin, kan det forårsage andre symptomer.
- Antidepressiva er medicin, der bruges til at behandle depression og andre sygdomme. Det er vigtigt at diskutere alle risiciene ved behandling af depression og også risiciene ved ikke at behandle den. Patienter og deres familier eller andre pårørende bør diskutere alle behandlingsvalg med sundhedsudbyderen, ikke kun brugen af antidepressiva.
- Antidepressiv medicin har andre bivirkninger. Tal med lægen om bivirkningerne af den medicin, der er ordineret til dig eller dit familiemedlem.
- Antidepressiv medicin kan interagere med anden medicin. Kend alle de lægemidler, du eller dit familiemedlem tager. Hold en liste over alle lægemidler for at vise sundhedsudbyderen. Start ikke med ny medicin uden først at tjekke med din læge.
Det vides ikke, om WELLBUTRIN er sikkert og effektivt til børn under 18 år.
Rygestop, rygestop, medicin, ændringer i tankegang og adfærd, depression og selvmordstanker eller -handlinger
Dette afsnit af medicinvejledningen handler kun om risikoen for ændringer i tænkning og adfærd, depression og selvmordstanker eller handlinger med stoffer, der bruges til at holde op med at ryge. Selvom WELLBUTRIN ikke er en behandling for rygestop, indeholder den den samme aktive ingrediens (bupropionhydrochlorid) som ZYBAN, der bruges til at hjælpe patienter med at holde op med at ryge.
Tal med din sundhedsplejerske eller dit familiemedlems sundhedsplejerske om:
- alle risici og fordele ved at holde op med at ryge medicin.
- alle behandlingsvalg for rygestop.
Når du forsøger at holde op med at ryge, med eller uden bupropion, kan du have symptomer, der kan skyldes nikotinabstinenser, herunder:
- trang til at ryge
- frustration
- rastløshed
- nedtrykt humør
- vrede
- nedsat puls
- problemer med at sove
- føler sig angst
- øget appetit
- irritabilitet
- koncentrationsbesvær
- vægtøgning
Nogle mennesker har endda oplevet selvmordstanker, når de forsøgte at holde op med at ryge uden medicin.
Nogle gange kan rygestop føre til forværring af psykiske problemer, som du allerede har, såsom depression.
Nogle mennesker har haft alvorlige bivirkninger, mens de har taget bupropion for at hjælpe dem med at holde op med at ryge, herunder: Nye eller værre psykiske problemer, såsom ændringer i adfærd eller tænkning, aggression, fjendtlighed, agitation, depression eller selvmordstanker eller -handlinger. Nogle mennesker havde disse symptomer, da de begyndte at tage bupropion, og andre udviklede dem efter flere ugers behandling eller efter at have stoppet bupropion. Disse symptomer forekom oftere hos personer, der havde en historie med psykiske problemer, før de tog bupropion, end hos personer uden en historie med psykiske problemer.
Stop med at tage WELLBUTRIN og ring til din læge med det samme, hvis du, din familie eller pårørende bemærker nogen af disse symptomer. Samarbejd med din læge for at beslutte, om du skal fortsætte med at tage WELLBUTRIN. Hos mange mennesker forsvandt disse symptomer efter at have stoppet WELLBUTRIN 300 mg, men hos nogle mennesker fortsatte symptomerne efter at have stoppet WELLBUTRIN. Det er vigtigt for dig at følge op med din læge, indtil dine symptomer forsvinder. Inden du tager WELLBUTRIN 150mg, skal du fortælle din læge, hvis du nogensinde har haft depression eller andre psykiske problemer. Du bør også fortælle din sundhedsplejerske om eventuelle symptomer, du havde under andre gange, du forsøgte at holde op med at ryge, med eller uden bupropion.
Hvilke andre vigtige oplysninger skal jeg vide om WELLBUTRIN?
- Anfald: Der er en chance for at få et anfald (kramper, anfald) med WELLBUTRIN 150 mg, især hos mennesker:
- med visse medicinske problemer.
- som tager visse lægemidler. Chancen for at få anfald øges med højere doser af WELLBUTRIN. For mere information, se afsnittene "Hvem bør ikke tage WELLBUTRIN?" og "Hvad skal jeg fortælle min sundhedsplejerske, før jeg tager WELLBUTRIN 300mg?" Fortæl din sundhedsudbyder om alle dine medicinske tilstande og al den medicin, du tager. Tag ikke anden medicin, mens du tager WELLBUTRIN 150mg, medmindre din læge har sagt, at det er okay at tage dem. Hvis du får et anfald, mens du tager WELLBUTRIN, skal du stoppe med at tage tabletterne og kontakte din læge med det samme. Tag ikke WELLBUTRIN 150mg igen, hvis du har et anfald.
- Højt blodtryk (hypertension). Nogle mennesker får forhøjet blodtryk, der kan være alvorligt, mens de tager WELLBUTRIN. Chancen for forhøjet blodtryk kan være højere, hvis du også bruger nikotinerstatningsterapi (såsom et nikotinplaster) for at hjælpe dig med at holde op med at ryge (se afsnittet i denne medicinvejledning kaldet "Hvordan skal jeg tage WELLBUTRIN 150mg?").
- Maniske episoder. Nogle mennesker kan have perioder med mani, mens de tager WELLBUTRIN 300mg, herunder:
- Kraftigt øget energi
- Alvorlige søvnbesvær
- Racing tanker
- Hensynsløs opførsel
- Usædvanligt store ideer
- Overdreven lykke eller irritabilitet
- Tal mere eller hurtigere end normalt Hvis du har nogen af ovenstående symptomer på mani, skal du ringe til din læge.
- Usædvanlige tanker eller adfærd. Nogle patienter har usædvanlige tanker eller adfærd, mens de tager WELLBUTRIN, herunder vrangforestillinger (tror, du er en anden), hallucinationer (at se eller høre ting, der ikke er der), paranoia (føle, at folk er imod dig) eller at føle dig forvirret. Hvis dette sker for dig, skal du ringe til din læge.
- Visuelle problemer.
- øjensmerter
- ændringer i synet
- hævelse eller rødme i eller omkring øjet Kun nogle mennesker har risiko for disse problemer. Det kan være en god idé at gennemgå en øjenundersøgelse for at se, om du er i fare, og få forebyggende behandling, hvis du er det.
- Alvorlige allergiske reaktioner. Nogle mennesker kan have alvorlige allergiske reaktioner over for WELLBUTRIN. Stop med at tage WELLBUTRIN 300mg og ring til din læge med det samme hvis du får udslæt, kløe, nældefeber, feber, hævede lymfekirtler, smertefulde sår i munden eller omkring øjnene, hævelse af læber eller tunge, brystsmerter eller har problemer med at trække vejret. Disse kan være tegn på en alvorlig allergisk reaktion.
Hvad er WELLBUTRIN?
WELLBUTRIN er en receptpligtig medicin, der bruges til at behandle voksne med en bestemt type depression kaldet svær depressiv lidelse.
Hvem bør ikke tage WELLBUTRIN 150mg?
Tag ikke WELLBUTRIN, hvis du
- har eller har haft en anfaldssygdom eller epilepsi.
- har eller haft en spiseforstyrrelse såsom anorexia nervosa eller bulimi.
- tager anden medicin, der indeholder bupropion, inklusive ZYBAN (bruges til at hjælpe folk med at holde op med at ryge), WELLBUTRIN 300mg SR, WELLBUTRIN 150mg XL, APLENZIN eller FORFIVO XL. Bupropion er den samme aktive ingrediens, som er i WELLBUTRIN.
- drikker meget alkohol og holder pludselig op med at drikke, eller brug medicin kaldet beroligende midler (disse gør dig søvnig), benzodiazepiner eller medicin mod anfald, og du holder pludselig op med at bruge dem.
- tage en monoaminoxidasehæmmer (MAOI). Spørg din læge eller apotekspersonalet, hvis du ikke er sikker på, om du tager en MAO-hæmmer, inklusive antibiotikummet linezolid.
- tag ikke en MAO-hæmmer inden for 2 uger efter at have stoppet WELLBUTRIN, medmindre din læge har bedt dig om det.
- start ikke med WELLBUTRIN 150 mg, hvis du stoppede med at tage en MAO-hæmmer inden for de sidste 2 uger, medmindre din læge har bedt dig om det.
- er allergisk over for den aktive ingrediens i WELLBUTRIN 300mg, bupropion eller over for nogen af de inaktive ingredienser. Se slutningen af denne medicinvejledning for en komplet liste over ingredienser i WELLBUTRIN.
Hvad skal jeg fortælle min læge, før jeg tager WELLBUTRIN?
Fortæl din læge, hvis du nogensinde har haft depression, selvmordstanker eller -handlinger eller andre psykiske problemer. Se "Antidepressiv medicin, depression og andre alvorlige psykiske sygdomme og selvmordstanker eller -handlinger."
- Fortæl din sundhedsplejerske om dine andre medicinske tilstande, herunder hvis du:
- har leverproblemer, især skrumpelever.
- har nyreproblemer.
- har eller har haft en spiseforstyrrelse, såsom anorexia nervosa eller bulimi.
- har haft en hovedskade.
- har haft et anfald (kramper, anfald).
- har en tumor i dit nervesystem (hjerne eller rygsøjle).
- har haft et hjerteanfald, hjerteproblemer eller forhøjet blodtryk.
- er en diabetiker, der tager insulin eller anden medicin for at kontrollere dit blodsukker.
- drik alkohol.
- misbruge receptpligtig medicin eller gademedicin.
- er gravid eller planlægger at blive gravid. Tal med din læge om risikoen for dit ufødte barn, hvis du tager WELLBUTRIN 300mg under graviditet.
- Fortæl det til din læge, hvis du bliver gravid eller tror, du er gravid under behandling med WELLBUTRIN.
- Hvis du bliver gravid under behandling med WELLBUTRIN, skal du tale med din læge om tilmelding til det nationale graviditetsregister for antidepressiva. Du kan tilmelde dig ved at ringe til 1-844-405-6185.
- ammer eller planlægger at amme under behandling med WELLBUTRIN. WELLBUTRIN udskilles i din mælk. Tal med din læge om den bedste måde at fodre din baby på under behandling med WELLBUTRIN.
Fortæl din læge om al den medicin, du tager, herunder receptpligtig medicin, håndkøbsmedicin, vitaminer og naturlægemidler. Mange lægemidler øger dine chancer for at få anfald eller andre alvorlige bivirkninger, hvis du tager dem, mens du tager WELLBUTRIN.
Hvordan skal jeg tage WELLBUTRIN 300mg?
- Tag WELLBUTRIN 300mg nøjagtigt som foreskrevet af din læge. Du må ikke ændre din dosis eller stoppe med at tage WELLBUTRIN uden først at tale med din læge.
- Synk WELLBUTRIN tabletter hele. WELLBUTRIN 300mg tabletter må ikke tygges, skæres eller knuses.
- Tag WELLBUTRIN 300 mg på samme tidspunkt hver dag.
- Tag dine doser af WELLBUTRIN 300 mg med mindst 6 timers mellemrum.
- Du kan tage WELLBUTRIN med eller uden mad.
- Hvis du glemmer en dosis, må du ikke tage en ekstra dosis for at kompensere for den glemte dosis. Vent og tag din næste dosis på det normale tidspunkt. Dette er meget vigtigt. For meget WELLBUTRIN kan øge din chance for at få et anfald.
- Hvis du tager for meget WELLBUTRIN eller overdosis, skal du ringe til din lokale skadestue eller giftkontrolcenter med det samme.
- Tag ikke anden medicin, mens du tager WELLBUTRIN 300mg, medmindre din læge har fortalt dig, at det er i orden.
- Hvis du tager WELLBUTRIN 150 mg til behandling af svær depressiv lidelse, kan det tage flere uger, før du føler, at WELLBUTRIN 150 mg virker. Når du har det bedre, er det vigtigt at blive ved med at tage WELLBUTRIN nøjagtigt som anvist af din læge. Ring til din læge, hvis du ikke føler, at WELLBUTRIN virker for dig.
Hvad skal jeg undgå, mens jeg tager WELLBUTRIN 300mg?
- Begræns eller undgå brug af alkohol under behandling med WELLBUTRIN. Hvis du normalt drikker meget alkohol, skal du tale med din læge, før du pludselig stopper. Hvis du pludselig holder op med at drikke alkohol, kan du øge din risiko for at få anfald.
- Kør ikke bil eller brug tunge maskiner, før du ved, hvordan WELLBUTRIN 150 mg påvirker dig. WELLBUTRIN kan påvirke din evne til at gøre disse ting sikkert.
Hvad er mulige bivirkninger af WELLBUTRIN 300mg?
WELLBUTRIN kan forårsage alvorlige bivirkninger. Se afsnittene i begyndelsen af denne medicinvejledning for information om alvorlige bivirkninger af WELLBUTRIN.
De mest almindelige bivirkninger af WELLBUTRIN omfatter:
- nervøsitet
- kraftig svedtendens
- tør mund
- rysten (rysten)
- forstoppelse
- problemer med at sove
- hovedpine
- sløret syn
- kvalme eller opkastning
- hurtig hjerterytme
- svimmelhed
Hvis du har kvalme, skal du tage din medicin sammen med mad. Hvis du har problemer med at sove, må du ikke tage din medicin for tæt på sengetid.
Fortæl din læge med det samme om eventuelle bivirkninger, der generer dig.
Disse er ikke alle mulige bivirkninger af WELLBUTRIN. For mere information, spørg din læge eller apotek.
Ring til din læge for at få medicinsk rådgivning om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Du kan også indberette bivirkninger til GlaxoSmithKline på 1-888-825-5249.
Hvordan skal jeg opbevare WELLBUTRIN 300mg?
- Opbevar WELLBUTRIN ved stuetemperatur mellem 68°F og 77°F (20°C til 25°C).
- Opbevar WELLBUTRIN-tabletter tørre og ude af lys.
Opbevar WELLBUTRIN og al medicin utilgængeligt for børn.
Generel information om sikker og effektiv brug af WELLBUTRIN.
Lægemidler ordineres nogle gange til andre formål end dem, der er anført i en medicinvejledning. Brug ikke WELLBUTRIN 300mg til en tilstand, som det ikke er ordineret til. Giv ikke WELLBUTRIN til andre mennesker, selvom de har de samme symptomer, som du har. Det kan skade dem.
Hvis du tager en urinstofscreeningstest, kan WELLBUTRIN gøre testresultatet positivt for amfetamin. Hvis du fortæller den person, der giver dig lægemiddelscreeningstesten, at du tager WELLBUTRIN 300mg, kan de lave en mere specifik lægemiddelscreeningstest, som ikke burde have dette problem.
Denne medicinvejledning opsummerer vigtig information om WELLBUTRIN. Hvis du vil have mere information, så tal med din sundhedsplejerske. Du kan bede din sundhedsplejerske eller dit apotek om oplysninger om WELLBUTRIN, der er skrevet til sundhedspersonale.
For mere information om WELLBUTRIN, ring på 1-888-825-5249.
Hvad er ingredienserne i WELLBUTRIN 300mg?
Aktiv ingrediens: bupropionhydrochlorid.
Inaktive ingredienser: 75 mg tablet - D&C Yellow No. 10 Lake, FD&C Yellow No. 6 Lake, hydroxypropylcellulose, hypromellose, mikrokrystallinsk cellulose, polyethylenglycol, talkum og titaniumdioxid; 100 mg tablet - FD&C Red No. 40 Lake, FD&C Yellow No. 6 Lake, hydroxypropylcellulose, hypromellose, mikrokrystallinsk cellulose, polyethylenglycol, talkum og titaniumdioxid.
Denne medicinvejledning er godkendt af US Food and Drug Administration.
