Paxil 10mg, 20mg, 30mg, 40mg Paroxetine Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Paxil, og hvordan bruges det?
Paxil 20mg er en receptpligtig medicin, der bruges til at behandle symptomer på depression, obsessiv-kompulsiv lidelse (OCD), panikangst, social fobi, generaliseret angstlidelse, posttraumatisk stresslidelse (PTSD) og præmenstruelle dysohoriske lidelser (PMDD). Paxil kan bruges alene eller sammen med anden medicin.
- Paxil 40mg tilhører en klasse af lægemidler kaldet antidepressiva, SSRI'er.
- Det vides ikke, om Paxil er sikkert og effektivt til børn.
Hvad er de mulige bivirkninger af Paxil 30mg?
Paxil 10mg kan forårsage alvorlige bivirkninger, herunder:
- race tanker,
- nedsat søvnbehov,
- usædvanlig risikoopførsel,
- følelser af ekstrem lykke eller tristhed,
- være mere snakkesalig end normalt,
- sløret syn,
- tunnelsyn,
- øjensmerter eller hævelse,
- ser glorier omkring lys,
- usædvanlige knoglesmerter eller ømhed, hævelse eller blå mærker,
- ændringer i vægt,
- ændringer i appetit,
- let blå mærker,
- usædvanlig blødning fra din næse, mund, skede eller endetarm,
- hoste blod op,
- meget stive eller stive muskler,
- høj feber,
- svedeture,
- forvirring,
- hurtige eller ujævne hjerteslag,
- rystelser,
- besvimelse,
- hovedpine,
- forvirring,
- utydelig tale,
- svær svaghed,
- tab af koordination, og
- føler sig ustabil
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Paxil 30mg omfatter:
- synsforandringer,
- svaghed,
- døsighed,
- svimmelhed,
- træthed,
- svedeture,
- angst,
- ryster,
- søvnproblemer (søvnløshed),
- mistet appetiten,
- kvalme,
- opkastning,
- diarré,
- forstoppelse,
- tør mund,
- infektion,
- hovedpine,
- nedsat sexlyst,
- impotens,
- unormal ejakulation, og
- svært ved at få orgasme
Suicidalitet og antidepressive stoffer
Antidepressiva øgede risikoen sammenlignet med placebo for selvmordstanker og -adfærd (suicidalitet) hos børn, unge og unge voksne i korttidsstudier af svær depressiv lidelse (MDD) og andre psykiatriske lidelser. Enhver, der overvejer at bruge PAXIL 40 mg eller ethvert andet antidepressivt middel til et barn, en teenager eller en ung voksen, skal balancere denne risiko med det kliniske behov. Korttidsundersøgelser viste ikke en stigning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne efter 24 år; der var en reduktion i risikoen med antidepressiva sammenlignet med placebo hos voksne på 65 år og derover. Depression og visse andre psykiatriske lidelser er i sig selv forbundet med øget risiko for selvmord. Patienter i alle aldre, der påbegyndes med antidepressiv behandling, bør overvåges passende og observeres nøje for klinisk forværring, suicidalitet eller usædvanlige ændringer i adfærd. Familier og pårørende bør informeres om behovet for tæt observation og kommunikation med den ordinerende læge. PAXIL 30mg er ikke godkendt til brug hos pædiatriske patienter. (Se ADVARSLER: Klinisk forværring og selvmordsrisiko, PATIENTINFORMATION og FORHOLDSREGLER: Pædiatrisk brug.)
BESKRIVELSE
PAXIL (paroxetinhydrochlorid) er et oralt indgivet psykotropt lægemiddel. Det er hydrochloridsaltet af en phenylpiperidinforbindelse identificeret kemisk som (-)-trans-4R-(4'fluorphenyl)-3S-[(3',4'-methylendioxyphenoxy)methyl]piperidinhydrochloridhemihydrat og har den empiriske formel C19H20FNO3•HCl•½H2O. Molekylvægten er 374,8 (329,4 som en fri base). Strukturformlen for paroxetinhydrochlorid er:
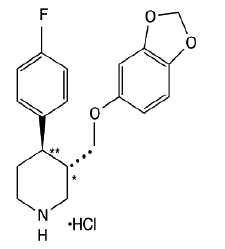
Paroxetinhydrochlorid er et lugtfrit, råhvidt pulver med et smeltepunktsområde på 120° til 138°C og en opløselighed på 5,4 mg/ml i vand.
Hver filmovertrukket tablet indeholder paroxetinhydrochlorid svarende til paroxetin som følger: 10 mg-gul (skåren); 20 mg-lyserød (bedømt); 30 mg-blå, 40 mg-grøn. Inaktive ingredienser består af dibasisk calciumphosphatdihydrat, hypromellose, magnesiumstearat, polyethylenglycoler, polysorbat 80, natriumstivelsesglykolat, titaniumdioxid og 1 eller flere af følgende: D&C Red No. 30 aluminium lake, D&C Yellow No. 10 aluminum lake , FD&C Blå nr. 2 aluminiumssø, FD&C Gul nr. 6 aluminiumssø.
Suspension til oral administration
Hver 5 ml orangefarvet væske med orange smag indeholder paroxetinhydrochlorid svarende til paroxetin, 10 mg. Inaktive ingredienser består af polacrilin kalium, mikrokrystallinsk cellulose, propylenglycol, glycerin, sorbitol, methylparaben, propylparaben, natriumcitrat dihydrat, citronsyre vandfri, natriumsaccharin, smagsstoffer, FD&C Yellow No. 6 aluminium lake, og simethicone emulsion, USP.
INDIKATIONER
PAXIL 20mg er indiceret til voksne til behandling af:
- Major depressiv lidelse (MDD)
- Obsessiv-kompulsiv lidelse (OCD)
- Panikangst (PD)
- Social angstlidelse (SAD)
- Generaliseret angstlidelse (GAD)
- Posttraumatisk stresslidelse (PTSD)
DOSERING OG ADMINISTRATION
Administrationsoplysninger
Administrer PAXIL som en enkelt daglig dosis om morgenen, med eller uden mad.
Ryst den orale suspension godt før administration.
Anbefalet dosering til MDD, OCD, PD og PTSD
De anbefalede startdoser og maksimale doser af PAXIL 20 mg til patienter med MDD, OCD, PD og PTSD er vist i tabel 1.
Hos patienter med utilstrækkelig respons øges dosis i trin på 10 mg dagligt med intervaller på mindst 1 uge, afhængig af tolerabilitet.
Anbefalet dosering til SAD og GAD
TRIST
Startdosis og anbefalet dosis til patienter med SAD er 20 mg dagligt. I kliniske forsøg blev effektiviteten af PAXIL 30 mg påvist hos patienter doseret i et interval på 20 mg til 60 mg dagligt. Selvom sikkerheden af PAXIL er blevet evalueret hos patienter med SAD ved doser op til 60 mg dagligt, tyder tilgængelig information ikke på nogen yderligere fordel for doser over 20 mg dagligt [se Kliniske Studier ].
GAD
Startdosis og anbefalet dosis til patienter med GAD er 20 mg dagligt. I kliniske forsøg blev effektiviteten af PAXIL 10 mg i GAD påvist hos patienter doseret i et interval på 20 mg til 50 mg dagligt. Der er ikke tilstrækkelig evidens til at foreslå en større fordel ved doser højere end 20 mg dagligt [se Kliniske Studier ].
Hos patienter med utilstrækkelig respons øges dosis i trin på 10 mg dagligt med intervaller på mindst 1 uge, afhængig af tolerabilitet.
Skærm for bipolar lidelse før start af PAXIL
Inden påbegyndelse af behandling med PAXIL 10mg eller et andet antidepressivum skal patienter screenes for en personlig eller familiehistorie med bipolar lidelse, mani eller hypomani [se ADVARSLER OG FORHOLDSREGLER ].
Anbefalet dosering til ældre patienter, patienter med svært nedsat nyrefunktion og patienter med svært nedsat leverfunktion
Den anbefalede startdosis er 10 mg dagligt til ældre patienter, patienter med svært nedsat nyrefunktion og patienter med svært nedsat leverfunktion. Dosis bør ikke overstige 40 mg/dag.
At skifte patienter til eller fra en monoaminoxidasehæmmer (MAOI)
Der skal gå mindst 14 dage mellem seponering af en monoaminoxidasehæmmer (MAO-hæmmer og påbegyndelse af PAXIL. Derudover skal der gå mindst 14 dage efter ophør med PAXIL, før man starter et MAO-antidepressivt middel [se KONTRAINDIKATIONER , ADVARSLER OG FORHOLDSREGLER ].
Seponering af behandling med PAXIL
Bivirkninger kan forekomme ved seponering af PAXIL [se ADVARSLER OG FORHOLDSREGLER ]. Reducer gradvist dosis i stedet for at stoppe PAXIL brat, når det er muligt.
HVORDAN LEVERET
Doseringsformer og styrker
PAXIL tabletter findes som:
- 10 mg gul tablet med delekærv indgraveret på forsiden med "PAXIL" og på bagsiden med "10".
- 20 mg lyserød tablet med delekærv indgraveret på forsiden med "PAXIL" og på bagsiden med "20".
- 30 mg blå tablet præget på forsiden med "PAXIL" og på bagsiden med "30".
- 40 mg grøn tablet indgraveret på forsiden med "PAXIL" og på bagsiden med "40".
PAXIL 20 mg oral suspension findes som:
- 10 mg/5 ml orangefarvet suspension med orange smag i flasker indeholdende 250 ml.
Opbevaring og håndtering
PAXIL (paroxetin) tabletter er ovale tabletter, der leveres som:
Opbevar tabletter mellem 15° og 30°C (59° og 86°F).
PAXIL (paroxetin) oral suspension leveres som:
Opbevar suspension ved eller under 25°C (77°F)
Fremstillet af: Apotex Inc., Toronto, Ontario, Canada M9L 1T9. Revideret: februar 2021
BIVIRKNINGER
Følgende bivirkninger er inkluderet mere detaljeret i andre afsnit af ordinationsinformationen:
- Overfølsomhedsreaktioner over for paroxetin [se KONTRAINDIKATIONER ]
- Selvmordstanker og -adfærd [se ADVARSLER OG FORHOLDSREGLER ]
- Serotoninsyndrom [se ADVARSLER OG FORHOLDSREGLER ]
- Embryofetal og neonatal toksicitet [se ADVARSLER OG FORHOLDSREGLER ]
- Øget risiko for blødning [se ADVARSLER OG FORHOLDSREGLER ]
- Aktivering af mani/hypomani [se ADVARSLER OG FORHOLDSREGLER ]
- Afbrydelsessyndrom [se ADVARSLER OG FORHOLDSREGLER ]
- Anfald [se ADVARSLER OG FORHOLDSREGLER ]
- Vinkellukkende glaukom [se ADVARSLER OG FORHOLDSREGLER ]
- Hyponatriæmi [se ADVARSLER OG FORHOLDSREGLER ]
- Knoglebrud [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring med kliniske forsøg
Fordi kliniske forsøg udføres under vidt forskellige forhold, kan bivirkningsrater observeret i de kliniske forsøg med et lægemiddel ikke direkte sammenlignes med hastigheder i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de frekvenser, der observeres i praksis.
Sikkerhedsdataene for PAXIL er fra:
- 6-ugers kliniske forsøg med MDD-patienter, der fik PAXIL 20 mg til 50 mg én gang dagligt
- 12-ugers kliniske forsøg med OCD-patienter, som fik PAXIL 20 mg til 60 mg én gang dagligt
- 10- til 12-ugers kliniske forsøg med PD-patienter, der fik PAXIL 10 mg til 60 mg én gang dagligt
- 12-ugers kliniske forsøg med SAD-patienter, som fik PAXIL 20 mg til 50 mg én gang dagligt
- 8-ugers kliniske forsøg med GAD-patienter, der fik PAXIL 10 mg til 50 mg én gang dagligt
- 12-ugers kliniske forsøg med PTSD-patienter, der fik PAXIL 20 mg til 50 mg én gang dagligt
Bivirkninger, der fører til seponering
Tyve procent (1.199/6.145) af patienter behandlet med PAXIL i kliniske forsøg i MDD og 16,1% (84/522), 11,8% (64/542), 9,4% (44/469), 10,7% (79/735), og 11,7 % (79/676) af patienter behandlet med PAXIL i kliniske forsøg med henholdsvis SAD, OCD, PD, GAD og PTSD afbrød behandlingen på grund af en bivirkning. De mest almindelige bivirkninger (≥1 %) i forbindelse med seponering (dvs. de bivirkninger, der er forbundet med frafald med en hastighed på ca. to gange eller mere for PAXIL 10 mg sammenlignet med placebo) er vist i tabel 3:
Mest almindelige bivirkninger
De mest almindeligt observerede bivirkninger forbundet med brugen af PAXIL (hyppighed på 5 % eller mere og mindst det dobbelte af placebo) var:
MDD
Asteni, svedtendens, kvalme, nedsat appetit, somnolens, svimmelhed, søvnløshed, tremor, nervøsitet, ejakulationsforstyrrelser og andre mandlige kønsorganer.
OCD
Kvalme, mundtørhed, nedsat appetit, forstoppelse, svimmelhed, somnolens, tremor, svedtendens, impotens og unormal ejakulation.
PD
Asteni, svedtendens, nedsat appetit, nedsat libido, tremor, unormal ejakulation, kvindelige kønsorganer og impotens.
TRIST
Sveden, kvalme, mundtørhed, forstoppelse, nedsat appetit, somnolens, tremor, nedsat libido, gaben, unormal ejakulation, kvindelige kønsorganer og impotens.
GAD
Asteni, infektion, forstoppelse, nedsat appetit, mundtørhed, kvalme, nedsat libido, somnolens, tremor, svedtendens og unormal ejakulation.
PTSD
Asteni, svedtendens, kvalme, mundtørhed, diarré, nedsat appetit, somnolens, nedsat libido, unormal ejakulation, kvindelige kønsorganer og impotens.
Bivirkninger hos patienter med MDD
Tabel 4 viser de bivirkninger, der opstod med en incidens på 1 % eller mere og mere end placebo i kliniske forsøg med PAXIL-behandlede patienter med MDD.
Bivirkninger hos patienter med OCD, PD og SAD
Tabel 5 viser bivirkninger, der opstod med en frekvens på 2 % eller mere i kliniske forsøg hos patienter med OCD, PD og SAD.
Bivirkninger hos patienter med GAD og PTSD
Tabel 6 viser bivirkninger, der opstod med en frekvens på 2 % eller mere i kliniske forsøg hos patienter med GAD og PTSD.
Dosisafhængige bivirkninger
MDD
En sammenligning af bivirkningsrater i et fastdosisstudie, der sammenlignede PAXIL 10 mg, 20 mg, 30 mg og 40 mg én gang dagligt med placebo i behandlingen af MDD afslørede dosisafhængige bivirkninger, som vist i tabel 7:
OCD
I en fastdosisundersøgelse, der sammenlignede placebo og PAXIL 20 mg, 40 mg og 60 mg i behandlingen af OCD, var der ingen klar sammenhæng mellem bivirkninger og den dosis af PAXIL 30 mg, som patienterne blev tildelt.
PD
et studie med fast dosis, der sammenlignede placebo og PAXIL 10 mg, 20 mg og 40 mg til behandling af PD, blev følgende bivirkninger vist at være dosisafhængige: asteni, mundtørhed, angst, nedsat libido, tremor og unormal ejakulation.
TRIST
I et studie med fast dosis, der sammenlignede placebo og PAXIL 20 mg, 40 mg og 60 mg i behandlingen af SAD, var der for de fleste af bivirkningerne ingen klar sammenhæng mellem bivirkninger og den dosis af PAXIL 10 mg, som patienterne blev tildelt. .
GAD
I en fastdosisundersøgelse, der sammenlignede placebo og PAXIL 20 mg og 40 mg i behandlingen af GAD, blev følgende bivirkninger vist at være dosisafhængige: asteni, forstoppelse og unormal ejakulation.
PTSD
I en fastdosisundersøgelse, der sammenlignede placebo og PAXIL 20 mg og 40 mg i behandlingen af PTSD, blev følgende bivirkninger vist at være dosisafhængige: impotens og unormal ejakulation.
Mandlig og kvindelig seksuel dysfunktion
Selvom ændringer i seksuel lyst, seksuel præstation og seksuel tilfredsstillelse ofte forekommer som manifestationer af en psykiatrisk lidelse, kan de også være en konsekvens af SSRI-behandling. Pålidelige skøn over forekomsten og sværhedsgraden af uheldige oplevelser, der involverer seksuel lyst, ydeevne og tilfredshed, er dog vanskelige at opnå, delvist fordi patienter og sundhedsudbydere kan være tilbageholdende med at diskutere dem. Følgelig kan skøn over forekomsten af uønsket seksuel oplevelse og ydeevne, der er nævnt i mærkningen, undervurdere deres faktiske forekomst.
Procentdelen af patienter, der rapporterer symptomer på seksuel dysfunktion hos mænd og kvinder med MDD, OCD, PD, SAD, GAD og PTSD, er vist i tabel 8.
PAXIL 20 mg-behandling har været forbundet med flere tilfælde af priapisme. I de tilfælde med et kendt udfald kom patienterne sig uden følgesygdomme.
Hallucinationer
poolede kliniske forsøg med PAXIL blev hallucinationer observeret hos 0,2 % af de PAXIL-behandlede patienter sammenlignet med 0,1 % af patienterne, der fik placebo.
Mindre almindelige bivirkninger
Følgende bivirkninger opstod under de kliniske undersøgelser af PAXIL og er ikke inkluderet andre steder i mærkningen.
Bivirkninger er kategoriseret efter kropssystem og opstillet i rækkefølge efter faldende frekvens i henhold til følgende definitioner: Hyppige bivirkninger er dem, der forekommer ved 1 eller flere lejligheder hos mindst 1/100 patienter; sjældne bivirkninger er dem, der forekommer hos 1/100 til 1/1.000 patienter; sjældne bivirkninger er dem, der forekommer hos færre end 1/1.000 patienter.
Kroppen som helhed
Sjælden: Allergisk reaktion, kulderystelser, ansigtsødem, utilpashed, nakkesmerter; sjælden: Adrenerg syndrom, cellulitis, moniliasis, nakkestivhed, bækkensmerter, peritonitis, sepsis, ulcus.
Kardiovaskulære system
Hyppig: Hypertension, takykardi; sjældent: Bradykardi, hæmatom, hypotension, migræne, postural hypotension, synkope; sjælden: Angina pectoris, arytmi nodal, atrieflimren, bundle branch block, cerebral iskæmi, cerebrovaskulær ulykke, kongestiv hjerteinsufficiens, hjerteblok, lavt hjertevolumen, myokardieinfarkt, myokardieiskæmi, bleghed, flebitis, lungeemboli, lungeemboli, supplestoles. trombose, åreknuder, vaskulær hovedpine, ventrikulære ekstrasystoler.
Fordøjelsessystemet
Sjælden: Bruxisme, colitis, dysfagi, udbrud, gastritis, gastroenteritis, tandkødsbetændelse, glossitis, øget salivation, abnorme leverfunktionsprøver, rektal blødning, ulcerøs stomatitis; sjælden: Aftøs stomatitis, blodig diarré, bulimi, kardiospasme, kolelithiasis, duodenitis, enteritis, esophagitis, fækale påvirkninger, fækal inkontinens, tandkødsblødning, hæmatemese, hepatitis, ileitis, ileus, intestinal obstruktion, gulsot, mundhule, melenticum, melenticum spytkirtelforstørrelse, sialadenitis, mavesår, stomatitis, misfarvning af tungen, tungeødem, tandcaries.
Endokrine system
Sjælden: Diabetes mellitus, struma, hyperthyroidisme, hypothyroidisme, thyroiditis.
Hemiske og lymfatiske systemer
Sjælden: Anæmi, leukopeni, lymfadenopati, purpura; sjælden: Unormale erytrocytter, basofili, øget blødningstid, eosinofili, hypokrom anæmi, jernmangelanæmi, leukocytose, lymfødem, unormale lymfocytter, lymfocytose, mikrocytisk anæmi, monocytose, normocytisk anæmi, trombocytopeni, trombocytopeni.
Metabolisk og ernæringsmæssig
Hyppig: Vægtøgning; sjældent: Ødem, perifert ødem, øget SGOT, øget SGPT, tørst, vægttab; sjælden: Forhøjet alkalisk fosfatase, bilirubinæmi, øget BUN, øget kreatininfosfokinase, dehydrering, forhøjet gammaglobuliner, gigt, hypercalcæmi, hyperkolesteræmi, hyperglykæmi, hyperkaliæmi, hyperfosfatæmi, hypocalcæmi, hypoglykæmi, hypoglykæmi, hypogenakaliæmi, forhøjet laproteinase, non-proteinaskemi, hypoglykæmi. nitrogen (NPN) steg.
Muskuloskeletale system
Hyppig: Artralgi; sjældent: Gigt, artrose; sjælden: Bursitis, myositis, osteoporose, generaliseret spasmer, seneskedehindebetændelse, tetany.
Nervesystem
Hyppig: Følelsesmæssig labilitet, vertigo; sjældent: Unormal tænkning, alkoholmisbrug, ataksi, dystoni, dyskinesi, eufori, fjendtlighed, hypertoni, hypestesi, hypokinesi, ukoordination, mangel på følelser, øget libido, manisk reaktion, neurose, lammelse, paranoid reaktion; sjælden: Unormal gang, akinesi, antisocial reaktion, afasi, choreoathetosis, cirkumorale paræstesier, kramper, delirium, vrangforestillinger, diplopi, lægemiddelafhængighed, dysartri, ekstrapyramidalt syndrom, fascikulationer, grand mal-kramper, hyperalgesi, hysteri, manisk reaktion, meningitis, manisk reaktion. myelitis, neuralgi, neuropati, nystagmus, perifer neuritis, psykotisk depression, psykose, nedsatte reflekser, øgede reflekser, stupor, torticollis, trismus, abstinenssyndrom.
Åndedrætsorganerne
Sjælden: Astma, bronkitis, dyspnø, næseblod, hyperventilation, lungebetændelse, luftvejsinfluenza; sjældne: Emfysem, hæmoptyse, hikke, lungefibrose, lungeødem, øget sputum, stridor, stemmeændring.
Hud og vedhæng
Hyppig: Kløe; sjældent: Acne, alopeci, kontaktdermatitis, tør hud, ekkymose, eksem, herpes simplex, lysfølsomhed, nældefeber; sjældne: Angioødem, erythema nodosum, erythema multiforme, eksfoliativ dermatitis, svampe dermatitis, furunkulose; herpes zoster, hirsutisme, makulopapulært udslæt, seborrhea, misfarvning af huden, hypertrofi i huden, hudsår, nedsat svedtendens, blæreformet udslæt.
Særlige sanser
Hyppig: Tinnitus; sjældent: Akkommodationsabnormitet, conjunctivitis, øresmerter, øjensmerter, keratoconjunctivitis, mydriasis, otitis media; sjældne: Amblyopi, anisocoria, blepharitis, katarakt, konjunktival ødem, hornhindesår, døvhed, exophthalmos, øjenblødning, glaukom, hyperacusis, natteblindhed, otitis externa, parosmi, fotofobi, ptosis, retinal blødning, synsfeltdefekt, smagsfejl.
Urogenitale system
Sjælden: Amenoré, brystsmerter, blærebetændelse, dysuri, hæmaturi, menorrhagia, nocturi, polyuri, pyuri, urininkontinens, urinretention, urintrang, vaginitis; sjælden: Abort, brystatrofi, brystforstørrelse, endometrielidelse, epididymitis, kvindelig laktation, fibrocystisk bryst, nyresten, nyresmerter, leukorrhea, mastitis, metroragi, nefritis, oliguri, salpingitis, urethritis, uterine spasm, urinvejsgips blødning, vaginal moniliasis.
Postmarketing oplevelse
Følgende reaktioner er blevet identificeret under brug af PAXIL efter godkendelse. Fordi disse reaktioner rapporteres frivilligt fra en population af ukendt størrelse, er det ikke altid muligt pålideligt at estimere deres hyppighed eller etablere en årsagssammenhæng til lægemiddeleksponering.
Akut pancreatitis, forhøjede leverfunktionsprøver (de mest alvorlige tilfælde var dødsfald som følge af levernekrose og kraftigt forhøjede transaminaser forbundet med alvorlig leverdysfunktion), Guillain-Barrés syndrom, Stevens-Johnsons syndrom, toksisk epidermal nekrolyse, upassende ADH-sekretionssyndrom, prolactinæmi og galaktoré; ekstrapyramidale symptomer, som har inkluderet akatisi, bradykinesi, tandhjulsstivhed, okulogyrisk krise, som har været forbundet med samtidig brug af pimozid; status epilepticus, akut nyresvigt, pulmonal hypertension, allergisk alveolitis, anafylaksi, eclampsia, laryngismus, optisk neuritis, porfyri, restless legs syndrome (RLS), ventrikulær fibrillation, ventrikulær takykardi (herunder torsade relateret til anemia), hæmohændelser hæmatopoiese (herunder aplastisk anæmi, pancytopeni, knoglemarvsaplasi og agranulocytose), vaskulitiske syndromer (såsom Henoch-Schönlein purpura) og for tidlige fødsler hos gravide kvinder. Der har været en caserapport om alvorlig hypotension, når PAXIL 20 mg blev tilføjet til kronisk metoprololbehandling.
DRUGSINTERAKTIONER
Tabel 9 viser klinisk signifikante lægemiddelinteraktioner med PAXIL.
ADVARSLER
Inkluderet som en del af "FORHOLDSREGLER" Afsnit
FORHOLDSREGLER
Selvmordstanker og -adfærd hos unge og unge voksne
I poolede analyser af placebo-kontrollerede forsøg med antidepressive lægemidler (SSRI'er og andre antidepressiva klasser), som omfattede ca. 77.000 voksne patienter og 4.500 pædiatriske patienter, var forekomsten af selvmordstanker og -adfærd hos antidepressiva-behandlede patienter i alderen 24 år og yngre større end hos placebobehandlede patienter. Der var betydelig variation i risikoen for selvmordstanker og -adfærd blandt stoffer, men der var en øget risiko identificeret hos unge patienter for de fleste undersøgte stoffer. Der var forskelle i den absolutte risiko for selvmordstanker og -adfærd på tværs af de forskellige indikationer, med den højeste forekomst hos patienter med MDD. Lægemiddel-placebo-forskellene i antallet af tilfælde af selvmordstanker og -adfærd pr. 1000 behandlede patienter er angivet i tabel 2.
PAXIL 30mg er ikke godkendt til brug hos pædiatriske patienter.
Det er ukendt, om risikoen for selvmordstanker og -adfærd hos børn, unge og unge voksne strækker sig til længerevarende brug, dvs. ud over fire måneder. Der er dog væsentlige beviser fra placebokontrollerede vedligeholdelsesforsøg hos voksne med MDD, at antidepressiva forsinker tilbagefald af depression, og at depression i sig selv er en risikofaktor for selvmordstanker og -adfærd.
Overvåg alle antidepressiva-behandlede patienter for enhver indikation for klinisk forværring og fremkomst af selvmordstanker og -adfærd, især i løbet af de første par måneder med lægemiddelbehandling og ved dosisændringer. Rådgive familiemedlemmer eller pårørende til patienter til at overvåge for ændringer i adfærd og advare sundhedsplejersken. Overvej at ændre det terapeutiske regime, herunder eventuelt seponering af PAXIL, hos patienter, hvis depression er vedvarende værre, eller som oplever nye selvmordstanker eller -adfærd.
Serotonin syndrom
SSRI'er, inklusive PAXIL, kan fremkalde serotonergt syndrom, en potentielt livstruende tilstand. Risikoen er øget ved samtidig brug af andre serotonerge lægemidler (herunder triptaner, tricykliske antidepressiva, fentanyl, lithium, tramadol, tryptofan, buspiron, amfetamin og perikon) og med lægemidler, der hæmmer metabolismen af serotonin, dvs. MAO-hæmmere [se KONTRAINDIKATIONER , DRUGSINTERAKTIONER ]. Serotonergt syndrom kan også forekomme, når disse lægemidler bruges alene.
Symptomer på serotonergt syndrom kan omfatte mentale statusændringer (f.eks. agitation, hallucinationer, delirium og koma), autonom ustabilitet (f.eks. takykardi, labilt blodtryk, svimmelhed, diaforese, rødmen, hypertermi), neuromuskulære symptomer (f.eks. tremor, rigiditet, myoklonus, hyperrefleksi, inkoordination), kramper og/eller gastrointestinale symptomer (f.eks. kvalme, opkastning, diarré).
Samtidig brug af PAXIL og MAO-hæmmere er kontraindiceret. Derudover må PAXIL 30 mg ikke påbegyndes hos en patient, der behandles med MAO-hæmmere såsom linezolid eller intravenøs methylenblåt. Ingen rapporter involverede administration af methylenblåt ad andre veje (såsom orale tabletter eller lokal vævsinjektion) eller ved lavere doser. Hvis det er nødvendigt at påbegynde behandling med en MAO-hæmmer såsom linezolid eller intravenøs methylenblåt hos en patient, der tager PAXIL 10 mg, skal PAXIL 40 mg afbrydes, før behandling med MAO-hæmmeren påbegyndes [se KONTRAINDIKATIONER , DRUGSINTERAKTIONER ].
Overvåg alle patienter, der tager PAXIL 20 mg, for forekomsten af serotonergt syndrom. Afbryd behandlingen med PAXIL 20 mg og eventuelle samtidige serotonerge midler omgående, hvis ovenstående symptomer opstår, og påbegynd understøttende symptomatisk behandling. Hvis samtidig brug af PAXIL og andre serotonerge lægemidler er klinisk berettiget, skal du informere patienterne om den øgede risiko for serotonergt syndrom og overvåge for symptomer.
Lægemiddelinteraktioner, der fører til QT-forlængelse
De CYP2D6-hæmmende egenskaber af paroxetin kan hæve plasmaniveauer af thioridazin og pimozid. Da thioridazin og pimozid givet alene giver forlængelse af QTc-intervallet og øger risikoen for alvorlige ventrikulære arytmier, er brugen af PAXIL 40 mg kontraindiceret i kombination med thioridazin og pimozid [se KONTRAINDIKATIONER , DRUGSINTERAKTIONER , KLINISK FARMAKOLOGI ].
Embryofetal og neonatal toksicitet
PAXIL kan forårsage fosterskader, når det administreres til en gravid kvinde. Epidemiologiske undersøgelser har vist, at spædbørn udsat for paroxetin i graviditetens første trimester har en øget risiko for kardiovaskulære misdannelser. Eksponering for paroxetin i slutningen af graviditeten kan føre til en øget risiko for vedvarende pulmonal hypertension hos den nyfødte (PPNH) og/eller neonatale komplikationer, der kræver langvarig hospitalsindlæggelse, respiratorisk støtte og sondeernæring.
Hvis PAXIL 20mg anvendes under graviditet, eller hvis patienten bliver gravid, mens hun tager PAXIL 30mg, skal patienten informeres om den potentielle fare for fosteret [se Brug i specifikke populationer ].
Øget risiko for blødning
Lægemidler, der interfererer med hæmning af serotoningenoptagelse, inklusive PAXIL 40mg, øger risikoen for blødningshændelser. Samtidig brug af aspirin, ikke-steroide antiinflammatoriske lægemidler (NSAIDS), andre trombocythæmmende lægemidler, warfarin og andre antikoagulantia kan øge denne risiko. Caserapporter og epidemiologiske undersøgelser (case-kontrol og kohortedesign) har vist en sammenhæng mellem brug af lægemidler, der interfererer med serotonin-genoptagelse og forekomsten af gastrointestinal blødning. Blødningshændelser relateret til lægemidler, der interfererer med serotonin-genoptagelsen, har varieret fra ekkymoser, hæmatomer, epistaxis og petekkier til livstruende blødninger.
Informer patienterne om den øgede risiko for blødning forbundet med samtidig brug af PAXIL 20 mg og blodpladehæmmende midler eller antikoagulantia. For patienter, der tager warfarin, skal det internationale normaliserede forhold nøje overvåges.
Aktivering af mani eller hypomani
Hos patienter med bipolar lidelse kan behandling af en depressiv episode med PAXIL 30 mg eller et andet antidepressivum udløse en blandet/manisk episode. Under kontrollerede kliniske forsøg med PAXIL forekom hypomani eller mani hos ca. 1 % af PAXIL-behandlede unipolære patienter sammenlignet med 1,1 % af aktiv kontrol og 0,3 % af placebobehandlede unipolære patienter. Inden påbegyndelse af behandling med PAXIL 20mg, screene patienter for enhver personlig eller familiehistorie med bipolar lidelse, mani eller hypomani.
Afbrydelsessyndrom
Bivirkninger efter seponering af serotonerge antidepressiva, især efter brat seponering, omfatter: kvalme, svedtendens, dysforisk stemning, irritabilitet, agitation, svimmelhed, føleforstyrrelser (f.eks. paræstesi, såsom elektrisk stød), tremor, angst, forvirring, hovedpine, sløvhed, følelsesmæssig labilitet, søvnløshed, hypomani, tinnitus og anfald. En gradvis reduktion af dosis i stedet for pludseligt ophør anbefales, når det er muligt [se DOSERING OG ADMINISTRATION ].
Under kliniske forsøg med GAD og PTSD blev der anvendt gradvise fald i den daglige dosis med 10 mg/dag med ugentlige intervaller efterfulgt af 1 uge ved 20 mg/dag, før behandlingen blev afbrudt. Følgende bivirkninger blev rapporteret med en incidens på 2 % eller mere for PAXIL 20 mg og var mindst dobbelt så høj som rapporteret for placebo: Unormale drømme, paræstesi og svimmelhed Der er rapporteret bivirkninger efter seponering af behandling med PAXIL hos pædiatriske patienter. Sikkerheden og effektiviteten af PAXIL hos pædiatriske patienter er ikke blevet fastslået [se KASSET ADVARSEL , Selvmordstanker og -adfærd hos unge og unge voksne , Brug i specifikke populationer ].
Anfald
PAXIL 10 mg tabletter og oral suspension er ikke blevet systematisk evalueret hos patienter med krampeanfald. Patienter med anfaldshistorie blev udelukket fra kliniske undersøgelser. Under kliniske undersøgelser forekom anfald hos 0,1 % af patienterne behandlet med PAXIL. PAXIL bør ordineres med forsigtighed til patienter med krampeanfald. Afbryd PAXIL 30mg hos enhver patient, der udvikler anfald.
Vinkel-lukkende glaukom
Pupiludvidelsen, der opstår efter brug af mange antidepressive lægemidler, inklusive PAXIL, kan udløse et vinkellukkeangreb hos en patient med anatomisk snævre vinkler, som ikke har en patenteret iridektomi. Der er rapporteret tilfælde af vinkel-lukkende glaukom i forbindelse med brug af PAXIL 40mg. Undgå brug af antidepressiva, inklusive PAXIL, til patienter med ubehandlede anatomisk snævre vinkler.
Hyponatriæmi
Hyponatriæmi kan forekomme som følge af behandling med SSRI'er, herunder PAXIL. Tilfælde med serumnatrium lavere end 110 mmol/L er blevet rapporteret. Tegn og symptomer på hyponatriæmi omfatter hovedpine, koncentrationsbesvær, hukommelsessvækkelse, forvirring, svaghed og ustabilitet, som kan føre til fald. Tegn og symptomer forbundet med mere alvorlige og/eller akutte tilfælde har inkluderet hallucinationer, synkope, krampeanfald, koma, åndedrætsstop og død. I mange tilfælde ser denne hyponatriæmi ud til at være resultatet af syndromet med uhensigtsmæssig antidiuretisk hormonsekretion (SIADH).
Hos patienter med symptomatisk hyponatriæmi skal PAXIL afbrydes og passende medicinsk intervention iværksættes. Ældre patienter, patienter, der tager diuretika, og dem, der er volumenfattige, kan have større risiko for at udvikle hyponatriæmi med SSRI'er [se Brug i specifikke populationer ].
Reduktion af Tamoxifens effekt
Nogle undersøgelser har vist, at effekten af tamoxifen, målt ved risikoen for brystkræfttilbagefald/dødelighed, kan reduceres ved samtidig brug af PAXIL som følge af paroxetins irreversible hæmning af CYP2D6 og lavere blodniveauer af tamoxifen [se DRUGSINTERAKTIONER ]. En undersøgelse tyder på, at risikoen kan stige med længere varighed af samtidig administration. Men andre undersøgelser har ikke kunnet påvise en sådan risiko. Når tamoxifen anvendes til behandling eller forebyggelse af brystkræft, bør ordinerende læger overveje at bruge et alternativt antidepressivum med ringe eller ingen CYP2D6-hæmning.
Knoglebrud
Epidemiologiske undersøgelser af risiko for knoglebrud under eksponering for nogle antidepressiva, herunder SSRI'er, har rapporteret en sammenhæng mellem antidepressiv behandling og frakturer. Der er flere mulige årsager til denne observation, og det er ukendt, i hvilket omfang frakturrisiko direkte kan tilskrives SSRI-behandling.
Patientrådgivningsinformation
Råd patienten til at læse den FDA-godkendte patientmærkning ( Medicinvejledning ).
Selvmordstanker og -adfærd
Rådgiv patienter og pårørende om at se efter fremkomsten af suicidalitet, især tidligt under behandlingen, og når dosis justeres op eller ned, og instruer dem om at rapportere sådanne symptomer til sundhedspersonalet [se KASSET ADVARSEL og ADVARSLER OG FORHOLDSREGLER ].
Serotonin syndrom
Pas på patienter med risikoen for serotonergt syndrom, især ved samtidig brug af PAXIL med andre serotonerge lægemidler, herunder triptaner, tricykliske antidepressiva, fentanyl, lithium, tramadol, tryptofan, buspiron, amfetamin, perikon og med lægemidler, der hæmmer stofskiftet af serotonin (især MAO-hæmmere, både dem, der er beregnet til at behandle psykiatriske lidelser og også andre, såsom linezolid). Instruer patienterne i at kontakte deres læge eller rapportere til skadestuen, hvis de oplever tegn eller symptomer på serotonergt syndrom [se ADVARSLER OG FORHOLDSREGLER , DRUGSINTERAKTIONER ].
Samtidig medicinering
Rådgive patienter om at informere deres læge, hvis de tager eller planlægger at tage receptpligtig eller håndkøbsmedicin, da der er mulighed for lægemiddel-interaktioner [se ADVARSEL OG FORHOLDSREGLER , DRUGSINTERAKTIONER ].
Øget risiko for blødning
Informer patienterne om samtidig brug af PAXIL og aspirin, NSAID'er, andre trombocythæmmende lægemidler, warfarin eller andre antikoagulantia, fordi den kombinerede brug har været forbundet med en øget risiko for blødning. Råd patienter til at informere deres sundhedspersonale, hvis de tager eller planlægger at tage receptpligtig eller håndkøbsmedicin, der øger risikoen for blødning [se ADVARSLER OG FORHOLDSREGLER ].
Aktivering af mani/hypomani
Råd til patienter og deres pårørende om at observere for tegn på aktivering af mani/hypomani og instruer dem i at rapportere sådanne symptomer til sundhedspersonalet [se ADVARSLER OG FORHOLDSREGLER ].
Afbrydelsessyndrom
Rådgiv patienterne om ikke pludselig at seponere PAXIL 40mg og at diskutere en eventuel nedtrapning med deres læge. Informer patienterne om, at der kan opstå bivirkninger, når PAXIL seponeres [se ADVARSLER OG FORHOLDSREGLER ].
Administrationsoplysninger til oral suspension
Instruer patienterne i at ryste den orale suspension godt før administration [se DOSERING OG ADMINISTRATION ].
Allergiske reaktioner
Råd patienter til at underrette deres læge, hvis de udvikler en allergisk reaktion såsom udslæt, nældefeber, hævelse eller åndedrætsbesvær [se BIVIRKNINGER ].
Embryo-føtal toksicitet
Informer kvinder om den potentielle risiko for fosteret [se ADVARSLER OG FORHOLDSREGLER , Brug i specifikke populationer ]. Råd til patienter om at underrette deres læge, hvis de bliver gravide eller har til hensigt at blive gravide under behandlingen på grund af risikoen for fosteret.
Ammende
Råd kvinder til at underrette deres læge, hvis de ammer et spædbarn [se Brug i specifikke populationer ].
Ikke-klinisk toksikologi
Karcinogenese, mutagenese, svækkelse af fertilitet
Karcinogenese
To-årige carcinogenicitetsundersøgelser blev udført på gnavere, der fik paroxetin i kosten med 1, 5 og 25 mg/kg/dag (mus) og 1, 5 og 20 mg/kg/dag (rotter). Disse doser er op til 2,0 (mus) og 3,2 (rotte) gange MRHD på 75 mg på mg/m2-basis. Der var et signifikant større antal hanrotter i højdosisgruppen med reticulumcellesarkomer (1/100, 0/50, 0/50 og 4/50 for kontrol-, lav-, mellem- og højdosisgrupper henholdsvis) og en signifikant øget lineær tendens på tværs af dosisgrupper for forekomsten af lymforetikulære tumorer hos hanrotter. Hunrotter blev ikke påvirket. Selvom der var en dosisrelateret stigning i antallet af tumorer hos mus, var der ingen lægemiddelrelateret stigning i antallet af mus med tumorer. Relevansen af disse fund for mennesker er ukendt.

Mutagenese
Paroxetin frembragte ingen genotoksiske virkninger i et batteri af 5 in vitro og 2 in vivo assays, der omfattede følgende: bakteriel mutationsanalyse, muse lymfom mutations assay, ikke-planlagt DNA syntese assay og test for cytogenetiske aberrationer in vivo i museknoglemarv og in vitro i humane lymfocytter og i en dominant letal test hos rotter.
Forringelse af fertilitet
Nogle kliniske undersøgelser har vist, at SSRI'er (inklusive paroxetin) kan påvirke sædkvaliteten under SSRI-behandling, hvilket kan påvirke fertiliteten hos nogle mænd.
En reduceret drægtighedsrate blev fundet i reproduktionsundersøgelser med rotter ved en dosis af paroxetin på 15 mg/kg/dag, hvilket er 2,4 gange MRHD på 75 mg på mg/m2-basis. Irreversible læsioner forekom i forplantningskanalen hos hanrotter efter dosering i toksicitetsundersøgelser i 2 til 52 uger. Disse læsioner bestod af vakuolation af epididymalt tubulært epitel ved 50 mg/kg/dag og atrofiske ændringer i sædrørene i testiklerne med standset spermatogenese ved 25 mg/kg/dag (8,2 og 4,1 gange MRHD på 75 mg på en mg/dag) m2 basis).
Brug i specifikke populationer
Graviditet
Graviditetskategori D [Se ADVARSLER OG FORHOLDSREGLER ]
Epidemiologiske undersøgelser har vist, at spædbørn udsat for paroxetin i graviditetens første trimester har en øget risiko for medfødte misdannelser, især kardiovaskulære misdannelser. Hvis paroxetin anvendes under graviditet, eller hvis patienten bliver gravid, mens du tager paroxetin, skal du informere patienten om den potentielle fare for fosteret.
Kliniske overvejelser
Medmindre fordelene ved paroxetin for moderen retfærdiggør fortsat behandling, bør det overvejes enten at seponere paroxetinbehandling eller skifte til et andet antidepressivum [se ADVARSLER OG FORHOLDSREGLER ]. Til
- En undersøgelse baseret på svenske nationale registerdata viste, at spædbørn udsat for paroxetin under graviditeten (n = 815) havde en øget risiko for kardiovaskulære misdannelser (2 % risiko hos paroxetin-eksponerede spædbørn) sammenlignet med hele registerpopulationen (1 % risiko). for et oddsforhold (OR) på 1,8 (95 % konfidensinterval 1,1 til 2,8). Der blev ikke set nogen stigning i risikoen for overordnede medfødte misdannelser hos de paroxetin-eksponerede spædbørn. Hjertemisdannelserne hos de paroxetin-eksponerede spædbørn var primært ventrikulære septale defekter (VSD'er) og atrielle septale defekter (ASD'er). Septale defekter varierer i sværhedsgrad fra dem, der forsvinder spontant til dem, der kræver operation.
- En separat retrospektiv kohorteundersøgelse fra USA (United Healthcare-data) evaluerede 5.956 spædbørn af mødre, der fik antidepressiva i løbet af første trimester (n = 815 for paroxetin). Denne undersøgelse viste en tendens til en øget risiko for kardiovaskulære misdannelser for paroxetin (risiko på 1,5 %) sammenlignet med andre antidepressiva (risiko på 1 %), for en OR på 1,5 (95 % konfidensinterval 0,8 til 2,9). Af de 12 paroxetin-eksponerede spædbørn med kardiovaskulære misdannelser havde 9 VSD'er. Denne undersøgelse antydede også en øget risiko for overordnede større medfødte misdannelser, herunder kardiovaskulære defekter for paroxetin (4 % risiko) sammenlignet med andre (2 % risiko) antidepressiva (OR 1,8; 95 % konfidensinterval 1,2 til 2,8).
- To store case-kontrol undersøgelser ved hjælp af separate databaser, hver med >9.000 fødselsdefekter og >4.000 kontroller, fandt, at moderens brug af paroxetin under graviditetens første trimester var forbundet med en 2- til 3 gange øget risiko for højre ventrikulær udstrømning forhindringer i kanalen. I den ene undersøgelse var OR 2,5 (95 % konfidensinterval, 1,0 til 6,0, 7 eksponerede spædbørn), og i den anden undersøgelse var OR 3,3 (95 % konfidensinterval, 1,3 til 8,8, 6 eksponerede spædbørn).
Andre undersøgelser har fundet forskellige resultater med hensyn til, om der var en øget risiko for overordnede, kardiovaskulære eller specifikke medfødte misdannelser. En metaanalyse af epidemiologiske data over en 16-årig periode (1992 til 2008) om brug af paroxetin i første trimester under graviditet og medfødte misdannelser inkluderede ovennævnte undersøgelser ud over andre (n = 17 undersøgelser, der omfattede overordnede misdannelser og n = 14 undersøgelser, der inkluderede kardiovaskulære misdannelser; n = 20 forskellige undersøgelser). Selvom denne metaanalyse var underlagt begrænsninger, antydede denne en øget forekomst af kardiovaskulære misdannelser (prævalens odds ratio [POR] 1,5; 95 % konfidensinterval 1,2 til 1,9) og overordnede misdannelser (POR 1,2; 95 % konfidensinterval 1,1 til 1,4) med paroxetin brug i første trimester. Det var ikke muligt i denne meta-analyse at bestemme, i hvilket omfang den observerede prævalens af kardiovaskulære misdannelser kunne have bidraget til den for overordnede misdannelser, og det var heller ikke muligt at fastslå, om nogen specifikke typer af kardiovaskulære misdannelser kunne have bidraget til den observerede prævalens. af alle kardiovaskulære misdannelser.
Medmindre fordelene ved paroxetin for moderen retfærdiggør fortsat behandling, bør det overvejes enten at seponere paroxetinbehandling eller skifte til et andet antidepressivum [se ADVARSLER OG FORHOLDSREGLER ]. For kvinder, der har til hensigt at blive gravide eller er i deres første trimester af graviditeten, bør paroxetin kun påbegyndes efter overvejelse af de andre tilgængelige behandlingsmuligheder [se ADVARSLER OG FORHOLDSREGLER ].
Behandling af gravide kvinder i deres tredje trimester
Nyfødte, der er udsat for SSRI'er eller serotonin- og noradrenalin-genoptagelseshæmmere (SNRI'er), inklusive PAXIL 40mg, sent i tredje trimester har udviklet komplikationer, der kræver langvarig hospitalsindlæggelse, respiratorisk støtte og sondeernæring. Sådanne komplikationer kan opstå umiddelbart efter levering. Rapporterede kliniske fund har inkluderet åndedrætsbesvær, cyanose, apnø, kramper, temperaturustabilitet, ernæringsbesvær, opkastning, hypoglykæmi, hypotoni, hypertoni, hyperrefleksi, tremor, nervøsitet, irritabilitet og konstant gråd. Disse egenskaber stemmer overens med enten en direkte toksisk virkning af SSRI'er og SNRI'er eller muligvis et lægemiddelafbrydelsessyndrom. Det skal bemærkes, at det kliniske billede i nogle tilfælde stemmer overens med serotonergt syndrom [se ADVARSLER OG FORHOLDSREGLER ].
Eksponering for SSRI'er i slutningen af graviditeten kan have en øget risiko for vedvarende pulmonal hypertension hos den nyfødte (PPHN). PPHN forekommer hos 1-2 ud af 1.000 levendefødte i den generelle befolkning og er forbundet med betydelig neonatal morbiditet og dødelighed. I et retrospektivt case-kontrolstudie af 377 kvinder, hvis spædbørn blev født med PPHN og 836 kvinder, hvis spædbørn blev født raske, var risikoen for at udvikle PPHN ca. seks gange højere for spædbørn, der blev udsat for SSRI efter 20. svangerskabsuge sammenlignet med spædbørn. som ikke havde været udsat for antidepressiva under graviditeten.
Der har også været rapporter efter markedsføring om for tidlige fødsler hos gravide kvinder, der er udsat for paroxetin eller andre SSRI'er.
Ved behandling af en gravid kvinde med paroxetin i tredje trimester, bør lægen nøje overveje både de potentielle risici og fordele ved behandlingen. En prospektiv longitudinel undersøgelse af 201 kvinder med en historie med svær depression, som var euthymic ved begyndelsen af graviditeten. De kvinder, der ophørte med antidepressiv medicin under graviditeten, var mere tilbøjelige til at opleve et tilbagefald af svær depression end kvinder, der fortsatte med antidepressiv medicin.
Dyrefund
Reproduktionsundersøgelser blev udført ved doser op til 50 mg/kg/dag hos rotter og 6 mg/kg/dag hos kaniner administreret under organogenese. Disse doser er ca. 6 (rotte) og mindre end 2 (kanin) gange den maksimalt anbefalede humane dosis (MRHD – 75 mg) på mg/m2-basis. Disse undersøgelser har ikke afsløret tegn på udviklingsmæssige effekter. Hos rotter var der dog en stigning i hvalpedødsfald i løbet af de første 4 dage af diegivningen, når doseringen fandt sted i det sidste trimester af drægtighedsperioden og fortsatte under hele diegivningen. Denne effekt opstod ved en dosis på 1 mg/kg/dag, hvilket er end MRHD på mg/m2-basis. Ingen-effektdosis for rotteungers dødelighed blev ikke bestemt. Årsagen til disse dødsfald kendes ikke.
Ammende mødre
Som mange andre lægemidler udskilles paroxetin i modermælk. På grund af risikoen for alvorlige bivirkninger hos ammende spædbørn fra PAXIL 20mg, bør der tages en beslutning, om man skal seponere med ammende spædbørn eller seponere lægemidlet under hensyntagen til lægemidlets betydning for moderen.
Pædiatrisk brug
Sikkerheden og effektiviteten af PAXIL hos pædiatriske patienter er ikke blevet fastslået [se KASSE ADVARSEL ]. Effektivitet blev ikke påvist i tre placebokontrollerede forsøg med 752 PAXIL-behandlede pædiatriske patienter med MDD.
Antidepressiva øger risikoen for selvmordstanker og -adfærd hos pædiatriske patienter [se KASSET ADVARSEL , ADVARSLER OG FORHOLDSREGLER ]. Nedsat appetit og vægttab er blevet observeret i forbindelse med brugen af SSRI'er.
placebokontrollerede kliniske forsøg udført med pædiatriske patienter blev følgende bivirkninger rapporteret hos mindst 2 % af de pædiatriske patienter behandlet med PAXIL og forekom med en hastighed, der var mindst dobbelt så stor som for pædiatriske patienter, der fik placebo: følelsesmæssig labilitet (inklusive selvskade) , selvmordstanker, selvmordsforsøg, gråd og humørsvingninger), fjendtlighed, nedsat appetit, tremor, svedtendens, hyperkinesi og agitation.
Bivirkninger efter seponering af behandling med PAXIL i de pædiatriske kliniske undersøgelser, som omfattede et nedtrapningsregime, som forekom hos mindst 2 % af patienterne og med en hastighed på mindst det dobbelte af placebo, var: følelsesmæssig labilitet (inklusive selvmordstanker, selvmord forsøg, humørsvingninger og tårefuldhed), nervøsitet, svimmelhed, kvalme og mavesmerter.
Geriatrisk brug
præmarketing kliniske forsøg med PAXIL 10 mg var 17 % af patienterne behandlet med PAXIL (ca. 700) 65 år eller ældre. Farmakokinetiske undersøgelser viste en nedsat clearance hos ældre, og en lavere startdosis anbefales; dog blev der ikke observeret nogen overordnede forskelle i sikkerhed eller effektivitet mellem ældre og yngre patienter [se DOSERING OG ADMINISTRATION , KLINISK FARMAKOLOGI ].
SSRI'er inklusive PAXIL er blevet forbundet med tilfælde af klinisk signifikant hyponatriæmi hos ældre patienter, som kan have større risiko for denne bivirkning [se ADVARSLER OG FORHOLDSREGLER ].
Nyre- og leverinsufficiens
Forhøjede plasmakoncentrationer af paroxetin forekommer hos patienter med nedsat nyre- og leverfunktion. Den initiale dosis af PAXIL bør reduceres hos patienter med svært nedsat nyrefunktion og hos patienter med svært nedsat leverfunktion [se DOSERING OG ADMINISTRATION , KLINISK FARMAKOLOGI ].
OVERDOSIS
Menneskelig oplevelse
Siden introduktionen af PAXIL 30 mg i USA, er spontane tilfælde af bevidst eller utilsigtet overdosering under paroxetinbehandling blevet rapporteret over hele verden. Disse omfatter overdoser med paroxetin alene og i kombination med andre stoffer. Der er rapporter om dødsfald, der ser ud til at involvere paroxetin alene.
Almindelige rapporterede bivirkninger forbundet med overdosering af paroxetin omfatter somnolens, koma, kvalme, tremor, takykardi, forvirring, opkastning og svimmelhed. Andre bemærkelsesværdige tegn og symptomer observeret ved overdosering af paroxetin (alene eller sammen med andre stoffer) omfatter mydriasis, kramper (inklusive status epilepticus), ventrikulære dysrytmier (inklusive torsade de pointes), hypertension, aggressive reaktioner, synkope, hypotension, stupor, bradynicardi. rhabdomyolyse, symptomer på leverdysfunktion (inklusive leversvigt, levernekrose, gulsot, hepatitis og hepatisk steatose), serotonergt syndrom, maniske reaktioner, myoklonus, akut nyresvigt og urinretention.
Overdoseringshåndtering
Der kendes ingen specifikke modgift til PAXIL. Hvis der opstår overdosering, skal du ringe til dit giftkontrolcenter på 1-800-222-1222 for at få de seneste anbefalinger.
KONTRAINDIKATIONER
PAXIL er kontraindiceret til patienter:
- Tager eller inden for 14 dage efter ophør med MAO-hæmmere (inklusive MAO-hæmmere linezolid og intravenøs methylenblåt) på grund af en øget risiko for serotonergt syndrom [se ADVARSLER OG FORHOLDSREGLER , DRUGSINTERAKTIONER ].
- At tage thioridazin på grund af risiko for QT-forlængelse [se ADVARSLER OG FORHOLDSREGLER og DRUGSINTERAKTIONER ]
- Tager pimozid på grund af risiko for QT-forlængelse [se ADVARSLER OG FORHOLDSREGLER , DRUGSINTERAKTIONER ].
- Med kendt overfølsomhed (f.eks. anafylaksi, angioødem, Stevens-Johnsons syndrom) over for paroxetin eller et af de inaktive ingredienser i PAXIL [se BIVIRKNINGER ].
KLINISK FARMAKOLOGI
Handlingsmekanisme
Virkningsmekanismen af PAXIL i behandlingen af MDD, SAD, OCD\, PD, GAD og PTSD er ukendt, men formodes at være forbundet med potensering af serotonerg aktivitet i centralnervesystemet som følge af hæmning af neuronal genoptagelse af serotonin (5-hydroxy-tryptamin, 5-HT).
Farmakodynamik
Studier med klinisk relevante doser hos mennesker har vist, at paroxetin blokerer optagelsen af serotonin i humane blodplader. In vitro undersøgelser på dyr tyder også på, at paroxetin er en potent og meget selektiv hæmmer af neuronal serotonin reuptake (SSRI) og kun har meget svag effekt på noradrenalin og dopamin neuronal genoptagelse.
Farmakokinetik
Ikke-linearitet i farmakokinetikken er observeret med stigende doser af PAXIL.
I en metaanalyse af paroxetin fra 4 undersøgelser udført med raske frivillige efter gentagen dosering på 20 mg/dag til 40 mg/dag, udviste mænd ikke en signifikant lavere Cmax eller AUC end kvinder.
Absorption
Paroxetinhydrochlorid absorberes fuldstændigt efter oral dosering af en opløsning af hydrochloridsaltet. I en undersøgelse, hvor normale mandlige forsøgspersoner (n = 15) modtog 30 mg tabletter dagligt i 30 dage, blev steady-state paroxetinkoncentrationer opnået med ca. 10 dage for de fleste forsøgspersoner, selvom det kan tage væsentligt længere tid hos en lejlighedsvis patient. Ved steady state var middelværdierne for Cmax, Tmax, Cmin og T½ 61,7 ng/ml (CV 45%), 5,2 timer. (CV 10%), henholdsvis 30,7 ng/ml (CV 67%) og 21,0 timer (CV 32%). Steady-state Cmax og Cmin værdierne var omkring 6 og 14 gange, hvad der ville blive forudsagt fra enkeltdosis undersøgelser. Steady-state lægemiddeleksponering baseret på AUC0-24 var omkring 8 gange større, end det ville have været forudsagt ud fra enkeltdosisdata hos disse forsøgspersoner. Den overskydende ophobning er en konsekvens af, at 1 af de enzymer, der omsætter paroxetin, er let mættende.
Paroxetin er lige så biotilgængeligt fra oral suspension og tablet.
Effekt af mad
Virkningerne af mad på biotilgængeligheden af paroxetin blev undersøgt hos forsøgspersoner, der fik en enkelt dosis med og uden mad. AUC var kun let øget (6%), når lægemidlet blev administreret sammen med mad, men Cmax var 29% højere, mens tiden til at nå maksimal plasmakoncentration faldt fra 6,4 timer efter dosering til 4,9 timer.
Fordeling
Paroxetin fordeler sig i hele kroppen, inklusive CNS, med kun 1 % tilbage i plasmaet.
Ca. 95 % og 93 % af paroxetin er bundet til plasmaprotein ved henholdsvis 100 ng/ml og 400 ng/ml. Under kliniske forhold vil paroxetinkoncentrationer normalt være mindre end 400 ng/ml. Paroxetin ændrer ikke in vitro-proteinbindingen af phenytoin eller warfarin.
Elimination
Metabolisme
Den gennemsnitlige eliminationshalveringstid er ca. 21 timer (CV 32%) efter oral dosering af 30 mg tabletter dagligt i 30 dage med PAXIL.
steady-state dosisproportionalitetsundersøgelser, der involverede ældre og ikke-ældre patienter, ved doser på 20 mg til 40 mg dagligt for ældre og 20 mg til 50 mg dagligt for ikke-ældre, blev der observeret en vis ikke-linearitet i begge populationer, hvilket igen afspejler en mættelig metabolisk vej. . Sammenlignet med Cmin-værdier efter 20 mg dagligt var værdierne efter 40 mg dagligt kun ca. 2 til 3 gange større end fordoblet.
Paroxetin metaboliseres i vid udstrækning efter oral administration. De vigtigste metabolitter er polære og konjugerede produkter af oxidation og methylering, som let fjernes. Konjugater med glucuronsyre og sulfat dominerer, og hovedmetabolitter er blevet isoleret og identificeret. Data indikerer, at metabolitterne ikke har mere end 1/50 af moderforbindelsens styrke til at hæmme serotoninoptagelsen. Metabolismen af paroxetin udføres delvist af CYP2D6. Mætning af dette enzym ved kliniske doser ser ud til at tage højde for ulineariteten af paroxetin-kinetikken med stigende dosis og stigende behandlingsvarighed. Rollen af dette enzym i paroxetin metabolisme antyder også potentielle lægemiddel-lægemiddel-interaktioner [se DRUGSINTERAKTIONER ]. Paroxetins farmakokinetiske adfærd er ikke blevet evalueret hos forsøgspersoner med mangel på CYP2D6 (dårlige metabolisatorer).
Udskillelse
Ca. 64 % af en 30 mg oral opløsning af paroxetin blev udskilt i urinen med 2 % som moderstof og 62 % som metabolitter over en 10-dages post-doseringsperiode. Ca. 36 % blev udskilt i fæces (sandsynligvis via galden), hovedsageligt som metabolitter og mindre end 1 % som moderstof i løbet af 10 dage efter dosering.
Lægemiddelinteraktionsstudier
Der er klinisk signifikante, kendte lægemiddelinteraktioner mellem paroxetin og andre lægemidler [se DRUGSINTERAKTIONER ].
Figur 1. Paroxetins indvirkning på farmakokinetikken af samtidig administrerede lægemidler (log-skala)
Figur 2. Indvirkning af samtidig administrerede lægemidler på paroxetins farmakokinetik
Theophyllin
Rapporter om forhøjede theophyllin-niveauer forbundet med PAXIL-behandling er blevet rapporteret. Selvom denne interaktion ikke er blevet formelt undersøgt, anbefales det, at theophyllinniveauer overvåges, når disse lægemidler administreres samtidigt.
Lægemidler metaboliseret af Cytokrom CYP3A4
Et in vivo interaktionsstudie, der involverede samtidig administration under steady-state forhold af paroxetin og terfenadin, et substrat for CYP3A4, viste ingen effekt af paroxetin på terfenadins farmakokinetik. Derudover har in vitro undersøgelser vist, at ketoconazol, en potent hæmmer af CYP3A4-aktivitet, er mindst 100 gange mere potent end paroxetin som en hæmmer af metabolismen af flere substrater for dette enzym, herunder terfenadin, astemizol, cisaprid, triazolam og cyclosporin. Paroxetins omfang af hæmning af CYP3A4-aktivitet forventes ikke at være af klinisk betydning.
Specifikke populationer
Indvirkningen af specifikke populationer på paroxetins farmakokinetik er vist i figur 3.
Den anbefalede startdosis og maksimale dosis af PAXIL er reduceret hos ældre patienter, patienter med svært nedsat nyrefunktion og patienter med svært nedsat leverfunktion [se DOSERING OG ADMINISTRATION ].
Figur 3. Indvirkning af specifik population på farmakokinetikken af paroxetin (log skala)
Kliniske Studier
Større depressiv lidelse
Effekten af PAXIL som behandling af svær depressiv lidelse (MDD) er blevet fastslået i 6 placebokontrollerede undersøgelser af patienter med MDD (i alderen 18 til 73). I disse undersøgelser blev PAXIL vist at være statistisk signifikant mere effektiv end placebo til behandling af MDD ved mindst 2 af følgende mål: Hamilton Depression Rating Scale (HDRS), Hamilton-depressiv stemning og Clinical Global Impression (CGI)- Sygdommens sværhedsgrad. PAXIL var statistisk signifikant bedre end placebo med hensyn til forbedring af HDRS-subfaktor-scorerne, inklusive det deprimerede humør, søvnforstyrrelsesfaktor og angstfaktor.
Langsigtet effekt af PAXIL 10 mg til behandling af MDD hos ambulante patienter blev påvist i et randomiseret abstinensstudie. Patienter, som reagerede på PAXIL (HDRS total score
Tvangslidelse
Effektiviteten af PAXIL til behandling af obsessiv-kompulsiv lidelse (OCD) blev påvist i to 12-ugers multicenter placebokontrollerede undersøgelser af voksne ambulante patienter (undersøgelse 1 og 2). Patienterne havde moderat til svær OCD (DSM-IIIR) med gennemsnitlige baseline-vurderinger på Yale Brown Obsessive Compulsive Scale (YBOCS) totalscore varierende fra 23 til 26. I undersøgelse 1, et dosisområdefundingsstudie, fik patienterne faste daglige doser af PAXIL 20 mg, 40 mg eller 60 mg. Undersøgelse 1 viste, at daglige doser af PAXIL 40 mg og 60 mg er effektive i behandlingen af OCD. Patienter, der fik doser af PAXIL 40 mg og 60 mg, oplevede en gennemsnitlig reduktion på henholdsvis ca. 6 og 7 point på YBOCS totalscore, som var statistisk signifikant større end den omtrentlige 4-point reduktion ved 20 mg og en 3-point reduktion i de placebobehandlede patienter. Studie 2 var et studie med fleksibel dosis, der sammenlignede PAXIL 20 mg til 60 mg dagligt med clomipramin 25 mg til 250 mg dagligt eller placebo). I denne undersøgelse oplevede patienter, der fik PAXIL, en gennemsnitlig reduktion på ca. 7 point på YBOCS totalscore, hvilket var statistisk signifikant større end den gennemsnitlige reduktion på ca. 4 point hos placebobehandlede patienter.
Følgende tabel viser udfaldsklassificeringen efter behandlingsgruppe på Global Improvement-elementer på Clinical Global Impression (CGI)-skalaen for undersøgelse 1.
Undergruppeanalyser indikerede ikke, at der var forskelle i behandlingsresultater som funktion af alder eller køn.
Den langsigtede effekt af PAXIL til behandling af OCD blev fastslået i en langsigtet forlængelse af undersøgelse 1. Patienter, der reagerede på PAXIL i den 3-måneders dobbeltblinde fase og en 6-måneders forlængelse af åben PAXIL 20 mg til 60 mg dagligt blev randomiseret til enten PAXIL 10mg eller placebo i en 6-måneders dobbeltblind tilbagefaldsforebyggelsesfase. Patienter randomiseret til PAXIL var statistisk signifikant mindre tilbøjelige til at få tilbagefald end placebobehandlede patienter.
Paniklidelse
Effektiviteten af PAXIL 20 mg til behandling af panikangst (PD) blev påvist i tre 10- til 12-ugers multicenter, placebokontrollerede undersøgelser af voksne ambulante patienter (undersøgelse 1, 2 og 3). Patienterne havde PD (DSM-IIIR), med eller uden agorafobi. I disse undersøgelser blev PAXIL vist at være statistisk signifikant mere effektiv end placebo til behandling af PD med mindst 2 ud af 3 mål for frekvensen af panikanfald og på Clinical Global Impression Severity of Illness-score.
Undersøgelse 1 var en 10-ugers dosis-interval fund undersøgelse; patienter fik faste doser af PAXIL 10 mg, 20 mg eller 40 mg dagligt eller placebo. En statistisk signifikant forskel fra placebo blev kun observeret for PAXIL 40 mg daglig gruppe. Ved endepunktet var 76 % af patienterne, der fik PAXIL 40 mg dagligt, fri for panikanfald sammenlignet med 44 % af placebobehandlede patienter.
Studie 2 var et 12-ugers studie med fleksibel dosis, der sammenlignede PAXIL 10 mg med 60 mg dagligt og placebo. Ved endepunktet var 51 % af de PAXIL-behandlede patienter fri for panikanfald sammenlignet med 32 % af de placebo-behandlede patienter.
Studie 3 var et 12-ugers studie med fleksibel dosis, der sammenlignede PAXIL 10 mg til 60 mg dagligt med placebo hos patienter, der samtidig fik standardiseret kognitiv adfærdsterapi. Ved endepunktet viste 33 % af de PAXIL-behandlede patienter en reduktion til 0 eller 1 panikanfald sammenlignet med 14 % af placebo-behandlede patienter.
I undersøgelse 2 og 3 var den gennemsnitlige PAXIL-dosis for fuldførere ved endepunktet ca. 40 mg dagligt.
Langsigtet effekt af PAXIL 10 mg i PD blev påvist i en forlængelse af undersøgelse 1. Patienter, der responderede på PAXIL 20 mg i den 10-ugers dobbeltblinde fase og under en 3-måneders dobbeltblindet forlængelsesfase, blev randomiseret til enten PAXIL 10 mg, 20 mg eller 40 mg dagligt eller placebo i en 3-måneders dobbeltblind fase til forebyggelse af tilbagefald. Patienter randomiseret til PAXIL 20 mg var statistisk signifikant mindre tilbøjelige til at få tilbagefald end placebobehandlede patienter.
Undergruppeanalyser indikerede ikke, at der var forskelle i behandlingsresultater som funktion af alder eller køn.
Social angst
Effektiviteten af PAXIL til behandling af social angstlidelse (SAD) blev påvist i tre 12-ugers, multicenter, placebo-kontrollerede undersøgelser (studier 1, 2 og 3) af voksne ambulante patienter med SAD (DSM-IV). I disse undersøgelser blev effektiviteten af PAXIL 30 mg sammenlignet med placebo evalueret på basis af (1) andelen af respondere, som defineret ved en Clinical Global Impression (CGI) Improvement-score på 1 (meget forbedret) eller 2 (meget forbedret) ), og (2) ændring fra baseline i Liebowitz Social Anxiety Scale (LSAS).
Studie 1 og 2 var fleksible dosisundersøgelser, der sammenlignede PAXIL 20 mg med 50 mg dagligt og placebo. PAXIL viste statistisk signifikant overlegenhed i forhold til placebo på både CGI Improvement responder-kriteriet og Liebowitz Social Anxiety Scale (LSAS). I undersøgelse 1 var 69 % af de PAXIL-behandlede patienter for patienter, der fuldførte til uge 12, sammenlignet med 29 % af placebo-behandlede patienter, der responderede på CGI Improvement. I undersøgelse 2 var CGI Improvement responders 77 % og 42 % for henholdsvis PAXIL- og placebobehandlede patienter.
Studie 3 var et 12-ugers studie, der sammenlignede faste doser af PAXIL 20 mg, 40 mg eller 60 mg dagligt med placebo. PAXIL 20 mg var statistisk signifikant bedre end placebo på både LSAS Total Score og CGI Improvement responder-kriteriet; der var tendenser til overlegenhed i forhold til placebo for PAXIL 40 mg og 60 mg daglig dosisgrupper. Der var ingen indikation i denne undersøgelse af nogen yderligere fordel ved doser højere end 20 mg dagligt.
Undergruppeanalyser indikerede generelt ikke forskelle i behandlingsresultater som funktion af alder, race eller køn.
Generaliseret angstlidelse
Effektiviteten af PAXIL til behandling af generaliseret angstlidelse (GAD) blev påvist i to 8-ugers, multicenter, placebokontrollerede undersøgelser (undersøgelse 1 og 2) af voksne ambulante patienter med GAD (DSM-IV).
Studie 1 var et 8-ugers studie, der sammenlignede faste doser af PAXIL 20 mg eller 40 mg dagligt med placebo. Doser af PAXIL 20 mg eller 40 mg blev begge vist at være statistisk signifikant bedre end placebo på Hamilton Rating Scale for Anxiety (HAM-A) totalscore.
Der var ikke tilstrækkelig evidens i denne undersøgelse til at foreslå en større fordel for PAXIL 40 mg daglig dosis sammenlignet med 20 mg daglig dosis.
Studie 2 var et studie med fleksibel dosis, der sammenlignede PAXIL 20 mg med 50 mg dagligt og placebo. PAXIL viste statistisk signifikant overlegenhed i forhold til placebo på Hamilton Rating Scale for Anxiety (HAM-A) totalscore.
Et tredje studie, et studie med fleksibel dosis, der sammenlignede PAXIL 20 mg til 50 mg dagligt med placebo, viste ikke statistisk signifikant overlegenhed af PAXIL i forhold til placebo på Hamilton Rating Scale for Anxiety (HAM-A) totalscore, det primære resultat.
Undergruppeanalyser indikerede ikke forskelle i behandlingsresultater som funktion af race eller køn. Der var ikke tilstrækkeligt med ældre patienter til at foretage undergruppeanalyser på baggrund af alder.
et langtidsforsøg blev 566 patienter, der opfyldte DSM-IV-kriterierne for GAD, som havde reageret i en enkelt-blind, 8-ugers akut behandlingsfase med PAXIL 20 mg til 50 mg dagligt, randomiseret til fortsættelse af PAXIL 30 mg ved deres samme dosis eller placebo i op til 24 ugers observation for tilbagefald. Respons under den enkeltblinde fase blev defineret ved at have et fald på ≥2 point sammenlignet med baseline på CGI-Severity of Illness-skalaen til en score på ≤3. Tilbagefald under den dobbeltblinde fase blev defineret som en stigning på ≥2 point sammenlignet med baseline på CGI-Severity of Illness-skalaen til en score på ≥4, eller seponering på grund af manglende effekt. Patienter, der fortsatte med at modtage PAXIL 40 mg, oplevede en statistisk signifikant lavere tilbagefaldsrate over de efterfølgende 24 uger sammenlignet med dem, der fik placebo.
Post traumatisk stress syndrom
Effektiviteten af PAXIL 20mg i behandlingen af posttraumatisk stresslidelse (PTSD) blev påvist i to 12-ugers, multicenter, placebokontrollerede undersøgelser (undersøgelse 1 og 2) af voksne ambulante patienter, som opfyldte DSM-IV-kriterierne for PTSD. Den gennemsnitlige varighed af PTSD-symptomer for de 2 undersøgelser tilsammen var 13 år (fra 0,1 år til 57 år). Procentdelen af patienter med sekundær MDD eller ikke-PTSD angstlidelser i de kombinerede 2 undersøgelser var henholdsvis 41 % (356 ud af 858 patienter) og 40 % (345 ud af 858 patienter). Undersøgelsesresultatet blev vurderet ved (1) Clinician-Administered PTSD Scale Part 2 (CAPS-2) score og (2) Clinical Global Impression-Global Improvement Scale (CGI-I). CAPS-2 er et multi-item instrument, der måler 3 aspekter af PTSD med følgende symptomklynger: Genoplevelse/indtrængen, undgåelse/bedøvelse og hyperarousal. De 2 primære resultater for hvert forsøg var (1) ændring fra baseline til endepunkt på CAPS-2 totalscore (17 elementer) og (2) andel af respondere på CGI-I, hvor respondere blev defineret som patienter med en score af 1 (meget forbedret) eller 2 (meget forbedret).
Studie 1 var et 12-ugers studie, der sammenlignede faste doser af PAXIL 20 mg eller 40 mg dagligt med placebo. Doser af PAXIL 20 mg og 40 mg blev vist at være statistisk signifikant bedre end placebo ved ændring fra baseline for CAPS-2 totalscore og andelen af respondere på CGI-I. Der var ikke tilstrækkelig evidens i denne undersøgelse til at foreslå en større fordel for den daglige dosis på 40 mg sammenlignet med den daglige dosis på 20 mg.
Studie 2 var et 12-ugers studie med fleksibel dosis, der sammenlignede PAXIL 20 mg til 50 mg dagligt med placebo. PAXIL 40 mg blev påvist at være signifikant bedre end placebo ved ændring fra baseline for CAPS-2 totalscore og andelen af respondere på CGI-I.
Et tredje studie, et studie med fleksibel dosis, der sammenlignede PAXIL 20 mg til 50 mg dagligt med placebo, viste, at PAXIL 20 mg var statistisk signifikant bedre end placebo ved ændring fra baseline for CAPS-2 total score, men ikke på andelen af respondere på CGI. -JEG.
Størstedelen af patienterne i disse undersøgelser var kvinder (68 % kvinder: 377 ud af 551 forsøgspersoner i undersøgelse 1 og 66 % kvinder: 202 ud af 303 forsøgspersoner i undersøgelse 2). Undergruppeanalyser indikerede ikke forskelle i behandlingsresultater som funktion af køn. Der var et utilstrækkeligt antal patienter, der var 65 år og ældre eller var ikke-kaukasiske til at udføre subgruppeanalyser på baggrund af henholdsvis alder eller race.
PATIENTOPLYSNINGER
PAXIL® (PAX-il)(paroxetin) tabletter og oral suspension
Hvad er den vigtigste information, jeg bør vide om PAXIL?
PAXIL kan forårsage alvorlige bivirkninger, herunder:
- Øget risiko for selvmordstanker eller -handlinger. PAXIL 10mg og anden antidepressiv medicin kan øge selvmordstanker og -handlinger hos nogle mennesker på 24 år og yngre, især inden for første par måneders behandling eller når dosis ændres. PAXIL er ikke beregnet til børn.
- Depression eller andre psykiske sygdomme er de vigtigste årsager til selvmordstanker og -handlinger.
Hvordan kan jeg holde øje med og forsøge at forhindre selvmordstanker og -handlinger?
- Vær meget opmærksom på ændringer, især pludselige ændringer i humør, adfærd, tanker eller følelser, eller hvis du udvikler selvmordstanker eller -handlinger. Dette er meget vigtigt, når en antidepressiv medicin påbegyndes, eller når dosis ændres.
- Ring til din sundhedsudbyder med det samme for at rapportere nye eller pludselige ændringer i humør, adfærd, tanker eller følelser, eller hvis du udvikler selvmordstanker eller -handlinger.
- Hold alle opfølgende besøg hos din sundhedsplejerske som planlagt. Ring til din læge mellem besøgene efter behov, især hvis du har bekymringer om symptomer.
Ring til din læge eller få akut lægehjælp med det samme, hvis du har nogle af følgende symptomer, især hvis de er nye, værre eller bekymrer dig:
- forsøg på at begå selvmord
- opfører sig aggressivt eller voldeligt
- ny eller værre depression
- føler sig ophidset, rastløs, vred eller irritabel
- øget aktivitet og taler mere end hvad der er normalt for dig
- handler på farlige impulser
- tanker om selvmord eller døende
- nye eller værre angst- eller panikanfald
- problemer med at sove
- andre usædvanlige ændringer i adfærd eller humør
Hvad er PAXIL?
PAXIL 30mg er en receptpligtig medicin, der bruges til voksne til behandling af:
- En bestemt type depression kaldet Major Depressive Disorder (MDD)
- Obsessiv-kompulsiv lidelse (OCD)
- Panikangst (PD)
- Social angstlidelse (SAD)
- Generaliseret angstlidelse (GAD)
- Posttraumatisk stresslidelse (PTSD)
Tag ikke PAXIL, hvis du:
- tage en monoaminoxidasehæmmer (MAOI)
- er holdt op med at tage en MAO-hæmmer inden for de sidste 14 dage
- behandles med antibiotikum linezolid eller intravenøs methylenblåt
- tager pimozid
- tager thioridazin
- er allergisk over for paroxetin eller et af indholdsstofferne i PAXIL. Se slutningen af denne medicinvejledning for en komplet liste over ingredienser i PAXIL.
Spørg din læge eller apotekspersonalet, hvis du ikke er sikker på, om du tager en MAO-hæmmer eller en af disse lægemidler, inklusive antibiotikum linezolid eller intravenøs methylenblåt.
Begynd ikke at tage en MAO-hæmmer i mindst 14 dage efter, at du stopper behandlingen med PAXIL.
Inden du tager PAXIL, skal du fortælle din læge om alle dine medicinske tilstande, inklusive hvis du:
- har hjerteproblemer
- har eller haft blødningsproblemer
- har eller har en familiehistorie med bipolar lidelse, mani eller hypomani
- har eller haft anfald eller kramper
- har glaukom (højt tryk i øjet)
- har lave natriumniveauer i dit blod
- har knogleproblemer
- har nyre- eller leverproblemer
- er gravid eller planlægger at blive gravid. PAXIL 40mg kan skade dit ufødte barn. Tal med din læge om risikoen for dit ufødte barn, hvis du tager PAXIL under graviditet. Fortæl din læge med det samme, hvis du bliver gravid eller tror, du er gravid under behandling med PAXIL.
- ammer eller planlægger at amme. PAXIL går over i din modermælk. Tal med din læge om den bedste måde at fodre din baby på under behandlingen med PAXIL.
Fortæl din læge om al den medicin, du tager, herunder receptpligtig og håndkøbsmedicin, vitaminer og naturlægemidler.
PAXIL og nogle andre lægemidler kan påvirke hinanden og forårsage mulige alvorlige bivirkninger. PAXIL 30 mg kan påvirke den måde, anden medicin virker på, og anden medicin kan påvirke den måde, hvorpå PAXIL virker.
Fortæl især din læge, hvis du tager:
- medicin, der bruges til at behandle migrænehovedpine kaldet triptaner
- tricykliske antidepressiva
- fentanyl
- lithium
- tramadol
- tryptofan
- buspiron
- amfetamin
- St. John's Wort
- medicin, der kan påvirke blodpropper såsom aspirin, ikke-steroide antiinflammatoriske lægemidler (NSAID), warfarin
- diuretika
- tamoxifen
- medicin, der bruges til at behandle humør-, angst-, psykotiske eller tankeforstyrrelser, herunder selektiv serontonin-genoptagelse (SSRI'er) og serotonin-noradrenalin-genoptagelseshæmmere (SNRI'er)
Spørg din læge, hvis du ikke er sikker på, om du tager nogen af disse lægemidler. Din læge kan fortælle dig, om det er sikkert at tage PAXIL 10mg sammen med din anden medicin.
Du må ikke starte eller stoppe anden medicin under behandling med PAXIL uden først at tale med din læge. Hvis du pludselig stopper PAXIL, kan det få dig til at få alvorlige bivirkninger. Se, "Hvad er de mulige bivirkninger af PAXIL 20mg?"
Kend den medicin du tager. Hold en liste over dem for at vise til din sundhedsplejerske og apotek, når du får en ny medicin.
Hvordan skal jeg tage PAXIL?
- Tag PAXIL nøjagtigt som foreskrevet. Din sundhedsplejerske skal muligvis ændre dosis af PAXIL 30 mg, indtil det er den rigtige dosis for dig.
- Tag PAXIL 1 gang hver dag om morgenen.
- PAXIL 30 mg kan tages med eller uden mad.
- Hvis du tager PAXIL oral suspension, skal du ryste suspensionen godt, før du tager den.
- Hvis du tager for meget PAXIL, skal du ringe til dit giftkontrolcenter på 1-800-222-1222 eller gå til den nærmeste skadestue på hospitalet med det samme.
Hvad er mulige bivirkninger af PAXIL 10mg?
PAXIL 40mg kan forårsage alvorlige bivirkninger, herunder:
- Se, "Hvad er den vigtigste information, jeg bør vide om PAXIL?"
- Serotonin syndrom. Et potentielt livstruende problem kaldet serotonergt syndrom kan opstå, når du tager PAXIL 20mg sammen med visse andre lægemidler. Se, "Hvem bør ikke tage PAXIL?" Ring til din sundhedsplejerske eller gå til nærmeste skadestue med det samme hvis du har nogle af følgende tegn og symptomer på serotonergt syndrom:
- agitation
- se eller høre ting, der ikke er ægte (hallucinationer)
- forvirring
- koma
- hurtig hjerterytme
- ændringer i blodtrykket
- svimmelhed
- svedtendens
- rødmen
- høj kropstemperatur (hypertermi)
- rysten (rysten), stive muskler eller muskeltrækninger
- tab af koordination
- anfald
- kvalme, opkastning, diarré
- Øjenproblemer (lukkende grøn stær). PAXIL 10mg kan forårsage en type øjenproblemer kaldet vinkel-lukkende glaukom hos personer med visse andre øjensygdomme. Det kan være en god idé at gennemgå en øjenundersøgelse for at se, om du er i fare, og få forebyggende behandling, hvis du er det. Ring til din læge, hvis du har øjensmerter, ændringer i dit syn eller hævelse eller rødme i eller omkring øjet.
- Medicin interaktioner. Indtagelse af PAXIL 20 mg sammen med visse andre lægemidler, herunder thioridazin og pimozid, kan øge risikoen for at udvikle et alvorligt hjerteproblem kaldet QT-forlængelse.
- Kramper (kramper).
- Maniske episoder. Maniske episoder kan forekomme hos personer med bipolar lidelse, som tager PAXIL. Symptomer kan omfatte:
- stærkt øget energi
- race tanker
- usædvanligt store ideer
- taler mere eller hurtigere end normalt
- svære søvnproblemer
- hensynsløs opførsel
- overdreven lykke eller irritabilitet
- Afbrydelsessyndrom. Pludselig ophør med PAXIL 20mg kan få dig til at få alvorlige bivirkninger. Din læge vil måske nedsætte din dosis langsomt. Symptomer kan omfatte:
- kvalme
- svedtendens
- ændringer i dit humør
- irritabilitet og agitation
- svimmelhed
- elektrisk stød følelse (paræstesi)
- rysten
- angst
- forvirring
- hovedpine
- træthed
- problemer med at sove
- hypomani
- ringen for dine ører (tinnitus)
- anfald
- Lavt natriumniveau i dit blod (hyponatriæmi). Lave natriumniveauer i dit blod, som kan være alvorlige og kan forårsage død, kan forekomme under behandling med PAXIL. Ældre mennesker og personer, der tager visse lægemidler, kan have en større risiko for at udvikle lave natriumniveauer i dit blod. Tegn og symptomer kan omfatte:
- hovedpine
- koncentrationsbesvær
- hukommelsesændringer
- forvirring
- svaghed og ustabilitet på dine fødder, som kan føre til fald
mere alvorlige eller mere pludselige tilfælde omfatter tegn og symptomer:
- se eller høre ting, der ikke er ægte (hallucinationer)
- besvimelse
- anfald
- koma
- vejrtrækningsstop (åndedrætsstop)
- Unormal blødning. At tage PAXIL sammen med aspirin, NSAID'er eller blodfortyndende medicin kan øge denne risiko. Fortæl din læge om enhver usædvanlig blødning eller blå mærker.
- Knoglebrud.
De mest almindelige bivirkninger af PAXIL 10mg omfatter:
- mandlige og kvindelige seksuelle funktionsproblemer
- forstoppelse
- diarré
- tør mund
- problemer med at sove
- nervøsitet
- svedtendens
- gaber
- svaghed (asteni)
- nedsat appetit
- svimmelhed
- infektion
- kvalme
- søvnighed
- rysten (rysten)
Disse er ikke alle de mulige bivirkninger af PAXIL.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan skal jeg opbevare PAXIL?
- Opbevar PAXIL-tabletter mellem 59°F til 86°F (15°C til 30°C).
- Opbevar PAXIL 10mg oral suspension ved eller under 77°F (25°C).
Opbevar PAXIL og al medicin utilgængeligt for børn.
Generel information om sikker og effektiv brug af PAXIL.
Lægemidler ordineres nogle gange til andre formål end dem, der er anført i en medicinvejledning. Tag ikke PAXIL for en tilstand, som det ikke er ordineret til. Giv ikke PAXIL til andre mennesker, selvom de har de samme symptomer, som du har. Det kan skade dem. Du kan bede din sundhedsudbyder eller apoteket om oplysninger om PAXIL, som er skrevet til sundhedspersonale.
Hvad er ingredienserne i PAXIL 30mg?
Aktiv ingrediens: paroxetin hydrochlorid
Inaktive ingredienser:
dibasisk calciumphosphatdihydrat, hypromellose, magnesiumstearat, polyethylenglycoler, polysorbat 80, natriumstivelsesglycolat, titaniumdioxid og 1 eller flere af følgende: D&C Red No. 30 aluminium lake, D&C Yellow No. 10 aluminium lake, No FD&C 2 aluminium sø, FD&C gul nr. 6 aluminium sø
Oral suspension: citronsyre (vandfri), FD&C gul nr. 6, smagsstoffer, glycerin, methylparaben, mikrokrystallinsk cellulose og carboxymethylcellulosenatrium, polacrilin kalium, propylenglycol, propylparaben, renset vand, saccharinnatrium, simeticonemulsion og natriumcitrat (dihydrat)
Denne medicinvejledning er godkendt af US Food and Drug Administration.
