Pamelor 25mg Nortriptyline Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Pamelor 25mg, og hvordan bruges det?
Pamelor 25mg er en receptpligtig medicin, der bruges til at behandle symptomerne på depression. Pamelor 25mg kan bruges alene eller sammen med anden medicin.
Pamelor tilhører en klasse af lægemidler kaldet antidepressiva, TCA'er.
Det vides ikke, om Pamelor er sikkert og effektivt til børn.
Hvad er de mulige bivirkninger af Pamelor 25mg?
Pamelor kan forårsage alvorlige bivirkninger, herunder:
- humørsvingninger,
- angst,
- Angstanfald,
- søvnbesvær,
- impulsiv adfærd,
- irritabilitet,
- agitation,
- fjendtlighed,
- aggression,
- rastløshed,
- hyperaktivitet (psykisk eller fysisk),
- øget depression,
- tanker om at skade dig selv,
- sløret syn,
- tunnelsyn,
- øjensmerter eller hævelse,
- ser glorier omkring lys,
- rastløse muskelbevægelser i dine øjne, tunge, kæbe eller nakke,
- svimmelhed,
- anfald,
- nye eller forværrede brystsmerter,
- bankende hjerteslag,
- flagrende i dit bryst,
- pludselig følelsesløshed eller svaghed,
- synsproblemer,
- besvær med tale eller balance,
- feber,
- ondt i halsen,
- let blå mærker,
- usædvanlig blødning,
- gulfarvning af huden eller øjnene (gulsot),
- smertefuld eller vanskelig vandladning,
- hurtig puls,
- overaktive reflekser,
- kvalme,
- opkastning,
- diarré,
- tab af koordination, og
- besvimelse
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Pamelor omfatter:
- kvalme,
- opkastning,
- mistet appetiten,
- angst,
- søvnproblemer (søvnløshed),
- tør mund,
- usædvanlig smag,
- lidt eller ingen vandladning,
- forstoppelse,
- synsforandringer,
- bryst hævelse (hos mænd eller kvinder),
- nedsat sexlyst,
- impotens, og
- svært ved at få orgasme
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Pamelor. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ADVARSEL
Suicidalitet og antidepressive stoffer
Antidepressiva øgede risikoen sammenlignet med placebo for selvmordstanker og -adfærd (suicidalitet) hos børn, unge og unge voksne i korttidsstudier af svær depressiv lidelse (MDD) og andre psykiatriske lidelser. Enhver, der overvejer at bruge nortriptylinhydrochlorid eller ethvert andet antidepressivt middel til et barn, en teenager eller en ung voksen, skal balancere denne risiko med det kliniske behov. Korttidsundersøgelser viste ikke en stigning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne efter 24 år; der var en reduktion i risikoen med antidepressiva sammenlignet med placebo hos voksne på 65 år og derover. Depression og visse andre psykiatriske lidelser er i sig selv forbundet med øget risiko for selvmord. Patienter i alle aldre, der påbegyndes med antidepressiv behandling, bør overvåges passende og observeres nøje for klinisk forværring, suicidalitet eller usædvanlige ændringer i adfærd. Familier og pårørende bør informeres om behovet for tæt observation og kommunikation med den ordinerende læge. Nortriptylinhydrochlorid er ikke godkendt til brug hos pædiatriske patienter (se ADVARSLER Klinisk forværring og selvmordsrisiko; PATIENTOPLYSNINGER ; og FORHOLDSREGLER , pædiatrisk brug).
BESKRIVELSE
Pamelor™ (nortriptylin HCI) er 1-propanamin, 3-(10,11-dihydro-5H-dibenzo[a,d]cyclohepten-5-yliden)-N-methyl-hydrochlorid.
Strukturformlen er som følger:
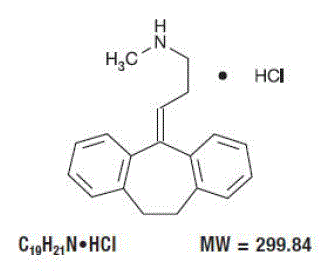
10 mg, 25 mg, 50 mg og 75 mg kapsler
Aktiv ingrediens
nortriptylinhydrochlorid USP.
10 mg, 25 mg og 75 mg kapsler
inaktive ingredienser
D&C Yellow #10, FD&C Yellow #6, gelatine, silikonevæske, stivelse og titaniumdioxid.
50 mg kapsler
inaktive ingredienser
gelatine, silikonevæske, stivelse og titaniumdioxid.
INDIKATIONER
Pamelor™ (nortriptylin HCl) er indiceret til lindring af symptomer på depression. Endogene depressioner er mere tilbøjelige til at blive lindret end andre depressive tilstande.
DOSERING OG ADMINISTRATION
Pamelor 25mg anbefales ikke til børn.
Pamelor indgives oralt i form af kapsler. Lavere end sædvanlige doser anbefales til ældre patienter og unge. Lavere doser anbefales også til ambulante patienter end til hospitalsindlagte patienter, som vil være under nøje opsyn. Lægen bør påbegynde doseringen på et lavt niveau og øge den gradvist, idet den omhyggeligt noterer det kliniske respons og eventuelle tegn på intolerance. Efter remission kan vedligeholdelsesmedicin være påkrævet i længere tid ved den laveste dosis, der vil opretholde remission.
Hvis en patient udvikler mindre bivirkninger, bør dosis reduceres. Lægemidlet skal seponeres omgående, hvis der opstår bivirkninger af alvorlig karakter eller allergiske manifestationer.
Sædvanlig voksendosis
25 mg tre eller fire gange dagligt; dosis bør begynde på et lavt niveau og øges efter behov. Som et alternativt regime kan den samlede daglige dosis gives én gang dagligt. Når doser over 100 mg dagligt administreres, bør plasmaniveauer af nortriptylin overvåges og holdes i det optimale område på 50 til 150 ng/ml. Doser over 150 mg/dag anbefales ikke.
Ældre og unge patienter
30 til 50 mg/dag, i opdelte doser, eller den samlede daglige dosis kan gives én gang dagligt.
At skifte en patient til eller fra en monoaminoxidasehæmmer (MAOI), beregnet til at behandle psykiatriske lidelser
Der bør gå mindst 14 dage mellem seponering af en MAO-hæmmer beregnet til behandling af psykiatriske lidelser og påbegyndelse af behandling med Pamelor. Omvendt bør der tillades mindst 14 dage efter ophør med Pamelor, før man starter en MAO-hæmmer beregnet til behandling af psykiatriske lidelser ( KONTRAINDIKATIONER ).
Brug af Pamelor 25mg med andre MAO-hæmmere, såsom linezolid eller methylenblåt
Start ikke Pamelor hos en patient, der er i behandling med linezolid eller intravenøs methylenblåt, da der er øget risiko for serotonergt syndrom. Hos en patient, som kræver mere akut behandling af en psykiatrisk tilstand, bør andre indgreb, herunder hospitalsindlæggelse, overvejes (se KONTRAINDIKATIONER ).
nogle tilfælde kan en patient, der allerede modtager Pamelor-behandling, have behov for akut behandling med linezolid eller intravenøs methylenblåt. Hvis acceptable alternativer til linezolid eller intravenøs methylenblåt behandling ikke er tilgængelige, og de potentielle fordele ved linezolid eller intravenøs methylenblåt behandling vurderes at opveje risikoen for serotonergt syndrom hos en bestemt patient, bør Pamelor 25 mg stoppes omgående, og linezolid eller intravenøs methylen blå kan administreres. Patienten skal overvåges for symptomer på serotonergt syndrom i to uger eller indtil 24 timer efter den sidste dosis linezolid eller intravenøs methylenblåt, alt efter hvad der kommer først. Behandling med Pamelor kan genoptages 24 timer efter den sidste dosis linezolid eller intravenøs methylenblåt (se ADVARSLER ).
Risikoen ved at administrere methylenblåt ad ikke-intravenøse veje (såsom orale tabletter eller ved lokal injektion) eller i intravenøse doser meget lavere end 1 mg/kg med Pamelor 25 mg er uklar. Lægen bør ikke desto mindre være opmærksom på muligheden for opståede symptomer på serotonergt syndrom ved sådan brug (se ADVARSLER ).
HVORDAN LEVERET
Pamelor™ (nortriptylin HCl) kapsler USP
Pamelor™ (nortriptylin HCl) kapsler USP, svarende til 10 mg, 25 mg, 50 mg og 75 mg base, er tilgængelige som følger:
10 mg : Lysorange uigennemsigtig hætte påtrykt " PAMELOR 10 mg" i sort og hvid uigennemsigtig krop påtrykt "M" i sort.
30 flasker: NDC 0406-9910-03
25 mg : Lysorange uigennemsigtig hætte påtrykt " PAMELOR 25 mg" i sort og hvid uigennemsigtig krop påtrykt "M" i sort.
30 flasker: NDC 0406-9911-03
50 mg : Hvid uigennemsigtig hætte påtrykt " PAMELOR 50 mg" i sort og hvid uigennemsigtig krop påtrykt "M" i sort.
30 flasker: NDC 0406-9912-03
75 mg Lysorange uigennemsigtig hætte påtrykt " PAMELOR 75 mg" i sort og lys orange uigennemsigtig krop påtrykt "M" i sort.
30 flasker: NDC 0406-9913-03
Opbevar og dispenser
Opbevares ved 20° til 25°C (68° til 77°F) [se USP kontrolleret rumtemperatur].
Dispenser i tæt beholder (USP) med en børnesikret lukning.
Mallinckrodt, mærket "M", Mallinckrodt Pharmaceuticals-logoet og andre mærker er varemærker tilhørende en Mallinckrodt-virksomhed.
Fremstillet af: Patheon Inc. Whitby, Ontario, Canada. L1N 5Z5. Revideret: oktober 2016
BIVIRKNINGER
Bemærk
Inkluderet i den følgende liste er nogle få bivirkninger, der ikke er blevet rapporteret med dette specifikke lægemiddel. Imidlertid kræver de farmakologiske ligheder blandt de tricykliske antidepressive lægemidler, at hver af reaktionerne tages i betragtning, når nortriptylin indgives.
Kardiovaskulær
Hypotension, hypertension, takykardi, hjertebanken, myokardieinfarkt, arytmier, hjerteblokade, slagtilfælde.
Psykiatrisk
Forvirringstilstande (især hos ældre) med hallucinationer, desorientering, vrangforestillinger; angst, rastløshed, agitation; søvnløshed, panik, mareridt; hypomani; forværring af psykose.
Neurologisk
Følelsesløshed, prikken, paræstesier i ekstremiteter; ukoordination, ataksi, rysten; perifer neuropati; ekstrapyramidale symptomer; krampeanfald, ændring i EEG-mønstre; tinnitus.
Antikolinergisk
Mundtørhed og sjældent associeret sublingual adenitis; sløret syn, forstyrrelse af indkvartering, mydriasis; obstipation, paralytisk ileus; urinretention, forsinket vandladning, udvidelse af urinvejene.
Allergisk
Hududslæt, petekkier, nældefeber, kløe, fotosensibilisering (undgå overdreven eksponering for sollys); ødem (generelt eller i ansigt og tunge), lægemiddelfeber, krydsfølsomhed med andre tricykliske lægemidler.
Hæmatologisk
Knoglemarvsdepression, herunder agranulocytose; eosinofili; purpura; trombocytopeni.
Gastrointestinale
Kvalme og opkastning, anoreksi, epigastrisk nød, diarré, ejendommelig smag, stomatitis, mavekramper, blacktongue.
Endokrine
Gynækomasti hos mænd, brystforstørrelse og galaktorrhea hos kvinden; øget eller nedsat libido, impotens; testikel hævelse; forhøjelse eller sænkning af blodsukkerniveauer; syndrom af uhensigtsmæssig ADH (antidiuretisk hormon) sekretion.
Andet
Gulsot (simulerer obstruktiv), ændret leverfunktion; vægtøgning eller -tab; sved; rødmen; urinfrekvens, nocturi; døsighed, svimmelhed, svaghed, træthed; hovedpine; parotis hævelse; alopeci.
Abstinenssymptomer
Selvom disse ikke er tegn på afhængighed, kan et pludseligt ophør af behandlingen efter langvarig behandling give kvalme, hovedpine og utilpashed.
Postmarketing oplevelse
Følgende bivirkning er blevet rapporteret under brug af Pamelor efter godkendelse. Fordi denne reaktion rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt at estimere hyppigheden pålideligt.
Hjertelidelser - Brugada syndrom
Øjenlidelser - vinkellukkende glaukom
DRUGSINTERAKTIONER
Administration af reserpin under behandling med et tricyklisk antidepressivum har vist sig at give en "stimulerende" effekt hos nogle deprimerede patienter.
Tæt overvågning og omhyggelig justering af dosis er påkrævet, når Pamelor 25 mg anvendes sammen med andre antikolinerge lægemidler og sympatomimetika.
Samtidig administration af cimetidin og tricykliske antidepressiva kan give klinisk signifikante stigninger i plasmakoncentrationerne af det tricykliske antidepressivum. Patienten skal informeres om, at reaktionen på alkohol kan være overdrevet.
Et tilfælde af signifikant hypoglykæmi er blevet rapporteret hos en type II diabetespatient, der blev holdt på chlorpropamid (250 mg/dag), efter tilsætning af nortriptylin (125 mg/dag).
Lægemidler metaboliseret af P450 2D6
Den biokemiske aktivitet af lægemidlets metaboliserende isozym cytochrom P450 2D6 (debrisoquinhydroxylase) er reduceret i en undergruppe af den kaukasiske befolkning (ca. 7% til 10% af kaukasiere er såkaldte "dårlige metabolisatorer"); pålidelige skøn over forekomsten af reduceret P450 2D6 isozymaktivitet blandt asiatiske, afrikanske og andre populationer er endnu ikke tilgængelige. Dårlige metabolisatorer har højere end forventet plasmakoncentrationer af tricykliske antidepressiva (TCA'er), når de gives sædvanlige doser. Afhængigt af fraktionen af lægemidlet, der metaboliseres af P450 2D6, kan stigningen i plasmakoncentration være lille eller ret stor (8 gange stigning i plasma AUC af TCA).
Derudover hæmmer visse lægemidler aktiviteten af dette isozym og får normale metabolisatorer til at ligne dårlige metabolisatorer. Et individ, der er stabilt på en given dosis af TCA, kan blive brat toksisk, når det gives et af disse hæmmende lægemidler som samtidig behandling. De lægemidler, der hæmmer cytochrom P450 2D6, omfatter nogle, der ikke metaboliseres af enzymet (quinidin; cimetidin) og mange, der er substrater for P450 2D6 (mange andre antidepressiva, phenothiaziner og Type 1C antiarytmika propafenon og flecainid). Mens alle de selektive serotoningenoptagelseshæmmere (SSRI'er), f.eks. fluoxetin, sertralin og paroxetin, hæmmer P450 2D6, kan de variere i omfanget af inhibering. I hvilket omfang SSRI TCA-interaktioner kan give kliniske problemer, vil afhænge af graden af hæmning og farmakokinetikken af det involverede SSRI. Ikke desto mindre er forsigtighed indiceret ved samtidig administration af TCA'er med nogen af SSRI'erne og også ved skift fra den ene klasse til den anden. Af særlig vigtighed skal der gå tilstrækkelig tid, før TCA-behandling påbegyndes hos en patient, der seponeres med fluoxetin, i betragtning af den lange halveringstid af forælderen og den aktive metabolit (mindst 5 uger kan være nødvendigt).
Samtidig brug af tricykliske antidepressiva og lægemidler, der kan hæmme cytochrom P450 2D6, kan kræve lavere doser end normalt foreskrevet for enten det tricykliske antidepressivum eller det andet lægemiddel. Desuden kan en øget dosis af tricyklisk antidepressivum være nødvendig, når et af disse andre lægemidler trækkes ud af samtidig behandling. Det er ønskeligt at overvåge TCA-plasmaniveauer, når en TCA skal administreres sammen med et andet lægemiddel, der vides at være en hæmmer af P450 2D6.
ADVARSLER
Klinisk forværring og selvmordsrisiko
Patienter med svær depressiv lidelse (MDD), både voksne og pædiatriske, kan opleve forværring af deres depression og/eller fremkomsten af selvmordstanker og -adfærd (suicidalitet) eller usædvanlige ændringer i adfærd, uanset om de tager antidepressiv medicin eller ej, og dette risikoen kan fortsætte, indtil der indtræffer betydelig remission. Selvmord er en kendt risiko for depression og visse andre psykiatriske lidelser, og disse lidelser er i sig selv de stærkeste forudsigere for selvmord. Der har imidlertid været en langvarig bekymring for, at antidepressiva kan have en rolle i at inducere forværring af depression og fremkomsten af suicidalitet hos visse patienter i de tidlige faser af behandlingen. Samlede analyser af kortsigtede placebokontrollerede forsøg med antidepressive lægemidler (SSRI'er og andre) viste, at disse lægemidler øger risikoen for selvmordstanker og -adfærd (suicidalitet) hos børn, unge og unge voksne (i alderen 18 til 24) med svær depression. lidelse (MDD) og andre psykiatriske lidelser. Korttidsundersøgelser viste ikke en stigning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne efter 24 år; der var en reduktion med antidepressiva sammenlignet med placebo hos voksne på 65 år og ældre.
De samlede analyser af placebokontrollerede forsøg med børn og unge med MDD, obsessiv-kompulsiv lidelse (OCD) eller andre psykiatriske lidelser omfattede i alt 24 korttidsforsøg med 9 antidepressive lægemidler hos over 4400 patienter. De samlede analyser af placebokontrollerede forsøg med voksne med MDD eller andre psykiatriske lidelser omfattede i alt 295 korttidsforsøg (median varighed på 2 måneder) med 11 antidepressive lægemidler hos over 77.000 patienter. Der var betydelig variation i risikoen for suicidalitet blandt stoffer, men en tendens til en stigning i de yngre patienter for næsten alle undersøgte stoffer. Der var forskelle i den absolutte risiko for suicidalitet på tværs af de forskellige indikationer, med den højeste forekomst af MDD. Risikoforskellene (lægemiddel vs. placebo) var dog relativt stabile inden for aldersgrupper og på tværs af indikationer. Disse risikoforskelle (lægemiddel-placeboforskel i antallet af tilfælde af suicidalitet pr. 1000 behandlede patienter) er angivet i .
Der forekom ingen selvmord i nogen af de pædiatriske forsøg. Der var selvmord i voksenforsøgene, men antallet var ikke tilstrækkeligt til at nå frem til nogen konklusion om lægemiddeleffekt på selvmord.
Det er uvist, om suicidalitetsrisikoen strækker sig til længerevarende brug, dvs. ud over flere måneder. Der er dog væsentlige beviser fra placebokontrollerede vedligeholdelsesforsøg hos voksne med depression, at brugen af antidepressiva kan forsinke tilbagefald af depression.
Alle patienter, der behandles med antidepressiva for enhver indikation, bør overvåges passende og observeres nøje for klinisk forværring, suicidalitet og usædvanlige ændringer i adfærd, især i løbet af de første par måneder af et lægemiddelbehandlingsforløb, eller i tidspunkter med dosisændringer, enten stigninger eller falder.
Følgende symptomer, angst, agitation, panikanfald, søvnløshed, irritabilitet, fjendtlighed, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshed), hypomani og mani er blevet rapporteret hos voksne og pædiatriske patienter, der også behandles med antidepressiva mod svær depressiv lidelse. som for andre indikationer, både psykiatriske og ikke-psykiatriske. Selvom der ikke er etableret en årsagssammenhæng mellem fremkomsten af sådanne symptomer og enten forværring af depression og/eller fremkomsten af selvmordsimpulser, er der bekymring for, at sådanne symptomer kan repræsentere forløbere for ny suicidalitet.
Det bør overvejes at ændre det terapeutiske regime, herunder eventuelt seponering af medicinen, hos patienter, hvis depression er vedvarende værre, eller som oplever ny suicidalitet eller symptomer, der kan være forløbere for forværring af depression eller suicidalitet, især hvis disse symptomer er alvorlige, pludselige i debut, eller var ikke en del af patientens tilstedeværende symptomer.
Familier og pårørende til patienter, der behandles med antidepressiva for svær depressiv lidelse eller andre indikationer, både psykiatriske og ikke-psykiatriske, bør advares om behovet for at overvåge patienter for fremkomsten af agitation, irritabilitet, usædvanlige ændringer i adfærd og de andre symptomer beskrevet ovenfor. , samt fremkomsten af suicidalitet, og at rapportere sådanne symptomer omgående til sundhedsudbydere. Sådan overvågning bør omfatte daglig observation af familier og omsorgspersoner. Recepter for nortriptylinhydrochlorid bør udskrives for den mindste mængde kapsler i overensstemmelse med god patientbehandling for at reducere risikoen for overdosering.
Screening af patienter for bipolar lidelse
En alvorlig depressiv episode kan være den første præsentation af bipolar lidelse. Det antages generelt (dog ikke etableret i kontrollerede forsøg), at behandling af en sådan episode med et antidepressivum alene kan øge sandsynligheden for udfældning af en blandet/manisk episode hos patienter med risiko for bipolar lidelse. Hvorvidt nogen af de ovenfor beskrevne symptomer repræsenterer en sådan omdannelse er ukendt. Inden behandling med et antidepressivum påbegyndes, bør patienter med depressive symptomer dog screenes tilstrækkeligt for at afgøre, om de har risiko for bipolar lidelse; sådan screening bør omfatte en detaljeret psykiatrisk historie, herunder en familiehistorie med selvmord, bipolar lidelse og depression. Det skal bemærkes, at nortriptylinhydrochlorid ikke er godkendt til brug ved behandling af bipolar depression.
Patienter med kardiovaskulær sygdom bør kun gives Pamelor 25 mg under nøje overvågning på grund af lægemidlets tendens til at producere sinustakykardi og forlænge ledningstiden. Myokardieinfarkt, arytmi og slagtilfælde er forekommet. Den antihypertensive virkning af guanethidin og lignende midler kan være blokeret. På grund af dets antikolinerge aktivitet bør Pamelor anvendes med stor forsigtighed til patienter, som tidligere har haft urinretention. Patienter med anfald i anamnesen bør følges nøje, når Pamelor 25 mg administreres, da dette lægemiddel vides at sænke krampetærsklen. Der kræves stor forsigtighed, hvis Pamelor gives til hyperthyreoideapatienter eller til dem, der får thyreoideamedicin, da der kan udvikles hjertearytmier.
Pamelor kan svække de mentale og/eller fysiske evner, der kræves for at udføre farlige opgaver, såsom at betjene maskiner eller køre bil; derfor bør patienten advares i overensstemmelse hermed.
Overdreven indtagelse af alkohol i kombination med nortriptylinbehandling kan have en potentierende effekt, som kan føre til fare for øgede selvmordsforsøg eller overdosering, især hos patienter med historier om følelsesmæssige forstyrrelser eller selvmordstanker.
Samtidig administration af quinidin og nortriptylin kan resultere i en signifikant længere plasmahalveringstid, højere AUC og lavere clearance af nortriptylin.
Serotonin syndrom
Udviklingen af et potentielt livstruende serotonergt syndrom er blevet rapporteret med SNRI og SSRI, inklusive Pamelor 25 mg, alene, men især ved samtidig brug af andre serotonerge lægemidler (inklusive triptaner, tricykliske antidepressiva, fentanyl, lithium, tramadol, tryptofan, buspiron, buspiron, perikon) og med lægemidler, der hæmmer metabolismen af serotonin (især MAO-hæmmere, både dem, der er beregnet til at behandle psykiatriske lidelser og også andre, såsom linezolid og intravenøs methylenblåt).
Symptomer på serotonergt syndrom kan omfatte ændringer i mental status (f.eks. agitation, hallucinationer, delirium og koma), autonom ustabilitet (f.eks. takykardi, labilt blodtryk, svimmelhed, diaforese, rødmen, hypertermi), neuromuskulære ændringer (f.eks. tremor, rigiditet, myoklonus, hyperrefleksi, inkoordination), kramper og/eller gastrointestinale symptomer (f.eks. kvalme, opkastning, diarré). Patienter bør overvåges for forekomsten af serotonergt syndrom.
Samtidig brug af Pamelor 25 mg og MAO-hæmmere beregnet til behandling af psykiatriske lidelser er kontraindiceret. Pamelor bør heller ikke startes hos en patient, der er i behandling med MAO-hæmmere såsom linezolid eller intravenøs methylenblåt. Alle rapporter med methylenblåt, der gav information om indgivelsesvejen, involverede intravenøs administration i dosisområdet fra 1 mg/kg til 8 mg/kg. Ingen rapporter involverede administration af methylenblåt ad andre veje (såsom orale tabletter eller lokal vævsinjektion) eller ved lavere doser. Der kan være omstændigheder, hvor det er nødvendigt at påbegynde behandling med en MAO-hæmmer såsom linezolid eller intravenøs methylenblåt hos en patient, der tager Pamelor. Pamelor 25 mg bør seponeres, før behandling med MAO-hæmmere påbegyndes (se KONTRAINDIKATIONER og DOSERING OG ADMINISTRATION ).
Hvis samtidig brug af Pamelor 25mg med andre serotonerge lægemidler, inklusive triptaner, tricykliske antidepressiva, fentanyl, lithium, tramadol, buspiron, tryptofan og perikon er klinisk berettiget, skal patienterne gøres opmærksomme på en potentiel øget risiko for serotonergt syndrom, især under behandlingsstart og dosisstigninger.
Behandling med Pamelor 25 mg og eventuelle samtidige serotonerge midler skal seponeres øjeblikkeligt, hvis ovennævnte hændelser opstår, og understøttende symptomatisk behandling bør påbegyndes.
Afsløring af Brugada syndrom
Der har efter markedsføring været rapporter om en mulig sammenhæng mellem behandling med Pamelor og afsløringen af Brugadas syndrom. Brugada syndrom er en lidelse karakteriseret ved synkope, unormale elektrokardiografiske (EKG) fund og en risiko for pludselig død. Pamelor bør generelt undgås hos patienter med Brugada syndrom eller dem, der mistænkes for at have Brugada syndrom.
Vinkel-lukkende glaukom
Pupiludvidelsen, der opstår efter brug af mange antidepressive lægemidler, inklusive Pamelor 25 mg, kan udløse et vinkel-lukningsangreb hos en patient med anatomisk snævre vinkler, som ikke har en patenteret iridektomi.
Brug under graviditet
Sikker brug af Pamelor under graviditet og amning er ikke blevet fastslået; Derfor, når lægemidlet administreres til gravide patienter, ammende mødre eller kvinder i den fødedygtige alder, skal de potentielle fordele afvejes mod de mulige farer. Dyreproduktionsundersøgelser har givet uafklarede resultater.
FORHOLDSREGLER
Information til patienter
Ordinerende læger eller andre sundhedsprofessionelle bør informere patienter, deres familier og deres pårørende om fordele og risici forbundet med behandling med nortriptylinhydrochlorid og bør rådgive dem om dens passende brug. En patient Medicinvejledning om "Antidepressiv medicin, depression og anden alvorlig psykisk sygdom og selvmordstanker eller handlinger" er tilgængelig for nortriptylinhydrochlorid. Den ordinerende læge eller sundhedspersonalet bør instruere patienter, deres familier og deres pårørende i at læse medicinvejledningen og skal hjælpe dem med at forstå dens indhold. Patienterne bør have mulighed for at diskutere indholdet af Medicinvejledning og få svar på de spørgsmål, de måtte have. Hele teksten til medicinvejledningen er genoptrykt i slutningen af dette dokument.
Patienter bør informeres om følgende problemer og bedes om at advare deres ordinerende læge, hvis disse opstår, mens de tager nortriptylinhydrochlorid.
Klinisk forværring og selvmordsrisiko
Patienter, deres familier og deres pårørende bør opmuntres til at være opmærksomme på fremkomsten af angst, agitation, panikanfald, søvnløshed, irritabilitet, fjendtlighed, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshed), hypomani, mani, andre usædvanlige ændringer i adfærd. , forværring af depression og selvmordstanker, især tidligt under antidepressiv behandling, og når dosis justeres op eller ned. Familier og pårørende til patienter bør rådes til at se efter forekomsten af sådanne symptomer på daglig basis, da ændringer kan være pludselige. Sådanne symptomer bør indberettes til patientens ordinerende læge eller sundhedspersonale, især hvis de er alvorlige, pludseligt opståede eller ikke var en del af patientens symptomer. Symptomer som disse kan være forbundet med en øget risiko for selvmordstanker og -adfærd og indikerer behov for meget tæt overvågning og muligvis ændringer i medicinen.
Brugen af Pamelor til skizofrene patienter kan resultere i en forværring af psykosen eller kan aktivere latente skizofrene symptomer. Hvis lægemidlet gives til overaktive eller ophidsede patienter, kan der opstå øget angst og agitation. Hos maniodepressive patienter kan Pamelor få symptomer på den maniske fase til at opstå.
Besværlig patientfjendtlighed kan vækkes ved brug af Pamelor. Epileptiforme anfald kan ledsage dets administration, som det er tilfældet med andre lægemidler af denne klasse.
Når det er vigtigt, kan lægemidlet administreres med elektrokonvulsiv terapi, selvom farerne kan være øget. Afbryd lægemidlet i flere dage, hvis det er muligt, før elektiv operation.
Muligheden for et selvmordsforsøg fra en deprimeret patient består efter påbegyndelse af behandlingen; i den forbindelse er det vigtigt, at den mindst mulige mængde lægemiddel udleveres til enhver tid.
Både forhøjede og sænkede blodsukkerniveauer er blevet rapporteret.
Patienter bør informeres om, at indtagelse af Pamelor 25 mg kan forårsage mild pupiludvidelse, som hos følsomme personer kan føre til en episode med vinkel-lukkende glaukom. Eksisterende glaukom er næsten altid åbenvinklet glaukom, fordi vinkel-lukkende glaukom, når det diagnosticeres, kan behandles definitivt med iridektomi. Åbenvinklet glaukom er ikke en risikofaktor for lukkevinklet glaukom. Patienter kan ønske at blive undersøgt for at afgøre, om de er modtagelige for vinkellukning, og have en profylaktisk procedure (f.eks. iridektomi), hvis de er modtagelige.
Monoaminoxidasehæmmere (MAO-hæmmere)
(Se KONTRAINDIKATIONER , ADVARSLER , og DOSERING OG ADMINISTRATION .)
Serotonerge lægemidler
(Se KONTRAINDIKATIONER , ADVARSLER , og DOSERING OG ADMINISTRATION .)
Pædiatrisk brug
Sikkerhed og effektivitet i den pædiatriske population er ikke blevet fastslået (se KASSE ADVARSEL og ADVARSLER , Clinical Wors ening og selvmordsrisiko k). Enhver, der overvejer at bruge nortriptylinhydrochlorid til et barn eller en ung, skal balancere de potentielle risici med det kliniske behov.
Geriatrisk brug
Kliniske undersøgelser af Pamelor omfattede ikke et tilstrækkeligt antal forsøgspersoner på 65 år og derover til at afgøre, om de reagerer anderledes end yngre forsøgspersoner. Andre rapporterede kliniske erfaringer indikerer, at som med andre tricykliske antidepressiva, er leverbivirkninger (hovedsageligt kendetegnet ved gulsot og forhøjede leverenzymer) observeret meget sjældent hos geriatriske patienter, og dødsfald forbundet med kolestatisk leverskade er blevet rapporteret i isolerede tilfælde. Kardiovaskulær funktion, især arytmier og fluktuationer i blodtrykket, bør overvåges. Der har også været rapporter om forvirringstilstande efter administration af tricykliske antidepressiva hos ældre. Højere plasmakoncentrationer af den aktive nortriptylinmetabolit, 10-hydroxynortriptylin, er også blevet rapporteret hos ældre patienter. Som med andre tricykliske antidepressiva bør dosisvalg til en ældre patient normalt begrænses til den mindste effektive samlede daglige dosis (se DOSERING OG ADMINISTRATION ).
OVERDOSIS
Dødsfald kan forekomme som følge af overdosering med denne klasse af lægemidler. Indtagelse af flere lægemidler (herunder alkohol) er almindelig ved bevidst overdosis af tricykliske antidepressiva. Da håndteringen er kompleks og skiftende, anbefales det, at lægen kontakter en giftcentral for løbende information om behandlingen. Tegn og symptomer på toksicitet udvikler sig hurtigt efter tricyklisk antidepressiv overdosis, derfor er hospitalsovervågning påkrævet så hurtigt som muligt.
Manifestationer
Kritiske manifestationer af overdosering omfatter: hjerterytmeforstyrrelser, alvorlig hypotension, shock, kongestiv hjertesvigt, lungeødem, kramper og CNS-depression, herunder koma. Ændringer i elektrokardiogrammet, især i QRS-aksen eller -bredden, er klinisk signifikante indikatorer for tricyklisk antidepressiv toksicitet.
Andre tegn på overdosering kan omfatte: forvirring, rastløshed, forstyrret koncentration, forbigående visuelle hallucinationer, udvidede pupiller, agitation, hyperaktive reflekser, stupor, døsighed, muskelstivhed, opkastning, hypotermi, hyperpyreksi eller nogen af de akutte symptomer, der er anført under BIVIRKNINGER . Der har været rapporter om patienter, der er kommet sig efter nortriptylin-overdoser på op til 525 mg.
Ledelse
Generel
Få et EKG og påbegynd straks hjerteovervågning. Beskyt patientens luftveje, opret en intravenøs linje og påbegynd gastrisk dekontaminering. Det er nødvendigt med mindst seks timers observation med hjerteovervågning og observation for tegn på CNS eller respirationsdepression, hypotension, hjerterytmeforstyrrelser og/eller ledningsblokke og kramper. Hvis der opstår tegn på toksicitet på noget tidspunkt i denne periode, er udvidet overvågning påkrævet. Der er tilfælde af patienter, der bukker under for fatale dysrytmier sent efter overdosering; disse patienter havde kliniske tegn på signifikant forgiftning før døden, og de fleste modtog utilstrækkelig gastrointestinal dekontaminering. Overvågning af plasmaniveauer af lægemiddel bør ikke vejlede behandlingen af patienten.
Gastrointestinal dekontaminering
Alle patienter, der mistænkes for overdosering af tricyklisk antidepressiv medicin, bør modtage gastrointestinal dekontaminering. Dette bør omfatte stor volumen maveskylning efterfulgt af aktivt kul. Hvis bevidstheden er svækket, skal luftvejene sikres før udskylning. EMESIS ER KONTRAINDICERET.
Kardiovaskulær
En maksimal QRS-varighed på ≥0,10 sekunder kan være den bedste indikation af sværhedsgraden af overdoseringen. Intravenøst natriumbicarbonat bør anvendes for at opretholde serum-pH i området 7,45 til 7,55. Hvis pH-responsen er utilstrækkelig, kan hyperventilation også anvendes. Samtidig brug af hyperventilation og natriumbicarbonat bør ske med ekstrem forsigtighed med hyppig pH-overvågning. En pH >7,60 eller en pCO
CNS
Hos patienter med CNS-depression tilrådes tidlig intubation på grund af risikoen for pludselig forværring. Anfald bør kontrolleres med benzodiazepiner, eller hvis disse er ineffektive, andre antikonvulsiva (f.eks. phenobarbital, phenytoin). Physostigmin anbefales ikke undtagen til behandling af livstruende symptomer, der ikke har reageret på andre behandlinger, og da kun i samråd med et giftkontrolcenter.
Psykiatrisk opfølgning
Da overdosering ofte er bevidst, kan patienter forsøge selvmord på andre måder i genopretningsfasen. Psykiatrisk henvisning kan være passende.
Pædiatrisk ledelse
Principperne for håndtering af overdosering af børn og voksne er ens. Det anbefales kraftigt, at lægen kontakter det lokale giftkontrolcenter for specifik pædiatrisk behandling.
KONTRAINDIKATIONER
Monoaminoxidasehæmmere (MAO-hæmmere)
Brugen af MAO-hæmmere beregnet til behandling af psykiatriske lidelser med Pamelor 25 mg eller inden for 14 dage efter ophør af behandling med Pamelor 25 mg er kontraindiceret på grund af en øget risiko for serotonergt syndrom. Brugen af Pamelor 25 mg inden for 14 dage efter ophør med en MAO-hæmmer beregnet til behandling af psykiatriske lidelser er også kontraindiceret (se ADVARSLER og DOSERING OG ADMINISTRATION ).
Begyndelse af Pamelor 25 mg hos en patient, der er i behandling med MAO-hæmmere såsom linezolid eller intravenøs methylenblåt, er også kontraindiceret på grund af en øget risiko for serotonergt syndrom (se ADVARSLER og DOSERING OG ADMINISTRATION ).
Overfølsomhed over for tricykliske antidepressiva
Krydsfølsomhed mellem Pamelor og andre dibenzazepiner er en mulighed.
Myokardieinfarkt
Pamelor 25mg er kontraindiceret i den akutte restitutionsperiode efter myokardieinfarkt.
KLINISK FARMAKOLOGI
Mekanismen for humørforhøjelse af tricykliske antidepressiva er på nuværende tidspunkt ukendt. Pamelor 25mg er ikke en monoaminoxidasehæmmer. Det hæmmer aktiviteten af så forskellige midler som histamin, 5-hydroxytryptamin og acetylcholin. Det øger pressoreffekten af noradrenalin, men blokerer for phenethylamins pressorrespons. Undersøgelser tyder på, at Pamelor 25mg interfererer med transport, frigivelse og opbevaring af katekolaminer. Operante konditioneringsteknikker hos rotter og duer tyder på, at Pamelor har en kombination af stimulerende og depressive egenskaber.
PATIENTOPLYSNINGER
Pamelor™ (nortriptylin HCI) Kapsler USP
Antidepressiv medicin, depression og andre alvorlige psykiske sygdomme og selvmordstanker eller -handlinger
Læs medicinvejledningen, der følger med dig eller dit familiemedlems antidepressive medicin. Denne medicinvejledning handler kun om risikoen for selvmordstanker og -handlinger med antidepressiv medicin.
Tal med din eller dit familiemedlems sundhedsplejerske om:
- alle risici og fordele ved behandling med antidepressiv medicin
- alle behandlingsvalg for depression eller anden alvorlig psykisk sygdom
Hvad er den vigtigste information, jeg bør vide om antidepressiv medicin, depression og andre alvorlige psykiske sygdomme og selvmordstanker eller -handlinger?
- Vær meget opmærksom på ændringer, især pludselige ændringer, i humør, adfærd, tanker eller følelser. Dette er meget vigtigt, når en antidepressiv medicin startes, eller når dosis ændres.
- Ring til sundhedsudbyderen med det samme for at rapportere nye eller pludselige ændringer i humør, adfærd, tanker eller følelser.
- Hold alle opfølgende besøg hos sundhedsplejersken som planlagt. Ring til lægen mellem besøgene efter behov, især hvis du har bekymringer om symptomer.
Ring til en sundhedsudbyder med det samme, hvis du eller dit familiemedlem har nogle af følgende symptomer, især hvis de er nye, værre eller bekymrer dig:
- tanker om selvmord eller døende
- forsøg på at begå selvmord
- ny eller værre depression
- ny eller værre angst
- føler sig meget ophidset eller rastløs
- Angstanfald
- søvnbesvær (søvnløshed)
- ny eller værre irritabilitet
- opfører sig aggressivt, er vred eller voldelig
- handler på farlige impulser
- en ekstrem stigning i aktivitet og tale (mani)
- andre usædvanlige ændringer i adfærd eller humør
Visuelle problemer
- øjensmerter
- ændringer i synet
- hævelse eller rødme i eller omkring øjet
Kun nogle mennesker er i fare for disse problemer. Det kan være en god idé at gennemgå en øjenundersøgelse for at se, om du er i fare, og få forebyggende behandling, hvis du er det.
Hvem bør ikke tage Pamelor?
Tag ikke Pamelor, hvis du:
- tage en monoaminoxidasehæmmer (MAOI). Spørg din læge eller apotekspersonalet, hvis du ikke er sikker på, om du tager en MAO-hæmmer, inklusive antibiotikummet linezolid.
- Tag ikke en MAO-hæmmer inden for 2 uger efter at have stoppet Pamelor 25 mg, medmindre din læge har bedt det om det.
- Start ikke Pamelor 25 mg, hvis du stoppede med at tage en MAO-hæmmer inden for de sidste 2 uger, medmindre din læge har bedt dig om det.
Hvad skal jeg ellers vide om antidepressiv medicin?
- Stop aldrig en antidepressiv medicin uden først at tale med en læge. Hvis du pludselig stopper en antidepressiv medicin, kan det forårsage andre symptomer.
- Antidepressiva er medicin, der bruges til at behandle depression og andre sygdomme. Det er vigtigt at diskutere alle risiciene ved behandling af depression og også risiciene ved ikke at behandle den. Patienter og deres familier eller andre pårørende bør diskutere alle behandlingsvalg med sundhedsudbyderen, ikke kun brugen af antidepressiva.
- Antidepressiv medicin har andre bivirkninger. Tal med lægen om bivirkningerne af den medicin, der er ordineret til dig eller dit familiemedlem.
- Antidepressiv medicin kan interagere med anden medicin. Kend alle de lægemidler, du eller dit familiemedlem tager. Hold en liste over alle lægemidler for at vise sundhedsudbyderen. Start ikke med ny medicin uden først at tjekke med din læge.
- Ikke alle antidepressive lægemidler ordineret til børn er FDA godkendt til brug hos børn. Tal med dit barns sundhedsplejerske for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Denne medicinvejledning er godkendt af US Food and Drug Administration.
