Ditropan 2.5mg, 5mg Oxybutynin Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Ditropan, og hvordan bruges det?
Ditropan er en receptpligtig medicin, der bruges til at behandle symptomerne på en overaktiv blære. Ditropan 5mg kan bruges alene eller sammen med anden medicin.
Ditropan tilhører en klasse af lægemidler kaldet Antispasmodic Agents, Urinary.
Det vides ikke, om Ditropan er sikkert og effektivt til børn under 5 år.
Hvad er de mulige bivirkninger af Ditropan?
Ditropan kan forårsage alvorlige bivirkninger, herunder:
- stærke mavesmerter,
- forstoppelse,
- sløret syn,
- tunnelsyn,
- øjensmerter,
- ser glorier omkring lys,
- lidt eller ingen vandladning,
- smertefuld eller vanskelig vandladning,
- føler sig tørstig eller varm,
- ude af stand til at tisse,
- kraftig svedtendens, og
- varm og tør hud
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Ditropan omfatter:
- svimmelhed,
- døsighed,
- sløret syn,
- tør mund,
- diarré, og
- forstoppelse
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Ditropan. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Hver bikonveks, indgraveret blå DITROPAN® (oxybutyninchlorid) tablet indeholder 5 mg oxybutyninchlorid. Kemisk er oxybutyninchlorid d,l (racemisk) 4-diethylamino-2-butynylphenylcyclohexylglycolathydrochlorid. Det
empirisk formel for oxybutyninchlorid er C22H31NO3•HCl. Strukturformlen ses nedenfor:
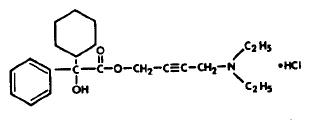
Oxybutyninchlorid er et hvidt krystallinsk fast stof med en molekylvægt på 393,9. Det er letopløseligt i vand og syrer, men relativt uopløseligt i alkalier.
DITROPAN tabletter indeholder også calciumstearat, FD&C Blue #1 Lake, laktose og mikrokrystallinsk cellulose.
DITROPAN tabletter er til oral administration.
Terapeutisk kategori: Antispasmodisk, antikolinerg.
INDIKATIONER
DITROPAN 2,5 mg XL® (oxybutyninchlorid) er en muskarin antagonist indiceret til behandling af overaktiv blære med symptomer på urge-inkontinens, trang og hyppighed.
DITROPAN XL® er også indiceret til behandling af pædiatriske patienter i alderen 6 år og ældre med symptomer på detrusoroveraktivitet forbundet med en neurologisk tilstand (f.eks. spina bifida).
DOSERING OG ADMINISTRATION
DITROPAN 2,5mg XL® skal sluges hel ved hjælp af væsker og må ikke tygges, deles eller knuses.
DITROPAN XL® kan indgives med eller uden mad.
Voksne
Den anbefalede startdosis af DITROPAN 5mg XL® er 5 eller 10 mg én gang dagligt på omtrent samme tidspunkt hver dag. Dosis kan justeres i trin på 5 mg for at opnå en balance mellem effektivitet og tolerabilitet (op til et maksimum på 30 mg/dag). Generelt kan dosisjustering ske med ca. ugentlige intervaller.
Pædiatriske patienter i alderen 6 år og ældre
Den anbefalede startdosis af DITROPAN 5mg XL® er 5 mg én gang dagligt på omtrent samme tidspunkt hver dag. Dosis kan justeres i trin på 5 mg for at opnå en balance mellem effektivitet og tolerabilitet (op til et maksimum på 20 mg/dag).
HVORDAN LEVERET
Doseringsformer og styrker
DITROPAN 5mg XL® tabletter med forlænget frigivelse fås som 5 og 10 mg tabletter til oral brug:
5 mg : Lysegul, rund tablet med "5 XL" trykt på den ene side med sort blæk.
10 mg Lyserød, rund tablet med "10 XL" trykt på den ene side med sort blæk.
Opbevaring og håndtering
DITROPAN XL® tabletter med forlænget frigivelse fås i to doseringsstyrker, 5 mg (lysegul) og 10 mg (lyserød) og er præget på den ene side med "5 XL" eller "10 XL" med sort blæk. DITROPAN XL® tabletter med forlænget frigivelse leveres i flasker med 100 tabletter.
Opbevaring
Opbevares ved 25°C (77°F); udflugter tilladt til 15–30°C (59–86°F) [se USP kontrolleret rumtemperatur ]. Beskyt mod fugt og fugt.
Holde utilgængeligt for børn.
Fremstillet af: ALZA Corporation, Vacaville, CA 95688, et ALZA OROS-teknologiprodukt. Fremstillet for: Janssen Pharmaceuticals, Inc., Titusville, NJ 08560. Revideret: sep 2019
BIVIRKNINGER
Erfaring med kliniske forsøg
Fordi kliniske forsøg udføres under vidt forskellige forhold, kan de bivirkninger, der er observeret i de kliniske forsøg med et lægemiddel, ikke direkte sammenlignes med hastigheder i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de frekvenser, der observeres i klinisk praksis.
Sikkerheden og effekten af DITROPAN 2,5 mg XL® (5 til 30 mg/dag) blev evalueret hos 774 voksne forsøgspersoner, som deltog i fem dobbeltblindede, kontrollerede kliniske forsøg. I fire af de fem undersøgelser var Ditropan 5 mg IR (5 til 20 mg/dag hos 199 forsøgspersoner) en aktiv komparator. Bivirkninger rapporteret af ≥ 1 % af forsøgspersonerne er vist i tabel 1.
Seponeringsraten på grund af bivirkninger var 4,4 % med DITROPAN XL® sammenlignet med 0 % med Ditropan IR. Den hyppigste bivirkning, der forårsagede seponering af undersøgelsesmedicin, var mundtørhed (0,7%).
Følgende bivirkninger blev rapporteret af Metabolisme og ernæringsforstyrrelser: anoreksi, væskeretention; Vaskulære lidelser: hedeture; Åndedræts-, thorax- og mediastinumsygdomme: dysfoni; Gastrointestinale lidelser: dysfagi, hyppige afføringer; Generelle lidelser og tilstande på administrationsstedet: ubehag i brystet, tørst.
Postmarketing oplevelse
Følgende yderligere bivirkninger er blevet rapporteret fra verdensomspændende erfaring efter markedsføring med DITROPAN 5mg XL®. Fordi postmarketingreaktioner rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt pålideligt at estimere deres hyppighed eller etablere en årsagssammenhæng til lægemiddeleksponering.
Infektioner og angreb: Urinvejsinfektion; Psykiatriske lidelser: psykotisk lidelse, agitation, forvirringstilstand, hallucinationer, hukommelsessvækkelse, unormal adfærd; Forstyrrelser i nervesystemet: kramper; Øjenlidelser: glaukom; Åndedræts-, thorax- og mediastinale lidelser: tilstoppet næse; Hjertelidelser: arytmi, takykardi, hjertebanken, forlængelse af QT-intervallet; Vaskulære lidelser: rødmen, hypertension; Hud- og subkutane vævsforstyrrelser: udslæt; Nyre- og urinvejslidelser: impotens; Generelle lidelser og administrationsbetingelser: overfølsomhedsreaktioner, herunder angioødem med luftvejsobstruktion, nældefeber og ansigtsødem; anafylaktiske reaktioner, der kræver hospitalsindlæggelse for akut behandling; Skade, forgiftning og proceduremæssige komplikationer: fald.
Yderligere bivirkninger rapporteret med nogle andre oxybutyninchloridformuleringer omfatter: cycloplegi, mydriasis og undertrykkelse af laktation. I et rapporteret tilfælde var samtidig brug af oxybutynin med carbamazepin og dantrolen forbundet med bivirkninger i form af opkastning, døsighed, forvirring, ustabilitet, sløret tale og nystagmus, hvilket tyder på carbamazepin-toksicitet.
DRUGSINTERAKTIONER
Samtidig brug af oxybutynin med andre antikolinerge lægemidler eller med andre midler, der forårsager mundtørhed, forstoppelse, døsighed (døsighed) og/eller andre antikolinergiske virkninger kan øge hyppigheden og/eller sværhedsgraden af sådanne virkninger.
Anticholinerge midler kan potentielt ændre absorptionen af visse samtidig administrerede lægemidler på grund af antikolinerge virkninger på gastrointestinal motilitet. Dette kan give anledning til bekymring for lægemidler med et snævert terapeutisk indeks. Anticholinerge midler kan også antagonisere virkningerne af prokinetiske midler, såsom metoclopramid.
Gennemsnitlige plasmakoncentrationer af oxybutynin var ca. 2 gange højere, når DITROPAN 5mg XL® blev administreret sammen med ketoconazol, en potent CYP3A4-hæmmer. Andre hæmmere af cytochrom P450 3A4-enzymsystemet, såsom antimykotiske midler (f.eks. itraconazol og miconazol) eller makrolidantibiotika (f.eks. erythromycin og clarithromycin), kan ændre oxybutynins gennemsnitlige farmakokinetiske parametre (dvs. Cmax og AUC). Den kliniske relevans af sådanne potentielle interaktioner kendes ikke. Der bør udvises forsigtighed, når sådanne lægemidler administreres samtidigt.
ADVARSLER
Inkluderet som en del af FORHOLDSREGLER afsnit.
FORHOLDSREGLER
Angioødem
Angioødem i ansigt, læber, tunge og/eller strubehoved er blevet rapporteret med oxybutynin. I nogle tilfælde opstod angioødem efter den første dosis. Angioødem forbundet med hævelse af øvre luftveje kan være livstruende. Hvis der opstår involvering af tungen, hypopharynx eller strubehovedet, skal oxybutynin omgående seponeres, og passende behandling og/eller nødvendige foranstaltninger for at sikre frie luftveje bør straks gives.
Virkninger på centralnervesystemet
Oxybutynin er forbundet med antikolinerge virkninger på centralnervesystemet (CNS) [se BIVIRKNINGER ]. En række antikolinerge CNS-effekter er blevet rapporteret, herunder hallucinationer, agitation, forvirring og somnolens. Patienter bør overvåges for tegn på antikolinerge CNS-effekter, især i de første par måneder efter påbegyndelse af behandling eller øgning af dosis. Rådgive patienter om ikke at køre bil eller betjene tunge maskiner, før de ved, hvordan DITROPAN XL® påvirker dem. Hvis en patient oplever antikolinerge CNS-effekter, bør dosisreduktion eller seponering af lægemidlet overvejes.
DITROPAN XL® bør anvendes med forsigtighed til patienter med allerede eksisterende demens behandlet med kolinesterasehæmmere på grund af risikoen for forværring af symptomer.
DITROPAN XL® bør anvendes med forsigtighed til patienter med Parkinsons sygdom på grund af risikoen for forværring af symptomer.
Forværring af symptomer på myasthenia gravis
DITROPAN XL® bør anvendes med forsigtighed til patienter med myasthenia gravis på grund af risikoen for forværring af symptomer.
Forværring af symptomer på nedsat gastrointestinal motilitet hos patienter med autonom neuropati
DITROPAN 2,5 mg XL® bør anvendes med forsigtighed til patienter med autonom neuropati på grund af risikoen for forværring af symptomer på nedsat gastrointestinal motilitet.
Urinretention
DITROPAN 5mg XL® bør administreres med forsigtighed til patienter med klinisk signifikant blæreudstrømningsobstruktion på grund af risikoen for urinretention [se KONTRAINDIKATIONER ].
Gastrointestinale bivirkninger
DITROPAN 2,5 mg XL® bør administreres med forsigtighed til patienter med gastrointestinale obstruktive lidelser på grund af risikoen for gastrisk retention [se KONTRAINDIKATIONER ].
DITROPAN XL® kan ligesom andre antikolinerge lægemidler nedsætte gastrointestinal motilitet og bør anvendes med forsigtighed til patienter med tilstande som colitis ulcerosa og intestinal atoni.
DITROPAN 2,5 mg XL® bør anvendes med forsigtighed til patienter, som har gastroøsofageal refluks og/eller som samtidig tager medicin (såsom bisfosfonater), der kan forårsage eller forværre esophagitis.
Som med ethvert andet ikke-deformerbart materiale skal der udvises forsigtighed ved administration af DITROPAN XL® til patienter med allerede eksisterende alvorlig gastrointestinal forsnævring (patologisk eller iatrogen). Der har været sjældne rapporter om obstruktive symptomer hos patienter med kendte strikturer i forbindelse med indtagelse af andre lægemidler i ikke-deformerbare formuleringer med kontrolleret frigivelse.
Ikke-klinisk toksikologi
Karcinogenese, mutagenese, svækkelse af fertilitet
Et 24-måneders studie med rotter i doser af oxybutyninchlorid på 20, 80 og 160 mg/kg/dag viste ingen tegn på carcinogenicitet. Disse doser er ca. 6, 25 og 50 gange den maksimale humane eksponering, baseret på en human ækvivalent dosis under hensyntagen til normalisering af kropsoverfladen.
Oxybutyninchlorid viste ingen stigning i mutagen aktivitet ved test i Schizosaccharomyces pompholiciformis, Saccharomyces cerevisiae og Salmonella typhimurium testsystemer.
Reproduktionsundersøgelser med oxybutyninchlorid hos mus, rotte, hamster og kanin viste ingen tegn på nedsat fertilitet.
Brug i specifikke populationer
Graviditet
Graviditetskategori B
Der er ingen tilstrækkelige og velkontrollerede undersøgelser med DITROPAN 5mg XL® hos gravide kvinder. DITROPAN XL® bør kun anvendes under graviditet, hvis den potentielle fordel for patienten opvejer risikoen for patienten og fosteret. Kvinder, der bliver gravide under behandlingen med DITROPAN XL®, opfordres til at kontakte deres læge.
Risikooversigt
Baseret på dyredata forventes oxybutynin at have en lav sandsynlighed for at øge risikoen for uønskede udviklingseffekter over baggrundsrisikoen.
Dyredata
Reproduktionsundersøgelser med oxybutyninchlorid hos mus, rotte, hamster og kanin viste ingen tegn på nedsat fertilitet eller skade på dyrefosteret.
Ammende mødre
Det vides ikke, om oxybutynin udskilles i modermælk. Da mange lægemidler udskilles i modermælk, bør der udvises forsigtighed, når DITROPAN 5mg XL® administreres til en ammende kvinde.
Pædiatrisk brug
Sikkerheden og effekten af DITROPAN XL® blev undersøgt hos 60 børn i et 24-ugers, åbent, ikke-randomiseret forsøg. Patienterne var i alderen 6-15 år, alle havde symptomer på detrusor-overaktivitet i forbindelse med en neurologisk tilstand (f.eks. spina bifida), alle brugte ren intermitterende kateterisering, og alle var nuværende brugere af oxybutyninchlorid. Undersøgelsesresultater viste, at administration af DITROPAN 2,5 mg XL® 5 til 20 mg/dag var forbundet med en stigning fra baseline i gennemsnitlig urinvolumen pr. kateterisation fra 108 mL til 136 mL, en stigning fra baseline i gennemsnitlig urinvolumen efter morgenvågning fra 148 ml til 189 ml og en stigning fra baseline i den gennemsnitlige procentdel af kateteriseringer uden lækage fra 34 % til 51 %.
Urodynamiske resultater var i overensstemmelse med kliniske resultater. Administration af DITROPAN XL® resulterede i en stigning fra baseline i den gennemsnitlige maksimale cystometriske kapacitet fra 185 mL til 254 mL, et fald fra baseline i det gennemsnitlige detrusortryk ved maksimal cystometrisk kapacitet fra 44 cm H2O til 33 cm H2O og en reduktion i procentdelen af patienter, der udviser uhæmmede detrusorkontraktioner (på mindst 15 cm HO) fra 60 % til 28 %.
Farmakokinetikken af DITROPAN 5mg XL® hos disse patienter var i overensstemmelse med dem, der blev rapporteret for voksne [se KLINISK FARMAKOLOGI ].
DITROPAN 5mg XL® anbefales ikke til pædiatriske patienter, som ikke kan sluge tabletten hel uden at tygge, dele eller knuse, eller til børn under 6 år.
Geriatrisk brug
Hyppigheden og sværhedsgraden af antikolinerge virkninger rapporteret af patienter under 65 år og patienter på 65 år og ældre var ens. Farmakokinetikken af DITROPAN XL® var ens hos alle undersøgte patienter (op til 78 år).
Nedsat nyrefunktion
Der er ikke udført undersøgelser med DITROPAN XL® hos patienter med nedsat nyrefunktion.
Nedsat leverfunktion
Der er ikke udført undersøgelser med DITROPAN 2,5 mg XL® hos patienter med nedsat leverfunktion.
OVERDOSIS
Kontinuerlig frigivelse af oxybutynin fra DITROPAN 5mg XL® bør overvejes ved behandling af overdosering. Patienter bør overvåges i mindst 24 timer. Behandlingen skal være symptomatisk og støttende. Et kathartisk middel kan indgives.
Overdosering med oxybutyninchlorid er blevet forbundet med antikolinerge virkninger, herunder excitation af centralnervesystemet, rødmen, feber, dehydrering, hjertearytmi, opkastning og urinretention.
Indtagelse af 100 mg oxybutyninchlorid i forbindelse med alkohol er blevet rapporteret hos en 13-årig dreng, der oplevede hukommelsestab, og en 34-årig kvinde, der udviklede stupor, efterfulgt af desorientering og agitation ved opvågning, udvidede pupiller, tørre hud, hjertearytmi og tilbageholdelse af urin. Begge patienter kom sig fuldt ud med symptomatisk behandling.
KONTRAINDIKATIONER
DITROPAN 2,5 mg XL® er kontraindiceret til patienter med urinretention, gastrisk retention og andre alvorlige nedsatte gastrointestinale motilitetstilstande, ukontrolleret snævervinklet glaukom.
DITROPAN 2,5mg XL® er også kontraindiceret til patienter, der har udvist overfølsomhed over for lægemiddelstoffet eller andre komponenter i produktet. Der har været rapporter om overfølsomhedsreaktioner, herunder anafylaksi og angioødem.
KLINISK FARMAKOLOGI
Handlingsmekanisme
Oxybutynin afslapper blærens glatte muskler. Oxybutyninchlorid udøver en direkte krampeløsende effekt på glat muskulatur og hæmmer den muskarine virkning af acetylcholin på glat muskulatur. Der forekommer ingen blokerende virkninger ved skelet neuromuskulære forbindelser eller autonome ganglier (antinikotiniske virkninger).
Antimuskarin aktivitet ligger overvejende i R-isomeren. En metabolit, desethyloxybutynin, har farmakologisk aktivitet svarende til oxybutynins i in vitro undersøgelser.
Farmakodynamik
Hos patienter med tilstande karakteriseret ved ufrivillige blærekontraktioner, har cystometriske undersøgelser vist, at oxybutynin øger blærekapaciteten (vesikal) kapacitet, mindsker hyppigheden af uhæmmede sammentrækninger af detrusormusklen og forsinker det indledende ønske om at void.
Farmakokinetik
Absorption
Efter den første dosis DITROPAN XL® stiger plasmakoncentrationen af oxybutynin i 4 til 6 timer; derefter opretholdes stabile koncentrationer i op til 24 timer, hvilket minimerer udsving mellem top- og bundkoncentrationer forbundet med oxybutynin.
Den relative biotilgængelighed af R- og S-oxybutynin fra DITROPAN XL® er henholdsvis 156 % og 187 % sammenlignet med oxybutynin. De gennemsnitlige farmakokinetiske parametre for R- og S-oxybutynin er opsummeret i tabel 2. Plasmakoncentration-tidsprofilerne for R- og S-oxybutynin er ens i form; Figur 1 viser profilen for R-oxybutynin.
Figur 1: Gennemsnitlige R-oxybutynin plasmakoncentrationer efter en enkelt dosis DITROPAN XL® 10 mg og oxybutynin 5 mg administreret hver 8. time (n=23 for hver behandling).
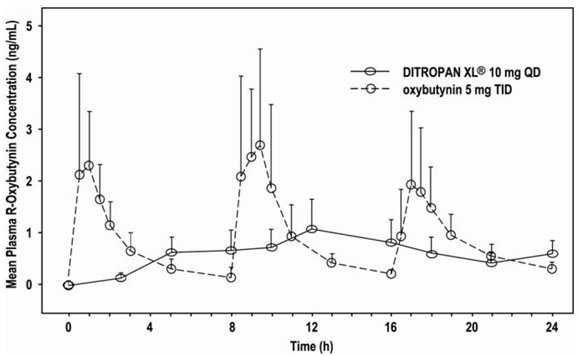
Steady state oxybutynin plasmakoncentrationer opnås på dag 3 af gentagen DITROPAN XL® dosering, uden observeret lægemiddelakkumulering eller ændring i oxybutynin og desethyloxybutynin farmakokinetiske parametre.
DITROPAN 5mg XL® steady state farmakokinetik blev undersøgt hos 19 børn i alderen 5-15 år med detrusoroveraktivitet forbundet med en neurologisk tilstand (f.eks. spina bifida). Børnene fik DITROPAN 2,5 mg XL® total daglig dosis i området fra 5 til 20 mg (0,10 til 0,77 mg/kg). Sparsom prøvetagningsteknik blev brugt til at opnå serumprøver. Når alle tilgængelige data er normaliseret til en ækvivalent på 5 mg pr. dag af DITROPAN XL®, er de gennemsnitlige farmakokinetiske parametre afledt for R- og S-oxybutynin og R- og S-desethyloxybutynin opsummeret i tabel 3. Plasma-tidskoncentrationsprofilerne for R- og S-oxybutynin er ens i form; Figur 2 viser profilen for R-oxybutynin, når alle tilgængelige data er normaliseret til et ækvivalent på 5 mg pr. dag.
Figur 2: Gennemsnitlige steady state (± SD) R-oxybutynin plasmakoncentrationer efter administration af 5 til 20 mg DITROPAN 5mg XL® én gang dagligt til børn i alderen 5-15 år. Plot repræsenterer alle tilgængelige data normaliseret til en ækvivalent af DITROPAN XL® 5 mg én gang dagligt.
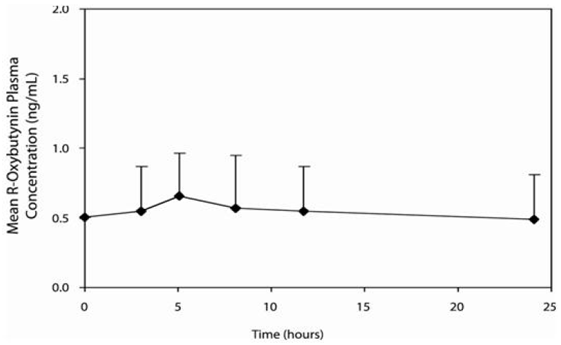
Mad effekter
Hastigheden og omfanget af absorption og metabolisme af oxybutynin er ens under fodrede og fastende forhold.
Fordeling
Oxybutynin er bredt fordelt i kropsvæv efter systemisk absorption. Fordelingsvolumenet er 193 l efter intravenøs administration af 5 mg oxybutyninchlorid. Begge enantiomerer af oxybutynin er stærkt bundet (>99%) til plasmaproteiner. Begge enantiomerer af N-desethyloxybutynin er også stærkt bundet (>97%) til plasmaproteiner. Det vigtigste bindingsprotein er alfa-1 surt glycoprotein.
Metabolisme
Oxybutynin metaboliseres primært af cytochrom P450-enzymsystemerne, især CYP3A4, der hovedsageligt findes i leveren og tarmvæggen. Dets metaboliske produkter omfatter phenylcyclohexylglycolsyre, som er farmakologisk inaktiv, og desethyloxybutynin, som er farmakologisk aktiv. Efter administration af DITROPAN 2,5 mg XL® er plasmakoncentrationer af R- og S-desethyloxybutynin henholdsvis 73 % og 92 % af koncentrationer observeret med oxybutynin.
Udskillelse
Oxybutynin metaboliseres i vid udstrækning i leveren, hvor mindre end 0,1 % af den administrerede dosis udskilles uændret i urinen. Desuden udskilles mindre end 0,1 % af den administrerede dosis som metabolitten desethyloxybutynin.
Dosisproportionalitet
Farmakokinetiske parametre for oxybutynin og desethyloxybutynin (Cmax og AUC) efter administration af 5-20 mg DITROPAN 5mg XL® er dosisproportionale.
Brug i specifikke populationer
Pædiatrisk
Farmakokinetikken af DITROPAN 2,5 mg XL® blev evalueret hos 19 børn i alderen 5-15 år med detrusoroveraktivitet forbundet med en neurologisk tilstand (f.eks. spina bifida). Farmakokinetikken af DITROPAN 2,5 mg XL® hos disse pædiatriske patienter var i overensstemmelse med dem, der blev rapporteret for voksne (se tabel 2 og 3 samt figur 1 og 2 ovenfor).
Køn
Der er ingen signifikante forskelle i farmakokinetikken af oxybutynin hos raske mandlige og kvindelige frivillige efter administration af DITROPAN 2,5 mg XL®.
Race
Tilgængelige data tyder på, at der ikke er signifikante forskelle i farmakokinetikken af oxybutynin baseret på race hos raske frivillige efter administration af DITROPAN 2,5 mg XL®.
Kliniske Studier
DITROPAN 5mg XL® blev evalueret til behandling af patienter med overaktiv blære med symptomer på urge-inkontinens, trang og hyppighed i tre kontrollerede effektstudier. Størstedelen af patienterne var kaukasiske (89,0 %) og kvinder (91,9 %) med en gennemsnitsalder på 59 år (interval, 18 til 98 år). Indgangskriterier krævede, at patienterne har trang- eller blandet inkontinens (med en overvægt af trang), hvilket fremgår af ≥ 6 urge-inkontinensepisoder om ugen og ≥ 10 vandladninger om dagen. Studie 1 var et eskaleringsdesign med faste doser, hvorimod de to andre studier brugte et dosisjusteringsdesign, hvor hver patients endelige dosis blev justeret til en balance mellem forbedring af inkontinenssymptomer og tolerabilitet af bivirkninger. Alle tre undersøgelser omfattede patienter, der vides at reagere på oxybutynin eller andre antikolinerge lægemidler, og disse patienter blev holdt på en endelig dosis i op til 2 uger.
Effektresultaterne for de tre kontrollerede forsøg er vist i de følgende tabel 4, 5 og 6 og figur 3, 4 og 5.
Figur 3: Gennemsnitlig ændring (±SD) i urge-urininkontinensepisoder pr. uge fra baseline (undersøgelse 1)
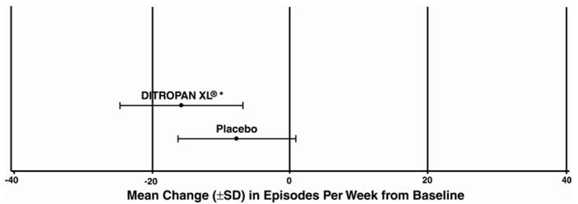
Figur 4: Gennemsnitlig ændring (±SD) i urge-urininkontinensepisoder pr. uge fra baseline (undersøgelse 2)
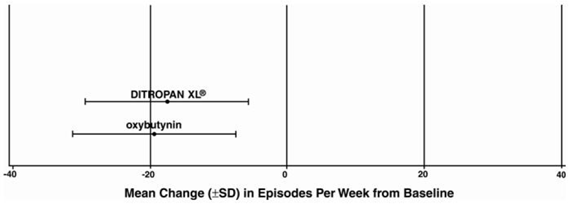
Figur 5: Gennemsnitlig ændring (±SD) i urge-urininkontinensepisoder pr. uge fra baseline (undersøgelse 3)
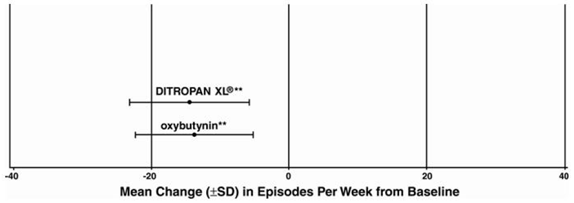
PATIENTOPLYSNINGER
- Patienter bør informeres om, at oxybutynin kan producere angioødem, der kan resultere i livstruende luftvejsobstruktion. Patienter bør rådes til omgående at afbryde behandlingen med oxybutynin og søge omgående lægehjælp, hvis de oplever hævelse af tungen, ødem i strubehovedet eller åndedrætsbesvær.
- Patienter bør informeres om, at antikolinerge (antimuskarine) midler, såsom DITROPAN XL®, kan give klinisk signifikante bivirkninger relateret til antikolinerg aktivitet, såsom:
- Urinretention og forstoppelse
- Varme udmattelse på grund af nedsat svedtendens. Varmeudmattelse kan forekomme, når antikolinerge lægemidler administreres i nærvær af høj miljøtemperatur.
- Patienter bør informeres om, at antikolinerge lægemidler såsom DITROPAN 5mg XL® kan forårsage døsighed (somnolens), svimmelhed eller sløret syn. Patienter bør rådes til at udvise forsigtighed i beslutninger om at deltage i potentielt farlige aktiviteter, indtil virkningerne af DITROPAN XL® er blevet fastslået.
- Patienterne skal informeres om, at alkohol kan øge døsigheden forårsaget af antikolinerge midler såsom DITROPAN XL®.
- Patienterne skal informeres om, at DITROPAN 5mg XL® skal synkes hel ved hjælp af væske. Patienter bør ikke tygge, dele eller knuse tabletter. Medicinen er indeholdt i en ikke-absorberbar skal designet til at frigive lægemidlet med en kontrolleret hastighed. Tabletskallen fjernes fra kroppen; patienter bør ikke være bekymrede, hvis de lejlighedsvis bemærker noget i deres afføring, der ligner en tablet.
- DITROPAN 5mg XL® bør tages på omtrent samme tidspunkt hver dag.
