Estrace 1mg, 2mg Estradiol Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Estrace, og hvordan bruges det?
Estrace er en receptpligtig medicin, der bruges til at behandle symptomerne på metastatisk brystkræft, osteoporose, lavt østrogen (hypoøstrogenisme), vulva og vaginal atrofi i overgangsalderen. Estrace 1mg kan bruges alene eller sammen med anden medicin.
Estrace 1mg tilhører en klasse af lægemidler kaldet østrogenderivater.
Det vides ikke, om Estrace 1mg er sikkert og effektivt til børn.
Hvad er de mulige bivirkninger af Estrace 1mg?
Estrace kan forårsage alvorlige bivirkninger, herunder:
- brystsmerter eller tryk,
- smerte breder sig til din kæbe eller skulder,
- kvalme,
- svedeture,
- pludselig følelsesløshed eller svaghed (især på den ene side af kroppen),
- pludselig kraftig hovedpine,
- utydelig tale,
- problemer med dit syn eller balance,
- pludseligt synstab,
- stikkende brystsmerter,
- følelse af åndenød,
- hoste blod op,
- smerte eller varme i et eller begge ben,
- hævelse eller ømhed i maven,
- gulfarvning af huden eller øjnene (gulsot),
- hukommelsesproblemer,
- forvirring,
- usædvanlig adfærd,
- usædvanlig vaginal blødning,
- bækkensmerter,
- klump i dit bryst,
- opkastning,
- forstoppelse,
- øget tørst eller vandladning,
- muskelsvaghed,
- knoglesmerter, en
- d
- mangel på energi
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Estrace omfatter:
- kvalme,
- opkastning,
- diarré,
- mavekramper,
- humørsvingninger,
- søvnproblemer (søvnløshed),
- hovedpine,
- rygsmerte,
- brystsmerter,
- forkølelsessymptomer (tilstoppet næse, bihulesmerter, ondt i halsen),
- vægtøgning,
- tyndere hovedhår,
- vaginal kløe eller udflåd,
- ændringer i dine menstruationer, og
- gennembrudsblødning
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Estrace. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ØTROGENER ØGER RISIKOEN FOR ENDOMETRELCANCER
Tæt klinisk overvågning af alle kvinder, der tager østrogener, er vigtig. Der bør udføres passende diagnostiske foranstaltninger, herunder endometrieprøver, når det er indiceret, for at udelukke malignitet i alle tilfælde af udiagnosticeret vedvarende eller tilbagevendende unormal vaginal blødning. Der er ingen beviser for, at brugen af "naturlige" østrogener resulterer i en anden endometrierisikoprofil end "syntetiske" østrogener ved tilsvarende østrogendoser. (Se ADVARSLER , Ondartede neoplasmer , Endometriecancer .)
Hjerte- og kar- og andre risici
Østrogener med eller uden progestiner bør ikke anvendes til forebyggelse af hjerte-kar-sygdomme. (Se ADVARSLER , Kardiovaskulære lidelser .)
Women's Health Initiative (WHI) undersøgelsen rapporterede øget risiko for myokardieinfarkt, troke, invasiv brystkræft, lungeemboli og dyb venetrombose hos postmenopausale kvinder (50 til 79 år) i løbet af 5 års behandling med oral behandling konjugerede østrogener (CE 0,625 mg) kombineret med medroxyprogesteronacetat (MPA 2,5 mg) i forhold til placebo. (Se KLINISK FARMAKOLOGI , Kliniske Studier .)
Women's Health Initiative Memory Study (WHIMS), en delundersøgelse af WHI, rapporterede øget risiko for at udvikle sandsynlig demens hos postmenopausale kvinder 65 år eller ældre i løbet af 4 års behandling med orale konjugerede østrogener plus medroxyprogesteronacetat i forhold til placebo . Det vides ikke, om dette fund gælder for yngre postmenopausale kvinder eller kvinder, der tager østrogen alene. (Se KLINISK FARMAKOLOGI , Kliniske Studier .)
Andre doser af orale konjugerede østrogener med medroxyprogesteronacetat og andre kombinationer og doseringsformer af østrogener og progestiner blev ikke undersøgt i WHI kliniske forsøg, og i mangel af sammenlignelige data bør disse risici antages at være ens. På grund af disse risici bør østrogener med eller uden progestiner ordineres i de laveste effektive doser og i den korteste varighed i overensstemmelse med behandlingsmål og -risici for den enkelte kvinde.
BESKRIVELSE
ESTRACE ® (østradioltabletter, USP) til oral administration indeholder 0,5, 1 eller 2 mg mikroniseret østradiol pr. tablet. Estradiol (17ø-estradiol) er et hvidt, krystallinsk fast stof, kemisk beskrevet som estra-1,3,5,(10)-trien-3, 17ø-diol. Strukturformlen er:
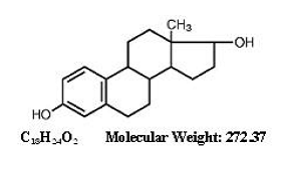
Inaktive ingredienser : Kolloid siliciumdioxid, majsstivelse, dibasisk calciumphosphat, lactosemonohydrat, magnesiumstearat og natriumstivelsesglykolat. Derudover indeholder 1 mg også FD&C blå nr. 1 aluminium sø og D&C rødt nr. 27 aluminium sø. De 2 mg indeholder også FD&C blå nr. 1 aluminium sø og FD&C gul nr. 5 (tartrazin) aluminium sø.
INDIKATIONER
ESTRACE (østradioltabletter, USP) er indiceret i:
DOSERING OG ADMINISTRATION
Når østrogen ordineres til en postmenopausal kvinde med livmoder, bør der også påbegyndes et gestagen for at reducere risikoen for endometriecancer. En kvinde uden livmoder har ikke brug for gestagen. Anvendelse af østrogen, alene eller i kombination med et gestagen, bør være med den laveste effektive dosis og i den korteste varighed i overensstemmelse med behandlingens mål og risici for den enkelte kvinde. Patienter bør revurderes med jævne mellemrum, alt efter hvad der er klinisk passende (f.eks. 3-6 måneders intervaller) for at afgøre, om behandling stadig er nødvendig (se ADVARSLER I BOKS og ADVARSLER ). For kvinder, der har en livmoder, bør passende diagnostiske foranstaltninger, såsom endometrieprøvetagning, når det er indiceret, udføres for at udelukke malignitet i tilfælde af udiagnosticeret vedvarende eller tilbagevendende unormal vaginal blødning.
Patienter skal startes med den laveste dosis til indikationen.
1. Til behandling af moderate til svære vasomotoriske symptomer, vulval og vaginal atrofi i forbindelse med overgangsalderen, bør den laveste dosis og regime, der vil kontrollere symptomerne, vælges, og medicineringen bør seponeres så hurtigt som muligt.
Forsøg på at seponere eller nedtrappe medicinen bør foretages med 3-måneders intervaller. Det sædvanlige indledende dosisinterval er 1 til 2 mg dagligt østradiol justeret efter behov for at kontrollere de fremkomne symptomer. Den minimale effektive dosis til vedligeholdelsesbehandling bør bestemmes ved titrering. Administrationen skal være cyklisk (f.eks. 3 uger på og 1 uge fri).
2. Til behandling af kvindelig hypoøstrogenisme på grund af hypogonadisme, kastration eller primær ovariesvigt.
Behandlingen påbegyndes sædvanligvis med en dosis på 1 til 2 mg østradiol dagligt, justeret efter behov for at kontrollere de fremkomne symptomer; den minimale effektive dosis til vedligeholdelsesbehandling bør bestemmes ved titrering.
3. Til behandling af brystkræft, kun til palliation, hos passende udvalgte kvinder og mænd med metastatisk sygdom.
Foreslået dosis er 10 mg tre gange dagligt i en periode på mindst tre måneder.
4. Til behandling af fremskreden androgenafhængig karcinom i prostata, kun til palliation.
Foreslået dosis er 1 til 2 mg tre gange dagligt. Effektiviteten af terapien kan bedømmes ud fra fosfatasebestemmelser såvel som ved symptomatisk forbedring af patienten.
5. Til forebyggelse af osteoporose.
Når der udelukkende ordineres til forebyggelse af postmenopausal osteoporose, bør behandling kun overvejes til kvinder med betydelig risiko for osteoporose, og for hvem ikke-østrogenmedicin ikke anses for at være passende.
Den laveste effektive dosis af ESTRACE 2 mg er ikke blevet bestemt.
HVORDAN LEVERET
ESTRACE® (østradioltabletter, USP) fås som:
0,5 mg Hvid til råhvid, oval, flad, skrå kant, tablet med delekærv. Præget med 720 / ½ på den scorede side og Toilet på den anden side. Fås i flasker med:
100 tabletter NDC 0430-0720-24
1 mg : Lyslilla, oval, flad, skrå kant, tablet med delekærv. Præget med 721 / 1 på den scorede side og Toilet på den anden side. Fås i flasker med:
100 tabletter NDC 0430-0721-24
2 mg : Grøn, oval, flad, skrå kant, tablet med delekærv. Præget med 722 / 2 på den scorede side og Toilet på den anden side. Fås i flasker med:
100 tabletter NDC 0430-0722-24
Opbevares ved 20° til 25° C (68° til 77°F) [Se USP kontrolleret rumtemperatur ].
Dispenser i en tæt, lysbestandig beholder som defineret i USP, med en børnesikret lukning (efter behov).
OPBEVAR DETTE OG ALLE MEDICINER UTILGÆNGELIGT FOR BØRN.
Produceret af: TEVA PHARMACEUTICALS USA Sellersville, PA 18960. Markedsført af: Warner Chilcott (US), LLC, Rockaway, NJ 07866, 1-800-521-8813. Revideret: september 2013
BIVIRKNINGER
Se ADVARSLER I BOKS , ADVARSLER og FORHOLDSREGLER .
Følgende yderligere bivirkninger er blevet rapporteret ved østrogen- og/eller gestagenbehandling.
Genitourinært system
Ændringer i vaginalt blødningsmønster og unormal abstinensblødning eller flow; gennembrudsblødning, pletblødning, dysmenoré Øget størrelse af uterine leiomyomata Vaginitis, herunder vaginal candidiasis Ændring i mængden af cervikal sekretion Ændringer i cervikal ektropion Ovariecancer; endometriehyperplasi; endometriecancer
Bryster
Ømhed, forstørrelse, smerte, udflåd fra brystvorten, galaktoré; fibrocystiske brystforandringer; brystkræft
Kardiovaskulær
Dyb og overfladisk venøs trombose; lungeemboli; tromboflebitis; myokardieinfarkt; slag; stigning i blodtrykket
Gastrointestinale
Kvalme, opkastning Mavekramper, oppustethed Kolestatisk gulsot Øget forekomst af galdeblæresygdom Pancreatitis Forstørrelse af hepatiske hæmangiomer
Hud
Kloasma eller melasma, der kan vare ved, når lægemidlet seponeres Erythema multiforme Erythema nodosum Hæmoragisk udbrud Tab af hår i hovedbunden Hirsutisme Kløe, udslæt
Øjne
Retinal vaskulær trombose Stejlere hornhindens krumning Intolerance over for kontaktlinser
Centralnervesystemet
Hovedpine, migræne, svimmelhed Psykisk depression Chorea Nervøsitet, humørforstyrrelser, irritabilitet Forværring af epilepsi Demens
Diverse
Forøgelse eller fald i vægt Reduceret kulhydrattolerance Forværring af porfyri Ødem Artralgier; kramper i benene Ændringer i libido Urticaria Angioødem Anafylaktoide/anafylaktiske reaktioner Hypokalcæmi Forværring af astma Forhøjede triglycerider
DRUGSINTERAKTIONER
Interaktioner med lægemiddel/laboratorietest
ADVARSLER
Inkluderet som en del af FORHOLDSREGLER afsnit.
Se ADVARSLER I BOKS .
Kardiovaskulære lidelser
Behandling med østrogen og østrogen/progestin er blevet forbundet med en øget risiko for kardiovaskulære hændelser såsom myokardieinfarkt og slagtilfælde, såvel som venøs trombose og lungeemboli (venøs tromboemboli eller VTE). Hvis nogen af disse forekommer eller er mistanke om, bør østrogener seponeres med det samme.
Risikofaktorer for arteriel vaskulær sygdom (f.eks. hypertension, diabetes mellitus, tobaksbrug, hyperkolesterolæmi og fedme) og/eller venøs tromboemboli (f.eks. personlig historie eller familiehistorie med VTE, fedme og systemisk lupus erythematosus) bør håndteres korrekt.
Koronar hjertesygdom og slagtilfælde
I Women's Health Initiative (WHI) undersøgelsen er en stigning i antallet af myokardieinfarkter og slagtilfælde blevet observeret hos kvinder, der får CE sammenlignet med placebo. Disse observationer er foreløbige, og undersøgelsen fortsætter. (Se KLINISK FARMAKOLOGI , Kliniske Studier .)
I CE/MPA-underundersøgelsen af WHI blev en øget risiko for koronar hjertesygdom (CHD) (defineret som ikke-dødelig myokardieinfarkt og CHD-død) observeret hos kvinder, der fik CE/MPA sammenlignet med kvinder, der fik placebo (37 vs. 30 pr. 10.000 personer) flere år). Stigningen i risiko blev observeret i år et og fortsatte.
samme delstudie af WHI blev der observeret en øget risiko for slagtilfælde hos kvinder, der fik CE/MPA, sammenlignet med kvinder, der fik placebo (29 vs. 21 pr. 10.000 kvindeår). Stigningen i risiko blev observeret efter det første år og fortsatte.
Hos postmenopausale kvinder med dokumenteret hjertesygdom (n = 2.763, gennemsnitsalder 66,7 år) et kontrolleret klinisk forsøg med sekundær forebyggelse af kardiovaskulær sygdom (Heart and Estrogen/Progestin Replacement Study; HERS) behandling med CE/MPA (0,625 mg/2,5 mg pr. dag) viste ingen kardiovaskulær fordel. I løbet af en gennemsnitlig opfølgning på 4,1 år reducerede behandling med CE/MPA ikke den samlede frekvens af CHD-hændelser hos postmenopausale kvinder med etableret koronar hjertesygdom. Der var flere CHD-hændelser i den CE/MPA-behandlede gruppe end i placebogruppen i år 1, men ikke i de efterfølgende år. To tusinde tre hundrede og enogtyve kvinder fra det oprindelige HERS-forsøg indvilligede i at deltage i en åben udvidelse af HERS, HERS II. Den gennemsnitlige opfølgning i HERS II var yderligere 2,7 år, i alt 6,8 år samlet. Hyppigheden af CHD-hændelser var sammenlignelige blandt kvinder i CE/MPA-gruppen og placebogruppen i HERS, HERS II og generelt.
Store doser af østrogen (5 mg konjugerede østrogener pr. dag), der kan sammenlignes med dem, der anvendes til behandling af kræft i prostata og bryst, har i et stort prospektivt klinisk forsøg hos mænd vist sig at øge risikoen for ikke-fatalt myokardieinfarkt, lungeemboli og tromboflebitis.
Venøs tromboembolisme (VTE).
I Women's Health Initiative (WHI) undersøgelsen er en stigning i VTE blevet observeret hos kvinder, der får CE sammenlignet med placebo. Disse observationer er foreløbige, og undersøgelsen fortsætter. (Se KLINISK FARMAKOLOGI , Kliniske Studier .)
I CE/MPA-understudiet af WHI blev der observeret en 2 gange større frekvens af VTE, inklusive dyb venetrombose og lungeemboli, hos kvinder, der fik CE/MPA, sammenlignet med kvinder, der fik placebo. Hyppigheden af VTE var 34 pr. 10.000 kvindeår i CE/MPA-gruppen sammenlignet med 16 pr. 10.000 kvindeår i placebogruppen. Stigningen i VTE-risiko blev observeret i løbet af det første år og fortsatte.
Hvis det er muligt, bør østrogener seponeres mindst 4 til 6 uger før operation af den type, der er forbundet med en øget risiko for tromboemboli, eller i perioder med længerevarende immobilisering.
Maligne neoplasmer
Endometriecancer
Brugen af østrogener uden modsætning til kvinder med intakt livmoder har været forbundet med en øget risiko for endometriecancer. Den rapporterede risiko for endometriecancer blandt østrogenbrugere uden modstand er omkring 2-12 gange større end hos ikke-brugere og ser ud til at være afhængig af behandlingens varighed og østrogendosis. De fleste undersøgelser viser ingen signifikant øget risiko forbundet med brug af østrogener i mindre end et år. Den største risiko ser ud til at være forbundet med langvarig brug - med øget risiko på 15 til 24 gange i fem til ti år eller mere - og denne risiko varer ved i 8 til over 15 år efter, at østrogenbehandlingen er afbrudt.
Klinisk overvågning af alle kvinder, der tager østrogen/progestin-kombinationer er vigtig (se FORHOLDSREGLER ). Der bør udføres passende diagnostiske foranstaltninger, herunder endometrieprøver, når det er indiceret, for at udelukke malignitet i alle tilfælde af udiagnosticeret vedvarende eller tilbagevendende unormal vaginal blødning. Der er ingen beviser for, at brugen af naturlige østrogener resulterer i en anden endometrierisikoprofil end syntetiske østrogener med tilsvarende østrogendosis. Tilføjelse af et gestagen til østrogenbehandling har vist sig at reducere risikoen for endometriehyperplasi, som kan være en forløber for endometriecancer.
Brystkræft
Det er rapporteret, at postmenopausale kvinders brug af østrogener og gestagen øger risikoen for brystkræft. Det vigtigste randomiserede kliniske forsøg, der giver oplysninger om dette spørgsmål, er Women's Health Initiative (WHI) underundersøgelse af CE/MPA (se KLINISK FARMAKOLOGI , Kliniske Studier ). Resultaterne fra observationsstudier er generelt i overensstemmelse med resultaterne fra det kliniske WHI-studie og rapporterer ingen signifikant variation i risikoen for brystkræft blandt forskellige østrogener eller progestiner, doser eller administrationsveje.
CE/MPA-underundersøgelsen af WHI rapporterede en øget risiko for brystkræft hos kvinder, der tog CE/MPA i en gennemsnitlig opfølgning på 5,6 år. Observationsstudier har også rapporteret en øget risiko for østrogen/progestin kombinationsbehandling og en mindre øget risiko for østrogen alene-terapi efter flere års brug. I WHI-studiet og fra observationsstudier steg overrisikoen med varigheden af brugen. Ud fra observationsstudier så risikoen ud til at vende tilbage til baseline omkring fem år efter behandlingens ophør. Derudover tyder observationsundersøgelser på, at risikoen for brystkræft var større og blev tydelig tidligere med østrogen/progestin-kombinationsterapi sammenlignet med østrogen alene-terapi.
CE/MPA-underundersøgelsen rapporterede 26 % af kvinderne tidligere brug af østrogen alene og/eller østrogen/progestin kombinationshormonbehandling. Efter en gennemsnitlig opfølgning på 5,6 år under det kliniske forsøg var den samlede relative risiko for invasiv brystkræft 1,24 (95 % konfidensinterval 1,01-1,54), og den samlede absolutte risiko var 41 vs. 33 tilfælde pr. 10.000 kvindeår, for CE/MPA sammenlignet med placebo. Blandt kvinder, der rapporterede tidligere brug af hormonbehandling, var den relative risiko for invasiv brystkræft 1,86, og den absolutte risiko var 46 vs. 25 tilfælde pr. 10.000 kvindeår for CE/MPA sammenlignet med placebo. Blandt kvinder, der ikke rapporterede nogen tidligere brug af hormonbehandling, var den relative risiko for invasiv brystkræft 1,09, og den absolutte risiko var 40 vs. 36 tilfælde pr. 10.000 kvindeår for CE/MPA sammenlignet med placebo. I samme delstudie var invasive brystkræftformer større og diagnosticeret på et mere fremskredent stadium i CE/MPA-gruppen sammenlignet med placebogruppen. Metastatisk sygdom var sjælden uden nogen åbenbar forskel mellem de to grupper. Andre prognostiske faktorer såsom histologisk undertype, grad og hormonreceptorstatus var ikke forskellige mellem grupperne.
Brugen af østrogen plus gestagen er blevet rapporteret at resultere i en stigning i unormale mammografier, der kræver yderligere evaluering. Alle kvinder bør modtage årlige brystundersøgelser af en sundhedsudbyder og udføre månedlige brystselvundersøgelser. Derudover bør mammografiundersøgelser planlægges baseret på patientens alder, risikofaktorer og tidligere mammografiresultater.
Demens
Women's Health Initiative Memory Study (WHIMS) blev 4.532 generelt raske postmenopausale kvinder på 65 år og ældre undersøgt, hvoraf 35 % var 70 til 74 år og 18 % var 75 år eller ældre. Efter en gennemsnitlig opfølgning på 4 år fik 40 kvinder i behandling med CE/MPA (1,8 %, n = 2.229) og 21 kvinder i placebogruppen (0,9 %, n = 2.303) diagnosen sandsynlig demens. Den relative risiko for CE/MPA versus placebo var 2,05 (95 % konfidensinterval 1,21 – 3,48), og var ens for kvinder med og uden historie om overgangsalderens hormonbrug før WHIMS. Den absolutte risiko for sandsynlig demens for CE/MPA versus placebo var 45 versus 22 tilfælde pr. 10.000 kvindeår, og den absolutte overrisiko for CE/MPA var 23 tilfælde pr. 10.000 kvindeår. Det er uvist, om disse resultater gælder for yngre postmenopausale kvinder. (Se KLINISK FARMAKOLOGI , Kliniske Studier og FORHOLDSREGLER , Geriatrisk brug .)
Det er ukendt, om disse resultater gælder for østrogen alene-terapi.
Galdeblære sygdom
En 2- til 4-dobling af risikoen for galdeblæresygdom, der kræver operation hos postmenopausale kvinder, der får østrogener, er blevet rapporteret.
Hypercalcæmi
Østrogenadministration kan føre til alvorlig hypercalcæmi hos patienter med brystkræft og knoglemetastaser. Hvis der opstår hypercalcæmi, skal brugen af lægemidlet stoppes, og der skal træffes passende foranstaltninger for at reducere serumcalciumniveauet.
Visuelle abnormiteter
Retinal vaskulær trombose er blevet rapporteret hos patienter, der får østrogener. Seponer medicinen i afventning af undersøgelse, hvis der er pludselig delvist eller fuldstændigt tab af synet, eller en pludselig indtræden af proptose, diplopi eller migræne. Hvis undersøgelse afslører papilleødem eller retinale vaskulære læsioner, bør østrogener seponeres permanent.
FORHOLDSREGLER
Generel
Tilsætning af et gestagen, når en kvinde ikke har fået foretaget en hysterektomi
Undersøgelser af tilsætning af et progestin i 10 eller flere dage af en cyklus med østrogenadministration eller dagligt med østrogen i et kontinuerligt regime har rapporteret en lavere forekomst af endometriehyperplasi, end det ville være induceret af østrogenbehandling alene. Endometriehyperplasi kan være en forløber for endometriecancer.
Der er dog mulige risici, som kan være forbundet med brugen af progestiner med østrogener sammenlignet med østrogen-alene regimer. Disse omfatter en mulig øget risiko for brystkræft.
Forhøjet blodtryk
I et lille antal case-rapporter er væsentlige stigninger i blodtrykket blevet tilskrevet idiosynkratiske reaktioner på østrogener. I et stort, randomiseret, placebokontrolleret klinisk forsøg blev der ikke set en generaliseret effekt af østrogener på blodtrykket. Blodtrykket bør overvåges med jævne mellemrum ved brug af østrogen.
Hypertriglyceridæmi
Hos patienter med allerede eksisterende hypertriglyceridæmi kan østrogenbehandling være forbundet med forhøjede plasmatriglycerider, hvilket fører til pancreatitis og andre komplikationer.
Nedsat leverfunktion og tidligere historie om kolestatisk gulsot
Østrogener kan metaboliseres dårligt hos patienter med nedsat leverfunktion. For patienter med en anamnese med kolestatisk gulsot forbundet med tidligere østrogenbrug eller med graviditet, bør der udvises forsigtighed, og i tilfælde af tilbagefald bør medicineringen seponeres.
Hypothyroidisme
Østrogenadministration fører til øgede niveauer af thyreoideabindende globulin (TBG). Patienter med normal skjoldbruskkirtelfunktion kan kompensere for den øgede TBG ved at lave mere thyreoideahormon og dermed opretholde frie T4- og T3-serumkoncentrationer i normalområdet. Patienter, der er afhængige af thyreoideahormonerstatningsterapi, og som også får østrogener, kan have behov for øgede doser af deres thyreoideasubstitutionsterapi. Disse patienter bør have deres skjoldbruskkirtelfunktion overvåget for at opretholde deres frie thyreoideahormonniveauer i et acceptabelt interval.
Væskeretention
Da østrogener kan forårsage en vis grad af væskeretention, berettiger patienter med tilstande, der kan være påvirket af denne faktor, såsom astma, epilepsi, migræne og hjerte- eller nyredysfunktion, omhyggelig observation, når østrogener ordineres.
Hypokalcæmi
Østrogener bør anvendes med forsigtighed hos personer med svær hypocalcæmi.
Livmoderhalskræft
CE/MPA-underundersøgelsen af WHI rapporterede, at østrogen plus gestagen øgede risikoen for kræft i æggestokkene. Efter en gennemsnitlig opfølgning på 5,6 år var den relative risiko for ovariecancer for CE/MPA versus placebo 1,58 (95 % konfidensinterval 0,77 – 3,24), men var ikke statistisk signifikant. Den absolutte risiko for CE/MPA versus placebo var 4,2 versus 2,7 tilfælde pr. 10.000 kvindeår. I nogle epidemiologiske undersøgelser har brugen af østrogen alene, især i ti eller flere år, været forbundet med en øget risiko for kræft i æggestokkene. Andre epidemiologiske undersøgelser har ikke fundet disse sammenhænge.
Forværring af endometriose
Endometriose kan forværres ved administration af østrogener. Nogle få tilfælde af malign transformation af resterende endometrieimplantater er blevet rapporteret hos kvinder behandlet efter hysterektomi med østrogen alene. For patienter, der vides at have resterende endometriose efter hysterektomi, bør tilsætning af gestagen overvejes.
Forværring af andre tilstande
Østrogener kan forårsage en forværring af astma, diabetes mellitus, epilepsi, migræne eller porfyri, systemisk lupus erythematosus og hepatiske hæmangiomer og bør anvendes med forsigtighed hos kvinder med disse tilstande.
ESTRACE (estradioltabletter, USP), 2 mg, indeholder FD&C Yellow No. 5 (tartrazin), som kan forårsage allergiske reaktioner (inklusive bronkial astma) hos visse modtagelige personer. Selvom den samlede forekomst af FD&C Yellow No. 5 (tartrazin) følsomhed i den generelle befolkning er lav, ses den hyppigt hos patienter, som også har aspirinoverfølsomhed.
Patientinformation
Læger rådes til at diskutere PATIENTOPLYSNINGER folder med patienter, som de ordinerer ESTRACE til.
Laboratorieprøver
Østrogenadministration bør påbegyndes med den laveste dosis, der er godkendt til indikationen og derefter styret af klinisk respons snarere end af serumhormonniveauer (f.eks. østradiol, FSH). (Se DOSERING OG ADMINISTRATION afsnit.)
Karcinogenese, mutagenese, svækkelse af fertilitet
Langvarig kontinuerlig administration af østrogen, med og uden gestagen, hos kvinder med og uden livmoder har vist en øget risiko for endometriecancer, brystkræft og ovariecancer. (Se ADVARSLER I BOKS , ADVARSLER og FORHOLDSREGLER .)
Langsigtet kontinuerlig administration af naturlige og syntetiske østrogener i visse dyrearter øger hyppigheden af karcinomer i bryst, livmoder, livmoderhals, vagina, testikler og lever.
Graviditetskategori X
Estrace 2mg bør ikke anvendes under graviditet. (Se KONTRAINDIKATIONER .)
Ammende mødre
Østrogenadministration til ammende mødre har vist sig at reducere mængden og kvaliteten af mælken. Påviselige mængder af østrogener er blevet identificeret i mælken hos mødre, der får dette lægemiddel. Der skal udvises forsigtighed, når ESTRACE 1 mg administreres til en ammende kvinde.
Pædiatrisk brug
Sikkerhed og effektivitet hos pædiatriske patienter er ikke blevet fastslået. Store og gentagne doser af østrogen over en længere periode har vist sig at fremskynde epifyselukning, hvilket resulterer i kort voksen statur, hvis behandlingen påbegyndes før afslutningen af den fysiologiske pubertet hos normalt udviklende børn. Hos patienter, hvor knoglevæksten ikke er fuldstændig, anbefales periodisk overvågning af knoglemodning og effekt på epifysecentre.
Østrogenbehandling af præpubertale børn inducerer også for tidlig brystudvikling og vaginal cornification, og kan potentielt inducere vaginal blødning hos piger. Hos drenge kan østrogenbehandling ændre den normale pubertetsproces. Alle andre fysiologiske og bivirkninger, der er vist at være forbundet med østrogenbehandling af voksne, kan potentielt forekomme i den pædiatriske population, herunder tromboemboliske lidelser og vækststimulering af visse tumorer. Derfor bør østrogener kun administreres til pædiatriske patienter, når det er klart indiceret, og den laveste effektive dosis bør altid anvendes.
Geriatrisk brug
Sikkerheden og virkningen af ESTRACE-tabletter hos geriatriske patienter er ikke blevet fastslået. Generelt bør dosisvalg for en ældre patient være forsigtigt, sædvanligvis begyndende i den lave ende af doseringsområdet, hvilket afspejler den største hyppighed af nedsat lever-, nyre- eller hjertefunktion og af samtidig sygdom eller anden lægemiddelbehandling.
Women's Health Initiative Memory Study, inklusive 4.532 kvinder på 65 år og ældre, fulgt i et gennemsnit på 4 år, var 82 % (n = 3.729) 65 til 74, mens 18 % (n = 803) var 75 og derover. De fleste kvinder (80 %) havde ikke tidligere brugt hormonbehandling. Kvinder behandlet med konjugerede østrogener plus medroxyprogesteronacetat blev rapporteret at have en dobbelt stigning i risikoen for at udvikle sandsynlig demens. Alzheimers sygdom var den mest almindelige klassificering af sandsynlig demens i både gruppen med konjugerede østrogener plus medroxyprogesteronacetat og placebogruppen. Halvfems procent af tilfældene af sandsynlig demens forekom hos de 54 % af kvinder, der var ældre end 70. (Se ADVARSLER , Demens .)
Det er ukendt, om disse resultater gælder for østrogen alene-terapi.
OVERDOSIS
Alvorlige bivirkninger er ikke blevet rapporteret efter akut indtagelse af store doser østrogenholdige orale præventionsmidler af små børn. Overdosering af østrogen kan forårsage kvalme og opkastning, og abstinensblødninger kan forekomme hos kvinder.
KONTRAINDIKATIONER
Østrogener bør ikke anvendes til personer med nogen af følgende tilstande:
KLINISK FARMAKOLOGI
Endogene østrogener er i høj grad ansvarlige for udvikling og vedligeholdelse af det kvindelige reproduktive system og sekundære seksuelle egenskaber. Selvom cirkulerende østrogener eksisterer i en dynamisk ligevægt af metaboliske interkonversioner, er østradiol det vigtigste intracellulære humane østrogen og er væsentligt mere potent end dets metabolitter, østron og østriol på receptorniveau.
Den primære kilde til østrogen hos normalt cyklende voksne kvinder er ovariefolliklen, som udskiller 70 til 500 mcg østradiol dagligt, afhængigt af fasen af menstruationscyklussen. Efter overgangsalderen produceres det meste endogene østrogen ved omdannelse af androstenedion, udskilt af binyrebarken, til østron af perifert væv. Således er østron og den sulfatkonjugerede form, østronsulfat, de mest udbredte cirkulerende østrogener hos postmenopausale kvinder.
Østrogener virker gennem binding til nukleare receptorer i østrogen-reagerende væv. Til dato er to østrogenreceptorer blevet identificeret. Disse varierer i forhold fra væv til væv.
Cirkulerende østrogener modulerer hypofysekretionen af gonadotropinerne, luteiniserende hormon (LH) og follikelstimulerende hormon (FSH) gennem en negativ feedback-mekanisme. Østrogener virker ved at reducere de forhøjede niveauer af disse hormoner, som ses hos postmenopausale kvinder.
Farmakokinetik
Fordeling
Fordelingen af eksogene østrogener svarer til fordelingen af endogene østrogener. Østrogener er vidt udbredt i kroppen og findes generelt i højere koncentrationer i kønshormonets målorganer. Østrogener cirkulerer i blodet stort set bundet til kønshormonbindende globulin (SHBG) og albumin.
Metabolisme
Eksogene østrogener metaboliseres på samme måde som endogene østrogener. Cirkulerende østrogener eksisterer i en dynamisk ligevægt af metaboliske interkonversioner. Disse transformationer finder hovedsageligt sted i leveren. Østradiol omdannes reversibelt til østron, og begge kan omdannes til østriol, som er den vigtigste urinmetabolit. Østrogener gennemgår også enterohepatisk recirkulation via sulfat- og glucuronidkonjugering i leveren, galdeudskillelse af konjugater i tarmen og hydrolyse i tarmen efterfulgt af reabsorption. Hos postmenopausale kvinder eksisterer en betydelig del af de cirkulerende østrogener som sulfatkonjugater, især østronsulfat, der tjener som et cirkulerende reservoir for dannelsen af mere aktive østrogener.
Udskillelse
Østradiol, østron og østriol udskilles i urinen sammen med glucuronid- og sulfatkonjugater.
Særlige Populationer
Der er ikke udført farmakokinetiske undersøgelser i særlige populationer, inklusive patienter med nedsat nyre- eller leverfunktion.
Lægemiddelinteraktioner
In vitro og in vivo undersøgelser har vist, at østrogener metaboliseres delvist af cytokrom P450 3A4 (CYP3A4). Derfor kan inducere eller hæmmere af CYP3A4 påvirke østrogen-lægemiddelmetabolismen. Inducere af CYP3A4 såsom perikonpræparater (Hypericum perforatum), phenobarbital, carbamazepin og rifampin kan reducere plasmakoncentrationer af østrogener, hvilket muligvis kan resultere i et fald i terapeutiske virkninger og/eller ændringer i uterin blødningsprofil. Hæmmere af CYP3A4 såsom erythromycin, clarithromycin, ketoconazol, itraconazol, ritonavir og grapefrugtjuice kan øge plasmakoncentrationerne af østrogener og kan resultere i bivirkninger.
Kliniske Studier
Osteoporose
De fleste prospektive undersøgelser af virkningen af denne indikation er blevet udført hos hvide kvinder i overgangsalderen, uden stratificering af andre risikofaktorer, og har tendens til at vise en universelt gavnlig effekt på knogler.
Resultaterne af et to-årigt, randomiseret, placebokontrolleret, dobbeltblindt, dosisvarierende studie har vist, at behandling med 0,5 mg østradiol dagligt i 23 dage (af en 28 dages cyklus) forhindrer tab af vertebralt knoglemasse hos postmenopausale kvinder. Når østrogenbehandlingen seponeres, falder knoglemassen med en hastighed, der kan sammenlignes med den umiddelbare postmenopausale periode. Der er ingen evidens for, at østrogenerstatningsterapi genopretter knoglemassen til præmenopausale niveauer.
Kvinders sundhedsinitiativ undersøgelser
Women's Health Initiative (WHI) tilmeldte i alt 27.000 overvejende raske postmenopausale kvinder til at vurdere risici og fordele ved enten brugen af orale 0,625 mg konjugerede østrogener (CE) per dag alene eller brugen af oral 0,625 mg konjugeret østrogener plus 2,5 mg medroxyprogesteronacetat (MPA) om dagen sammenlignet med placebo i forebyggelsen af visse kroniske sygdomme. Det primære endepunkt var forekomsten af koronar hjertesygdom (CHD) (nonfatal myokardieinfarkt og CHD-død), med invasiv brystkræft som det primære undersøgte uønskede resultat. Et "globalt indeks" inkluderede den tidligste forekomst af CHD, invasiv brystkræft, slagtilfælde, lungeemboli (PE), endometriecancer, kolorektal cancer, hoftebrud eller død på grund af anden årsag. Undersøgelsen evaluerede ikke virkningerne af CE eller CE/MPA på menopausale symptomer.
CE/MPA-underundersøgelsen blev stoppet tidligt, fordi den øgede risiko for brystkræft og kardiovaskulære hændelser ifølge den foruddefinerede stopregel oversteg de specificerede fordele inkluderet i det "globale indeks". Resultaterne af CE/MPA-underundersøgelsen, som omfattede 16.608 kvinder (gennemsnitsalder på 63 år, spænder fra 50 til 79; 83,9 % hvid, 6,5 % sort, 5,5 % latinamerikansk), efter en gennemsnitlig opfølgning på 5,2 år er vist i tabel 1 nedenfor:
For de resultater, der er inkluderet i det "globale indeks", var de absolutte overrisici pr. 10.000 kvindeår i gruppen behandlet med CE/MPA 7 flere CHD-hændelser, 8 flere slagtilfælde, 8 flere PE'er og 8 flere invasive brystkræftformer, mens de absolutte risikoreduktioner pr. 10.000 kvindeår var 6 færre kolorektale cancere og 5 færre hoftebrud. Den absolutte overrisiko for hændelser inkluderet i det "globale indeks" var 19 pr. 10.000 kvindeår. Der var ingen forskel mellem grupperne med hensyn til dødelighed af alle årsager. (Se ADVARSLER I BOKS , ADVARSLER , og FORHOLDSREGLER .)
Women's Health Initiative Memory Study
Women's Health Initiative Memory Study (WHIMS), en underundersøgelse af WHI, indskrev 4.532 overvejende raske postmenopausale kvinder 65 år og ældre (47 % var i alderen 65 til 69 år, 35 % var 70 til 74 år og 18 år). % var 75 år og ældre) for at evaluere virkningerne af CE/MPA (0,625 mg konjugerede østrogener plus 2,5 mg medroxyprogesteronacetat) på forekomsten af sandsynlig demens (primært resultat) sammenlignet med placebo.
Efter en gennemsnitlig opfølgning på 4 år blev 40 kvinder i østrogen/progestin-gruppen (45 pr. 10.000 kvindeår) og 21 i placebogruppen (22 pr. 10.000 kvindeår) diagnosticeret med sandsynlig demens. Den relative risiko for sandsynlig demens i hormonbehandlingsgruppen var 2,05 (95 % CI, 1,21 til 3,48) sammenlignet med placebo. Forskelle mellem grupperne blev tydelige i det første behandlingsår. Det er uvist, om disse resultater gælder for yngre postmenopausale kvinder. (Se KASSET ADVARSEL og ADVARSLER , Demens .)
PATIENTOPLYSNINGER
INTRODUKTION
Læs denne patientinformation, før du begynder at tage ESTRACE 2mg, og læs, hvad du får, hver gang du genopfylder ESTRACE. Der kan være nye oplysninger. Disse oplysninger træder ikke i stedet for at tale med din sundhedsplejerske om din medicinske tilstand eller din behandling.
HVAD ER DE VIGTIGSTE OPLYSNINGER JEG BØR VIDE OM ESTRACE (ET ØTROGENHORMON)?
- Østrogener øger chancerne for at få kræft i livmoderen.
Rapporter enhver usædvanlig vaginal blødning med det samme, mens du tager østrogener. Vaginal blødning efter overgangsalderen kan være et advarselstegn på kræft i livmoderen (livmoderen). Din læge bør kontrollere enhver usædvanlig vaginal blødning for at finde ud af årsagen.
- Brug ikke østrogener med eller uden progestiner for at forhindre hjertesygdomme, hjerteanfald eller slagtilfælde.
Brug af østrogener med eller uden progestiner kan øge dine chancer for at få hjerteanfald, slagtilfælde, brystkræft og blodpropper. Brug af østrogener med gestagen kan øge din risiko for demens. Du og din sundhedsplejerske bør regelmæssigt tale om, hvorvidt du stadig har brug for behandling med ESTRACE.
HVAD ER ESTRACE?
ESTRACE er et lægemiddel, der indeholder østrogenhormoner.
HVAD ANVENDES ESTRACE TIL?
ESTRACE 1mg bruges til:
- reducere moderate til svære hedeture
Østrogener er hormoner lavet af en kvindes æggestokke. Mellem 45 og 55 år holder æggestokkene normalt op med at danne østrogener. Dette fører til et fald i kroppens østrogenniveauer, som forårsager "livsændringen" eller overgangsalderen (slutningen af månedlige menstruationer). Nogle gange fjernes begge æggestokke under en operation, før den naturlige overgangsalder finder sted. Det pludselige fald i østrogenniveauet forårsager "kirurgisk overgangsalder".
Når østrogenniveauet begynder at falde, udvikler nogle kvinder meget ubehagelige symptomer, såsom varmefølelse i ansigtet, halsen og brystet, eller pludselige stærke følelser af varme og sveden ("hedeture" eller "hedeture"). Hos nogle kvinder er symptomerne milde, og de har ikke brug for østrogener. Hos andre kvinder kan symptomerne være mere alvorlige. Du og din sundhedsplejerske bør regelmæssigt tale om, hvorvidt du stadig har brug for behandling med ESTRACE.
Vægtbærende motion, som at gå eller løbe, og at tage calcium med D-vitamintilskud kan også reducere dine chancer for at få postmenopausal osteoporose. Det er vigtigt at tale om træning og kosttilskud med din sundhedsplejerske, før du starter dem.
behandle tørhed, kløe og svie i eller omkring skeden, besvær eller svie ved vandladning i forbindelse med overgangsalderen
Du og din sundhedsplejerske bør regelmæssigt tale om, hvorvidt du stadig har brug for behandling med ESTRACE for at kontrollere disse problemer. Hvis du kun bruger ESTRACE til at behandle din tørhed, kløe og svie i og omkring din vagina, skal du tale med din læge om, hvorvidt et lokalt vaginalt produkt ville være bedre for dig.
- behandle visse tilstande, hvor en ung kvindes æggestokke ikke producerer nok østrogen naturligt
- behandle visse typer unormal vaginal blødning på grund af hormonel ubalance, når din læge ikke har fundet nogen alvorlig årsag til blødningen
- behandle visse kræftformer i særlige situationer, hos mænd og kvinder
- forhindre udtynding af knogler
Osteoporose fra overgangsalderen er en udtynding af knoglerne, der gør dem svagere og nemmere at knække. Hvis du kun bruger ESTRACE 1mg for at forhindre osteoporose fra overgangsalderen, så tal med din læge om, hvorvidt en anden behandling eller medicin uden østrogener kan være bedre for dig. Du og din sundhedsplejerske bør regelmæssigt tale om, hvorvidt du skal fortsætte med ESTRACE.
HVEM BØR IKKE BRUGE ESTRACE 2mg?
Begynd ikke at tage ESTRACE 2mg, hvis du:
- har usædvanlig vaginal blødning, som ikke er blevet vurderet af din læge (se ADVARSLER I INDKAMMET)
Usædvanlig vaginal blødning kan være et advarselstegn på kræft i livmoderen, især hvis det sker efter overgangsalderen. Din læge skal finde ud af årsagen til blødningen, så han eller hun kan anbefale den rette behandling. At tage østrogener uden at besøge din læge kan forårsage alvorlig skade, hvis din vaginale blødning er forårsaget af kræft i livmoderen.
- i øjeblikket har eller har haft visse kræftformer
Østrogener kan øge risikoen for visse typer kræft, herunder kræft i brystet eller livmoderen. Hvis du har eller har haft kræft, skal du tale med din læge om, hvorvidt du skal tage ESTRACE.
(For visse patienter med bryst- eller prostatacancer kan østrogener hjælpe.)
- haft et slagtilfælde eller hjerteanfald inden for det seneste år
- i øjeblikket har eller har haft blodpropper
- har eller har haft leverproblemer
- er allergiske over for ESTRACE eller nogen af dets ingredienser
Se slutningen af denne indlægsseddel for en liste over ingredienser i ESTRACE.
ESTRACE 2 mg tabletter indeholder tartrazin, som kan forårsage allergiske reaktioner (inklusive bronkial astma) hos visse modtagelige personer. Selvom den samlede forekomst af FD&C Yellow No. 5 (tartrazin) følsomhed i den generelle befolkning er lav, ses den hyppigt hos patienter, som også har aspirinoverfølsomhed.
- tror du kan være gravid
Fortæl din sundhedsplejerske:
- hvis du ammer
Hormonet i ESTRACE 1mg kan gå over i din mælk
- om alle dine medicinske problemer
Din sundhedsplejerske skal muligvis tjekke dig mere omhyggeligt, hvis du har visse tilstande, såsom astma (hvæsen), epilepsi (anfald), migræne, endometriose, lupus, problemer med dit hjerte, lever, skjoldbruskkirtel, nyrer eller har høje calciumniveauer i dit blod.
- om al den medicin, du tager
Dette omfatter receptpligtig og ikke-receptpligtig medicin, vitaminer og naturlægemidler. Nogle lægemidler kan påvirke, hvordan ESTRACE 1mg virker. ESTRACE 1mg kan også påvirke, hvordan din anden medicin virker.
- hvis du skal opereres eller skal ligge i seng
Du skal muligvis stoppe med at tage østrogener.
HVORDAN SKAL JEG TAGE ESTRACE?
1. Start med den laveste dosis og tal med din læge om, hvor godt den dosis virker for dig.
2. Østrogener bør kun anvendes i den lavest mulige dosis til din behandling, så længe det er nødvendigt. Du og din læge bør tale regelmæssigt (for eksempel hver 3. til 6. måned) om den dosis, du tager, og om du stadig har brug for behandling med ESTRACE.
HVAD ER DE MULIGE BIVIRKNINGER AF ØTROGENER?
Mindre almindelige, men alvorlige bivirkninger omfatter:
- Brystkræft
- Kræft i livmoderen
- Slag
- Hjerteanfald
- Blodpropper
- Demens
- Galdeblære sygdom
- Livmoderhalskræft
Dette er nogle af advarselstegnene på de alvorlige bivirkninger:
- Bryst klumper
- Usædvanlig vaginal blødning
- Svimmelhed og besvimelse
- Ændringer i tale
- Svær hovedpine
- Brystsmerter
- Stakåndet
- Smerter i dine ben
- Ændringer i synet
- Opkastning
Ring til din læge med det samme, hvis du får nogle af disse advarselstegn eller andre usædvanlige symptomer, der bekymrer dig.
Almindelige bivirkninger omfatter:
- Hovedpine
- Brystsmerter
- Uregelmæssig vaginal blødning eller pletblødning
- Mave/mavekramper, oppustethed
- Kvalme og opkast
- Hårtab
Andre bivirkninger omfatter:
- Højt blodtryk
- Leverproblemer
- Højt blodsukker
- Væskeretention
- Forstørrelse af godartede tumorer ("fibromer") i livmoderen
- En plettet mørkfarvning af huden, især i ansigtet
- Vaginal gærinfektion
Disse er ikke alle mulige bivirkninger af ESTRACE. For mere information, spørg din læge eller apotek.
HVAD KAN JEG GØRE FOR AT SÆNKKE MINE CHANCER FOR EN ALVORLIG BIVIRKNING VED ESTRACE?
Hvis du bruger østrogener, kan du reducere dine risici ved at gøre disse ting:
- Tal med din sundhedsplejerske:
- Vær opmærksom på tegn på problemer
Hvis nogle af disse advarselssignaler (eller andre usædvanlige symptomer) opstår, mens du bruger østrogener, skal du straks kontakte din læge:
Unormal blødning fra skeden (mulig livmoderkræft)
Smerter i læggene eller brystet, pludselig åndenød eller hostende blod (mulig blodprop i benene eller lungerne)
Alvorlig hovedpine eller opkastning, svimmelhed, besvimelse, ændringer i syn eller tale, svaghed eller følelsesløshed i en arm eller et ben (mulig blodprop i hjernen eller øjet)
Brystklumper (mulig brystkræft; spørg din læge eller sundhedspersonale om at vise dig, hvordan du undersøger dine bryster hver måned)
Gulfarvning af hud eller øjne (muligt leverproblem)
Smerter, hævelse eller ømhed i maven (mulig galdeblæreproblem)
GENEREL INFORMATION OM SIKKER OG EFFEKTIV ANVENDELSE AF ESTRACE
Lægemidler ordineres nogle gange til tilstande, der ikke er nævnt i indlægssedler. Tag ikke ESTRACE 2mg til tilstande, som det ikke er ordineret til. Giv ikke ESTRACE 1 mg til andre mennesker, selvom de har de samme symptomer, som du har. Det kan skade dem.
OPBEVAR ESTRACE UTILGÆNGELIGT FOR BØRN
Denne folder giver en oversigt over de vigtigste oplysninger om ESTRACE. Hvis du vil have mere information, så tal med din læge eller apotek. Du kan bede om information om ESTRACE, der er skrevet til sundhedspersonale. Du kan få flere oplysninger ved at ringe til det gratis nummer 1-800-521-8813.
HVILKE INGREDIENSER I ESTRACE?
Inaktive ingredienser : Kolloid siliciumdioxid, majsstivelse, dibasisk calciumphosphat, lactosemonohydrat, magnesiumstearat og natriumstivelsesglykolat. Derudover indeholder 1 mg også FD&C blå nr. 1 aluminium sø og D&C rødt nr. 27 aluminium sø. De 2 mg indeholder også FD&C blå nr. 1 aluminium sø og FD&C gul nr. 5 (tartrazin) aluminium sø.
