Danazol 50mg, 100mg, 200mg Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Danazol 100mg, og hvordan bruges det?
Danazol 50mg er en receptpligtig medicin, der bruges til at behandle symptomer på endometriose, arvelig angioødem og fibrocystisk brystsygdom. Danazol kan bruges alene eller sammen med anden medicin.
Danazol tilhører en klasse af lægemidler kaldet androgener.
Det vides ikke, om Danazol er sikkert og effektivt hos børn.
Hvad er de mulige bivirkninger af Danazol?
Danazol 100mg kan forårsage alvorlige bivirkninger, herunder:
- hævelse af dine hænder og fødder,
- menstruationsændringer (pletter, udeblevne menstruationer),
- humørsvingninger,
- nervøsitet,
- humørsvingninger,
- udslæt,
- kløe,
- hævelse af ansigt, tunge eller svælg,
- svær svimmelhed og
- vejrtrækningsbesvær
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Danazol 200mg omfatter:
- vægtøgning,
- acne,
- fedtet hud eller hår,
- rødmen,
- svedeture,
- hårtab,
- stemmeændringer (hæshed, ændringer i tonehøjde),
- ondt i halsen,
- unormal vækst af kropsbehåring (hos kvinder),
- vaginal tørhed, irritation, svie eller kløe,
- nedsat bryststørrelse,
- vandophobning,
- depression,
- oppustethed,
- irritabilitet,
- ændringer i menstruationscyklus (pletter, uregelmæssig blødning, udeblevne menstruationer),
- nervøsitet, og
- humørsvingninger
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Danazol. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Danazol 50mg er et syntetisk steroid afledt af ethisteron. Det er et hvidt til bleggult krystallinsk pulver, praktisk talt uopløseligt eller uopløseligt i vand og tungtopløseligt i alkohol. Kemisk er danazol 100 mg 17a-Pregna-2,4-dien-20-yno[2,3-d]-isoxazol-17-ol. Molekylformlen er C22H27NO2. Det har en molekylvægt på 337,46 og følgende strukturformel:
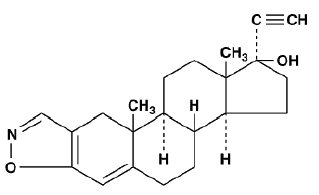
Danazol kapsler til oral administration indeholder 50 mg, 100 mg eller 200 mg danazol.
inaktive ingredienser
vandfri lactose, lactosemonohydrat, magnesiumstearat, prægelatineret stivelse, natriumlaurylsulfat, talkum. Kapselskaller til 200 mg danazol indeholder D&C Yellow #10, FD&C Red #40, D&C Red #28, gelatine og titaniumdioxid. Kapselskaller til 50 mg og 100 mg danazol 50 mg indeholder D&C Yellow # 10, FD&C Red # 40, gelatine og titaniumdioxid. Kapselprægningsblækket indeholder: shellakglasur i ethanol, sort jernoxid, n-butylalkohol, propylenglycol, ethanol, methanol, FD&C Blue No. 2 Aluminium Lake, FD&C Red No. 40 Aluminium Lake, FD&C Blue No. 1 Aluminium Lake , og D&C Yellow No. 10 Aluminium Lake.
INDIKATIONER
Endometriose
Danazol 100 mg kapsler er indiceret til behandling af endometriose, der er modtagelig for hormonbehandling.
Arveligt angioødem
Danazol-kapsler er indiceret til forebyggelse af angioødem af alle typer (kutan, abdominal, larynx) hos mænd og kvinder.
DOSERING OG ADMINISTRATION
Endometriose
Ved moderat til svær sygdom eller hos patienter, der er infertile på grund af endometriose, anbefales en startdosis på 800 mg givet i to opdelte doser. Amenoré og hurtig reaktion på smertefulde symptomer opnås bedst ved dette dosisniveau. Gradvis nedadgående titrering til en dosis, der er tilstrækkelig til at opretholde amenoré, kan overvejes afhængigt af patientens respons. For milde tilfælde anbefales en indledende daglig dosis på 200 mg til 400 mg givet i to opdelte doser og kan justeres afhængigt af patientens respons. Terapi bør begynde under menstruation. I modsat fald bør der udføres passende tests for at sikre, at patienten ikke er gravid under behandling med danazol 50 mg kapsler (se KONTRAINDIKATIONER og ADVARSLER ). Det er vigtigt, at behandlingen fortsætter uafbrudt i 3 til 6 måneder, men kan om nødvendigt forlænges til 9 måneder. Efter afslutning af behandlingen kan behandlingen genoptages, hvis symptomerne opstår igen .
Arveligt angioødem
Dosiskravene til kontinuerlig behandling af arveligt angioødem med danazolkapsler bør individualiseres på basis af patientens kliniske respons. Det anbefales, at patienten startes med 200 mg, to eller tre gange dagligt. Efter et gunstigt indledende respons er opnået med hensyn til forebyggelse af episoder med ødematøse anfald, bør den korrekte fortsatte dosis bestemmes ved at reducere dosis med 50 % eller mindre med intervaller på en til tre måneder eller længere, hvis hyppigheden af anfald forud for behandlingen tilsiger . Hvis der opstår et anfald, kan den daglige dosis øges med op til 200 mg. Under dosisjusteringsfasen er tæt overvågning af patientens respons indiceret, især hvis patienten tidligere har været involveret i luftvejene.
HVORDAN LEVERET
Danazol 50 mg kapsler USP, 50 mg fås som majs uigennemsigtige/hvide uigennemsigtige kapsler præget med logoet "LANNETT" på hætten og "1392" på kroppen og leveres i:
Flasker med 100 stk. NDC 0527-1392-01)
Danazol Kapsler USP, 100 mg fås som majs uigennemsigtige/majs uigennemsigtige kapsler præget med logoet "LANNETT" på hætten og "1368" på kroppen og leveres i:
Flasker med 100 stk. NDC 0527-1368-01)
Danazol Kapsler USP, 200 mg fås som orange uigennemsigtige/orange uigennemsigtige kapsler præget med logoet "LANNETT" på hætten og "1369" på kroppen og leveres i:
Flasker med 60 stk. NDC 0527-1369-06) Flasker á 100 ( NDC 0527-1369-01)
Opbevares ved 20° til 25°C (68° til 77°F) [se USP kontrolleret rumtemperatur].
Dispenser i en godt lukket beholder med en børnesikret lukning som defineret i USP.
Distribueret af: Lannett Company, Inc. Philadelphia, PA 19154. Revideret: maj 2018
BIVIRKNINGER
Følgende hændelser er blevet rapporteret i forbindelse med brugen af danazol 100 mg kapsler:
Androgenlignende effekter omfatter vægtøgning, acne og seborrhea. Mild hirsutisme, ødem, hårtab, stemmeændring, som kan tage form af hæshed, ondt i halsen eller af ustabilitet eller fordybning af tonehøjde, kan forekomme og kan vare ved efter behandlingens ophør. Hypertrofi af klitoris er sjælden.
Andre mulige endokrine virkninger er menstruationsforstyrrelser, herunder pletblødninger, ændring af tidspunktet for cyklussen og amenoré. Selvom cyklisk blødning og ægløsning normalt vender tilbage inden for 60-90 dage efter seponering af behandlingen med danazol-kapsler, er vedvarende amenoré lejlighedsvis blevet rapporteret.
Rødmen, svedtendens, vaginal tørhed og irritation og reduktion i bryststørrelse kan afspejle sænkning af østrogen. Nervøsitet og følelsesmæssig labilitet er blevet rapporteret. Hos mænd kan en beskeden reduktion i spermatogenese være tydelig under behandlingen. Abnormiteter i sædvolumen, viskositet, sædtal og motilitet kan forekomme hos patienter, der får langtidsbehandling.
Leverdysfunktion, som påvist af reversible forhøjede serumenzymer og/eller gulsot, er blevet rapporteret hos patienter, der får en daglig dosis danazol-kapsler på 400 mg eller mere. Det anbefales, at patienter, der får danazol-kapsler, overvåges for leverdysfunktion ved laboratorietest og klinisk observation. Alvorlig levertoksicitet inklusive kolestatisk gulsot, peliosis hepatis, hepatisk adenom, hepatocellulær skade, hepatocellulær gulsot og leversvigt er blevet rapporteret (se ADVARSLER og FORHOLDSREGLER ).
Abnormiteter i laboratorietests kan forekomme under behandling med danazol 50 mg kapsler, inklusive CPK, glucosetolerance, glucagon, thyreoideabindende globulin, kønshormonbindende globulin, andre plasmaproteiner, lipider og lipoproteiner.
Følgende reaktioner er blevet rapporteret, en årsagssammenhæng til administration af danazol-kapsler er hverken blevet bekræftet eller afkræftet;
Allergisk: nældefeber, kløe og sjældent tilstoppet næse;
CNS effekter: hovedpine, nervøsitet og følelsesmæssig labilitet, svimmelhed og besvimelse, depression, træthed, søvnforstyrrelser, tremor, paræstesier, svaghed, synsforstyrrelser og sjældent godartet intrakraniel hypertension, angst, ændringer i appetit, kulderystelser og sjældent kramper, Guillain-Barre syndrom ;
Gastrointestinale: gastroenteritis, kvalme, opkastning, forstoppelse og sjældent pancreatitis og miltpeliose;
Muskuloskeletale: muskelkramper eller spasmer eller smerter, ledsmerter, ledlåsning, ledhævelser, smerter i ryg, nakke eller ekstremiteter og sjældent karpaltunnelsyndrom, som kan være sekundært til væskeretention;
Genitourinære: hæmaturi, langvarig postterapi amenoré;
Hæmatologisk: en stigning i antallet af røde blodlegemer og blodplader. Reversibel erytrocytose, leukocytose eller polycytæmi kan være fremkaldt. Eosinofili, leukopeni og trombocytopeni er også blevet bemærket.
Hud: udslæt (makulopapulær, vesikulær, papulær, purpurisk, petechial) og sjældent solfølsomhed, Stevens-Johnsons syndrom og erythema multiforme;
Andet: øget insulinbehov hos diabetespatienter, ændring i libido, myokardieinfarkt, hjertebanken, takykardi, forhøjet blodtryk, interstitiel pneumonitis og sjældent grå stær, blødende tandkød, feber, bækkensmerter, udflåd fra brystvorten. Maligne levertumorer er blevet rapporteret i sjældne tilfælde efter langvarig brug.
DRUGSINTERAKTIONER
Forlængelse af protrombintid forekommer hos patienter stabiliseret på warfarin.
Behandling med danazol 50 mg kan forårsage en stigning i carbamazepinniveauer hos patienter, der tager begge lægemidler.

Danazol 50mg kan forårsage insulinresistens. Der skal udvises forsigtighed, når det bruges sammen med antidiabetika.
Danazol 100 mg kan hæve plasmaniveauerne af cyclosporin og tacrolimus, hvilket fører til en stigning i nyretoksiciteten af disse lægemidler. Overvågning af systemiske koncentrationer af disse lægemidler og passende dosisjusteringer kan være nødvendige, når de bruges samtidig med danazol.
Danazol 100mg kan øge den calcæmiske respons på syntetiske D-vitaminanaloger ved primær hypoparathyroidisme.
Risikoen for myopati og rhabdomyolyse øges ved samtidig administration af danazol 50 mg og statiner såsom simvastatin, atorvastatin og lovastatin. Der skal udvises forsigtighed ved samtidig brug. Se produktmærkningen for statiner for specifik information om dosisbegrænsninger ved tilstedeværelse af danazol.
ADVARSLER
Brug af danazol 100mg under graviditet er kontraindiceret. En følsom test (f.eks. beta-underenhedstest, hvis tilgængelig), der er i stand til at bestemme tidlig graviditet, anbefales umiddelbart før påbegyndelse af behandlingen. Derudover bør en ikke-hormonel præventionsmetode anvendes under behandlingen. Hvis en patient bliver gravid, mens han tager danazol 200 mg, skal administrationen af lægemidlet afbrydes, og patienten skal informeres om den potentielle risiko for fosteret. Eksponering for danazol 200mg in utero kan resultere i androgene virkninger på det kvindelige foster; der er modtaget rapporter om klitorishypertrofi, labial fusion, urogenital sinusdefekt, vaginal atresi og tvetydige kønsorganer (se FORHOLDSREGLER : Graviditet, teratogene virkninger).
Tromboemboli, trombotiske og tromboflebitiske hændelser inklusive sagittal sinus-trombose og livstruende eller fatale slagtilfælde er blevet rapporteret.
Erfaring med langtidsbehandling med danazol 100mg er begrænset. Peliosis hepatis og benignt hepatisk adenom er blevet observeret ved langtidsbrug. Peliosis hepatis og hepatisk adenom kan være stille, indtil de kompliceres af akut, potentielt livstruende intraabdominal blødning. Lægen bør derfor være opmærksom på denne mulighed. Der bør gøres forsøg på at bestemme den laveste dosis, der vil give tilstrækkelig beskyttelse. Hvis lægemidlet blev påbegyndt på et tidspunkt med forværring af arvelig angioneurotisk ødem på grund af traumer, stress eller anden årsag, bør periodiske forsøg på at reducere eller seponere behandlingen overvejes.
Danazol 100mg er blevet forbundet med adskillige tilfælde af benign intrakraniel hypertension også kendt som pseudotumor cerebri. Tidlige tegn og symptomer på benign intrakraniel hypertension omfatter papilleødem, hovedpine, kvalme og opkastning og synsforstyrrelser. Patienter med disse symptomer bør screenes for papilleødem, og hvis de er til stede, bør patienterne rådes til straks at seponere danazol 100 mg og henvises til en neurolog for yderligere diagnose og pleje.
En midlertidig ændring af lipoproteiner i form af nedsatte højdensitetslipoproteiner og muligvis øgede lavdensitetslipoproteiner er blevet rapporteret under danazolbehandling. Disse ændringer kan være markante, og ordinerende læger bør overveje den potentielle indvirkning på risikoen for aterosklerose og koronararteriesygdom i overensstemmelse med den potentielle fordel af behandlingen for patienten.
Patienter bør overvåges nøje for tegn på androgene virkninger, hvoraf nogle muligvis ikke er reversible, selv når lægemiddeladministrationen stoppes.
FORHOLDSREGLER
Da danazol-kapsler kan forårsage en vis grad af væskeretention, kræver tilstande, der kan være påvirket af denne faktor, såsom epilepsi, migræne eller hjerte- eller nyredysfunktion, polycytæmi og hypertension omhyggelig observation. Brug med forsigtighed til patienter med diabetes mellitus.
Da leverdysfunktion manifesteret ved beskedne stigninger i serumtransaminaser er blevet rapporteret hos patienter behandlet med danazol-kapsler, bør der udføres periodiske leverfunktionstests (se ADVARSLER og BIVIRKNINGER ).
Administration af danazol 50 mg er blevet rapporteret at forårsage forværring af manifestationerne af akut intermitterende porfyri (se KONTRAINDIKATIONER ).
Laboratorieovervågning af den hæmatologiske tilstand bør overvejes.
Laboratorieprøver
Danazolbehandling kan interferere med laboratoriebestemmelser af testosteron, androstenedion og dehydroepiandrosteron. Andre metaboliske hændelser omfatter en reduktion i thyreoideabindende globulin og T4 med øget optagelse af T3, men uden forstyrrelse af thyroidstimulerende hormon eller af frit thyroxinindeks.
Karcinogenese, mutagenese, svækkelse af fertilitet
Aktuelle data er utilstrækkelige til at vurdere danazols carcinogenicitet.
Graviditet Teratogene virkninger
(se KONTRAINDIKATIONER .) Danazol 50 mg indgivet oralt til drægtige rotter fra den 6. til den 15. drægtighedsdag i doser op til 250 mg/kg/dag (7-15 gange den humane dosis) resulterede ikke i lægemiddelinduceret embryotoksicitet eller teratogenicitet, ej heller forskel i kuld størrelse, levedygtighed eller vægt af afkom sammenlignet med kontroller. Hos kaniner resulterede administration af danazol 200 mg på dag 6-18 af drægtighed ved doser på 60 mg/kg/dag og derover (2-4 gange human dosis) i hæmning af fosterudviklingen.
Ammende mødre
(se KONTRAINDIKATIONER .)
Pædiatrisk brug
Sikkerhed og effektivitet hos pædiatriske patienter er ikke blevet fastslået.
Geriatrisk brug
Kliniske undersøgelser af danazolkapsler omfattede ikke et tilstrækkeligt antal forsøgspersoner på 65 år og derover til at bestemme sikkerheden og effektiviteten af Danocrine hos ældre patienter.
OVERDOSIS
Ingen oplysninger givet
KONTRAINDIKATIONER
Danazol 50 mg kapsler bør ikke administreres til patienter med:
KLINISK FARMAKOLOGI
Danazol undertrykker hypofyse-ovarieaksen. Denne suppression er sandsynligvis en kombination af deprimeret hypothalamus-hypofyse-respons på nedsat østrogenproduktion, ændring af kønssteroidmetabolisme og interaktion af danazol med kønshormonreceptorer. Den eneste anden påviselige hormonelle virkning er svag androgen aktivitet. Danazol 50mg sænker produktionen af både follikelstimulerende hormon (FSH) og luteiniserende hormon (LH).
Nylige beviser tyder på en direkte hæmmende virkning på gonadale steder og en binding af danazol til receptorer af gonadale steroider ved målorganer. Derudover har danazol 50mg vist sig at sænke IgG-, IgM- og IgA-niveauer signifikant, såvel som fosfolipid- og IgG-isotopautoantistoffer hos patienter med endometriose og associerede forhøjelser af autoantistoffer, hvilket tyder på, at dette kunne være en anden mekanisme, hvorved det letter regression af sygdommen .
Ved behandling af endometriose ændrer danazol det normale og ektopiske endometrievæv, så det bliver inaktivt og atrofiskt. Fuldstændig opløsning af endometrielæsioner forekommer i de fleste tilfælde.
Ændringer i vaginal cytologi og cervikal slim afspejler den undertrykkende effekt af danazol på hypofyse-ovarieaksen.
Ændringer i menstruationsmønsteret kan forekomme.
Generelt er den hypofyse-undertrykkende virkning af danazol 200mg reversibel. Ægløsning og cyklisk blødning vender normalt tilbage inden for 60 til 90 dage, når behandlingen med danazol 100 mg seponeres.
Ved behandling af arveligt angioødem forhindrer danazol i effektive doser anfald af sygdommen karakteriseret ved episodisk ødem i abdominale indvolde, ekstremiteter, ansigt og luftveje, som kan være invaliderende og, hvis luftvejene er involveret, dødelige. Derudover korrigerer danazol 100mg delvist eller fuldstændigt den primære biokemiske abnormitet ved arvelig angioødem ved at øge niveauerne af den mangelfulde C1-esterasehæmmer (C1El). Som et resultat af denne virkning øges serumniveauerne af C4-komponenten i komplementsystemet også.
Farmakokinetik
Absorption
Efter oral administration af en dosis på 400 mg til raske mandlige frivillige, nås maksimale plasmakoncentrationer af danazol mellem 2 og 8 timer med en median Tmax-værdi på 4 timer. Steady state-tilstande observeres efter 6 dage med to gange daglig dosering af danazol 100 mg kapsler.
De farmakokinetiske parametre for danazol 100 mg kapsler efter indgivelse af en 400 mg oral dosis til raske mænd er opsummeret i følgende tabel:
De farmakokinetiske parametre for danazol-kapsler efter oral administration af 100, 200 og 400 mg enkeltdoser til raske kvindelige frivillige er opsummeret i følgende tabel:
Dosis proportionalitet
Biotilgængelighedsundersøgelser indikerer, at blodniveauerne ikke stiger proportionalt med stigninger i den administrerede dosis.
Enkeltdosisadministration af danazolkapsler til raske kvindelige frivillige fandt, at en 4-dobling af dosis kun gav en 1,6 og 2,5 gange stigning i AUC og en 1,3 og 2,2 gange stigning i Cmax i henholdsvis fastende og foderstat. En lignende grad af ikke-dosis proportionalitet blev observeret ved steady state.
Mad effekt
Enkeltdosisadministration af 100 mg og 200 mg kapsler af danazol til kvindelige frivillige viste, at både omfanget af tilgængelighed og den maksimale plasmakoncentration steg med henholdsvis 3 til 4 gange efter et måltid (> 30 gram fedt), sammenlignet med den fastende tilstand. Ydermere forsinkede mad også den gennemsnitlige tid til maksimal koncentration af danazol med omkring 30 minutter. Selv efter gentagen dosering under mindre ekstreme foder-/fasteforhold forblev der en forskel på ca. 2 til 2,5 gange i biotilgængelighed mellem den fodrede og fastende tilstand.
Fordeling
Danazol 100mg er lipofilt og kan opdeles i cellemembraner, hvilket indikerer sandsynligheden for distribution i dybe vævsrum.
Metabolisme og udskillelse
Danazol 200 mg ser ud til at blive metaboliseret, og metabolitterne elimineres via nyrerne og fæces. De to primære metabolitter, der udskilles i urinen, er 2-hydroxymethyldanazol 50 mg og ethisteron. Mindst ti forskellige produkter blev identificeret i afføring.
Den rapporterede eliminationshalveringstid for danazol 100 mg varierer på tværs af undersøgelser. Den gennemsnitlige halveringstid for danazol hos raske mænd er 9,7 timer. Efter 6 måneders dosering på 200 mg tre gange dagligt til endometriosepatienter blev halveringstiden for danazol rapporteret til 23,7 timer.
PATIENTOPLYSNINGER
Ingen oplysninger angivet. Der henvises til ADVARSLER og FORHOLDSREGLER sektioner.
