Ventolin Inhaler 100mcg Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Ventolin, og hvordan bruges det?
Ventolin HFA er en receptpligtig medicin, der bruges til at behandle symptomer på akut eller svær eller anstrengelsesinduceret astma (bronkospasme). Ventolin HFA kan bruges alene eller sammen med anden medicin.
Ventolin HFA tilhører en klasse af lægemidler kaldet Beta2-agonister.
Det vides ikke, om Ventolin HFA er sikkert og effektivt til børn under 4 år.
Hvad er de mulige bivirkninger af Ventolin?
Ventolin kan forårsage alvorlige bivirkninger, herunder:
- hvæsen,
- kvælning,
- vejrtrækningsproblemer,
- brystsmerter,
- hurtig puls,
- bankende hjerteslag,
- flagrende i dit bryst,
- svær hovedpine,
- dunkende i nakken eller ørerne,
- smerte eller svie, når du tisser,
- øget tørst,
- øget vandladning,
- tør mund,
- frugtig ånde lugt,
- kramper i benene,
- forstoppelse
- uregelmæssige hjerteslag,
- følelsesløshed eller prikken,
- muskelsvaghed, og
- slap følelse
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Ventolin omfatter:
- brystsmerter,
- hurtige eller bankende hjerteslag,
- svimmelhed,
- føler sig rystende,
- nervøsitet,
- hovedpine,
- rygsmerte,
- kropssmerter,
- dårlig mave,
- ondt i halsen,
- bihulesmerter, og
- løbende eller tilstoppet næse
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Ventolin. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Den aktive komponent i VENTOLIN HFA er albuterolsulfat, USP, den racemiske form af albuterol og en relativt selektiv beta-adrenerg bronkodilatator. Albuterolsulfat har det kemiske navn α1 - [(tert-butylamino)methyl]-4-hydroxy-m-xylen-α, α'-diolsulfat (2:1)(salt) og følgende kemiske struktur:
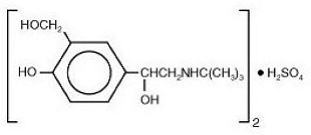
Albuterolsulfat er et hvidt krystallinsk pulver med en molekylvægt på 576,7, og den empiriske formel er (C13H21NO3)2•H2SO4. Det er opløseligt i vand og lidt opløseligt i ethanol.
Verdenssundhedsorganisationens anbefalede navn for albuterolbase er salbutamol.
VENTOLIN HFA er en blå plastikinhalator med en blå remhætte indeholdende en tryksat aerosolbeholder med en tæller. Hver beholder indeholder en mikrokrystallinsk suspension af albuterolsulfat i drivmiddel HFA-134a (1,1,1,2-tetrafluorethan). Det indeholder ingen andre hjælpestoffer.
Efter priming afgiver hver aktivering af inhalatoren 120 mcg albuterolsulfat, USP i 75 mg suspension fra ventilen og 108 mcg albuterolsulfat, USP fra mundstykket (svarende til 90 mcg albuterolbase fra mundstykket).
Spæd VENTOLIN HFA før brug første gang, når inhalatoren ikke har været brugt i mere end 2 uger, eller når inhalatoren er blevet tabt. For at prime VENTOLIN HFA skal du frigive 4 sprays i luften væk fra ansigtet, mens du ryster godt før hver spray.
INDIKATIONER
Bronkospasme
VENTOLIN® HFA inhalationsaerosol er indiceret til behandling eller forebyggelse af bronkospasme hos patienter i alderen 4 år og ældre med reversibel obstruktiv luftvejssygdom.
Trænings-induceret bronkospasme
VENTOLIN HFA er indiceret til forebyggelse af anstrengelsesudløst bronkospasme hos patienter i alderen 4 år og ældre.
DOSERING OG ADMINISTRATION
Bronkospasme
Til behandling af akutte episoder med bronkospasme eller forebyggelse af symptomer forbundet med bronkospasme er den sædvanlige dosis til voksne og børn 2 inhalationer gentaget hver 4. til 6. time; hos nogle patienter kan 1 inhalation hver 4. time være tilstrækkeligt. Hyppigere administration eller et større antal inhalationer anbefales ikke.
Trænings-induceret bronkospasme
Til forebyggelse af anstrengelsesudløst bronkospasme er den sædvanlige dosis for voksne og børn i alderen 4 år og ældre 2 inhalationer 15 til 30 minutter før træning.
Administrationsoplysninger
VENTOLIN HFA bør kun administreres ad oralt inhaleret vej.
Grunding
Grunding af VENTOLIN HFA er afgørende for at sikre passende albuterolindhold i hver aktivering. Spæd VENTOLIN HFA før brug første gang, når inhalatoren ikke har været brugt i mere end 2 uger, eller når inhalatoren er blevet tabt. For at prime VENTOLIN HFA skal du frigive 4 sprays i luften væk fra ansigtet, mens du ryster godt før hver spray.
Rengøring
For at sikre korrekt dosering og for at forhindre blokering af aktuatoråbningen, vask aktuatoren med varmt vand og lad den lufttørre fuldstændigt mindst en gang om ugen.
HVORDAN LEVERET
Doseringsformer og styrker
Indånding Aerosol. Blå plastinhalator med en blå remhætte indeholdende en tryksat aerosolbeholder med afmålt dosis indeholdende 60 eller 200 afmålte inhalationer og udstyret med en tæller. Hver aktivering afgiver 108 mcg albuterolsulfat (90 mcg albuterolbase) fra mundstykket.
Opbevaring og håndtering
VENTOLIN HFA Inhalationsaerosol leveres i følgende kasser af 1 som trykbeholder af aluminium forsynet med tæller og forsynet med blå plastaktuator med blå remhætte:
NDC 0173-0682-20 18 g beholder indeholdende 200 aktiveringer NDC 0173-0682-21 8-g beholder indeholdende 60 aktiveringer NDC 0173-0682-24 8-g institutionspakkebeholder indeholdende 60 aktiveringer
Hver inhalator er forseglet i en fugtbeskyttende foliepose med et tørremiddel, som skal kasseres, når posen åbnes. Hver inhalator er pakket med en patientinformationsfolder.
Den blå aktuator, der leveres med VENTOLIN HFA, bør ikke bruges sammen med andre produktbeholdere, og aktuatorer fra andre produkter bør ikke bruges med en VENTOLIN HFA-beholder.
VENTOLIN HFA har en tæller fastgjort til beholderen. Tælleren starter ved 204 eller 64 og tæller ned, hver gang en spray frigives. Den korrekte mængde medicin i hver aktivering kan ikke sikres, efter at tælleren viser 000, selvom beholderen ikke er helt tom og vil fortsætte med at fungere. Inhalatoren skal kasseres, når tælleren viser 000 eller 12 måneder efter fjernelse fra den fugtbeskyttende foliepose, alt efter hvad der kommer først.
Holde utilgængeligt for børn. Undgå at sprøjte i øjnene.
Indhold under tryk: Må ikke punkteres. Må ikke bruges eller opbevares i nærheden af varme eller åben ild. Udsættelse for temperaturer over 120°F kan forårsage sprængning. Smid aldrig beholder i ild eller forbrændingsovn.
Opbevares ved stuetemperatur mellem 68°F og 77°F (20°C og 25°C); udflugter tilladt fra 59°F til 86°F (15°C til 30°C) [Se USP kontrolleret rumtemperatur ]. Opbevar inhalatoren med mundstykket nede. For de bedste resultater skal inhalatoren have stuetemperatur før brug. RYST GODT FØR HVER SPRAY.
GlaxoSmithKline, Research Triangle Park, NC 27709. Revideret: Dec 2014
BIVIRKNINGER
Brug af VENTOLIN HFA kan være forbundet med følgende:
- Paradoksal bronkospasme [se ADVARSLER OG FORHOLDSREGLER ]
- Kardiovaskulære virkninger [se ADVARSLER OG FORHOLDSREGLER ]
- Øjeblikkelige overfølsomhedsreaktioner [se ADVARSLER OG FORHOLDSREGLER ]
- Hypokaliæmi [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring med kliniske forsøg
Fordi kliniske forsøg udføres under vidt forskellige forhold, kan de bivirkninger, der er observeret i de kliniske forsøg med et lægemiddel, ikke direkte sammenlignes med hastigheder i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de frekvenser, der observeres i praksis.
Sikkerhedsdataene beskrevet nedenfor afspejler eksponering for VENTOLIN HFA hos 248 forsøgspersoner behandlet med VENTOLIN HFA i 3 placebokontrollerede kliniske forsøg af 2 til 12 ugers varighed. Data fra voksne og unge er baseret på 2 kliniske forsøg, hvor 202 forsøgspersoner med astma i alderen 12 år og ældre blev behandlet med VENTOLIN HFA 2 inhalationer 4 gange dagligt i 12 ugers varighed. Den voksne/ungdomspopulation var 92 kvinder, 110 mænd og 163 hvide, 19 sorte, 18 latinamerikanske, 2 andre. Data fra pædiatriske forsøgspersoner er baseret på 1 klinisk forsøg, hvor 46 forsøgspersoner med astma i alderen 4 til 11 år blev behandlet med VENTOLIN HFA 2 inhalationer 4 gange dagligt i 2 ugers varighed. Befolkningen var 21 kvinder, 25 mænd og 25 hvide, 17 sorte, 3 latinamerikanske, 1 anden.
Voksne og unge forsøgspersoner i alderen 12 år og ældre: De to 12-ugers, randomiserede, dobbeltblindede forsøg med 610 voksne og teenagere med astma, der sammenlignede VENTOLIN HFA, en CFC 11/12-drevet albuterol-inhalator og en HFA-134a placebo-inhalator. Samlet set var forekomsten og arten af de rapporterede bivirkninger for VENTOLIN HFA og en CFC 11/12-drevet albuterol-inhalator sammenlignelig. Tabel 1 viser forekomsten af alle uønskede reaktioner (uanset om den af investigator anses for at være relateret eller ikke-relateret til lægemidlet) fra disse forsøg, som forekom med en frekvens på 3 % eller mere i gruppen behandlet med VENTOLIN HFA og hyppigere i gruppen behandlet med VENTOLIN HFA end i HFA-134a placebo-inhalatorgruppen.
Bivirkninger rapporteret af mindre end 3 % af de voksne og unge forsøgspersoner, der får VENTOLIN HFA, og af en større andel af forsøgspersonerne, der får VENTOLIN HFA, end de får HFA-134a placebo-inhalator, og som har potentiale til at være relateret til VENTOLIN HFA, omfatter diarré, laryngitis, orofaryngealt ødem, hoste, lungesygdomme, takykardi og ekstrasystoler. Hjertebanken og svimmelhed er også blevet observeret med VENTOLIN HFA.
Pædiatriske forsøgspersoner i alderen 4 til 11 år: Resultater fra det 2-ugers kliniske forsøg med pædiatriske forsøgspersoner med astma i alderen 4 til 11 år viste, at denne pædiatriske population havde en bivirkningsprofil svarende til den for den voksne og den unge population.
Tre forsøg er blevet udført for at evaluere sikkerheden og effektiviteten af VENTOLIN HFA hos forsøgspersoner mellem fødslen og 4 år. Resultaterne af disse forsøg påviste ikke effekten af VENTOLIN HFA i denne aldersgruppe [se Brug i specifikke populationer ]. Da effekten af VENTOLIN HFA ikke er blevet påvist hos børn mellem fødslen og 48 måneders alderen, kan sikkerheden af VENTOLIN HFA i denne aldersgruppe ikke fastslås. Den sikkerhedsprofil, der blev observeret i den pædiatriske population yngre end 4 år, var imidlertid sammenlignelig med den, der blev observeret hos de ældre pædiatriske forsøgspersoner og hos voksne og unge. Hvor forekomsten af bivirkninger var højere hos forsøgspersoner under 4 år sammenlignet med ældre forsøgspersoner, blev de højere forekomster noteret i alle behandlingsgrupper, inklusive placebo. Disse bivirkninger omfattede øvre luftvejsinfektion, nasopharyngitis, pyreksi og takykardi.
Postmarketing oplevelse
Ud over bivirkninger rapporteret fra kliniske forsøg er følgende bivirkninger blevet identificeret under brug af albuterolsulfat efter godkendelse. Fordi disse reaktioner rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt pålideligt at estimere deres hyppighed eller etablere en årsagssammenhæng til lægemiddeleksponering. Disse hændelser er blevet valgt til inklusion på grund af enten deres alvor, hyppighed af rapportering eller årsagssammenhæng med albuterol eller en kombination af disse faktorer.
Tilfælde af paradoksal bronkospasme, hæshed, arytmier (inklusive atrieflimren, supraventrikulær takykardi) og overfølsomhedsreaktioner (inklusive nældefeber, angioødem, udslæt) er blevet rapporteret efter brug af VENTOLIN HFA.
Derudover kan albuterol, ligesom andre sympatomimetiske midler, forårsage bivirkninger såsom hypokaliæmi, hypertension, perifer vasodilatation, angina, tremor, stimulering af centralnervesystemet, hyperaktivitet, søvnløshed, hovedpine, muskelkramper, udtørring eller irritation af oropharynx og metabolisk acidose.
DRUGSINTERAKTIONER
Andre korttidsvirkende sympatomimetiske aerosol-bronkodilatatorer bør ikke anvendes samtidig med albuterol. Hvis yderligere adrenerge lægemidler skal administreres ad en hvilken som helst måde, bør de anvendes med forsigtighed for at undgå skadelige kardiovaskulære effekter.
Beta-adrenerge receptorblokerende midler
Betablokkere blokerer ikke kun den pulmonale virkning af beta-agonister, såsom VENTOLIN HFA, men kan også forårsage alvorlig bronkospasme hos patienter med astma. Patienter med astma bør derfor normalt ikke behandles med betablokkere. Men under visse omstændigheder er der muligvis ingen acceptable alternativer til brugen af beta-adrenerge blokerende midler til disse patienter; kardioselektive betablokkere kan overvejes, selvom de bør administreres med forsigtighed.
Ikke-kaliumbesparende diuretika
EKG-forandringer og/eller hypokaliæmi, der kan være et resultat af administration af ikke-kaliumbesparende diuretika (såsom loop- eller thiaziddiuretika) kan blive akut forværret af beta-agonister, især når den anbefalede dosis af beta-agonisten overskrides. Selvom den kliniske betydning af disse virkninger ikke er kendt, tilrådes forsigtighed ved samtidig administration af VENTOLIN HFA og ikke-kaliumbesparende diuretika.
Digoxin
Gennemsnitlige fald på 16 % til 22 % i serumdigoxinniveauer blev påvist efter henholdsvis intravenøs enkeltdosis og oral administration af albuterol til normale frivillige, som havde fået digoxin i 10 dage. Den kliniske relevans af disse fund for patienter med obstruktiv luftvejssygdom, som får inhaleret albuterol og digoxin på kronisk basis, er uklar. Ikke desto mindre ville det være klogt at omhyggeligt evaluere serumdigoxinniveauerne hos patienter, som i øjeblikket får digoxin og albuterol.
Monoaminoxidasehæmmere og tricykliske antidepressiva
VENTOLIN HFA bør administreres med ekstrem forsigtighed til patienter, der behandles med monoaminoxidasehæmmere eller tricykliske antidepressiva, eller inden for 2 uger efter seponering af sådanne midler, fordi virkningen af albuterol på det vaskulære system kan forstærkes.
ADVARSLER
Inkluderet som en del af FORHOLDSREGLER afsnit.
FORHOLDSREGLER
Paradoksal bronkospasme
VENTOLIN HFA kan producere paradoksal bronkospasme, som kan være livstruende. Hvis der opstår paradoksal bronkospasme efter dosering med VENTOLIN HFA, skal den seponeres med det samme, og alternativ behandling bør iværksættes. Det bør erkendes, at paradoksal bronkospasme, når den er forbundet med inhalerede formuleringer, ofte forekommer ved den første brug af en ny beholder.
Forværring af astma
Astma kan forværres akut over en periode på timer eller kronisk over flere dage eller længere. Hvis patienten har behov for flere doser af VENTOLIN HFA end normalt, kan dette være en markør for destabilisering af astma og kræver revurdering af patienten og behandlingsregimet, idet der tages særligt hensyn til det mulige behov for antiinflammatorisk behandling, f.eks. kortikosteroider.
Brug af antiinflammatoriske midler
Brugen af beta-adrenerge agonistiske bronkodilatatorer alene er muligvis ikke tilstrækkelig til at kontrollere astma hos mange patienter. Det bør tidligt overvejes at tilføje antiinflammatoriske midler, f.eks. kortikosteroider, til det terapeutiske regime.
Kardiovaskulære effekter
VENTOLIN HFA kan, som alle andre beta2-adrenerge agonister, give klinisk signifikante kardiovaskulære effekter hos nogle patienter, såsom ændringer i puls eller blodtryk. Hvis sådanne virkninger opstår, skal VENTOLIN HFA muligvis seponeres. Derudover er beta-agonister blevet rapporteret at producere elektrokardiogram (EKG) ændringer, såsom udfladning af T-bølgen, forlængelse af QTc-intervallet og ST-segmentdepression. Den kliniske relevans af disse fund er ukendt. Derfor bør VENTOLIN HFA, ligesom alle andre sympatomimetiske aminer, anvendes med forsigtighed til patienter med underliggende kardiovaskulære lidelser, især koronar insufficiens, hjertearytmier og hypertension.
Overskrid ikke den anbefalede dosis
Dødsfald er blevet rapporteret i forbindelse med overdreven brug af inhalerede sympatomimetika hos patienter med astma. Den nøjagtige dødsårsag er ukendt, men der er mistanke om hjertestop efter en uventet udvikling af en alvorlig akut astmatisk krise og efterfølgende hypoxi.
Øjeblikkelige overfølsomhedsreaktioner
Umiddelbare overfølsomhedsreaktioner (f.eks. nældefeber, angioødem, udslæt, bronkospasme, hypotension), inklusive anafylaksi, kan forekomme efter administration af VENTOLIN HFA [se KONTRAINDIKATIONER ].
Sameksisterende forhold
VENTOLIN HFA bør, ligesom andre sympatomimetiske aminer, anvendes med forsigtighed hos patienter med krampesygdomme, hyperthyroidisme eller diabetes mellitus og hos patienter, som er usædvanligt reagerende på sympatomimetiske aminer. Store doser af intravenøs albuterol er blevet rapporteret at forværre allerede eksisterende diabetes mellitus og ketoacidose.
Hypokaliæmi
Beta-adrenerge agonister kan forårsage betydelig hypokaliæmi hos nogle patienter, muligvis gennem intracellulær shunting, som har potentiale til at fremkalde uønskede kardiovaskulære virkninger [se KLINISK FARMAKOLOGI ]. Faldet i serumkalium er normalt forbigående og kræver ikke tilskud.
Patientrådgivningsinformation
Råd patienten til at læse den FDA-godkendte patientmærkning ( PATIENTINFORMATION og brugsanvisning ).
Brugshyppighed
Informer patienterne om, at virkningen af VENTOLIN HFA bør vare op til 4 til 6 timer. Brug ikke VENTOLIN HFA oftere end anbefalet. Instruer patienterne i ikke at øge dosis eller hyppighed af doser af VENTOLIN HFA uden at konsultere lægen. Instruer patienterne i at søge læge med det samme, hvis behandling med VENTOLIN HFA bliver mindre effektiv til symptomatisk lindring, symptomerne bliver værre, og/eller de skal bruge produktet oftere end normalt.
Grunding
Instruer patienterne i at prime VENTOLIN HFA før brug første gang, når inhalatoren ikke har været brugt i mere end 2 uger, eller når inhalatoren er blevet tabt. For at prime VENTOLIN HFA skal du frigive 4 sprays i luften væk fra ansigtet, mens du ryster godt før hver spray.
Rengøring
For at sikre korrekt dosering og for at forhindre blokering af aktuatoråbningen, instruer patienterne i at vaske aktuatoren med varmt vand og lade den lufttørre fuldstændigt mindst en gang om ugen. Informer patienterne om, at detaljerede rengøringsinstruktioner er inkluderet i patientinformationsfolderen.
Paradoksal bronkospasme
Informer patienterne om, at VENTOLIN HFA kan fremkalde paradoksal bronkospasme. Instruer dem om at seponere VENTOLIN HFA, hvis der opstår paradoksal bronkospasme.
Samtidig medicinbrug
Rådgiv patienterne, at mens de bruger VENTOLIN HFA, bør andre inhalationspræparater og astmamedicin kun tages som anvist af lægen.
Almindelige bivirkninger
Almindelige bivirkninger ved behandling med inhaleret albuterol omfatter hjertebanken, brystsmerter, hurtig puls, tremor og nervøsitet.
Graviditet
Rådgiv patienter, der er gravide eller ammer, om at kontakte deres læger om brugen af VENTOLIN HFA.
VENTOLIN er et registreret varemærke tilhørende GSK-gruppen af virksomheder. De øvrige anførte mærker er varemærker tilhørende deres respektive ejere og er ikke varemærker tilhørende GSK-gruppen af virksomheder. Producenterne af disse mærker er ikke tilknyttet og støtter ikke GSK-gruppen af virksomheder eller dens produkter.
Ikke-klinisk toksikologi
Karcinogenese, mutagenese, svækkelse af fertilitet
et 2-årigt studie med Sprague-Dawley-rotter forårsagede albuterolsulfat en dosisrelateret stigning i forekomsten af benigne leiomyomer i mesovarium ved og over diætdoser på 2,0 mg/kg (ca. 14 og 6 gange MRHDID for voksne og børn, henholdsvis på mg/m-basis). I en anden undersøgelse blev denne effekt blokeret af samtidig administration af propranolol, en ikke-selektiv betaadrenerg antagonist. I et 18-måneders studie i CD-1-mus viste albuterolsulfat ingen tegn på tumorigenicitet ved diætdoser på op til 500 mg/kg (ca. 1.700 og 800 gange MRHDID for henholdsvis voksne og børn på mg/m²-basis). ). I et 22-måneders studie med guldhamstere viste albuterolsulfat ingen tegn på tumorfremkaldende virkning ved diætdoser på op til 50 mg/kg (ca. 225 og 110 gange MRHDID for henholdsvis voksne og børn på mg/m²-basis).
Albuterolsulfat var ikke mutagent i Ames-testen eller en mutationstest i gær. Albuterolsulfat var ikke klastogent i et humant perifert lymfocytassay eller i et AH1-stamme muse mikronukleusassay.
Reproduktionsstudier med rotter viste ingen tegn på nedsat fertilitet ved orale doser af albuterolsulfat op til 50 mg/kg (ca. 340 gange MRHDID for voksne på mg/m-basis).
Brug i specifikke populationer
Graviditet
Teratogene virkninger
Graviditetskategori C. Der er ingen tilstrækkelige og velkontrollerede forsøg med VENTOLIN HFA eller albuterolsulfat hos gravide kvinder. I løbet af verdensomspændende markedsføringserfaringer er der rapporteret om forskellige medfødte anomalier, herunder ganespalte og lemmerdefekter, hos afkom fra patienter, der behandles med albuterol. Nogle af mødrene tog flere lægemidler under deres graviditeter. Intet konsistent mønster af defekter kan skelnes, og en sammenhæng mellem brug af albuterol og medfødte anomalier er ikke blevet etableret. Dyreproduktionsundersøgelser på mus og kaniner afslørede tegn på teratogenicitet. VENTOLIN HFA bør kun anvendes under graviditet, hvis den potentielle fordel opvejer den potentielle risiko for fosteret. Kvinder bør rådes til at kontakte deres læge, hvis de bliver gravide, mens de tager VENTOLIN HFA.
et reproduktionsstudie med mus frembragte subkutant administreret albuterolsulfat dannelse af ganespalte hos 5 ud af 111 (4,5 %) fostre ved eksponeringer mindre end den maksimale anbefalede humane daglige inhalationsdosis (MRHDID) for voksne på mg/m²-basis og hos 10 ud af 108 (9,3 %) fostre ved ca. 8 gange MRHDID. Lignende virkninger blev ikke observeret ved ca. en ellevtedel af MRHDID. Ganespalte forekom også hos 22 ud af 72 (30,5 %) fostre fra hunner behandlet subkutant med isoproterenol (positiv kontrol).
I en reproduktionsundersøgelse af kaniner frembragte oralt administreret albuterolsulfat kranioschisis hos 7 ud af 19 fostre (37 %) ved ca. 680 gange MRHDID.
I en anden kaninundersøgelse frembragte en albuterolsulfat/HFA-134a-formulering administreret ved inhalation forstørrelse af den frontale del af fosterfontanellerne ved ca. en tredjedel af MRHDID.
Ikke-ratatogene virkninger
En undersøgelse, hvor gravide rotter blev doseret med radioaktivt mærket albuterolsulfat, viste, at lægemiddelrelateret materiale overføres fra moderens kredsløb til fosteret.
Arbejde og levering
Der er ingen velkontrollerede forsøg på mennesker, som har undersøgt virkningerne af VENTOLIN HFA på præmatur fødsel eller fødsel ved termin. På grund af potentialet for beta-agonistinterferens med uterus kontraktilitet, bør brugen af VENTOLIN HFA under fødslen begrænses til de patienter, hvor fordelene klart opvejer risikoen.
Ammende mødre
Plasmaniveauer af albuterolsulfat og HFA-134a efter inhalerede terapeutiske doser er meget lave hos mennesker, men det vides ikke, om komponenterne i VENTOLIN HFA udskilles i modermælk. På grund af potentialet for tumorigenicitet vist for albuterol i dyreforsøg og manglende erfaring med brugen af VENTOLIN HFA hos ammende mødre, bør der tages en beslutning om, hvorvidt amningen skal afbrydes eller lægemidlet skal seponeres under hensyntagen til lægemidlets betydning for moderen. Der skal udvises forsigtighed, når VENTOLIN HFA administreres til en ammende kvinde.
Pædiatrisk brug
Sikkerheden og effektiviteten af VENTOLIN HFA hos børn i alderen 4 år og derover er blevet fastslået baseret på to 12-ugers kliniske forsøg med personer i alderen 12 år og ældre med astma og et 2-ugers klinisk forsøg med forsøgspersoner i alderen 4 til 11 år med astma [se BIVIRKNINGER , Kliniske Studier ]. Sikkerheden og effektiviteten af VENTOLIN HFA hos børn under 4 år er ikke blevet fastslået. Tre forsøg er blevet udført for at evaluere sikkerheden og effektiviteten af VENTOLIN HFA hos forsøgspersoner yngre end 4 år, og resultaterne er beskrevet nedenfor.
To 4-ugers randomiserede, dobbeltblindede, placebokontrollerede forsøg blev udført med 163 pædiatriske forsøgspersoner i alderen fra fødslen til 48 måneder med symptomer på bronkospasme forbundet med obstruktiv luftvejssygdom (med symptomer inkluderet: hvæsen, hoste, dyspnø eller trykken for brystet) . VENTOLIN HFA eller placebo HFA blev leveret med enten et AeroChamber Plus® ventilholdekammer eller et Optichamber® ventilholdekammer med maske 3 gange dagligt. I et forsøg blev VENTOLIN HFA 90 mcg (n = 26), VENTOLIN HFA 180 mcg (n = 25) og placebo HFA (n = 26) administreret til børn i alderen mellem 24 og 48 måneder. I det andet forsøg blev VENTOLIN HFA 90 mcg (n = 29), VENTOLIN HFA 180 mcg (n = 29) og placebo HFA (n = 28) administreret til børn i alderen mellem fødslen og 24 måneder. I løbet af den 4-ugers behandlingsperiode var der ingen behandlingsforskelle i astmasymptom-score mellem grupperne, der fik VENTOLIN HFA 90 mcg, VENTOLIN HFA 180 mcg og placebo i begge forsøg.
et tredje forsøg blev VENTOLIN HFA evalueret hos 87 pædiatriske forsøgspersoner yngre end 24 måneder til behandling af akut hvæsende vejrtrækning. VENTOLIN HFA blev leveret med et AeroChamber Plus-ventilholdekammer i dette forsøg. Der var ingen signifikante forskelle i astmasymptomscore og gennemsnitlig ændring fra baseline i en astmasymptomscore mellem VENTOLIN HFA 180 mcg og VENTOLIN HFA 360 mcg.
In vitro dosiskarakteriseringsundersøgelser blev udført for at evaluere leveringen af VENTOLIN HFA via holdekamre med påsatte masker. Undersøgelserne blev udført med 2 forskellige holdekamre med masker (små og mellemstore). In vitro-undersøgelsesdataene ved simulering af patientåndedræt tyder på, at dosen af VENTOLIN HFA præsenteret til inhalation via et ventilkammer med maske vil være sammenlignelig med den dosis, der leveres til voksne uden spacer og maske pr. kilogram kropsvægt (tabel 2). Kliniske forsøg med børn under 4 år beskrevet ovenfor tyder dog på, at enten den optimale dosis af VENTOLIN HFA ikke er blevet defineret i denne aldersgruppe, eller at VENTOLIN HFA ikke er effektiv i denne aldersgruppe. Sikkerheden og effektiviteten af VENTOLIN HFA administreret med eller uden en spacer-anordning til børn under 4 år er ikke blevet påvist.
Geriatrisk brug
Kliniske forsøg med VENTOLIN HFA omfattede ikke et tilstrækkeligt antal forsøgspersoner i alderen 65 år og ældre til at afgøre, om ældre forsøgspersoner reagerer anderledes end yngre forsøgspersoner. Andre rapporterede kliniske erfaringer har ikke identificeret forskelle i respons mellem ældre og yngre patienter. Generelt bør dosisvalg for en ældre patient være forsigtigt, sædvanligvis begyndende i den lave ende af doseringsområdet, hvilket afspejler den større hyppighed af nedsat lever-, nyre- eller hjertefunktion og af samtidig sygdom eller anden lægemiddelbehandling.
OVERDOSIS
De forventede tegn og symptomer ved overdosering af albuterol er dem af overdreven beta-adrenerg stimulering og/eller forekomst eller overdrivelse af nogen af tegnene og symptomerne på beta-adrenerg stimulering (f.eks. krampeanfald, angina, hypertension eller hypotension, takykardi med højere hastigheder til 200 slag/min, arytmier, nervøsitet, hovedpine, tremor, muskelkramper, mundtørhed, hjertebanken, kvalme, svimmelhed, træthed, utilpashed, søvnløshed, hyperglykæmi, hypokaliæmi, metabolisk acidose).
Som med alle inhalerede sympatomimetiske lægemidler, kan hjertestop og endda død være forbundet med en overdosis af VENTOLIN HFA inhalationsaerosol.
Behandlingen består af seponering af VENTOLIN HFA sammen med passende symptomatisk behandling. Den fornuftige brug af en kardioselektiv beta-receptorblokker kan overvejes i betragtning af, at sådan medicin kan fremkalde bronkospasme. Der er ikke tilstrækkelig evidens til at afgøre, om dialyse er gavnligt for overdosering af VENTOLIN HFA.
KONTRAINDIKATIONER
VENTOLIN HFA er kontraindiceret til patienter med en historie med overfølsomhed over for et eller flere af indholdsstofferne [se ADVARSLER OG FORHOLDSREGLER , BESKRIVELSE ].
KLINISK FARMAKOLOGI
Handlingsmekanisme
In vitro undersøgelser og in vivo farmakologiske undersøgelser har vist, at albuterol har en præferencevirkning på beta2-adrenerge receptorer sammenlignet med isoproterenol. Selvom beta2-adrenoceptorer er de dominerende adrenerge receptorer i bronkial glat muskulatur, og beta1-adrenoceptorer er de dominerende receptorer i hjertet, er der også beta2-adrenoceptorer i det menneskelige hjerte, der udgør 10% til 50% af de samlede beta-adrenoceptorer. Den præcise funktion af disse receptorer er ikke blevet fastslået, men deres tilstedeværelse rejser muligheden for, at selv selektive beta2-agonister kan have hjerteeffekter.
Aktivering af beta2-adrenerge receptorer på glat muskulatur i luftvejene fører til aktivering af adenylcyclase og til en stigning i den intracellulære koncentration af cyklisk-3',5'-adenosinmonofosfat (cyklisk AMP). Denne stigning af cyklisk AMP fører til aktivering af proteinkinase A, som hæmmer phosphoryleringen af myosin og sænker intracellulære ioniske calciumkoncentrationer, hvilket resulterer i afslapning. Albuterol afslapper de glatte muskler i alle luftveje, fra luftrøret til de terminale bronkioler. Albuterol fungerer som en funktionel antagonist til at slappe af luftvejene uanset det involverede spasmogen og beskytter dermed mod alle bronkokonstriktor-udfordringer. Øgede cykliske AMP-koncentrationer er også forbundet med inhibering af frigivelse af mediatorer fra mastceller i luftvejene.
Albuterol har i de fleste kontrollerede kliniske forsøg vist sig at have mere effekt på luftvejene i form af afslapning af den glatte bronkialmuskel end isoproterenol ved sammenlignelige doser, samtidig med at det producerer færre kardiovaskulære effekter. Kontrollerede kliniske undersøgelser og anden klinisk erfaring har vist, at inhaleret albuterol, ligesom andre beta-adrenerge agonister, kan give en signifikant kardiovaskulær effekt hos nogle patienter, målt ved pulsfrekvens, blodtryk, symptomer og/eller elektrokardiografiske ændringer [se ADVARSLER OG FORHOLDSREGLER ].
Farmakokinetik
De systemiske niveauer af albuterol er lave efter inhalation af anbefalede doser. Et forsøg udført med 12 raske mandlige og kvindelige forsøgspersoner ved anvendelse af en højere dosis (1.080 mcg albuterolbase) viste, at gennemsnitlige maksimale plasmakoncentrationer på ca. 3 ng/ml forekom efter dosering, når albuterol blev leveret med drivmiddel HFA-134a. Den gennemsnitlige tid til maksimale koncentrationer (Tmax) var forsinket efter administration af VENTOLIN HFA (Tmax= 0,42 timer) sammenlignet med CFC-drevet albuterolinhalator (Tmax=0,17 timer). Tilsyneladende terminal plasmahalveringstid for albuterol er ca. 4,6 timer. Der blev ikke udført yderligere farmakokinetiske undersøgelser for VENTOLIN HFA hos nyfødte, børn eller ældre forsøgspersoner.
Dyretoksikologi og/eller farmakologi
Præklinisk
Intravenøse undersøgelser på rotter med albuterolsulfat har vist, at albuterol krydser blod-hjerne-barrieren og når hjernekoncentrationer på ca. 5,0 % af plasmakoncentrationerne. I strukturer uden for blod-hjerne-barrieren (pineal- og hypofyse) blev albuterolkoncentrationerne fundet at være 100 gange højere end i hele hjernen.
Forsøg med laboratoriedyr (minigrise, gnavere og hunde) har vist forekomsten af hjertearytmier og pludselig død (med histologiske tegn på myokardienekrose), når beta-agonister og methylxanthiner administreres samtidigt. Den kliniske relevans af disse fund er ukendt.
Drivmiddel HFA-134a
Hos dyr og mennesker blev drivmidlet HFA-134a fundet hurtigt at blive absorberet og hurtigt elimineret med en eliminationshalveringstid på 3 til 27 minutter hos dyr og 5 til 7 minutter hos mennesker. Tid til maksimal plasmakoncentration (Tmax) og gennemsnitlig opholdstid er begge ekstremt korte, hvilket fører til en forbigående forekomst af HFA-134a i blodet uden tegn på akkumulering.
Drivmiddel HFA-134a er blottet for farmakologisk aktivitet undtagen ved meget høje doser hos dyr (dvs. 380 til 1.300 gange den maksimale menneskelige eksponering baseret på sammenligninger af areal under plasmakoncentration versus tidskurveværdier [AUC]), hvilket primært producerer ataksi, rysten , dyspnø eller savlen. Disse hændelser ligner virkninger produceret af de strukturelt beslægtede CFC'er, som er blevet brugt i vid udstrækning i inhalatorer med afmålt dosis.
Kliniske Studier
Bronkospasme forbundet med astma
Voksne og unge forsøgspersoner i alderen 12 år og ældre
Effekten af VENTOLIN HFA blev evalueret i to 12-ugers, randomiserede, dobbeltblindede, placebokontrollerede forsøg med forsøgspersoner i alderen 12 år og ældre med mild til moderat astma. Disse forsøg omfattede i alt 610 forsøgspersoner (323 mænd, 287 kvinder). I hvert forsøg modtog forsøgspersoner 2 inhalationer af VENTOLIN HFA, CFC 11/12-drevet albuterol eller HFA-134a placebo 4 gange dagligt i 12 ugers varighed. Forsøgspersoner, der tog HFA-134a placebo-inhalatoren, tog også VENTOLIN HFA til lindring af astmasymptomer efter behov. Nogle forsøgspersoner, der deltog i disse kliniske forsøg, brugte samtidig inhalationssteroidbehandling. Effektiviteten blev vurderet ved seriel forceret eksspiratorisk volumen på 1 sekund (FEV ). I hvert af disse forsøg gav 2 inhalationer af VENTOLIN HFA signifikant større forbedring af FEV1 i forhold til førbehandlingsværdien end placebo. Resultater fra de 2 kliniske forsøg er beskrevet nedenfor.
et 12-ugers, randomiseret, dobbeltblindet forsøg blev VENTOLIN HFA (101 forsøgspersoner) sammenlignet med CFC 11/12-drevet albuterol (99 forsøgspersoner) og en HFA-134a placebo-inhalator (97 forsøgspersoner) hos unge og voksne forsøgspersoner i alderen 12 til 76 år med let til moderat astma. Serielle FEV1-målinger [vist nedenfor som procentvis ændring fra testdagens baseline på dag 1 (n = 297) og ved uge 12 (n = 249)] viste, at 2 inhalationer af VENTOLIN HFA gav signifikant større forbedring i FEV1 i forhold til forbehandlingsværdien end placebo.
FEV1 som procentvis ændring fra prædosis i et stort 12-ugers klinisk forsøg Dag 1 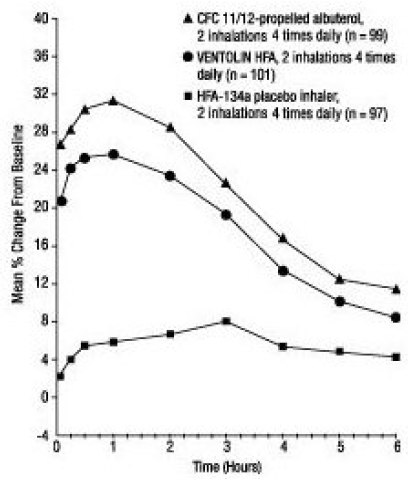
Uge 12 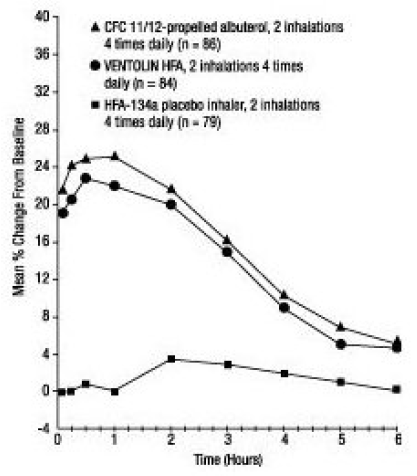
responderpopulationen (større end eller lig med 15 % stigning i FEV1 inden for 30 minutter efter dosis), der blev behandlet med VENTOLIN HFA, var den gennemsnitlige tid til indtræden af en 15 % stigning i FEV1 i forhold til førbehandlingsværdien 5,4 minutter, og middeltiden til maksimal effekt var 56 minutter. Den gennemsnitlige virkningsvarighed målt ved en 15 % stigning i FEV1 i forhold til forbehandlingsværdien var ca. 4 timer. Hos nogle forsøgspersoner var virkningen så lang som 6 timer.
Det andet 12-ugers randomiserede, dobbeltblinde forsøg blev udført for at evaluere effektiviteten og sikkerheden ved at skifte forsøgsperson fra CFC 11/12-drevet albuterol til VENTOLIN HFA. I løbet af forsøgets 3-ugers indkøringsfase modtog alle forsøgspersoner CFC 11/12-drevet albuterol. Under den dobbeltblindede behandlingsfase blev VENTOLIN HFA (91 forsøgspersoner) sammenlignet med CFC 11/12-drevet albuterol (100 forsøgspersoner) og en HFA-134a placebo-inhalator (95 forsøgspersoner) hos voksne og unge med mild til moderat astma. Serielle FEV1-målinger viste, at 2 inhalationer af VENTOLIN HFA gav signifikant større forbedring af lungefunktionen end placebo. Skiftet fra CFC 11/12-drevet albuterol-inhalator til VENTOLIN HFA afslørede ingen klinisk signifikante ændringer i effektivitetsprofilen.
de 2 voksenforsøg var effektresultaterne fra VENTOLIN HFA signifikant større end placebo og var klinisk sammenlignelige med dem opnået med CFC 11/12-drevet albuterol, selvom der blev observeret små numeriske forskelle i gennemsnitlig FEV-respons og andre mål. Læger bør erkende, at individuelle responser på beta-adrenerge agonister administreret via forskellige drivmidler kan variere, og at tilsvarende responser hos individuelle patienter ikke bør antages.
Pædiatriske forsøgspersoner i alderen 4 til 11 år
Effekten af VENTOLIN HFA blev evalueret i et 2-ugers, randomiseret, dobbeltblindet, placebokontrolleret forsøg med 135 pædiatriske forsøgspersoner i alderen 4 til 11 år med mild til moderat astma. I dette forsøg fik forsøgspersonerne VENTOLIN HFA, CFC 11/12-drevet albuterol eller HFA-134a placebo. Serielle lungefunktionsmålinger viste, at 2 inhalationer af VENTOLIN HFA gav signifikant større forbedring af lungefunktionen end placebo, og at der ikke var signifikante forskelle mellem grupperne behandlet med VENTOLIN HFA og CFC 11/12-drevet albuterol. I responderpopulationen behandlet med VENTOLIN HFA var den gennemsnitlige tid til indtræden af en 15 % stigning i peak ekspiratorisk flowhastighed (PEFR) i forhold til forbehandlingsværdien 7,8 minutter, og den gennemsnitlige tid til peak effekt var ca. 90 minutter. Den gennemsnitlige virkningsvarighed målt ved en 15 % stigning i PEFR i forhold til forbehandlingsværdien var mere end 3 timer. Hos nogle forsøgspersoner var virkningen så lang som 6 timer.
Trænings-induceret bronkospasme
Et kontrolleret klinisk forsøg med voksne forsøgspersoner med astma (N = 24) viste, at 2 inhalationer af VENTOLIN HFA taget ca. 30 minutter før træning signifikant forhindrede anstrengelsesinduceret bronkospasme (målt ved det maksimale procentvise fald i FEV1 efter træning) sammenlignet med en HFA-134a placebo inhalator. Derudover har VENTOLIN HFA vist sig at være klinisk sammenlignelig med en CFC 11/12-drevet albuterol-inhalator til denne indikation.
PATIENTOPLYSNINGER
VENTOLIN® [vent' o-lin] HFA (albuterolsulfat) Indånding Aerosol
Læs patientinformationen, der følger med VENTOLIN HFA inhalationsaerosol, før du begynder at bruge den, og hver gang du får en refill. Der kan være nye oplysninger. Denne patientinformation træder ikke i stedet for at tale med din sundhedsplejerske om din medicinske tilstand eller behandling.
Hvad er VENTOLIN HFA?
VENTOLIN HFA er en receptpligtig inhalationsmedicin, der bruges til personer i alderen 4 år og ældre til:
- behandle eller forebygge bronkospasme hos personer, der har reversibel obstruktiv luftvejssygdom
- forebygge anstrengelsesudløst bronkospasme
Det vides ikke, om VENTOLIN HFA er sikkert og effektivt til børn under 4 år.
Hvem bør ikke bruge VENTOLIN HFA?
Brug ikke VENTOLIN HFA hvis du er allergisk over for albuterolsulfat eller et af indholdsstofferne i VENTOLIN HFA. Se "Hvad er ingredienserne i VENTOLIN HFA?" nedenfor for en komplet liste over ingredienser.
Hvad skal jeg fortælle min læge, før jeg bruger VENTOLIN HFA?
Fortæl din sundhedsudbyder om alle dine helbredstilstande, herunder hvis du:
- har hjerteproblemer.
- har forhøjet blodtryk.
- har anfald.
- har problemer med skjoldbruskkirtlen.
- har diabetes.
- har lave kaliumniveauer i dit blod.
- er allergisk over for et eller flere af indholdsstofferne i VENTOLIN HFA eller enhver anden medicin. Se "Hvad er ingredienserne i VENTOLIN HFA?" nedenfor for en komplet liste over ingredienser.
- har andre medicinske tilstande.
- er gravid eller planlægger at blive gravid. Det vides ikke, om VENTOLIN HFA kan skade dit ufødte barn.
- ammer. Det vides ikke, om lægemidlet i VENTOLIN HFA udskilles i din mælk, og om det kan skade dit barn.
Fortæl din læge om al den medicin, du tager, herunder receptpligtig og håndkøbsmedicin, vitaminer og naturlægemidler. VENTOLIN HFA og visse andre lægemidler kan interagere med hinanden. Dette kan forårsage alvorlige bivirkninger.
Fortæl især din læge, hvis du tager:
- anden inhalationsmedicin eller astmamedicin
- beta-blokker medicin
- diuretika
- digoxin
- monoaminoxidasehæmmere
- tricykliske antidepressiva
Spørg din sundhedsudbyder eller apoteket om en liste over disse lægemidler, hvis du ikke er sikker.
Kend den medicin du tager. Hold en liste over dem for at vise din læge og apotek, når du får en ny medicin.
Hvordan skal jeg bruge VENTOLIN HFA?
Læs trin-for-trin instruktionerne for brug af VENTOLIN HFA i slutningen af denne patientinformation.
- Lade være med brug VENTOLIN HFA, medmindre din læge har lært dig, hvordan du bruger inhalatoren, og du forstår, hvordan du bruger den korrekt.
- Børn bør bruge VENTOLIN HFA med en voksens hjælp, som instrueret af barnets sundhedsplejerske.
- Brug VENTOLIN HFA nøjagtigt som din læge fortæller dig at bruge det. Brug ikke VENTOLIN HFA oftere end foreskrevet.
- Lade være med øge din dosis eller tage ekstra doser af VENTOLIN HFA uden først at tale med din læge.
- Hver dosis af VENTOLIN HFA bør vare op til 4 timer til 6 timer.
- Få lægehjælp med det samme, hvis VENTOLIN HFA ikke længere hjælper på dine symptomer.
- Få lægehjælp med det samme, hvis dine symptomer bliver værre, eller hvis du skal bruge din inhalator oftere.
- Mens du bruger VENTOLIN HFA, må du kun bruge anden inhalationsmedicin og astmamedicin som anvist af din læge.
- Ring til din læge, hvis dine astmasymptomer som hvæsen og vejrtrækningsbesvær bliver værre i løbet af et par timer eller dage. Din sundhedsplejerske skal muligvis give dig en anden medicin til at behandle dine symptomer.
Hvad er de mulige bivirkninger ved VENTOLIN HFA?
VENTOLIN HFA kan forårsage alvorlige bivirkninger, herunder:
- forværring af vejrtrækningsbesvær, hoste og hvæsende vejrtrækning (paradoksal bronkospasme). Hvis dette sker, skal du stoppe med at bruge VENTOLIN HFA og ringe til din læge eller få akut hjælp med det samme. Paradoksal bronkospasme er mere tilbøjelig til at opstå ved din første brug af en ny medicinbeholder.
- hjerteproblemer, herunder hurtigere puls og højere blodtryk
- mulig død hos personer med astma, der bruger for meget VENTOLIN HFA
- alvorlige allergiske reaktioner. Ring til din læge eller få akut lægehjælp, hvis du får nogle af følgende symptomer på en alvorlig allergisk reaktion:
- udslæt
- nældefeber
- hævelse af dit ansigt, mund og tunge
- vejrtrækningsproblemer
- ændringer i laboratorieniveauer i blodet (sukker, kalium)
Almindelige bivirkninger af VENTOLIN HFA omfatter:
- ondt i halsen
- øvre luftvejsinfektion, herunder virusinfektion
- hoste
- muskelsmerter
- dit hjerte føles som om det banker eller banker (hjertebanken)
- brystsmerter
- hurtig puls
- rystelse
- nervøsitet
- svimmelhed
Fortæl din læge om enhver bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle bivirkningerne med VENTOLIN HFA. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan skal jeg opbevare VENTOLIN HFA?
- Opbevar VENTOLIN HFA ved stuetemperatur mellem 68°F og 77°F (20°C og 25°C) med mundstykket nede.
- Indholdet af din VENTOLIN HFA er under pres: Må ikke punkteres. Må ikke bruges eller opbevares i nærheden af varme eller åben ild. Temperaturer over 120°F kan få beholderen til at briste.
- Smid ikke i ild eller et forbrændingsanlæg.
- Opbevar VENTOLIN HFA i den uåbnede foliepose og åbn kun, når den er klar til brug.
- Opbevar VENTOLIN HFA og al medicin utilgængeligt for børn.
Generel information om sikker og effektiv brug af VENTOLIN HFA
Lægemidler ordineres nogle gange til formål, der ikke er nævnt i en patientinformationsfolder. Brug ikke VENTOLIN HFA til en tilstand, som det ikke er ordineret til. Giv ikke din VENTOLIN HFA til andre mennesker, selvom de har samme tilstand, som du har. Det kan skade dem.
Denne patientinformationsfolder opsummerer de vigtigste oplysninger om VENTOLIN HFA. Hvis du vil have mere information, så tal med din læge eller apotek. Du kan bede din sundhedsplejerske eller dit apotek om oplysninger om VENTOLIN HFA, som er skrevet til sundhedspersonale.
For mere information om VENTOLIN HFA, ring på 1-888-825-5249 eller besøg vores hjemmeside på www.ventolin.com.
Hvad er ingredienserne i VENTOLIN HFA?
Aktiv ingrediens: albuterolsulfat
Inaktiv ingrediens: drivmiddel HFA-134a
Brugsanvisning
Kun til oral indånding
Din VENTOLIN HFA inhalator
- Metalbeholderen rummer medicinen. Se Figur A.
Figur A 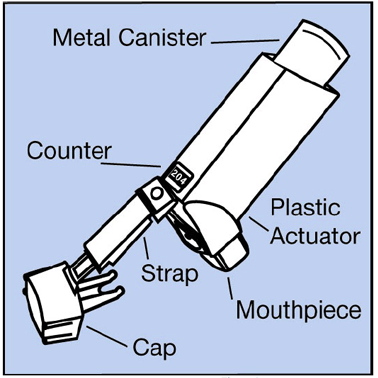
- Beholderen har en tæller, der viser, hvor mange sprays af medicin du har tilbage. Nummeret vises gennem et vindue på bagsiden af aktuatoren. Se figur B.
Figur B 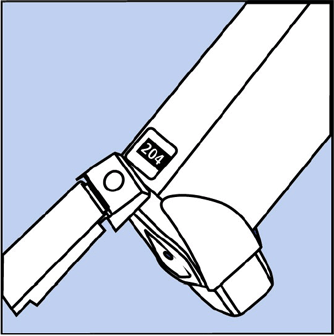
- Tælleren starter enten kl 204 eller 064 alt efter hvilken størrelse inhalator du har. Tallet tælles ned med 1, hver gang du sprayer inhalatoren. Tælleren stopper med at tælle ved 000.
- Forsøg ikke at ændre tallene eller tage tælleren af metalbeholderen. Tælleren kan ikke nulstilles, og den er permanent fastgjort til beholderen.
- Den blå plastikaktuator sprøjter medicinen fra beholderen. Aktuatoren har en beskyttelseshætte, der dækker mundstykket. Se Figur A . Opbevar beskyttelseshætten på mundstykket, når beholderen ikke er i brug. Remmen holder hætten fastgjort til aktuatoren.
- Lade være med brug aktuatoren med en medicinbeholder fra enhver anden inhalator.
- Lade være med brug en VENTOLIN HFA-beholder med en aktuator fra enhver anden inhalator.
Før du bruger din VENTOLIN HFA-inhalator
- Tag VENTOLIN HFA ud af folieposen, lige før du bruger den første gang. Smid posen og tørrepakken, der kommer inde i posen.
- Inhalatoren skal have stuetemperatur, før du bruger den.
- Hvis dit barn skal bruge VENTOLIN HFA, skal du holde øje med dit barn for at sikre, at dit barn bruger inhalatoren korrekt. Din læge vil vise dig, hvordan dit barn skal bruge VENTOLIN HFA.
Klargøring af din VENTOLIN HFA-inhalator
- Før du bruger VENTOLIN HFA første gang, skal du prime inhalatoren, så du får den rigtige mængde medicin, når du bruger den.
- For at spæde inhalatoren skal du tage hætten af mundstykket og ryste inhalatoren godt. Spray derefter inhalatoren 1 gang i luften væk fra dit ansigt. Se figur C. Undgå at sprøjte i øjnene.
Figur C 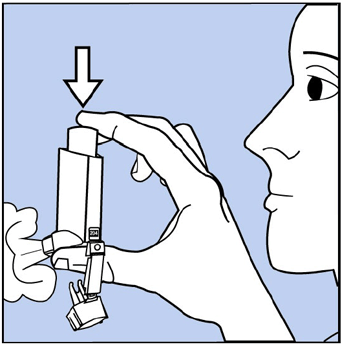
- Ryst og spray inhalatoren sådan 3 gange mere for at afslutte den. Tælleren skulle nu læse 200 eller 60 , alt efter hvilken størrelse inhalator du har. Se figur D.
Figur D 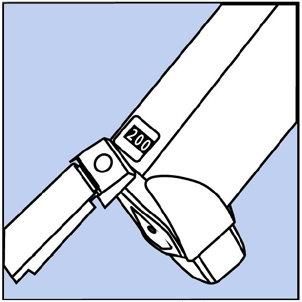
- Du skal prime din inhalator igen, hvis du ikke har brugt den i mere end 14 dage, eller hvis du taber den. Tag hætten af mundstykket og ryst og spray inhalatoren 4 gange i luften væk fra dit ansigt.
Sådan bruger du din VENTOLIN HFA-inhalator
Følg disse trin hver gang du bruger VENTOLIN HFA.
Trin 1. Sørg for, at beholderen sidder godt fast i aktuatoren. Tælleren skal vise gennem vinduet i aktuatoren.
Ryst inhalatoren godt før hver sprøjtning.
Tag hætten af mundstykket på aktuatoren. Kig inde i mundstykket for fremmedlegemer, og tag dem ud, du ser.
Trin 2. Hold inhalatoren med mundstykket nede. Se Figur E .
Figur E 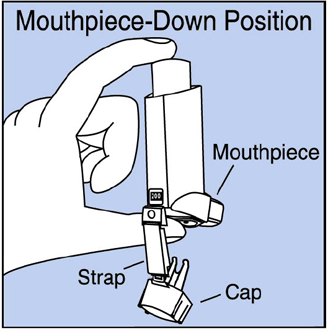
Trin 3. Træk vejret ud gennem munden og skub så meget luft fra lungerne som muligt. Sæt mundstykket i munden og luk læberne omkring det. Se figur F .
Figur F 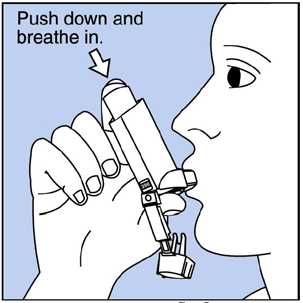
Trin 4. Skub toppen af beholderen helt ned, mens du trækker vejret dybt og langsomt ind gennem munden. Se Figur F .
Trin 5. Når sprayen kommer ud, skal du fjerne fingeren fra beholderen. Når du har trukket vejret hele vejen, skal du tage inhalatoren ud af munden og lukke munden.
Trin 6. Hold vejret i cirka 10 sekunder, eller så længe det er behageligt. Træk vejret lavt ud, så længe du kan.
Hvis din sundhedsplejerske har fortalt os, at du beder mere, vent 1 minut og ryst inhalatoren igen. Gentag trin 2 til trin 6.
Trin 7. Sæt hætten tilbage på mundstykket, hver gang du bruger inhalatoren. Sørg for, at den klikker godt på plads.
Rengøring af din VENTOLIN HFA inhalator
Rengør din inhalator mindst 1 gang om ugen. Du kan muligvis ikke se nogen ophobning af medicin på inhalatoren, men det er vigtigt at holde den ren, så ophobning af medicin ikke blokerer sprayen. Se figur G.
Figur G 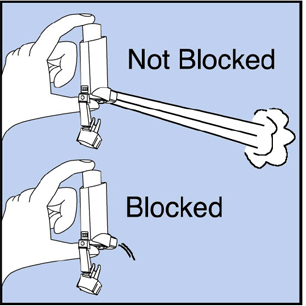
Trin 8. Tag beholderen ud af aktuatoren, og tag hætten af mundstykket. Remmen på hætten forbliver fastgjort til aktuatoren.
Trin 9. Hold aktuatoren under vandhanen og kør varmt vand igennem den i ca. 30 sekunder. Se Figur H.
Figur H 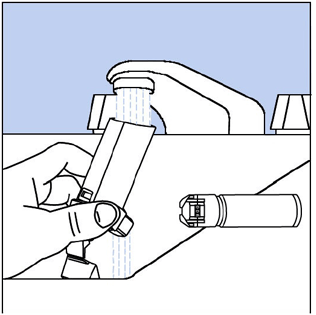
Trin 10. Vend aktuatoren på hovedet og kør varmt vand gennem mundstykket i ca. 30 sekunder. Se Figur I .
Figur I 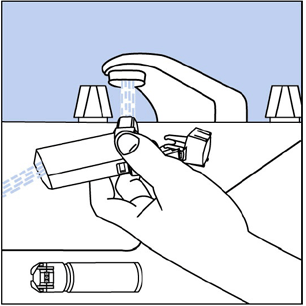
Trin 11. Ryst så meget vand fra aktuatoren som muligt. Kig ind i mundstykket for at sikre dig, at eventuel ophobning af medicin er vasket helt væk. Hvis der er opbygning, gentag trin 9 og 10.
Trin 12. Lad aktuatoren lufttørre natten over. Se figur J.
Figur J 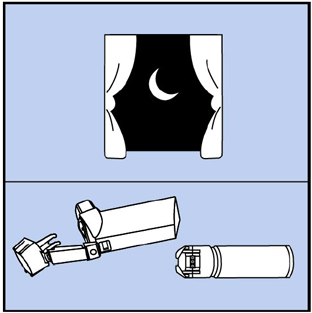
Trin 13. Når aktuatoren er tør, skal du sætte beskyttelseshætten på mundstykket og derefter sætte beholderen i aktuatoren og sørge for, at den sidder godt fast. Ryst inhalatoren godt, fjern hætten, og spray inhalatoren én gang i luften væk fra dit ansigt. (Tælleren tæller ned med 1 tal.) Sæt hætten tilbage på mundstykket.
Hvis du skal bruge din inhalator, før aktuatoren er helt tør:
- Ryst så meget vand af aktuatoren som muligt.
- Sæt hætten på mundstykket og sæt derefter beholderen i aktuatoren og sørg for, at den sidder godt fast.
- Ryst inhalatoren godt og spray den 1 gang i luften væk fra dit ansigt.
- Tag din VENTOLIN HFA dosis som foreskrevet.
- Følg rengøringstrin 8 til 13 ovenfor.
Udskiftning af din VENTOLIN HFA inhalator:
- Når tælleren viser 020, du skal genopfylde din recept eller spørge din læge, hvis du har brug for en anden recept til VENTOLIN HFA.
- Smid inhalatoren væk når tælleren læser 0 eller 12 måneder efter, at du åbnede folieposen, alt efter hvad der kommer først. Du bør ikke blive ved med at bruge inhalatoren, når tælleren viser 000, fordi du ikke får den rigtige mængde medicin.
- Brug ikke inhalatoren efter udløbsdatoen, som står på emballagen, den kommer i.
For korrekt brug af din VENTOLIN HFA inhalator, husk:
- Beholderen skal altid sidde godt fast i aktuatoren.
- Træk vejret dybt og langsomt ind for at sikre, at du får al medicinen.
- Hold vejret i cirka 10 sekunder efter indånding af medicinen. Derefter trække vejret helt ud.
- Opbevar altid beskyttelseshætten på mundstykket, når din inhalator ikke er i brug.
- Opbevar altid din inhalator med mundstykket pegende nedad.
- Rengør din inhalator mindst 1 gang om ugen.
Hvis du har spørgsmål om VENTOLIN HFA eller hvordan du bruger din inhalator, så ring til GlaxoSmithKline (GSK) på 1-888-825-5249 eller besøg www.ventolin.com.
Denne patientinformation og brugsanvisning er godkendt af US Food and Drug Administration.
