Uniphyl 400mg Theophylline Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Uniphyl 400mg, og hvordan bruges det?
Uniphyl er en receptpligtig medicin, der bruges til at behandle symptomer på astma, bronkitis, emfysem og andre vejrtrækningsproblemer (akut bronkospasme). Uniphyl 400mg kan bruges alene eller sammen med anden medicin.
Uniphyl tilhører en klasse af lægemidler kaldet Xanthin-derivater; Phosphodiesterase enzymhæmmere, ikke-selektive.
Det vides ikke, om Uniphyl 400mg er sikkert og effektivt til børn under 1 ½ måned.
Hvad er de mulige bivirkninger af Uniphyl?
Uniphyl kan forårsage alvorlige bivirkninger, herunder:
- nældefeber,
- åndedrætsbesvær,
- hævelse af dit ansigt, læber, tunge eller hals,
- alvorlig eller vedvarende opkastning,
- vedvarende hovedpine,
- søvnbesvær,
- hurtige hjerteslag,
- anfald,
- feber,
- kramper i benene,
- forstoppelse,
- uregelmæssige hjerteslag,
- flagrende i dit bryst,
- øget tørst eller vandladning,
- følelsesløshed eller prikken,
- muskelsvaghed,
- slap følelse,
- øget tørst,
- øget vandladning,
- mundtørhed, og
- frugtig ånde lugt
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Uniphyl omfatter:
- kvalme,
- opkastning,
- diarré,
- hovedpine,
- søvnproblemer (søvnløshed),
- rystelser,
- svedeture,
- rastløshed, og
- irritabilitet
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Uniphyl. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Uniphyl (vandfri theophyllin-tablet) ® (theophyllin, vandfri) Tabletter i et system med kontrolleret frigivelse tillader et 24-timers doseringsinterval for passende patienter.
Theophyllin er strukturelt klassificeret som en methylxanthin. Det forekommer som et hvidt, lugtfrit, krystallinsk pulver med en bitter smag.
Vandfri theophyllin har det kemiske navn 1H-Purine-2,6-dion, 3,7-dihydro-1,3-dimethyl-, og er repræsenteret af følgende strukturformel:
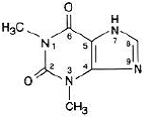
Molekylformlen for vandfri theophyllin er C7H8N4O2 med en molekylvægt på 180,17.
Hver tablet med kontrolleret frigivelse til oral administration indeholder 400 eller 600 mg vandfri theophyllin.
Inaktive ingredienser: cetostearylalkohol, hydroxyethylcellulose, magnesiumstearat, povidon og talkum.
INDIKATIONER
Theophyllin er indiceret til behandling af symptomer og reversibel luftstrømsobstruktion forbundet med kronisk astma og andre kroniske lungesygdomme, f.eks. emfysem og kronisk bronkitis.
DOSERING OG ADMINISTRATION
Uniphyl (vandfri theophyllin tablet) ® 400 eller 600 mg tabletter kan tages en gang dagligt morgen eller aften. Det anbefales, at Uniphyl (vandfri theophyllin-tablet) tages sammen med måltider. Patienter skal informeres om, at hvis de vælger at tage Uniphyl (vandfri theophyllin-tablet) sammen med mad, skal den tages konsekvent med mad, og hvis de tager den i fastende tilstand, skal den rutinemæssigt tages fastende. Det er vigtigt, at produktet, når det doseres, doseres konsekvent med eller uden mad.
Uniphyl (vandfri theophyllin tablet) ® tabletter må ikke tygges eller knuses, da det kan føre til en hurtig frigivelse af theophyllin med risiko for toksicitet. Tabletten med delekærv kan deles. Sjældent kan patienter, der får Uniphyl (vandfri theophyllin-tablet) 400 eller 600 mg tabletter passere en intakt matrix-tablet i afføringen eller via kolostomi. Disse matrixtabletter indeholder normalt kun lidt eller ingen resterende theophyllin.
Stabiliserede patienter på 12 år eller ældre, som tager et teophyllinprodukt med øjeblikkelig frigivelse eller kontrolleret frigivelse, kan overføres til én gang daglig administration af 400 mg eller 600 mg Uniphyl (vandfri theophyllin-tablet) tabletter på en mg-for- mg basis.
Det skal erkendes, at de maksimale og laveste serum-theophyllin-niveauer produceret ved dosering én gang dagligt kan variere fra dem, der blev produceret af det tidligere produkt og/eller regime.
Generelle betragtninger
Den steady-state maksimale serum-theophyllinkoncentration er en funktion af dosis, doseringsintervallet og hastigheden af theophyllinabsorption og -clearance hos den enkelte patient. På grund af markante individuelle forskelle i hastigheden af theophyllin-clearance, varierer den dosis, der kræves for at opnå en maksimal serum-theophyllin-koncentration i intervallet 10-20 mcg/mL, firedobbelt blandt ellers lignende patienter i fravær af faktorer, der vides at ændre theophyllin-clearance (f.eks. 400-1600 mg/dag hos voksne Dosis af theophyllin skal individualiseres på basis af maksimale serum-theophyllin-koncentrationsmålinger for at opnå en dosis, der vil give maksimal potentiel fordel med minimal risiko for bivirkninger.
Forbigående koffeinlignende bivirkninger og for høje serumkoncentrationer i langsomme metabolisatorer kan undgås hos de fleste patienter ved at starte med en tilstrækkelig lav dosis og langsomt øge dosis, hvis det vurderes at være klinisk indiceret, i små trin (Se ). Dosisforøgelser bør kun foretages, hvis den tidligere dosis tolereres godt og med intervaller på ikke mindre end 3 dage for at tillade serum-theophyllinkoncentrationen at nå den nye steady-state. Dosisjustering bør styres af serum-theophyllinkoncentrationsmåling (se FORHOLDSREGLER , Laboratorieprøver og DOSERING OG ADMINISTRATION ). Sundhedsudbydere bør instruere patienter og plejepersonale i at afbryde enhver dosis, der forårsager bivirkninger, at tilbageholde medicinen, indtil disse symptomer er væk og derefter genoptage behandlingen med en lavere, tidligere tolereret dosis (se ADVARSLER ).
Hvis patientens symptomer er godt kontrolleret, er der ingen tilsyneladende bivirkninger og ingen indgribende faktorer, der kan ændre dosiskravene (se ADVARSLER og FORHOLDSREGLER ), bør serumtheophyllinkoncentrationer overvåges med 6 måneders intervaller for hurtigt voksende børn og med årlige intervaller for alle andre. Hos akut syge patienter bør serumkoncentrationen af theophyllin monitoreres med hyppige intervaller, f.eks. hver 24. time.
Theophyllin fordeler sig dårligt i kropsfedt, derfor bør mg/kg dosis beregnes på basis af ideal kropsvægt.
Tabel V indeholder titreringsskema for theophyllin, der anbefales til patienter i forskellige aldersgrupper og kliniske forhold.
Tabel VI indeholder anbefalinger til justering af theophyllin-dosis baseret på serum-theophyllinkoncentrationer. Anvendelse af disse generelle doseringsanbefalinger til individuelle patienter skal tage hensyn til hver enkelt patients unikke kliniske karakteristika. Generelt bør disse anbefalinger tjene som den øvre grænse for dosisjusteringer for at mindske risikoen for potentielt alvorlige bivirkninger forbundet med uventede store stigninger i serumtheophyllinkoncentrationen.
B. Patienter med risikofaktorer for nedsat clearance, ældre (> 60 år) og dem, hos hvem det ikke er muligt at overvåge serumteophyllinkoncentrationer:
Hos børn i alderen 12-15 år bør theophyllin-dosis ikke overstige 16 mg/kg/dag op til et maksimum på 400 mg/dag i nærvær af risikofaktorer for reduceret theophyllin-clearance (se ADVARSLER ) eller hvis det ikke er muligt at overvåge serumtheophyllinkoncentrationer.
Hos unge ≥ 16 år og voksne, inklusive ældre, bør theophyllin-dosis ikke overstige 400 mg/dag i nærvær af risikofaktorer for reduceret theophyllin-clearance (se ADVARSLER ) eller hvis det ikke er muligt at overvåge serumtheophyllinkoncentrationer.
*Patienter med hurtigere metabolisme, klinisk identificeret ved højere dosiskrav end gennemsnittet, bør modtage en mindre dosis hyppigere (hver 12. time) for at forhindre gennembrudssymptomer som følge af lave bundkoncentrationer før næste dosis.
TABEL VI. Dosisjustering styret af serumtheophyllinkoncentrationen.
HVORDAN LEVERET
Uniphyl® (theophyllin, vandfri) tabletter med kontrolleret frigivelse 400 mg leveres i hvide, uigennemsigtige, børnesikrede plastikflasker indeholdende 100 tabletter ( NDC 67781-251-01) eller 500 tabletter ( NDC 67781-251-05). Hver rund, hvid 400 mg tablet bærer symbolet PF på siden med delekærv og U400 på den anden side.
Uniphyl® (theophyllin, vandfri) tabletter med kontrolleret frigivelse 600 mg leveres i hvide, uigennemsigtige, børnesikrede plastikflasker indeholdende 100 tabletter ( NDC 67781-252-01). Hver rektangulær, konkav, hvid 600 mg tablet bærer symbolet PF på siden med delekærv og U 600 på den anden side.
Opbevares ved 25°C (77°F); udflugter tilladt mellem 15°-30°C (59°-86°F).
Dispenser i en tæt, lysbestandig beholder.
Purdue Pharmaceutical Products LP, Dist. af: Purdue Pharmaceutical Products LP, Stamford, CT 06901-3431. 17. marts 2004.
BIVIRKNINGER
Bivirkninger forbundet med theophyllin er generelt milde, når de maksimale serum-theophyllinkoncentrationer er OVERDOSERING ). De forbigående koffeinlignende bivirkninger forekommer hos omkring 50 % af patienterne, når theophyllinbehandling påbegyndes ved doser, der er højere end anbefalede initialdoser (f.eks. > 300 mg/dag hos voksne og > 12 mg/kg/dag hos børn over > 1 år gamle ). Under påbegyndelse af teophyllinbehandling kan koffeinlignende bivirkninger forbigående ændre patientens adfærd, især hos børn i skolealderen, men denne reaktion varer sjældent ved. Påbegyndelse af theophyllinbehandling med en lav dosis med efterfølgende langsom titrering til en forudbestemt aldersrelateret maksimal dosis vil signifikant reducere hyppigheden af disse forbigående bivirkninger (se DOSERING OG ADMINISTRATION ). Hos en lille procentdel af patienterne (
Andre bivirkninger, der er blevet rapporteret ved serum-theophyllinkoncentrationer
TABEL IV. Manifestationer af theophyllin toksicitet. *
DRUGSINTERAKTIONER
Theophyllin interagerer med en bred vifte af lægemidler. Interaktionen kan være farmakodynamisk, dvs. ændringer i den terapeutiske respons på theophyllin eller et andet lægemiddel eller forekomst af bivirkninger uden ændring i serum-theophyllinkoncentrationen. Mere hyppigt er interaktionen imidlertid farmakokinetisk, dvs. hastigheden af theophyllin-clearance ændres af et andet lægemiddel, hvilket resulterer i øgede eller nedsatte serum-theophyllinkoncentrationer. Theophyllin ændrer kun sjældent andre lægemidlers farmakokinetik. Lægemidlerne anført i tabel II har potentiale til at producere klinisk signifikante farmakodynamiske eller farmakokinetiske interaktioner med theophyllin. Oplysningerne i kolonnen "Effekt" i tabel II antager, at det interagerende lægemiddel føjes til et steadystate theophyllin-regime. Hvis theophyllin initieres hos en patient, som allerede tager et lægemiddel, der hæmmer theophyllin-clearance (f.eks. cimetidin, erythromycin), vil den dosis af theophyllin, der kræves for at opnå en terapeutisk serum-theophyllinkoncentration, være mindre. Omvendt, hvis theophyllin påbegyndes hos en patient, som allerede tager et lægemiddel, der øger theophyllin-clearance (f.eks. rifampin), vil den dosis af theophyllin, der kræves for at opnå en terapeutisk serum-theophyllinkoncentration, være større. Seponering af et samtidig lægemiddel, der øger theophyllin-clearance, vil resultere i akkumulering af theophyllin til potentielt toksiske niveauer, medmindre theophyllin-dosis er passende reduceret. Seponering af et samtidig lægemiddel, der hæmmer theophyllin-clearance, vil resultere i nedsatte serum-theophyllin-koncentrationer, medmindre theophyllin-dosis er passende øget. Lægemidlerne anført i tabel III er enten blevet dokumenteret ikke at interagere med theophyllin eller producerer ikke en klinisk signifikant interaktion (dvs.
Listen over lægemidler i tabel II og III er gældende pr. 9. februar 1995. Nye interaktioner rapporteres løbende for theophyllin, især med nye kemiske enheder. Sundhedspersonalet bør ikke antage, at et lægemiddel ikke interagerer med theophyllin, hvis det ikke er anført i tabel II. Før tilføjelse af et nyligt tilgængeligt lægemiddel til en patient, der får theophyllin, bør indlægssedlen til det nye lægemiddel og/eller den medicinske litteratur konsulteres for at afgøre, om der er rapporteret en interaktion mellem det nye lægemiddel og theophyllin.
TABEL II. Klinisk signifikante lægemiddelinteraktioner med theophyllin.*
TABEL III. Lægemidler, der er dokumenteret ikke at interagere med theophyllin, eller lægemidler, der ikke producerer nogen klinisk signifikant interaktion med theophyllin. *
Lægemiddel-fødevareinteraktioner
Biotilgængeligheden af Uniphyl®-tabletter (theophyllin, vandfri) er blevet undersøgt ved samtidig administration af mad. I tre enkeltdosisundersøgelser blev forsøgspersoner, der fik Uniphyl (vandfri theophyllin-tablet) 400 mg eller 600 mg tabletter sammen med et standardiseret måltid med højt fedtindhold, sammenlignet med fastende tilstande. Under fodrede betingelser blev den maksimale plasmakoncentration og biotilgængelighed øget; en brat stigning i hastigheden og omfanget af absorption var dog ikke tydelig (se Farmakokinetik, Absorption ). Den øgede top og omfang af absorption under fodrede forhold tyder på, at doseringen ideelt set bør administreres konsekvent enten med eller uden mad.
Effekten af andre lægemidler på teophyllinserumkoncentrationsmålinger
De fleste serum-theophyllin-assays i klinisk brug er immunoassays, som er specifikke for theophyllin. Andre xanthiner såsom koffein, dyphyllin og pentoxifyllin påvises ikke af disse assays. Nogle lægemidler (f.eks. cefazolin, cephalothin) kan dog interferere med visse HPLC-teknikker. Koffein- og xanthinmetabolitter hos nyfødte eller patienter med nyreinsufficiens kan forårsage, at aflæsningen fra nogle tørre reagenskontormetoder er højere end den faktiske serumtheophyllinkoncentration.
ADVARSLER
Samtidig sygdom
Theophyllin bør anvendes med ekstrem forsigtighed til patienter med følgende kliniske tilstande på grund af den øgede risiko for forværring af den samtidige tilstand:
Aktiv mavesår sygdom Anfaldslidelser Hjertearytmier (ikke inklusive bradyarytmier)
Tilstande, der reducerer theophyllin-clearance
Der er flere let identificerbare årsager til reduceret theophyllin-clearance. Hvis den samlede daglige dosis ikke er passende reduceret i nærvær af disse risikofaktorer, kan der opstå alvorlig og potentielt dødelig theophyllintoksicitet. Der skal tages nøje hensyn til fordele og risici ved brug af theophyllin og behovet for mere intensiv overvågning af serum-theophyllinkoncentrationer hos patienter med følgende risikofaktorer:
Alder
Nyfødte (termature og for tidligt fødte) Børn 60 år)
Samtidige Sygdomme
Akut lungeødem Kongestiv hjertesvigt Cor-pulmonale Feber; ≥ 102° i 24 timer eller mere; eller mindre temperaturstigninger i længere perioder Hypothyroidisme Leversygdom; skrumpelever, akut hepatitis Nedsat nyrefunktion hos spædbørn
Rygestop
Lægemiddelinteraktioner
Tilføjelse af et lægemiddel, der hæmmer theophyllinmetabolismen (f.eks. cimetidin, erythromycin, tacrin) eller standsning af et samtidigt administreret lægemiddel, der øger theophyllinmetabolismen (f.eks. carbamazepin, rifampin). (Se SIKKERHEDSFORANSTALTNINGER: LÆKEMIDDELINTERAKTIONER , ).
Når tegn eller symptomer på teophyllin toksicitet er til stede
Når en patient, der får theophyllin, udvikler kvalme eller opkastning, især gentagne opkastninger, eller andre tegn eller symptomer, der stemmer overens med theophyllin-toksicitet (selvom der kan være mistanke om en anden årsag), skal yderligere doser af theophyllin tilbageholdes, og en serum-theophyllinkoncentration måles øjeblikkeligt. Patienter skal instrueres i ikke at fortsætte med nogen dosis, der forårsager bivirkninger, og at tilbageholde efterfølgende doser, indtil symptomerne er forsvundet, på hvilket tidspunkt sundhedspersonalet kan instruere patienten om at genoptage lægemidlet ved en lavere dosis (se DOSERING OG ADMINISTRATION , Doseringsvejledning, tabel VI ).
Dosis stiger
Forøgelser i dosis af theophyllin bør ikke foretages som reaktion på en akut forværring af symptomer på kronisk lungesygdom, da theophyllin giver ringe ekstra fordel for inhalerede beta2-selektive agonister og systemisk administrerede kortikosteroider i denne situation og øger risikoen for bivirkninger. En maksimal steady-state serum-theophyllinkoncentration bør måles, før dosis øges som reaktion på vedvarende kroniske symptomer for at fastslå, om en dosisstigning er sikker. Inden teophyllin-dosis øges på grundlag af en lav serumkoncentration, bør sundhedspersonalet overveje, om blodprøven blev taget på et passende tidspunkt i forhold til dosis, og om patienten har overholdt det foreskrevne regime (se FORHOLDSREGLER , Laboratorieprøver ).
Da hastigheden af theophyllin-clearance kan være dosisafhængig (dvs. steady-state serumkoncentrationer kan stige uforholdsmæssigt med stigningen i dosis), bør en stigning i dosis baseret på en subterapeutisk serumkoncentrationsmåling være konservativ. Generelt vil en begrænsning af dosisstigninger til ca. 25 % af den foregående totale daglige dosis reducere risikoen for utilsigtede overdreven stigninger i serumtheophyllinkoncentrationen (se DOSERING OG ADMINISTRATION , ).
FORHOLDSREGLER
Generel
Omhyggelig overvejelse af de forskellige interagerende lægemidler og fysiologiske tilstande, der kan ændre theophyllin-clearance og kræver dosisjustering, bør ske før påbegyndelse af theophyllin-behandling, før stigninger i theophyllin-dosis og under opfølgning (se ADVARSLER ). Den dosis af theophyllin, der vælges til påbegyndelse af behandlingen, bør være lav og, hvis den tolereres, øges langsomt over en periode på en uge eller længere med den endelige dosis styret af overvågning af serum-theophyllinkoncentrationer og patientens kliniske respons (se DOSERING OG ADMINISTRATION , ).
Overvågning af serum-theophyllinkoncentrationer
Serum-theophyllinkoncentrationsmålinger er let tilgængelige og bør bruges til at bestemme, om doseringen er passende. Specifikt skal serumtheophyllinkoncentrationen måles som følger:
For at vejlede en dosisforøgelse bør blodprøven tages på tidspunktet for den forventede maksimale serumtheophyllinkoncentration; 12 timer efter en aftendosis eller 9 timer efter en morgendosis ved steady-state. For de fleste patienter vil steady-state blive nået efter 3 dages dosering, når ingen doser er blevet glemt, ingen ekstra doser er blevet tilføjet, og ingen af doserne er blevet taget med ulige intervaller. En laveste koncentration (dvs. ved slutningen af doseringsintervallet) giver ingen yderligere nyttig information og kan føre til en uhensigtsmæssig dosisstigning, da den maksimale serum-theophyllinkoncentration kan være to eller flere gange større end bundkoncentrationen med en formulering med øjeblikkelig frigivelse . Hvis serumprøven udtages mere end 12 timer efter aftendosis, eller mere end 9 timer efter en morgendosis, skal resultaterne fortolkes med forsigtighed, da koncentrationen muligvis ikke afspejler topkoncentrationen. I modsætning hertil, når der er tegn eller symptomer på theophyllintoksicitet, skal der tages en serumprøve så hurtigt som muligt, analyseres straks, og resultatet rapporteres til sundhedspersonalet uden forsinkelse. Hos patienter, hvor der er mistanke om nedsat serumproteinbinding (f.eks. cirrose, kvinder i tredje trimester af graviditeten), bør koncentrationen af ubundet theophyllin måles, og dosis justeres for at opnå en ubundet koncentration på 6-12 mcg/ml. Spytkoncentrationer af theophyllin kan ikke bruges pålideligt til at justere dosis uden særlige teknikker.
Effekter på laboratorietests
Som et resultat af dets farmakologiske virkninger øger theophyllin i serumkoncentrationer inden for intervallet 10-20 mcg/mL beskedent plasmaglucose (fra et gennemsnit på 88 mg% til 98 mg%), urinsyre (fra et gennemsnit på 4 mg/dL) til 6 mg/dL), frie fedtsyrer (fra et gennemsnit på 451 μEq/L til 800 μEq/L, total kolesterol (fra et gennemsnit på 140 vs 160 mg/dL), HDL (fra et gennemsnit på 36 til 50 mg /dL), HDL/LDL-forhold (fra et gennemsnit på 0,5 til 0,7) og urinfri kortisoludskillelse (fra et gennemsnit på 44 til 63 mcg/24 timer) Theophyllin i serumkoncentrationer inden for 10-20 mcg/ml området kan også forbigående sænke serumkoncentrationer af triiodothyronin (144 før, 131 efter en uge og 142 ng/dL efter 4 uger med theophyllin) Den kliniske betydning af disse ændringer bør afvejes i forhold til den potentielle terapeutiske fordel ved theophyllin hos individuelle patienter.
Karcinogenese, mutagenese og svækkelse af fertilitet
Langtids carcinogenicitetsundersøgelser er blevet udført på mus (orale doser 30-150 mg/kg) og rotter (orale doser 5-75 mg/kg). Resultater afventer.
Theophyllin er blevet undersøgt i Ames salmonella, in vivo og in vitro cytogenetik, mikronucleus og kinesisk hamster ovarie testsystemer og har ikke vist sig at være genotoksisk.
en 14 ugers kontinuerlig avlsundersøgelse svækkede theophyllin administreret til parrende par af B6C3F1-mus i orale doser på 120, 270 og 500 mg/kg (ca. 1,0-3,0 gange den humane dosis på mg/m²-basis) fertiliteten, som det fremgår af fald i antallet af levende unger pr. kuld, fald i det gennemsnitlige antal kuld pr. fertile par, og stigninger i drægtighedsperioden ved den høje dosis samt fald i andelen af unger født i live ved mellem- og højdosis. I 13 ugers toksicitetsundersøgelser blev theophyllin administreret til F344-rotter og B6C3F1-mus i orale doser på 40-300 mg/kg (ca. 2,0 gange den humane dosis på mg/m²-basis). Ved den høje dosis blev der observeret systemisk toksicitet hos begge arter, herunder fald i testikelvægt.
Graviditet
Teratogene virkninger: Kategori C
I undersøgelser, hvor gravide mus, rotter og kaniner blev doseret i løbet af organogeneseperioden, frembragte theophyllin teratogene virkninger.
undersøgelser med mus frembragte en enkelt intraperitoneal dosis på og over 100 mg/kg (ca. lig den maksimalt anbefalede orale dosis til voksne på mg/m²-basis) under organogenese ganespalte og digitale abnormiteter. Mikromeli, mikrognathia, klumpfod, subkutant hæmatom, åbne øjenlåg og embryodødelighed blev observeret ved doser, der er ca. 2 gange den maksimalt anbefalede orale dosis til voksne på mg/m²-basis.
et studie med rotter doseret fra undfangelse til organogenese frembragte en oral dosis på 150 mg/kg/dag (ca. 2 gange den maksimalt anbefalede orale dosis til voksne på mg/m²-basis) digitale abnormiteter. Embryoletalitet blev observeret med en subkutan dosis på 200 mg/kg/dag (ca. 4 gange den maksimalt anbefalede orale dosis til voksne på mg/m²-basis). I en undersøgelse, hvor drægtige kaniner blev doseret gennem hele organogenesen, forårsagede en intravenøs dosis på 60 mg/kg/dag (ca. 2 gange den maksimale anbefalede orale dosis til voksne på mg/m²-basis), som forårsagede døden af én dåe og klinisk tegn hos andre, producerede ganespalte og var embryoletal. Doser på og over 15 mg/kg/dag (mindre end den maksimalt anbefalede orale dosis til voksne på mg/m²-basis) øgede forekomsten af skeletvariationer.
Der er ingen tilstrækkelige og velkontrollerede undersøgelser af gravide kvinder. Theophyllin bør kun anvendes under graviditet, hvis den potentielle fordel opvejer den potentielle risiko for fosteret.
Ammende mødre
Theophyllin udskilles i modermælken og kan forårsage irritabilitet eller andre tegn på mild toksicitet hos ammende menneskelige spædbørn. Koncentrationen af theophyllin i modermælk svarer omtrent til moderens serumkoncentration. Et spædbarn, der indtager en liter modermælk indeholdende 10-20 mcg/mL theophyllin om dagen, vil sandsynligvis modtage 10-20 mg theophyllin om dagen. Alvorlige bivirkninger hos spædbarnet er usandsynlige, medmindre moderen har toksiske serumtheophyllinkoncentrationer.
Pædiatrisk brug
Theophyllin er sikkert og effektivt til de godkendte indikationer hos pædiatriske patienter. Vedligeholdelsesdosis af theophyllin skal vælges med forsigtighed hos pædiatriske patienter, da hastigheden af theophyllin-clearance er meget variabel på tværs af det pædiatriske aldersinterval (se KLINISK FARMAKOLOGI , , ADVARSLER , og DOSERING OG ADMINISTRATION , ).
Geriatrisk brug
Ældre patienter har en signifikant større risiko for at opleve alvorlig toksicitet fra theophyllin end yngre patienter på grund af farmakokinetiske og farmakodynamiske ændringer forbundet med aldring. Clearance af theophyllin er i gennemsnit reduceret med 30 % hos raske ældre voksne (> 60 år) sammenlignet med raske unge voksne. Theophyllin-clearance kan reduceres yderligere af samtidige sygdomme, der er fremherskende hos ældre, som yderligere forringer clearance af dette lægemiddel og har potentiale til at øge serumniveauer og potentiel toksicitet. Disse tilstande omfatter nedsat nyrefunktion, kronisk obstruktiv lungesygdom, kongestiv hjertesvigt, leversygdom og en øget forekomst af brug af visse lægemidler (se FORHOLDSREGLER : DRUGSINTERAKTIONER ) med potentiale for farmakokinetisk og farmakodynamisk interaktion. Proteinbinding kan være nedsat hos ældre, hvilket resulterer i en øget andel af den totale serum-theophyllinkoncentration i den farmakologisk aktive ubundne form. Ældre patienter synes også at være mere følsomme over for de toksiske virkninger af theophyllin efter kronisk overdosering end yngre patienter. Omhyggelig opmærksomhed på dosisreduktion og hyppig monitorering af serumtheophyllinkoncentrationer er påkrævet hos ældre patienter (se FORHOLDSREGLER , Overvågning af serum-theophyllinkoncentrationer , og DOSERING OG ADMINISTRATION ).
Den maksimale daglige dosis af theophyllin hos patienter over 60 år bør normalt ikke overstige 400 mg/dag, medmindre patienten fortsætter med at være symptomatisk, og den maksimale steady-state serum-theophyllinkoncentration er DOSERING OG ADMINISTRATION ). Theophyllin doser større end 400 mg/d bør ordineres med forsigtighed til ældre patienter.
OVERDOSIS
Generel
Kroniciteten og mønsteret af overdosering af theophyllin har signifikant indflydelse på kliniske manifestationer af toksicitet, behandling og resultat. Der er to almindelige præsentationer: (1) akut overdosis, dvs. indtagelse af en enkelt stor overdosis (> 10 mg/kg), som forekommer i forbindelse med et selvmordsforsøg eller isoleret medicineringsfejl, og (2) kronisk overdosering, dvs. indtagelse af gentagne doser, der er for høje i forhold til patientens hastighed af theophyllin-clearance. De mest almindelige årsager til kronisk overdosering af theophyllin omfatter patientens eller omsorgspersonens fejl i doseringen, ordinering af en for høj dosis eller en normal dosis af sundhedspersonale i nærværelse af faktorer, der vides at reducere hastigheden af theophyllin-clearance, og øgning af dosis som reaktion på en eksacerbation af symptomer uden først at måle serumtheophyllinkoncentrationen for at afgøre, om en dosisforøgelse er sikker.
Alvorlig toksicitet fra overdosis af theophyllin er en relativt sjælden hændelse. I en sundhedsplejeorganisation var hyppigheden af hospitalsindlæggelser for kronisk overdosering af theophyllin omkring 1 pr. 1000 personår eksponering. I en anden undersøgelse, blandt 6000 blodprøver opnået til måling af serum-theophyllinkoncentrationen, uanset årsag, fra patienter behandlet på en akutafdeling, var 7 % i området 20-30 mcg/ml, og 3 % var > 30 mcg/ml. Omtrent to tredjedele af patienterne med serumtheophyllinkoncentrationer i intervallet 20-30 mcg/ml havde en eller flere manifestationer af toksicitet, mens > 90 % af patienterne med serumtheophyllinkoncentrationer > 30 mcg/ml var klinisk berusede. Tilsvarende ses alvorlig toksicitet fra theophyllin i andre rapporter primært ved serumkoncentrationer > 30 mcg/ml.
Adskillige undersøgelser har beskrevet de kliniske manifestationer af overdosis af theophyllin og forsøgt at bestemme de faktorer, der forudsiger livstruende toksicitet. Generelt er patienter, der oplever en akut overdosis, mindre tilbøjelige til at opleve anfald end patienter, der har oplevet en kronisk overdosering, medmindre den maksimale serum-theophyllinkoncentration er > 100 mcg/ml. Efter en kronisk overdosering kan generaliserede anfald, livstruende hjertearytmier og død forekomme ved serumtheophyllinkoncentrationer > 30 mcg/ml. Sværhedsgraden af toksicitet efter kronisk overdosering er stærkere korreleret med patientens alder end den maksimale serumtheophyllinkoncentration; patienter > 60 år har den største risiko for alvorlig toksicitet og dødelighed efter en kronisk overdosering. Eksisterende eller samtidig sygdom kan også signifikant øge en patients modtagelighed for en bestemt toksisk manifestation, f.eks. har patienter med neurologiske lidelser en øget risiko for anfald, og patienter med hjertesygdom har en øget risiko for hjertearytmier for en given serum-theophyllinkoncentration sammenlignet med til patienter uden den underliggende sygdom.
Hyppigheden af forskellige rapporterede manifestationer af overdosering af theophyllin i henhold til overdoseringsmåden er anført i tabel IV. Andre manifestationer af theophyllintoksicitet omfatter stigninger i serumcalcium, kreatinkinase, myoglobin og leukocyttal, fald i serumphosphat og magnesium, akut myokardieinfarkt og urinretention hos mænd med obstruktiv uropati. Anfald forbundet med serumtheophyllinkoncentrationer > 30 mcg/ml er ofte resistente over for antikonvulsiv behandling og kan resultere i irreversibel hjerneskade, hvis den ikke kontrolleres hurtigt. Død som følge af theophyllintoksicitet er oftest sekundær til kardiorespiratorisk standsning og/eller hypoxisk encefalopati efter langvarige generaliserede anfald eller intraktable hjertearytmier, der forårsager hæmodynamisk kompromittering.
Overdosishåndtering
Generelle anbefalinger til patienter med symptomer på overdosering af teophyllin eller serum-theophyllinkoncentrationer > 30 mcg/ml (Bemærk: Serum-theophyllinkoncentrationer kan fortsætte med at stige efter fremlæggelse af patienten til lægebehandling).
Mens du samtidig påbegynder behandling, skal du kontakte et regionalt giftcenter for at få opdateret information og råd om individualisering af de anbefalinger, der følger.
Institut for understøttende pleje, herunder etablering af intravenøs adgang, vedligeholdelse af luftvejene og elektrokardiografisk overvågning.
Behandling af anfald
På grund af den høje morbiditet og dødelighed forbundet med theophyllin-inducerede anfald, bør behandlingen være hurtig og aggressiv. Antikonvulsiv behandling bør påbegyndes med et intravenøst benzodiazepin, f.eks. diazepam, i intervaller på 0,1-0,2 mg/kg hvert 1.-3. minut, indtil anfaldene er afsluttet. Gentagne anfald bør behandles med en startdosis phenobarbital (20 mg/kg infunderet over 30-60 minutter). Caserapporter om overdosering af theophyllin hos mennesker og dyreforsøg tyder på, at phenytoin er ineffektivt til at afslutte theophyllin-inducerede anfald. De doser af benzodiazepiner og phenobarbital, der kræves for at afslutte theophyllin-inducerede anfald, er tæt på de doser, der kan forårsage alvorlig respirationsdepression eller respirationsstop; sundhedspersonalet bør derfor være forberedt på at sørge for assisteret ventilation. Ældre patienter og patienter med KOL kan være mere modtagelige for de respiratoriske depressive virkninger af antikonvulsiva. Barbituratinduceret koma eller administration af generel anæstesi kan være påkrævet for at afslutte gentagne anfald eller status epilepticus. Generel anæstesi bør anvendes med forsigtighed hos patienter med overdosering af theophyllin, fordi fluorholdige flygtige anæstetika kan sensibilisere myokardiet over for endogene katekolaminer frigivet af theophyllin. Enfluran ser ud til at være mindre tilbøjelig til at være forbundet med denne effekt end halothan og kan derfor være sikrere. Neuromuskulære blokerende midler alene bør ikke anvendes til at afslutte anfald, da de fjerner muskuloskeletale manifestationer uden at stoppe anfaldsaktiviteten i hjernen.
Forudse behovet for antikonvulsiva
Hos patienter med overdosering af theophyllin, som har høj risiko for theophyllin-inducerede anfald, f.eks. patienter med akutte overdoser og serumtheophyllinkoncentrationer > 100 mcg/mL eller kronisk overdosering hos patienter > 60 år med serumtheophyllinkoncentrationer > 30 mcg/mL , bør behovet for antikonvulsiv behandling forventes. Et benzodiazepin, såsom diazepam, skal trækkes i en sprøjte og opbevares ved patientens seng, og medicinsk personale, der er kvalificeret til at behandle anfald, skal være umiddelbart tilgængeligt. Hos udvalgte patienter med høj risiko for theophyllin-inducerede anfald bør administration af profylaktisk antikonvulsiv behandling overvejes. Situationer, hvor profylaktisk antikonvulsiv behandling bør overvejes hos højrisikopatienter, omfatter forventede forsinkelser i iværksættelse af metoder til ekstrakorporal fjernelse af theophyllin (f.eks. overførsel af en højrisikopatient fra en sundhedsfacilitet til en anden for ekstrakorporal fjernelse) og kliniske omstændigheder, der væsentligt interfererer med indsatsen. at øge theophyllin-clearance (f.eks. et nyfødt barn, hvor dialyse muligvis ikke er teknisk mulig, eller en patient med opkastning, der ikke reagerer på antiemetika, som ikke er i stand til at tolerere multiple doser oralt aktivt kul). I dyreforsøg har profylaktisk administration af phenobarbital, men ikke phenytoin, vist sig at forsinke starten af theophyllin-inducerede generaliserede anfald og øge den dosis af theophyllin, der kræves for at inducere anfald (dvs. øger LD50 markant). Selvom der ikke er nogen kontrollerede undersøgelser på mennesker, kan en startdosis af intravenøs phenobarbital (20 mg/kg infunderet over 60 minutter) forsinke eller forhindre livstruende anfald hos højrisikopatienter, mens bestræbelserne på at øge theophyllin-clearance fortsættes. Phenobarbital kan forårsage respirationsdepression, især hos ældre patienter og patienter med KOL.
Behandling af hjertearytmier
Sinustakykardi og simple ventrikulære præmature slag er ikke tegn på livstruende arytmier, de kræver ikke behandling i fravær af hæmodynamisk kompromittering, og de forsvinder med faldende serumtheophyllinkoncentrationer. Andre arytmier, især dem, der er forbundet med hæmodynamisk kompromittering, bør behandles med antiarytmisk behandling, der passer til typen af arytmi.
Gastrointestinal dekontaminering
Oralt aktivt kul (0,5 g/kg op til 20 g og gentag mindst en gang 1-2 timer efter den første dosis) er ekstremt effektivt til at blokere absorptionen af theophyllin i hele mave-tarmkanalen, selv når det administreres flere timer efter indtagelse. Hvis patienten kaster op, skal kullet indgives gennem en nasogastrisk sonde eller efter administration af et antiemetikum. Fenothiazin-antiemetika såsom prochlorperazin eller perphenazin bør undgås, da de kan sænke anfaldstærsklen og ofte forårsage dystoniske reaktioner. En enkelt dosis sorbitol kan anvendes til at fremme afføring for at lette fjernelse af theophyllin bundet til trækul fra mave-tarmkanalen. Sorbitol bør dog doseres med forsigtighed, da det er et potent afrensningsmiddel, som kan forårsage dybe væske- og elektrolytabnormiteter, især efter flere doser. Kommercielt tilgængelige faste kombinationer af flydende kul og sorbitol bør undgås hos små børn og efter den første dosis hos unge og voksne, da de ikke giver mulighed for individualisering af kul- og sorbitoldosering. Ipecac-sirup bør undgås ved overdosering af theophyllin. Selvom ipecac inducerer emesis, reducerer det ikke absorptionen af theophyllin, medmindre det administreres inden for 5 minutter efter indtagelse, og selv da er det mindre effektivt end oralt aktivt kul. Desuden kan ipecac-induceret emesis vare ved i flere timer efter en enkelt dosis og reducere retentionen og effektiviteten af oralt aktivt kul betydeligt.
Serum Theophy linie
Koncentrationsmonitorering Serumtheophyllinkoncentrationen skal måles umiddelbart efter præsentationen, 2-4 timer senere, og derefter med tilstrækkelige intervaller, f.eks. hver 4. time, for at vejlede behandlingsbeslutninger og for at vurdere behandlingens effektivitet. Serumtheophyllinkoncentrationer kan fortsætte med at stige efter fremlæggelse af patienten til lægebehandling som følge af fortsat absorption af theophyllin fra mave-tarmkanalen. Seriel monitorering af serumtheophyllinserumkoncentrationer bør fortsættes, indtil det er klart, at koncentrationen ikke længere stiger og er vendt tilbage til ikke-toksiske niveauer.
Generel overvågning
Procedurer Elektrokardiografisk monitorering bør påbegyndes ved præsentation og fortsættes, indtil serumtheophyllinniveauet er vendt tilbage til et ikke-toksisk niveau. Serumelektrolytter og glukose skal måles ved præsentation og med passende intervaller angivet af kliniske omstændigheder. Væske- og elektrolytabnormiteter skal straks korrigeres. Monitorering og behandling bør fortsættes, indtil serumkoncentrationen falder til under 20 mcg/ml.
Forbedre clearance af theophyllin
Multipel-dosis oralt aktivt kul (f.eks. 0,5 mg/kg op til 20 g, hver anden time) øger clearance af theophyllin mindst det dobbelte ved adsorption af theophyllin udskilt i gastrointestinale væsker. Trækul skal tilbageholdes i og passere gennem mave-tarmkanalen for at være effektivt; emesis bør derfor kontrolleres ved administration af passende antiemetika. Alternativt kan kullet administreres kontinuerligt gennem en nasogastrisk sonde i forbindelse med passende antiemetika. En enkelt dosis sorbitol kan indgives med det aktiverede kul for at fremme afføring for at lette clearance af den adsorberede theophyllin fra mave-tarmkanalen. Sorbitol alene øger ikke clearance af theophyllin og bør doseres med forsigtighed for at forhindre overdreven afføring, som kan resultere i alvorlig væske- og elektrolyt-ubalance. Kommercielt tilgængelige faste kombinationer af flydende kul og sorbitol bør undgås hos små børn og efter den første dosis hos unge og voksne, da de ikke giver mulighed for individualisering af kul- og sorbitoldosering. Hos patienter med vanskelige opkastninger bør ekstrakorporale metoder til fjernelse af theophyllin iværksættes (se OVERDOSERING , Ekstrakorporal fjernelse ).
Specifikke anbefalinger
Akut overdosis
Kronisk overdosering
Ekstrakorporal fjernelse
Forøgelse af hastigheden af theophyllin-clearance med ekstrakorporale metoder kan hurtigt reducere serumkoncentrationerne, men risikoen ved proceduren skal afvejes mod den potentielle fordel. Trækulshæmoperfusion er den mest effektive metode til ekstrakorporal fjernelse, der øger theophyllinclearance op til seks gange, men alvorlige komplikationer, herunder hypotension, hypocalcæmi, blodpladeforbrug og blødende diateser kan forekomme. Hæmodialyse er omtrent lige så effektiv som multiple doser oralt aktivt kul og har en lavere risiko for alvorlige komplikationer end trækulshæmoperfusion. Hæmodialyse bør overvejes som et alternativ, når trækulshæmoperfusion ikke er mulig, og flerdosis oralt trækul er ineffektivt på grund af vanskelig opkastning. Serumtheophyllinkoncentrationer kan vende tilbage med 5-10 mcg/ml efter seponering af kulhæmoperfusion eller hæmodialyse på grund af omfordeling af theophyllin fra vævsrummet. Peritonealdialyse er ineffektiv til fjernelse af theophyllin; udvekslingstransfusioner hos nyfødte har været minimalt effektive.
KONTRAINDIKATIONER
Uniphyl (vandfri theophyllin tablet) ® er kontraindiceret til patienter med en historie med overfølsomhed over for theophyllin eller andre komponenter i produktet.
KLINISK FARMAKOLOGI
Virkningsmekanisme
Theophyllin har to forskellige virkninger i luftvejene hos patienter med reversibel obstruktion; afslapning af glatte muskler (dvs. bronkodilatation) og undertrykkelse af luftvejenes reaktion på stimuli (dvs. ikke-bronkodilaterende profylaktiske virkninger). Selvom virkningsmekanismerne for theophyllin ikke kendes med sikkerhed, tyder dyreforsøg på, at bronkodilatation medieres af hæmning af to isozymer af phosphodiesterase (PDE III og i mindre grad PDE IV), mens ikke-bronkodilaterende profylaktiske virkninger sandsynligvis er medieret gennem en eller flere forskellige molekylære mekanismer, som ikke involverer hæmning af PDE III eller antagonisme af adenosinreceptorer. Nogle af de negative virkninger forbundet med theophyllin synes at være medieret af hæmning af PDE III (f.eks. hypotension, takykardi, hovedpine og emesis) og adenosinreceptorantagonisme (f.eks. ændringer i cerebral blodgennemstrømning).
Theophyllin øger sammentrækningskraften af diaphragmatiske muskler. Denne handling synes at skyldes forøgelse af calciumoptagelse gennem en adenosin-medieret kanal.
Serum koncentration-effekt forhold
Bronkodilatation forekommer over serumtheophyllinkoncentrationsområdet på 5-20 mcg/ml. Klinisk vigtig forbedring af symptomkontrol har i de fleste undersøgelser vist sig at kræve maksimale serum-theophyllinkoncentrationer > 10 mcg/ml, men patienter med mild sygdom kan have gavn af lavere koncentrationer. Ved serumtheophyllinkoncentrationer > 20 mcg/ml øges både hyppigheden og sværhedsgraden af bivirkninger. Generelt vil opretholdelse af maksimale serum-theophyllinkoncentrationer mellem 10 og 15 mcg/ml opnå det meste af lægemidlets potentielle terapeutiske fordel, samtidig med at risikoen for alvorlige bivirkninger minimeres.
Farmakokinetik
Oversigt
Theophyllin absorberes hurtigt og fuldstændigt efter oral administration i opløsning eller fast oral dosisform med øjeblikkelig frigivelse. Theophyllin gennemgår ikke nogen nævneværdig præ-systemisk eliminering, distribueres frit til fedtfrit væv og metaboliseres i vid udstrækning i leveren.
Theophyllins farmakokinetik varierer meget blandt lignende patienter og kan ikke forudsiges af alder, køn, kropsvægt eller andre demografiske karakteristika. Derudover kan visse samtidige sygdomme og ændringer i normal fysiologi (se tabel I) og samtidig administration af andre lægemidler (se tabel II) signifikant ændre theophyllins farmakokinetiske egenskaber. Variabilitet i metabolisme inden for individet er også blevet rapporteret i nogle undersøgelser, især hos akut syge patienter. Det anbefales derfor, at serumtheophyllinkoncentrationer måles hyppigt hos akut syge patienter (f.eks. med 24-timers intervaller) og periodisk hos patienter, der modtager langtidsbehandling, f.eks. med 6-12 måneders intervaller. Hyppigere målinger bør foretages ved tilstedeværelse af enhver tilstand, der væsentligt kan ændre theophyllin-clearance (se FORHOLDSREGLER, Laboratorieundersøgelser ).
TABEL I. Gennemsnit og rækkevidde af total kropsclearance og halveringstid for theophyllin relateret til alder og ændrede fysiologiske tilstande.¶
Bemærk: Ud over de faktorer, der er anført ovenfor, øges theophyllin-clearance og halveringstiden formindskes af diæter med lavt kulhydrat/højt proteinindhold, parenteral ernæring og dagligt forbrug af kulstegt oksekød. En diæt med højt kulhydrat/lavt proteinindhold kan mindske clearance og forlænge halveringstiden for theophyllin.
Absorption
Uniphyl (vandfri theophyllin tablet) ® administreret i fødetilstand absorberes fuldstændigt efter oral administration.
en enkeltdosis crossover-undersøgelse blev to 400 mg Uniphyl (vandfri theophyllin-tablet) administreret til 19 normale frivillige om morgenen eller aftenen umiddelbart efter det samme standardiserede måltid (769 kalorier bestående af 97 gram kulhydrater, 33 gram protein og 27 gram fed). Der var ingen beviser for dosisdumping, og der var heller ingen signifikante forskelle i farmakokinetiske parametre, der kan tilskrives tidspunktet for lægemiddeladministration. På morgenarmen var de farmakokinetiske parametre AUC = 241,9 ± 83,0 mcg time/mL, Cmax = 9,3 ± 2,0 mcg/ml, Tmax = 12,8 ± 4,2 timer. På aftenarmen var de farmakokinetiske parametre AUC = 219,7 ± 83,0 mcg time/mL, Cmax = 9,2 ± 2,0 mcg/ml, Tmax = 12,5 ± 4,2 timer.
En undersøgelse, hvor Uniphyl (vandfri theophyllin-tablet) 400 mg-tabletter blev administreret til 17 fodrede voksne astmatikere, frembragte lignende kurver for theophyllin-niveau-tid, når det blev administreret om morgenen eller aftenen. Serumniveauer var generelt højere i aftenkuren, men der var ingen statistisk signifikante forskelle mellem de to regimer.
En enkeltdosisundersøgelse med 15 normale fastende mandlige frivillige, hvis theophyllin iboende gennemsnitlige eliminationshalveringstid blev verificeret med et flydende theophyllinprodukt til at være 6,9 ± 2,5 (SD) timer, fik to eller tre 400 mg Uniphyl (vandfri theophyllin tablet) ® tabletter . Den relative biotilgængelighed af Uniphyl (vandfri theophyllin-tablet) givet i fastende tilstand sammenlignet med et produkt med øjeblikkelig frigivelse var 59 %. Maksimale serumtheophyllinniveauer forekom efter 6,9 ± 5,2 (SD) timer, med et normaliseret (til 800 mg) peakniveau på 6,2 ± 2,1 (SD). Den tilsyneladende eliminationshalveringstid for 400 mg Uniphyl (vandfri theophyllin-tablet) var 17,2 ± 5,8 (SD) timer.
Steady-state farmakokinetik blev bestemt i et studie med 12 fastende patienter med kronisk reversibel obstruktiv lungesygdom. Alle blev doseret med to 400 mg Uniphyl (vandfri theophyllintabletter) givet én gang dagligt om morgenen og et referenceprodukt med kontrolleret frigivelse BID administreret som to 200 mg tabletter givet med 12 timers mellemrum. De farmakokinetiske parametre opnået for Uniphyl (vandfri theophyllin-tablet) givet i doser på 800 mg én gang dagligt om morgenen var praktisk talt identiske med de tilsvarende parametre for referencelægemidlet, når de blev givet som 400 mg BID. Især AUC-, Cmax- og Cmin-værdierne opnået i denne undersøgelse var som følger:
Enkeltdosisundersøgelser, hvor forsøgspersoner fastede i tolv (12) timer før og yderligere fire (4) timer efter dosering, viste reduceret biotilgængelighed sammenlignet med dosering med mad. Et enkelt-dosis studie med 20 normale frivillige doseret med to (2) 400 mg tabletter om morgenen sammenlignede dosering under disse fastende forhold med dosering umiddelbart før en standardiseret morgenmad (769 kalorier, bestående af 97 gram kulhydrater, 33 gram protein og 27 gram fedt). Under fodrede forhold var de farmakokinetiske parametre: AUC = 231,7 ± 92,4 mcg time/mL, Cmax = 8,4 ± 2,6 mcg/ml, Tmax = 17,3 ± 6,7 timer. Under fastende forhold var disse parametre AUC = 141,2 ± 6,53 mcg time/mL, Cmax = 5,5 ± 1,5 mcg/ml, Tmax = 6,5 ± 2,1 timer.
En anden enkeltdosis undersøgelse med 21 normale mandlige frivillige, doseret om aftenen, sammenlignede faste med et standardiseret måltid med højt kalorieindhold og højt fedtindhold (870-1.020 kalorier, bestående af 33 gram protein, 55-75 gram fedt, 58 gram kulhydrater). I den fastende arm modtog forsøgspersonerne en Uniphyl (vandfri theophyllin tablet) ® 400 mg tablet kl. 20.00 efter en otte timers faste efterfulgt af yderligere fire timers faste. I den fodrede arm blev forsøgspersonerne igen doseret med en 400 mg Uniphyl (vandfri theophyllin-tablet) tablet, men kl. 20.00 umiddelbart efter det standardiserede måltid med højt fedtindhold, citeret ovenfor. De tilførte farmakokinetiske parametre (normaliseret til 800 mg) var AUC = 221,8 ± 40,9 mcg time/ml, Cmax = 10,9 ± 1,7 mcg/ml, Tmax = 11,8 ± 2,2 timer. I den fastende arm var de farmakokinetiske parametre (normaliseret til 800 mg) AUC = 146,4 ± 40,9 mcg time/mL, Cmax = 6,7 ± 1,7 mcg/ml, Tmax = 7,3 ± 2,2 timer.
Således resulterer administration af enkelt Uniphyl (vandfri theophyllin-tablet) doser til raske, normale frivillige under længerevarende fasteforhold (mindst 10 timers faste natten over før dosering efterfulgt af yderligere fire (4) timers faste efter dosering) i nedsat biotilgængelighed. Der var imidlertid ingen fejl i dette leveringssystem, der førte til en pludselig og uventet frigivelse af en stor mængde theophyllin med Uniphyl (vandfri theophyllin-tablet) tabletter, selv når de indgives sammen med et måltid med højt fedtindhold og højt kalorieindhold.
Lignende undersøgelser blev udført med 600 mg Uniphyl (vandfri theophyllintablet) tablet. En enkeltdosisundersøgelse med 24 forsøgspersoner med en etableret theophyllin-clearance på ≤ 4 l/time sammenlignede den farmakokinetiske evaluering af en 600 mg Uniphyl (vandfri theophyllin-tablet) og halvanden 400 mg Uniphyl (vandfri theophyllin-tablet) tabletter under fodring (ved at bruge en standard diæt med højt fedtindhold) og fasteforhold. Resultaterne af denne 4-vejs randomiserede crossover undersøgelse viser bioækvivalensen af 400 mg og 600 mg Uniphyl (vandfri theophyllin tablet) tabletter. Under fodrede forhold var de farmakokinetiske resultater for halvanden 400 mg tabletter AUC = 214,64 ± 55,88 mcg time/ml, Cmax = 10,58 ± 2,21 mcg/ml og Tmax = 9,00 ± 2,64 timer, og for mg de 2,64 timer. var AUC = 207,85 ± 48,9 mcg time/ml, Cmax = 10,39 ± 1,91 mcg/ml og Tmax = 9,58 ± 1,86 timer. Under fastende forhold var de farmakokinetiske resultater for halvanden 400 mg tabletter AUC = 191,85 ± 51,1 mcg time/ml, Cmax = 7,37 ± 1,83 mcg/ml og Tmax = 8,08 ± 4,39 timer; og for 600 mg tabletten var AUC = 199,39 ± 70,27 mcg time/ml, Cmax = 7,66 ± 2,09 mcg/ml og Tmax = 9,67 ± 4,89 timer.
denne undersøgelse var de gennemsnitlige foder/faste-forhold for halvanden 400 mg tabletter og 600 mg tabletter henholdsvis ca. 112 % og 104 %.
I en anden undersøgelse blev biotilgængeligheden af 600 mg Uniphyl (vandfri theophyllin-tablet) undersøgt med morgen- og aftenadministration. Denne enkeltdosis crossover-undersøgelse i 22 raske mænd blev udført under fodrede (standard fedtholdige diæter). Resultaterne viste ingen klinisk signifikant forskel i biotilgængeligheden af 600 mg Uniphyl (vandfri theophyllin-tablet) administreret om morgenen eller om aftenen. Resultaterne var: AUC = 233,6 ± 45,1 mcg time/mL, Cmax = 10,6 ± 1,3 mcg/ml og Tmax = 12,5 ± 3,2 timer med morgendosering; AUC = 209,8 ± 46,2 mcg time/mL, Cmax = 9,7 ± 1,4 mcg/mL og Tmax = 13,7 ± 3,3 timer med aftendosering. PM/AM-forholdet var 89,3%.
Absorptionsegenskaberne for Uniphyl®-tabletter (theophyllin, vandfri) er blevet grundigt undersøgt. En steady-state crossover biotilgængelighedsundersøgelse hos 22 normale mænd sammenlignede to Uniphyl (theophyllin vandfri tablet) 400 mg tabletter indgivet 24 timer i døgnet kl. 8 umiddelbart efter morgenmad med et reference-theophyllinprodukt med kontrolleret frigivelse administreret BID i fodrede forsøgspersoner kl. 8 umiddelbart efter morgenmad og 20.00 umiddelbart efter aftensmaden (769 kalorier, bestående af 97 gram kulhydrater, 33 gram protein og 27 gram fedt).
De farmakokinetiske parametre for Uniphyl (vandfri theophyllin tablet) 400 mg tabletter under disse steady-state betingelser var AUC = 203,3 ± 87,1 mcg time/mL, Cmax = 12,1 ± 3,8 mcg/ml, Cmin = 4,80 ± 4,8 ± max. timer. For reference BID-produktet var de farmakokinetiske parametre AUC = 219,2 ± 88,4 mcg time/mL, Cmax = 11,0 ± 4,1 mcg/mL, Cmin = 7,28 ± 3,5, Tmax = 6,9 ± 3,4 timer. Den gennemsnitlige procentvise fluktuation [(Cmax-Cmin/Cmin)x100] = 169 % for regimen én gang dagligt og 51 % for referenceproduktet BID-regimet.
Biotilgængeligheden af 600 mg Uniphyl (vandfri theophyllin-tablet) blev yderligere evalueret i et steady-state-studie med multiple doser med 26 raske mænd, der sammenlignede 600 mg-tabletten med halvanden 400 mg Uniphyl-tabletter (vandfri theophyllin-tablet). Alle forsøgspersoner havde tidligere etableret theophyllin-clearances på ≤ 4 l/time og blev doseret én gang dagligt i 6 dage under fodrede forhold. Resultaterne viste ingen klinisk signifikant forskel mellem 600 mg og halvanden 400 mg Uniphyl (vandfri theophyllin tablet) kur. Steady-state resultater var:
Biotilgængelighedsforholdet for 600/400 mg tabletterne var 98,8 %. Under alle undersøgelsesbetingelser er 600 mg-tabletten således bioækvivalent med halvanden 400 mg-tabletter.
Undersøgelser viser, at så længe forsøgspersonerne enten blev fodret konsekvent eller konsekvent fastede, er der lignende biotilgængelighed ved administration af Uniphyl (vandfri theophyllin-tablet) én gang dagligt, uanset om de doseres om morgenen eller om aftenen.
Fordeling
Når først theophyllin kommer ind i det systemiske kredsløb, er omkring 40 % bundet til plasmaprotein, primært albumin. Ubundet theophyllin fordeler sig i hele kroppens vand, men fordeler sig dårligt i kropsfedt. Theophyllins tilsyneladende fordelingsvolumen er ca. 0,45 l/kg (interval 0,3-0,7 l/kg) baseret på ideel kropsvægt. Theophyllin passerer frit over moderkagen, ind i modermælken og ind i cerebrospinalvæsken (CSF). Spyttheophyllinkoncentrationer er omtrentlige til ubundne serumkoncentrationer, men er ikke pålidelige til rutinemæssig eller terapeutisk monitorering, medmindre der anvendes specielle teknikker. En stigning i distributionsvolumenet af theophyllin, primært på grund af reduktion i plasmaproteinbinding, forekommer hos præmature nyfødte, patienter med levercirrhose, ukorrigeret acidæmi, ældre og hos kvinder i tredje trimester af graviditeten. I sådanne tilfælde kan patienten vise tegn på toksicitet ved totale (bundet+ubundet) serumkoncentrationer af theophyllin i det terapeutiske område (10-20 mcg/ml) på grund af forhøjede koncentrationer af det farmakologisk aktive ubundne lægemiddel. Tilsvarende kan en patient med nedsat theophyllinbinding have en subterapeutisk total lægemiddelkoncentration, mens den farmakologisk aktive ubundne koncentration er i det terapeutiske område. Hvis kun den totale serum-theophyllinkoncentration måles, kan dette føre til en unødvendig og potentielt farlig dosisstigning. Hos patienter med nedsat proteinbinding giver måling af ubundet serumtheophyllinkoncentration en mere pålidelig måde til dosisjustering end måling af total serumtheophyllinkoncentration. Generelt bør koncentrationer af ubundet theophyllin holdes i området 6-12 mcg/ml.
Metabolisme
Efter oral dosering gennemgår theophyllin ingen målbar first-pass-eliminering. Hos voksne og børn over et år metaboliseres ca. 90 % af dosis i leveren. Biotransformation sker gennem demethylering til 1-methylxanthin og 3-methylxanthin og hydroxylering til 1,3-dimethylurinsyre. 1-methylxanthin hydroxyleres yderligere ved hjælp af xanthinoxidase til 1-methylurinsyre. Omkring 6 % af en theophyllin-dosis er N-methyleret til koffein. Theophyllin-demethylering til 3-methylxanthin katalyseres af cytochrom P-450 1A2, mens cytochromerne P-450 2E1 og P-450 3A3 katalyserer hydroxyleringen til 1,3-dimethylurinsyre. Demethylering til 1-methylxanthin ser ud til at være katalyseret enten af cytochrom P-450 1A2 eller et nært beslægtet cytochrom. Hos nyfødte er N-demethyleringsvejen fraværende, mens hydroxyleringsvejens funktion er markant mangelfuld. Aktiviteten af disse veje stiger langsomt til maksimale niveauer ved et års alderen.
Koffein og 3-methylxanthin er de eneste theophyllinmetabolitter med farmakologisk aktivitet. 3-methylxanthin har ca. en tiendedel af theophyllins farmakologiske aktivitet, og serumkoncentrationer hos voksne med normal nyrefunktion er
Både N-demethylerings- og hydroxyleringsvejene for biotransformation af theophyllin er kapacitetsbegrænsede. På grund af den store interindividuelle variabilitet i hastigheden af theophyllinmetabolisme, kan ikke-linearitet af elimination begynde hos nogle patienter ved serumtheophyllinkoncentrationer DOSERING OG ADMINISTRATION, Tabel VI ). Nøjagtig forudsigelse af dosisafhængighed af theophyllin-metabolismen hos patienter a priori er ikke mulig, men patienter med meget høje initiale clearance-rater (dvs. lave steady-state serum-theophyllinkoncentrationer ved doser over gennemsnittet) har størst sandsynlighed for at opleve store ændringer i serum theophyllin koncentration som reaktion på dosisændringer.
Udskillelse
Hos nyfødte udskilles ca. 50 % af theophyllin-dosen uændret i urinen. Efter de første tre levemåneder udskilles ca. 10 % af theophyllin-dosis uændret i urinen. Resten udskilles hovedsageligt i urinen som 1,3-dimethylurinsyre (35-40%), 1-methylurinsyre (20-25%) og 3-methylxanthin (15-20%). Da lidt theophyllin udskilles uændret i urinen, og da aktive metabolitter af theophyllin (dvs. koffein, 3-methylxanthin) ikke akkumuleres til klinisk signifikante niveauer, selv i lyset af nyresygdom i slutstadiet, er det ikke nødvendigt at justere dosis for nyreinsufficiens. hos voksne og børn > 3 måneder. I modsætning hertil kræver den store del af theophyllin-dosis, der udskilles i urinen som uændret theophyllin og koffein hos nyfødte, omhyggelig opmærksomhed på dosisreduktion og hyppig overvågning af serum-theophyllinkoncentrationer hos nyfødte med nedsat nyrefunktion (se pkt. ADVARSLER ).
Serumkoncentrationer ved Steady-State
Efter flere doser af theophyllin nås steady-state efter 30-65 timer (gennemsnitligt 40 timer) hos voksne. Ved steady-state, på et doseringsregime med 24-timers intervaller, er den forventede gennemsnitlige laveste koncentration ca. 50 % af den gennemsnitlige maksimale koncentration, idet der antages en gennemsnitlig halveringstid for theophyllin på 8 timer. Forskellen mellem top- og bundkoncentrationer er større hos patienter med hurtigere theophyllin-clearance. Hos disse patienter kan administration af Uniphyl (vandfri theophyllin-tablet) ® være påkrævet hyppigere (hver 12. time).
Særlige populationer (se tabel I for gennemsnitlig clearance og halveringstid)
Geriatrisk
Clearance af theophyllin er i gennemsnit reduceret med 30 % hos raske ældre voksne (> 60 år) sammenlignet med raske unge voksne. Omhyggelig opmærksomhed på dosisreduktion og hyppig monitorering af serumtheophyllinkoncentrationer er påkrævet hos ældre patienter (se ADVARSLER ).
Pædiatri
Clearance af theophyllin er meget lav hos nyfødte (se ADVARSLER ). Theophyllinclearance når maksimale værdier ved et års alderen, forbliver relativt konstant indtil omkring 9 års alderen og falder derefter langsomt med ca. 50 % til voksne værdier ved ca. 16 års alderen. Renal udskillelse af uændret theophyllin hos nyfødte udgør ca. dosis sammenlignet med omkring 10 % hos børn over tre måneder og hos voksne. Omhyggelig opmærksomhed på dosisvalg og overvågning af serumtheophyllinkoncentrationer er påkrævet hos pædiatriske patienter (se ADVARSLER og DOSERING OG ADMINISTRATION ).
Køn
Kønsforskelle i theophyllin-clearance er relativt små og vil sandsynligvis ikke være af klinisk betydning. Signifikant reduktion i theophyllin-clearance er imidlertid blevet rapporteret hos kvinder på den 20. dag i menstruationscyklussen og i tredje trimester af graviditeten.
Race
Farmakokinetiske forskelle i theophyllin-clearance på grund af race er ikke blevet undersøgt.
Nyreinsufficiens
Kun en lille del, f.eks. ca. 10 %, af den administrerede theophyllin-dosis udskilles uændret i urinen hos børn over tre måneder og voksne. Da lidt theophyllin udskilles uændret i urinen, og da aktive metabolitter af theophyllin (dvs. koffein, 3-methylxanthin) ikke akkumuleres til klinisk signifikante niveauer, selv i lyset af nyresygdom i slutstadiet, er det ikke nødvendigt at justere dosis for nyreinsufficiens hos voksne og børn > 3 måneder. I modsætning hertil udskilles ca. 50 % af den administrerede theophyllin-dosis uændret i urinen hos nyfødte. Omhyggelig opmærksomhed på dosisreduktion og hyppig overvågning af serumtheophyllinkoncentrationer er påkrævet hos nyfødte med nedsat nyrefunktion (se ADVARSLER ).
Leverinsufficiens
Theophyllin-clearance er nedsat med 50 % eller mere hos patienter med leverinsufficiens (f.eks. cirrhose, akut hepatitis, kolestase). Omhyggelig opmærksomhed på dosisreduktion og hyppig monitorering af serumtheophyllinkoncentrationer er påkrævet hos patienter med nedsat leverfunktion (se ADVARSLER ).
Kongestiv hjertesvigt (CHF)
Theophyllin-clearance er nedsat med 50 % eller mere hos patienter med CHF. Omfanget af reduktion i theophyllin-clearance hos patienter med CHF ser ud til at være direkte korreleret til sværhedsgraden af hjertesygdommen. Da theophyllinclearance er uafhængig af leverens blodgennemstrømning, ser reduktionen i clearance ud til at skyldes nedsat hepatocytfunktion snarere end nedsat perfusion. Omhyggelig opmærksomhed på dosisreduktion og hyppig monitorering af serumtheophyllinkoncentrationer er påkrævet hos patienter med CHF (se ADVARSLER ).
Rygere
Tobaks- og marihuanarygning ser ud til at øge clearance af theophyllin ved induktion af metaboliske veje. Theophyllin-clearance har vist sig at stige med ca. 50 % hos unge voksne tobaksrygere og med ca. 80 % hos ældre tobaksrygere sammenlignet med ikke-rygere. Passiv røgeksponering har også vist sig at øge theophyllin-clearance med op til 50 %. Afholdenhed fra tobaksrygning i en uge medfører en reduktion på ca. 40 % i theophyllin-clearance. Omhyggelig opmærksomhed på dosisreduktion og hyppig overvågning af serumtheophyllinkoncentrationer er påkrævet hos patienter, der holder op med at ryge (se ADVARSLER ). Brug af nikotintyggegummi har vist sig ikke at have nogen effekt på theophyllin-clearance.
Feber
Feber, uanset dens underliggende årsag, kan mindske clearance af theophyllin. Størrelsen og varigheden af feberen ser ud til at være direkte korreleret til graden af fald i theophyllin-clearance. Der mangler præcise data, men en temperatur på 39°C (102°F) i mindst 24 timer er sandsynligvis nødvendig for at frembringe en klinisk signifikant stigning i serumtheophyllinkoncentrationer. Børn med hurtige hastigheder af theophyllin-clearance (dvs. dem, der kræver en dosis, der er væsentligt større end gennemsnittet [f.eks. > 22 mg/kg/dag] for at opnå en terapeutisk maksimal serum-theophyllinkoncentration, når de er afebrile) kan have større risiko for toksisk effekter fra nedsat clearance under vedvarende feber. Omhyggelig opmærksomhed på dosisreduktion og hyppig monitorering af serumtheophyllinkoncentrationer er påkrævet hos patienter med vedvarende feber (se ADVARSLER ).
Diverse
Andre faktorer forbundet med nedsat theophyllin-clearance omfatter graviditetens tredje trimester, sepsis med multipel organsvigt og hypothyroidisme. Omhyggelig opmærksomhed på dosisreduktion og hyppig monitorering af serumtheophyllinkoncentrationer er påkrævet hos patienter med nogen af disse tilstande (se ADVARSLER ). Andre faktorer forbundet med øget theophyllin-clearance omfatter hyperthyroidisme og cystisk fibrose.
Kliniske Studier
Hos patienter med kronisk astma, herunder patienter med svær astma, der kræver inhalerede kortikosteroider eller orale kortikosteroider til vekselvis dag, har mange kliniske undersøgelser vist, at theophyllin reducerer hyppigheden og sværhedsgraden af symptomer, herunder natlige eksacerbationer, og reducerer "efter behov" brugen af inhaleret beta-2 agonister. Theophyllin har også vist sig at reducere behovet for korte kure med daglig oral prednison for at lindre forværringer af luftvejsobstruktion, som ikke reagerer på bronkodilatatorer hos astmatikere.
Hos patienter med kronisk obstruktiv lungesygdom (KOL) har kliniske undersøgelser vist, at theophyllin reducerer dyspnø, luftindfangning, vejrtrækningsarbejdet og forbedrer kontraktiliteten af diafragmamuskler med ringe eller ingen forbedring i lungefunktionsmålinger.
PATIENTOPLYSNINGER
Patienten (eller forælder/plejer) skal instrueres i at søge læge, når der opstår kvalme, opkastning, vedvarende hovedpine, søvnløshed eller hurtig hjerterytme under behandling med theophyllin, selvom der er mistanke om en anden årsag. Patienten skal instrueres i at kontakte sin sundhedspersonale, hvis de udvikler en ny sygdom, især hvis de ledsages af vedvarende feber, hvis de oplever forværring af en kronisk sygdom, hvis de begynder eller holder op med at ryge cigaretter eller marihuana, eller hvis en anden sundhedsperson tilføjer en ny medicin eller ophører med en tidligere ordineret medicin. Patienterne bør informeres om, at theophyllin interagerer med en lang række lægemidler (se tabel II). Kosttilskuddet perikon (Hypericum perforatum) bør ikke tages samtidig med theophyllin, da det kan resultere i nedsatte theophyllinniveauer. Hvis patienter allerede tager perikon og teophyllin sammen, bør de konsultere deres sundhedspersonale, før de stopper med perikum, da deres teofyllinkoncentrationer kan stige, når dette gøres, hvilket resulterer i toksicitet. Patienter bør instrueres i at informere alt sundhedspersonale, der er involveret i deres behandling, om, at de tager theophyllin, især når en medicin tilføjes eller slettes fra deres behandling. Patienter skal instrueres i ikke at ændre dosis, tidspunkt for dosis eller administrationshyppighed uden først at konsultere deres sundhedspersonale. Hvis en dosis glemmes, skal patienten instrueres i at tage den næste dosis på det sædvanligvis planlagte tidspunkt og ikke forsøge at kompensere for den glemte dosis.
Uniphyl (vandfri theophyllin tablet) ® tabletter kan tages en gang dagligt morgen eller aften. Det anbefales, at Uniphyl (vandfri theophyllin-tablet) tages sammen med måltider. Patienter skal informeres om, at hvis de vælger at tage Uniphyl (vandfri theophyllin-tablet) sammen med mad, skal den tages konsekvent med mad, og hvis de tager den i fastende tilstand, skal den rutinemæssigt tages fastende. Det er vigtigt, at produktet, når det doseres, doseres konsekvent med eller uden mad.
Uniphyl (vandfri theophyllin-tablet) Tabletter må ikke tygges eller knuses, da det kan føre til en hurtig frigivelse af theophyllin med risiko for toksicitet. Tabletten med delekærv kan deles. Patienter, der får Uniphyl (vandfri theophyllin-tablet) tabletter kan passere en intakt matrix-tablet i afføringen eller via kolostomi. Disse matrixtabletter indeholder normalt kun lidt eller ingen resterende theophyllin.
