Buspar 5mg, 10mg Buspirone Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Buspar, og hvordan bruges det?
Buspar 5mg er en receptpligtig medicin, der bruges til at behandle symptomer på angstlidelser. Buspar 5mg kan bruges alene eller sammen med anden medicin.
Buspar tilhører en klasse af lægemidler kaldet angstdæmpende midler, anxiolytika, ikke-benzodiazepiner.
Hvad er de mulige bivirkninger af Buspar?
Hvad er de mulige bivirkninger af Buspar 5mg?
Buspar kan forårsage alvorlige bivirkninger, herunder:
- brystsmerter,
- åndenød, og
- svimmelhed
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Buspar omfatter:
- hovedpine,
- svimmelhed,
- døsighed,
- søvnproblemer (søvnløshed),
- kvalme,
- ondt i maven, og
- føler sig nervøs eller ophidset
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Buspar. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
Buspironhydrochlorid-tabletter, USP er et angstdæmpende middel, der ikke er kemisk eller farmakologisk relateret til benzodiazepinerne, barbituraterne eller andre beroligende/angstdæmpende lægemidler.
Buspironhydrochlorid, USP er et hvidt krystallinsk pulver. Det er meget opløseligt i vand; frit opløselig i methanol og i methylenchlorid; tungtopløselig i ethanol og i acetonitril; meget lidt opløselig i ethylacetat og praktisk talt uopløselig i hexaner. Dens molekylvægt er 422. Kemisk er buspironhydrochlorid 8-[4-[4-(2-pyrimidinyl)-1-piperazinyl]butyl]-8-azaspiro[4.5]decan-7,9-dionmonohydrochlorid. Molekylformlen C21H31N5O2•HCl er repræsenteret af følgende strukturformel:
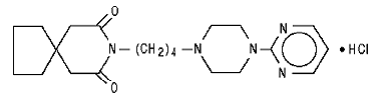
Hver buspironhydrochloridtablet beregnet til oral administration indeholder 5 mg eller 10 mg eller 15 mg eller 30 mg buspironhydrochlorid (svarende til henholdsvis 4,6 mg, 9,1 mg, 13,7 mg og 27,4 mg buspiron fri base). Derudover indeholder hver tablet følgende inaktive ingredienser: kolloid siliciumdioxid, lactosemonohydrat, magnesiumstearat, mikrokrystallinsk cellulose og natriumstivelsesglykolat. Tabletterne på 5 mg og 10 mg er delekærv, så de kan skæres i to. Således kan 5 mg tabletten også give 2,5 mg dosis, og 10 mg tabletten kan give en 5 mg dosis. Tabletterne på 15 mg og 30 mg har delekærv, så de enten kan skæres i to eller tre. En enkelt 15 mg tablet kan således give følgende doser: 15 mg (hel tablet), 10 mg (to tredjedele af en tablet), 7,5 mg (den halve tablet) eller 5 mg (en tredjedel af en tablet) . En enkelt 30 mg tablet kan give følgende doser: 30 mg (hel tablet), 20 mg (to tredjedele af en tablet), 15 mg (den halve tablet) eller 10 mg (en tredjedel af en tablet).
INDIKATIONER
Buspironhydrochlorid-tabletter er indiceret til behandling af angstlidelser eller kortvarig lindring af symptomer på angst. Angst eller spændinger forbundet med stress i hverdagen kræver normalt ikke behandling med et angstdempende middel.
Effekten af buspironhydrochlorid-tabletter er blevet påvist i kontrollerede kliniske forsøg med ambulante patienter, hvis diagnose stort set svarer til generaliseret angstlidelse (GAD). Mange af patienterne inkluderet i disse undersøgelser havde også sideløbende depressive symptomer, og buspironhydrochloridtabletter lindrede angst ved tilstedeværelse af disse sideløbende depressive symptomer. De patienter, der blev evalueret i disse undersøgelser, havde oplevet symptomer i perioder på 1 måned til over 1 år før undersøgelsen, med en gennemsnitlig symptomvarighed på 6 måneder. Generaliseret angstlidelse (300.02) er beskrevet i American Psychiatric Association's Diagnostic and Statistical Manual, III1 som følger:
Generaliseret, vedvarende angst (af mindst 1 måneds kontinuerlig varighed), manifesteret af symptomer fra tre af de fire følgende kategorier:
Motorspænding
Rystelse, nervøsitet, uroligheder, skælven, spændinger, muskelsmerter, træthed, manglende evne til at slappe af, øjenlågstrækninger, rynket øjenbryn, anstrengt ansigt, uroligheder, rastløshed, let forskrækkelse.
Autonom hyperaktivitet
Sveden, hjertet banker eller suser, kolde, klamme hænder, mundtørhed, svimmelhed, svimmelhed, paræstesier (prikken i hænder eller fødder), mavebesvær, varme eller kolde perioder, hyppig vandladning, diarré, ubehag i mavehulen, klump i halsen, rødmen, bleghed, høj hvilepuls og respirationsfrekvens.
Bekymret forventning
Angst, bekymring, frygt, grublerier og forventning om ulykke for sig selv eller andre.
Bevågenhed og scanning
Hyperopmærksomhed, der resulterer i distraherbarhed, koncentrationsbesvær, søvnløshed, følelse "på kanten", irritabilitet, utålmodighed.
Ovenstående symptomer skyldes ikke en anden psykisk lidelse, såsom en depressiv lidelse eller skizofreni. Men milde depressive symptomer er almindelige ved GAD.
Effektiviteten af buspironhydrochloridtabletter ved langtidsbrug, dvs. i mere end 3 til 4 uger, er ikke blevet påvist i kontrollerede forsøg. Der er ingen tilgængelig dokumentation, der systematisk adresserer den passende behandlingsvarighed for GAD. I en undersøgelse af langtidsbrug blev 264 patienter imidlertid behandlet med buspironhydrochloridtabletter i 1 år uden dårlig effekt. Derfor bør den læge, der vælger at bruge buspironhydrochloridtabletter i længere perioder, med jævne mellemrum revurdere brugen af lægemidlet for den enkelte patient.
DOSERING OG ADMINISTRATION
Den anbefalede startdosis er 15 mg dagligt (7,5 mg to gange dagligt). For at opnå en optimal terapeutisk respons kan dosis med intervaller på 2 til 3 dage øges med 5 mg dagligt efter behov. Den maksimale daglige dosis bør ikke overstige 60 mg pr. dag. I kliniske forsøg, der muliggjorde dosistitrering, blev opdelte doser på 20 mg til 30 mg dagligt almindeligvis anvendt.
Biotilgængeligheden af buspiron øges, når den gives sammen med mad sammenlignet med fastende tilstand (se KLINISK FARMAKOLOGI ). Derfor bør patienter tage buspiron på en konsekvent måde med hensyn til tidspunktet for dosering; enten altid med eller altid uden mad.
Når buspiron skal gives sammen med en potent hæmmer af CYP3A4, er dosisanbefalingerne beskrevet i DRUGSINTERAKTIONER afsnit skal følges.
HVORDAN LEVERET
Buspironhydrochlorid-tabletter USP, 5 mg er hvide til råhvide, kapselformede, flade tabletter med skrå kant præget med halvt på den ene side; den ene side af bisect er præget med 'ZE' og en anden er præget med '36' og den anden side er almindelig
Producentoplysninger: N/A. Revideret: maj 2016
BIVIRKNINGER
Ingen oplysninger angivet.
DRUGSINTERAKTIONER
Psykotrope midler
MAO-hæmmere
Det anbefales, at buspironhydrochloridtabletter ikke anvendes samtidig med MAO-hæmmere (se ADVARSLER ).
Amitriptylin
Efter tilføjelse af buspiron til amitriptylin-dosisregimet blev der ikke observeret statistisk signifikante forskelle i steady-state farmakokinetiske parametre (Cmax, AUC og Cmin) for amitriptylin eller dets metabolit nortriptylin.
Diazepam
Efter tilføjelse af buspiron til diazepam-dosisregimet blev der ikke observeret statistisk signifikante forskelle i steady-state farmakokinetiske parametre (Cmax, AUC og Cmin) for diazepam, men stigninger på ca. 15 % blev set for nordiazepam og mindre uønskede kliniske effekter. (svimmelhed, hovedpine og kvalme) blev observeret.
Haloperidol
I en undersøgelse med normale frivillige resulterede samtidig administration af buspiron og haloperidol i øgede serumhaloperidolkoncentrationer. Den kliniske betydning af dette fund er ikke klar.
Nefazodon
[se Hæmmere og inducere af Cytochrom P450 3A4 (CYP3A4) ].
Trazodon
Der er en rapport, der tyder på, at samtidig brug af Desyrel®# (trazodonhydrochlorid) og buspiron kan have forårsaget 3- til 6-dobbelte forhøjelser af SGPT (ALT) hos nogle få patienter. I en lignende undersøgelse, der forsøgte at replikere dette fund, blev der ikke identificeret nogen interaktiv effekt på hepatiske transaminaser.
Triazolam/Flurazepam
Samtidig administration af buspiron med enten triazolam eller flurazepam så ikke ud til at forlænge eller intensivere den sedative virkning af hverken benzodiazepin.
Andre psykotrope stoffer
Da virkningerne af samtidig administration af buspiron med de fleste andre psykotrope stoffer ikke er blevet undersøgt, bør samtidig brug af buspiron med andre CNS-aktive lægemidler behandles med forsigtighed.
Hæmmere og inducere af Cytochrom P450 3A4 (CYP3A4)
Buspiron er vist in vitro at blive metaboliseret af CYP3A4. Dette fund er i overensstemmelse med in vivo-interaktionerne observeret mellem buspiron og følgende:
Diltiazem og verapamil
en undersøgelse af ni raske frivillige øgede samtidig administration af buspiron (10 mg som en enkelt dosis) og verapamil (80 mg tid) eller diltiazem (60 mg tid) plasma buspironkoncentrationer (verapamil øgede AUC og Cmax for buspiron 3,4 gange, mens diltiazem øget AUC og Cmax henholdsvis 5,5 og 4 gange.) Bivirkninger, der kan tilskrives buspiron, kan være mere sandsynlige ved samtidig administration med enten diltiazem eller verapamil. Efterfølgende dosisjustering kan være nødvendig og bør være baseret på klinisk vurdering.
Erythromycin
et studie med raske frivillige øgede samtidig administration af buspiron (10 mg som en enkelt dosis) og erythromycin (1,5 g/dag i 4 dage) plasmakoncentrationen af buspiron (5 gange stigning i Cmax og 6 gange stigning i AUC). Disse farmakokinetiske interaktioner blev ledsaget af en øget forekomst af bivirkninger, der kan tilskrives buspiron. Hvis de to lægemidler skal bruges i kombination, anbefales en lav dosis buspiron (f.eks. 2,5 mg to gange dagligt). Efterfølgende dosisjustering af begge lægemidler bør baseres på klinisk vurdering.
Grapefrugtjuice
I en undersøgelse med raske frivillige øgede samtidig administration af buspiron (10 mg som en enkelt dosis) og grapefrugtjuice (200 ml dobbeltstyrke tid i 2 dage) plasmakoncentrationen af buspiron (4,3 gange stigning i Cmax; 9,2 gange stigning i AUC ). Patienter, der får buspiron, bør rådes til at undgå at drikke så store mængder grapefrugtjuice.
Itraconazol
et studie med raske frivillige øgede samtidig administration af buspiron (10 mg som en enkelt dosis) og itraconazol (200 mg/dag i 4 dage) plasmakoncentrationen af buspiron (13 gange stigning i Cmax og 19 gange stigning i AUC). Disse farmakokinetiske interaktioner blev ledsaget af en øget forekomst af bivirkninger, der kan tilskrives buspiron. Hvis de to lægemidler skal bruges i kombination, anbefales en lav dosis buspiron (f.eks. 2,5 mg qd). Efterfølgende dosisjustering af begge lægemidler bør baseres på klinisk vurdering.
Nefazodon
en undersøgelse af steady-state farmakokinetik hos raske frivillige resulterede samtidig administration af buspiron (2,5 eller 5 mg to gange dagligt) med nefazodon (250 mg to gange dagligt) i markante stigninger i plasma buspironkoncentrationer (stigninger op til 20 gange i Cmax og op til 50 gange). -fold i AUC) og statistisk signifikante fald (ca. 50%) i plasmakoncentrationer af buspironmetabolitten 1-PP. Med 5 mg daglige doser af buspiron blev der observeret små stigninger i AUC for nefazodon (23 %) og dets metabolitter hydroxynefazodon (HO-NEF) (17 %) og meta-chlorphenylpiperazin (9 %). Små stigninger i Cmax blev observeret for nefazodon (8 %) og dets metabolit HO-NEF (11 %).
Forsøgspersoner, der fik buspiron 5 mg to gange dagligt og nefazodon 250 mg to gange dagligt, oplevede svimmelhed, asteni, svimmelhed og somnolens, og bivirkninger blev også observeret med begge lægemidler alene. Hvis de to lægemidler skal bruges i kombination, anbefales en lav dosis buspiron (f.eks. 2,5 mg qd). Efterfølgende dosisjustering af begge lægemidler bør baseres på klinisk vurdering.
Rifampin
I en undersøgelse med raske frivillige reducerede samtidig administration af buspiron (30 mg som en enkelt dosis) og rifampin (600 mg/dag i 5 dage) plasmakoncentrationerne (83,7 % fald i Cmax; 89,6 % fald i AUC) og farmakodynamiske virkninger af buspiron. Hvis de to lægemidler skal bruges i kombination, kan det være nødvendigt at justere dosis af buspiron for at opretholde den angstdæmpende effekt.
Andre hæmmere og inducere af CYP3A4
Stoffer, der hæmmer CYP3A4, såsom ketoconazol eller ritonavir, kan hæmme buspironmetabolisme og øge plasmakoncentrationer af buspiron, mens stoffer, der inducerer CYP3A4, såsom dexamethason, eller visse antikonvulsiva (phenytoin, phenobarbital, carbamazepin) kan øge buspironets metabolismehastighed. Hvis en patient er blevet titreret til en stabil dosis af buspiron, kan en dosisjustering af buspiron være nødvendig for at undgå bivirkninger, der kan tilskrives buspiron eller nedsat anxiolytisk aktivitet. Når det administreres sammen med en potent hæmmer af CYP3A4, anbefales en lav dosis buspiron med forsigtighed. Når det bruges i kombination med en potent inducer af CYP3A4, kan det være nødvendigt at justere dosis af buspiron for at opretholde den angstdæmpende effekt.
Andre stoffer
Cimetidin
Samtidig administration af buspiron og cimetidin viste sig at øge Cmax (40%) og Tmax (2 gange), men havde minimal effekt på AUC for buspiron.
Proteinbinding
In vitro fortrænger buspiron ikke tæt bundne lægemidler som phenytoin, propranolol og warfarin fra serumproteiner. Der har dog været én rapport om forlænget protrombintid, når buspiron blev tilføjet til kuren for en patient behandlet med warfarin. Patienten fik også kronisk phenytoin, phenobarbital, digoxin og Synthroid®*. In vitro kan buspiron fortrænge mindre fast bundne lægemidler som digoxin. Den kliniske betydning af denne egenskab er ukendt.
Terapeutiske niveauer af aspirin, desipramin, diazepam, flurazepam, ibuprofen, propranolol, thioridazin og tolbutamid havde kun en begrænset effekt på omfanget af binding af buspiron til plasmaproteiner (se KLINISK FARMAKOLOGI ).
Interaktioner med lægemiddel/laboratorietest
Buspironhydrochlorid kan interferere med urinmetanephrin/catekolamin-analysen. Det er fejlagtigt blevet læst som metanephrin under rutinemæssig assaytestning for fæokromocytom, hvilket resulterer i et falsk positivt laboratorieresultat. Buspironhydrochlorid bør derfor seponeres i mindst 48 timer før urinopsamling for katekolaminer.
Stofmisbrug og afhængighed
Klasse kontrolleret stof
Buspironhydrochlorid er ikke et kontrolleret stof.
Fysisk og psykologisk afhængighed
menneske- og dyreforsøg har buspiron ikke vist noget potentiale for misbrug eller afledning, og der er ingen beviser for, at det forårsager tolerance eller hverken fysisk eller psykisk afhængighed. Menneskelige frivillige med en historie med rekreativt stof- eller alkoholforbrug blev undersøgt i to dobbeltblindede kliniske undersøgelser. Ingen af forsøgspersonerne var i stand til at skelne mellem buspironhydrochloridtabletter og placebo. I modsætning hertil viste forsøgspersoner en statistisk signifikant præference for methaqualon og diazepam. Undersøgelser af aber, mus og rotter har vist, at buspiron mangler potentiale for misbrug. Efter kronisk administration hos rotter resulterede pludselig ophævelse af buspiron ikke i tab af kropsvægt, der almindeligvis observeres med stoffer, der forårsager fysisk afhængighed.
Selvom der ikke er nogen direkte evidens for, at buspironhydrochloridtabletter forårsager fysisk afhængighed eller stofsøgningsadfærd, er det vanskeligt ud fra eksperimenter at forudsige, i hvilket omfang et CNS-aktivt lægemiddel vil blive misbrugt, omdirigeret og/eller misbrugt, når det først er markedsført. Derfor bør læger omhyggeligt vurdere patienterne for en historie med stofmisbrug og følge sådanne patienter nøje, observere dem for tegn på misbrug eller misbrug af buspironhydrochloridtabletter (f.eks. udvikling af tolerance, stigning i dosis, lægemiddelsøgende adfærd).
Klasse kontrolleret stof
Buspironhydrochlorid er ikke et kontrolleret stof.
Fysisk og psykologisk afhængighed
menneske- og dyreforsøg har buspiron ikke vist noget potentiale for misbrug eller afledning, og der er ingen beviser for, at det forårsager tolerance eller hverken fysisk eller psykisk afhængighed. Menneskelige frivillige med en historie med rekreativt stof- eller alkoholforbrug blev undersøgt i to dobbeltblindede kliniske undersøgelser. Ingen af forsøgspersonerne var i stand til at skelne mellem buspironhydrochloridtabletter og placebo. I modsætning hertil viste forsøgspersoner en statistisk signifikant præference for methaqualon og diazepam. Undersøgelser af aber, mus og rotter har vist, at buspiron mangler potentiale for misbrug. Efter kronisk administration hos rotter resulterede pludselig ophævelse af buspiron ikke i tab af kropsvægt, der almindeligvis observeres med stoffer, der forårsager fysisk afhængighed.
Selvom der ikke er nogen direkte evidens for, at buspironhydrochloridtabletter forårsager fysisk afhængighed eller stofsøgningsadfærd, er det vanskeligt ud fra eksperimenter at forudsige, i hvilket omfang et CNS-aktivt lægemiddel vil blive misbrugt, omdirigeret og/eller misbrugt, når det først er markedsført. Derfor bør læger omhyggeligt vurdere patienterne for en historie med stofmisbrug og følge sådanne patienter nøje, observere dem for tegn på misbrug eller misbrug af buspironhydrochloridtabletter (f.eks. udvikling af tolerance, stigning i dosis, lægemiddelsøgende adfærd).
ADVARSLER
Administration af buspironhydrochloridtabletter til en patient, der tager en monoaminoxidasehæmmer (MAOI), kan udgøre en fare. Der har været rapporter om forekomst af forhøjet blodtryk, når buspironhydrochlorid-tabletter er blevet tilføjet til et regime, der inkluderer en MAO-hæmmer. Derfor anbefales det, at buspironhydrochloridtabletter ikke anvendes samtidig med en MAO-hæmmer.
Da buspironhydrochloridtabletter ikke har nogen etableret antipsykotisk aktivitet, bør det ikke anvendes i stedet for passende antipsykotisk behandling.
FORHOLDSREGLER
Generel
Interferens med kognitiv og motorisk ydeevne
Undersøgelser tyder på, at buspironhydrochlorid-tabletter er mindre beroligende end andre angstdempende midler, og at det ikke giver signifikant funktionsnedsættelse. Dets CNS-virkninger hos enhver individuel patient er dog muligvis ikke forudsigelige. Derfor bør patienter advares om at betjene en bil eller bruge komplekse maskiner, indtil de er rimeligt sikre på, at buspironbehandling ikke påvirker dem negativt.
Selvom formelle undersøgelser af interaktionen mellem buspironhydrochlorid og alkohol indikerer, at buspiron ikke øger alkohol-induceret svækkelse af motorisk og mental præstation, er det klogt at undgå samtidig brug af alkohol og buspiron.
Potentiale for abstinensreaktioner hos beroligende/hypnotiske/anxiolytiske lægemiddelafhængige patienter
Fordi buspironhydrochloridtabletter ikke udviser krydstolerance med benzodiazepiner og andre almindelige beroligende/hypnotiske lægemidler, vil det ikke blokere det abstinenssyndrom, som ofte ses ved ophør af behandling med disse lægemidler. Inden behandling med buspironhydrochlorid-tabletter påbegyndes, er det derfor tilrådeligt at trække patienterne gradvist, især patienter, der har brugt et CNS-depressivt lægemiddel kronisk, fra deres tidligere behandling. Rebound- eller abstinenssymptomer kan forekomme over forskellige tidsperioder, delvist afhængigt af typen af lægemiddel og dets effektive halveringstid for eliminering.
Abstinenssyndromet fra beroligende/hypnotiske/anxiolytiske lægemidler kan forekomme som enhver kombination af irritabilitet, angst, agitation, søvnløshed, tremor, mavekramper, muskelkramper, opkastning, svedtendens, influenzalignende symptomer uden feber og lejlighedsvis endda som anfald. .
Mulige bekymringer relateret til buspirons binding til dopaminreceptorer
Fordi buspiron kan binde til centrale dopaminreceptorer, er der blevet rejst et spørgsmål om dets potentiale til at forårsage akutte og kroniske ændringer i dopamin-medieret neurologisk funktion (f.eks. dystoni, pseudoparkinsonisme, akatisi og tardiv dyskinesi). Klinisk erfaring i kontrollerede forsøg har ikke kunnet identificere nogen signifikant neuroleptika-lignende aktivitet; dog er et rastløshedssyndrom, der opstår kort efter påbegyndelse af behandlingen, blevet rapporteret hos en lille del af de buspironbehandlede patienter. Syndromet kan forklares på flere måder. For eksempel kan buspiron øge den centrale noradrenerge aktivitet; alternativt kan virkningen tilskrives dopaminerge virkninger (dvs. repræsentere akatisi). Se BIVIRKNINGER : Postmarketing oplevelse .
Information til patienter
For at sikre sikker og effektiv brug af buspironhydrochloridtabletter bør følgende information og instruktioner gives til patienter:
Informer din læge om medicin, receptpligtig eller ikke-receptpligtig medicin, alkohol eller medicin, som du nu tager eller planlægger at tage under din behandling med buspironhydrochloridtabletter.
Informer din læge, hvis du er gravid, eller hvis du planlægger at blive gravid, eller hvis du bliver gravid, mens du tager buspironhydrochloridtabletter.
Informer din læge, hvis du ammer et spædbarn.
Indtil du oplever, hvordan denne medicin påvirker dig, må du ikke køre bil eller betjene potentielt farlige maskiner.
Du bør tage buspironhydrochlorid konsekvent, enten altid med eller altid uden mad.
Under din behandling med buspironhydrochloridtabletter skal du undgå at drikke store mængder grapefrugtjuice.
Laboratorieprøver
Der anbefales ingen specifikke laboratorietests.
Karcinogenese, mutagenese, svækkelse af fertilitet
Der blev ikke observeret tegn på kræftfremkaldende potentiale hos rotter under et 24 måneders studie med ca. 133 gange den maksimalt anbefalede orale dosis til mennesker; eller hos mus, under et 18 måneders studie med ca. 167 gange den maksimalt anbefalede orale dosis til mennesker.
Med eller uden metabolisk aktivering inducerede buspiron ikke punktmutationer i fem stammer af Salmonella typhimurium (Ames Test) eller muselymfom L5178YTK+ cellekulturer, og der blev heller ikke observeret DNA-skade med buspiron i Wi-38 humane celler. Kromosomafvigelser eller abnormiteter forekom ikke i knoglemarvsceller hos mus, der fik en eller fem daglige doser buspiron.
Graviditet
Teratogene virkninger
Graviditetskategori B
Der blev ikke observeret nedsat fertilitet eller fosterskade i reproduktionsundersøgelser udført på rotter og kaniner ved buspirondoser på ca. 30 gange den maksimalt anbefalede humane dosis. Hos mennesker er der imidlertid ikke udført tilstrækkelige og velkontrollerede undersøgelser under graviditet. Da reproduktionsstudier på dyr ikke altid forudsiger human respons, bør dette lægemiddel kun anvendes under graviditet, hvis det er klart nødvendigt.
Arbejde og levering
Effekten af buspironhydrochlorid på fødsel og fødsel hos kvinder er ukendt. Der blev ikke observeret nogen bivirkninger i reproduktionsundersøgelser hos rotter.
Ammende mødre
Omfanget af udskillelsen i modermælk af buspiron eller dets metabolitter kendes ikke. Hos rotter udskilles buspiron og dets metabolitter imidlertid i mælk. Administration af buspironhydrochloridtabletter til ammende kvinder bør undgås, hvis det er klinisk muligt.
Pædiatrisk brug
Sikkerheden og effektiviteten af buspiron blev evalueret i to placebokontrollerede 6 ugers forsøg med i alt 559 pædiatriske patienter (fra 6 til 17 år) med GAD. Undersøgte doser var 7,5 mg til 30 mg to gange dagligt (15 til 60 mg/dag). Der var ingen signifikante forskelle mellem buspiron og placebo med hensyn til symptomerne på GAD efter doser anbefalet til behandling af GAD hos voksne. Farmakokinetiske undersøgelser har vist, at plasmaeksponeringen for buspiron og dets aktive metabolit, 1-PP, for identiske doser er lig med eller højere hos pædiatriske patienter end voksne. Ingen uventede sikkerhedsfund blev forbundet med buspiron i disse forsøg. Der er ingen langsigtede sikkerheds- eller effektdata i denne population.
Geriatrisk brug
en undersøgelse af 6632 patienter, som fik buspiron til behandling af angst, var 605 patienter ≥ 65 år og 41 var ≥ 75 år gamle; sikkerheds- og effektprofilerne for disse 605 ældre patienter (gennemsnitsalder = 70,8 år) svarede til dem i den yngre population (gennemsnitsalder = 43,3 år). Gennemgang af spontant rapporterede kliniske hændelser har ikke identificeret forskelle mellem ældre og yngre patienter, men større følsomhed hos nogle ældre patienter kan ikke udelukkes.
Der var ingen effekt af alder på farmakokinetikken af buspiron (se KLINISK FARMAKOLOGI , Særlige Populationer ).
Brug hos patienter med nedsat lever- eller nyrefunktion
Buspiron metaboliseres af leveren og udskilles af nyrerne. Et farmakokinetisk studie med patienter med nedsat lever- eller nyrefunktion viste øgede plasmaniveauer og forlænget halveringstid af buspiron. Derfor kan administration af buspironhydrochloridtabletter til patienter med svært nedsat lever- eller nyrefunktion ikke anbefales (se KLINISK FARMAKOLOGI ).
OVERDOSIS
Ingen oplysninger angivet.
KONTRAINDIKATIONER
Buspironhydrochlorid-tabletter er kontraindiceret til patienter, der er overfølsomme over for buspironhydrochlorid.
KLINISK FARMAKOLOGI
Virkningsmekanismen af buspiron er ukendt. Buspiron adskiller sig fra typiske benzodiazepiner anxiolytika ved, at det ikke udøver antikonvulsive eller muskelafslappende virkninger. Det mangler også den fremtrædende beroligende effekt, der er forbundet med mere typiske anxiolytika. In vitro prækliniske undersøgelser har vist, at buspiron har en høj affinitet til serotonin (5-HT1A) receptorer. Buspiron har ingen signifikant affinitet for benzodiazepinreceptorer og påvirker ikke GABA-binding in vitro eller in vivo, når det testes i prækliniske modeller.
Buspiron har moderat affinitet til hjernens D2-dopaminreceptorer. Nogle undersøgelser tyder på, at buspiron kan have indirekte virkninger på andre neurotransmittersystemer.
Buspironhydrochlorid absorberes hurtigt hos mennesker og gennemgår omfattende first-pass metabolisme. I en radioaktivt mærket undersøgelse udgjorde uændret buspiron i plasmaet kun ca. 1 % af radioaktiviteten i plasmaet. Efter oral administration er plasmakoncentrationerne af uændret buspiron meget lave og varierende mellem forsøgspersoner. Maksimale plasmaniveauer på 1 ng/ml til 6 ng/ml er blevet observeret 40 til 90 minutter efter enkelt orale doser på 20 mg. Enkeltdosisbiotilgængeligheden af uændret buspiron, når den tages som tablet, er i gennemsnit ca. 90 % af en ækvivalent dosis opløsning, men der er stor variation.
Virkningerne af mad på biotilgængeligheden af buspironhydrochloridtabletter er blevet undersøgt hos otte forsøgspersoner. De fik en dosis på 20 mg med og uden mad; arealet under plasmakoncentration-tidskurven (AUC) og maksimal plasmakoncentration (Cmax) af uændret buspiron steg med henholdsvis 84 % og 116 %, men den samlede mængde af buspironimmunreaktivt materiale ændrede sig ikke. Dette tyder på, at mad kan reducere omfanget af præsystemisk clearance af buspiron (se DOSERING OG ADMINISTRATION ).
En flerdosisundersøgelse udført i 15 forsøgspersoner tyder på, at buspiron har en ikke-lineær farmakokinetik. Dosisstigninger og gentagen dosering kan således føre til noget højere blodniveauer af uændret buspiron, end det ville blive forudsagt ud fra resultater af enkeltdosisundersøgelser.
En in vitro proteinbindingsundersøgelse viste, at ca. 86 % af buspiron er bundet til plasmaproteiner. Det blev også observeret, at aspirin øgede plasmaniveauerne af fri buspiron med 23 %, mens flurazepam reducerede plasmaniveauerne af fri buspiron med 20 %. Det vides dog ikke, om disse lægemidler forårsager lignende virkninger på plasmaniveauer af fri buspiron in vivo, eller om sådanne ændringer, hvis de forekommer, forårsager klinisk signifikante forskelle i behandlingsresultatet. En in vitro undersøgelse viste, at buspiron ikke fortrængte stærkt proteinbundne lægemidler såsom phenytoin, warfarin og propranolol fra plasmaprotein, og at buspiron kan fortrænge digoxin.
Buspiron metaboliseres primært ved oxidation, som in vitro har vist sig at være medieret af cytochrom P450 3A4 (CYP3A4) (se DRUGSINTERAKTIONER ). Der produceres adskillige hydroxylerede derivater og en farmakologisk aktiv metabolit, 1-pyrimidinylpiperazin (1-PP). I dyremodeller, der forudsiger anxiolytisk potentiale, har 1-PP omkring en fjerdedel af aktiviteten af buspiron, men er til stede i op til 20 gange større mængder. Dette er dog sandsynligvis ikke vigtigt for mennesker: blodprøver fra mennesker, der er kronisk udsat for buspironhydrochlorid, udviser ikke høje niveauer af 1-PP; gennemsnitsværdier er ca. 3 ng/ml, og det højeste humane blodniveau registreret blandt 108 kronisk doserede patienter var 17 ng/mL, mindre end 1/200 af 1-PP-niveauer fundet hos dyr, der fik store doser buspiron uden tegn på toksicitet.
I et enkeltdosisstudie med 14C-mærket buspiron blev 29 % til 63 % af dosis udskilt i urinen inden for 24 timer, primært som metabolitter; fækal udskillelse tegnede sig for 18 % til 38 % af dosis. Den gennemsnitlige eliminationshalveringstid for uændret buspiron efter enkeltdoser på 10 mg til 40 mg er ca. 2 til 3 timer.
Særlige Populationer
Effekter på alder og køn
Efter enkelte eller flere doser til voksne blev der ikke observeret signifikante forskelle i buspirons farmakokinetik (AUC og Cmax) mellem ældre og yngre forsøgspersoner eller mellem mænd og kvinder.
Nedsat leverfunktion
Efter flere doser administration af buspiron til patienter med nedsat leverfunktion, steg steady-state AUC for buspiron 13 gange sammenlignet med raske forsøgspersoner (se FORHOLDSREGLER ).
Nedsat nyrefunktion
Efter administration af buspiron i flere doser til patienter med nyrefunktion (Clcr = 10 til 70 ml/min/1,73 m2) steg steady-state AUC for buspiron 4 gange sammenlignet med raske (Clcr ≥ 80 ml/min/1,73 m2) forsøgspersoner. (se FORHOLDSREGLER ).
Race effekter
Effekten af race på buspirons farmakokinetik er ikke blevet undersøgt.
PATIENTOPLYSNINGER
Buspironhydrochlorid Tabletter, USP Til 15 mg og 30 mg tabletter
SÅDAN BRUGER DU
Respons på buspiron varierer fra person til person. Din læge kan finde det nødvendigt at justere din dosis for at opnå den korrekte respons.
Hver tablet har delekærv og kan brydes nøjagtigt.
For at bryde en tablet præcist og let skal du holde tabletten mellem dine tommelfingre og pegefingre tæt på den relevante tabletskæring (rille). Tryk derefter på tabletsegmenterne, og tryk tabletsegmenterne fra hinanden (segmenter, der knækker forkert, bør ikke bruges).
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
