Anafranil 10mg, 25mg, 50mg Clomipramine Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Anafranil 10mg, og hvordan bruges det?
Anafranil 50mg er en receptpligtig medicin, der bruges til at behandle symptomer på obsessiv-kompulsiv lidelse. Anafranil 50mg kan bruges alene eller sammen med anden medicin.
Anafranil tilhører en klasse af lægemidler kaldet antidepressiva, TCA'er.
Det vides ikke, om Anafranil 50mg er sikkert og effektivt til børn under 10 år.
Hvad er de mulige bivirkninger af Anafranil 25mg?
Anafranil 50mg kan forårsage alvorlige bivirkninger, herunder:
- udslæt,
- feber,
- hævede kirtler,
- influenzalignende symptomer,
- muskelsmerter,
- svær svaghed,
- usædvanlige blå mærker,
- gulfarvning af din hud og øjne (gulsot),
- adfærdsændringer,
- angst,
- Angstanfald,
- søvnbesvær,
- impulsiv adfærd,
- irritabilitet,
- agitation,
- fjendtlighed,
- aggressivitet,
- hyperaktiv (psykisk eller fysisk),
- depression,
- selvmordstanker,
- sløret syn,
- tunnelsyn,
- øjensmerter eller hævelse,
- ser glorier omkring lys,
- hurtig puls,
- rysten eller rysten,
- forvirring,
- ekstrem frygt,
- smertefuld eller vandladningsbesvær,
- anfald,
- feber,
- hallucinationer,
- svedeture,
- rystende,
- hurtig puls,
- muskelstivhed,
- trækninger,
- manglende koordination,
- kvalme,
- opkastning, og
- diarré
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Anafranil omfatter:
- tør mund,
- kvalme,
- dårlig mave,
- mistet appetiten,
- forstoppelse,
- føler angst,
- svimmel,
- døsighed,
- træt,
- søvnproblemer,
- ændringer i appetit eller vægt,
- hukommelsesproblemer,
- koncentrationsbesvær,
- øget svedtendens,
- følelsesløshed eller prikken,
- synsforandringer,
- nedsat sexlyst,
- impotens, og
- svært ved at få orgasme
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Anafranil. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ADVARSEL
Suicidalitet og antidepressive stoffer
Antidepressiva øgede risikoen sammenlignet med placebo for selvmordstanker og -adfærd (suicidalitet) hos børn, unge og unge voksne i korttidsstudier af svær depressiv lidelse (MDD) og andre psykiatriske lidelser. Enhver, der overvejer at bruge clomipraminhydrochlorid eller ethvert andet antidepressivt middel til et barn, en teenager eller en ung voksen, skal balancere denne risiko med det kliniske behov. Korttidsundersøgelser viste ikke en stigning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne efter 24 år; der var en reduktion i risikoen med antidepressiva sammenlignet med placebo hos voksne på 65 år og derover. Depression og visse andre psykiatriske lidelser er i sig selv forbundet med øget risiko for selvmord. Patienter i alle aldre, der påbegyndes med antidepressiv behandling, bør overvåges passende og observeres nøje for klinisk forværring, suicidalitet eller usædvanlige ændringer i adfærd. Familier og pårørende bør informeres om behovet for tæt observation og kommunikation med den ordinerende læge. Clomipraminhydrochlorid er ikke godkendt til brug hos pædiatriske patienter undtagen til patienter med obsessiv-kompulsiv lidelse (OCD) (se ADVARSLER , Klinisk forværring og selvmordsrisiko ; PATIENTOPLYSNINGER ; og FORHOLDSREGLER , Pædiatrisk brug ).
BESKRIVELSE
Anafranil™ (clomipraminhydrochlorid) kapsler USP er et antiobsessionelt lægemiddel, der tilhører klassen (dibenzazepin) af farmakologiske midler kendt som tricykliske antidepressiva. Anafranil fås som kapsler på 25, 50 og 75 mg til oral administration.
Clomipraminhydrochlorid USP er 3-chlor-5-[3-(dimethylamino)propyl]-10,11-dihydro5H-dibenz[b,f]azepinmonohydrochlorid, og dets strukturformel er:
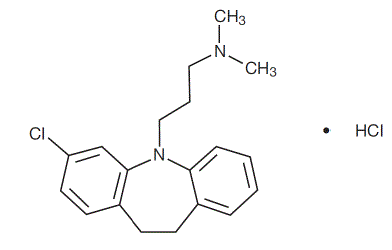
C19H23ClN2 • HCI MW = 351,31
Clomipraminhydrochlorid USP er et hvidt til råhvidt krystallinsk pulver. Det er frit opløseligt i vand, i methanol og i methylenchlorid og uopløseligt i ethylether og i hexan.
Inaktive ingredienser. D&C Red No. 33 (kun 25 mg kapsler), D&C Yellow No. 10, FD&C Blue No. 1 (kun 50 mg kapsler), FD&C Yellow No. 6, gelatine, magnesiumstearat, methylparaben, propylparaben, stivelse (majs), og titaniumdioxid.
INDIKATIONER
Anafranil™ (clomipraminhydrochlorid) kapsler USP er indiceret til behandling af tvangstanker og tvangshandlinger hos patienter med obsessiv-kompulsiv lidelse (OCD). Tvangstanker eller tvangstanker skal forårsage markant nød, være tidskrævende eller væsentligt forstyrre social eller erhvervsmæssig funktion for at opfylde DSM-III-R (ca. 1989) diagnosen OCD.
Tvangstanker er tilbagevendende, vedvarende ideer, tanker, billeder eller impulser, der er ego-dystoniske. Tvangshandlinger er gentagne, målrettede og bevidste adfærd, der udføres som reaktion på en besættelse eller på en stereotyp måde, og er anerkendt af personen som overdreven eller urimelig.
Effektiviteten af Anafranil 25 mg til behandling af OCD blev påvist i multicenter, placebokontrollerede parallelgruppeundersøgelser, herunder to 10-ugers undersøgelser med voksne og en 8-ugers undersøgelse med børn og unge i alderen 10 til 17 år. Patienter i alle undersøgelser havde moderat til svær OCD (DSM-III), med gennemsnitlige baseline ratings på Yale-Brown Obsessive Compulsive Scale (YBOCS) varierende fra 26 til 28 og en gennemsnitlig baseline rating på 10 på NIMH Clinical Global Obsessive Compulsive Scale (NIMH-OC). Patienter, der tog CMI, oplevede en gennemsnitlig reduktion på cirka 10 på YBOCS, hvilket repræsenterer en gennemsnitlig forbedring på denne skala på 35 % til 42 % blandt voksne og 37 % blandt børn og unge. CMI-behandlede patienter oplevede et fald på 3,5 enheder på NIMH-OC. Patienter på placebo viste ingen vigtig klinisk respons på nogen af skalaerne. Den maksimale dosis var 250 mg/dag for de fleste voksne og 3 mg/kg/dag (op til 200 mg) for alle børn og unge.
Effektiviteten af Anafranil 25 mg til langtidsbrug (dvs. i mere end 10 uger) er ikke blevet systematisk evalueret i placebokontrollerede forsøg. Lægen, der vælger at bruge Anafranil 10mg i længere perioder, bør med jævne mellemrum revurdere lægemidlets langsigtede anvendelighed for den enkelte patient (se DOSERING OG ADMINISTRATION ).
DOSERING OG ADMINISTRATION
Behandlingsregimerne beskrevet nedenfor er baseret på dem, der blev brugt i kontrollerede kliniske forsøg med Anafranil 50 mg hos 520 voksne og 91 børn og unge med OCD. Under indledende titrering bør Anafranil gives i opdelte doser med måltider for at reducere gastrointestinale bivirkninger. Målet med denne indledende titreringsfase er at minimere bivirkninger ved at tillade tolerance over for bivirkninger at udvikle sig eller give patienten tid til at tilpasse sig, hvis tolerance ikke udvikler sig.
Da både CMI og dets aktive metabolit, DMI, har lange eliminationshalveringstider, bør den ordinerende læge tage i betragtning, at steady-state plasmaniveauer muligvis ikke opnås før 2 til 3 uger efter dosisændring (se KLINISK FARMAKOLOGI ). Derfor kan det efter indledende titrering være hensigtsmæssigt at vente 2 til 3 uger mellem yderligere dosisjusteringer.
Indledende behandling/dosisjustering (voksne)
Behandling med Anafranil 25 mg bør påbegyndes med en dosis på 25 mg dagligt og gradvist øges, som tolereret, til ca. 100 mg i løbet af de første 2 uger. Under den indledende titrering bør Anafranil 50 mg gives i opdelte doser med måltider for at reducere gastrointestinale bivirkninger. Derefter kan dosis øges gradvist over de næste adskillige uger, op til et maksimum på 250 mg dagligt. Efter titrering kan den samlede daglige dosis gives én gang dagligt ved sengetid for at minimere sedation i dagtimerne.
Indledende behandling/dosisjustering (børn og unge)
Som for voksne er startdosis 25 mg dagligt og bør gradvist øges (også givet i opdelte doser med måltider for at reducere gastrointestinale bivirkninger) i løbet af de første 2 uger, som tolereret, op til et dagligt maksimum på 3 mg/kg eller 100 mg, alt efter hvad der er mindst. Derefter kan dosis øges gradvist over de næste adskillige uger op til et dagligt maksimum på 3 mg/kg eller 200 mg, alt efter hvad der er mindst (se FORHOLDSREGLER , Pædiatrisk brug ). Som for voksne kan den samlede daglige dosis efter titrering gives én gang dagligt ved sengetid for at minimere sedation i dagtimerne.
Vedligeholdelse/fortsættelsesbehandling (voksne, børn og unge)
Selvom der ikke er nogen systematiske undersøgelser, der besvarer spørgsmålet om, hvor længe man skal fortsætte Anafranil 10mg, er OCD en kronisk tilstand, og det er rimeligt at overveje fortsættelse for en responderende patient. Selvom effekten af Anafranil 50 mg efter 10 uger ikke er blevet dokumenteret i kontrollerede undersøgelser, er patienterne fortsat i behandling under dobbeltblinde tilstande i op til 1 år uden tab af fordele. Der bør dog foretages dosisjusteringer for at fastholde patienten på den laveste effektive dosis, og patienterne bør periodisk revurderes for at bestemme behovet for behandling. Under vedligeholdelse kan den samlede daglige dosis gives én gang dagligt ved sengetid.
At skifte en patient til eller fra en monoaminoxidasehæmmer (MAOI), beregnet til at behandle psykiatriske lidelser
Der bør gå mindst 14 dage mellem seponering af en MAO-hæmmer beregnet til behandling af psykiatriske lidelser og påbegyndelse af behandling med Anafranil. Omvendt bør der tillades mindst 14 dage efter ophør med Anafranil, før man starter en MAO-hæmmer beregnet til behandling af psykiatriske lidelser (se KONTRAINDIKATIONER ).
Brug af Anafranil 25mg med andre MAO-hæmmere, såsom linezolid eller methylenblåt
Start ikke Anafranil 50 mg hos en patient, der behandles med linezolid eller intravenøs methylenblåt, fordi der er øget risiko for serotonergt syndrom. Hos en patient, som kræver mere akut behandling af en psykiatrisk tilstand, bør andre indgreb, herunder hospitalsindlæggelse, overvejes (se KONTRAINDIKATIONER ).
nogle tilfælde kan en patient, der allerede får Anafranil 25 mg-behandling, have behov for akut behandling med linezolid eller intravenøs methylenblåt. Hvis acceptable alternativer til linezolid eller intravenøs methylenblåt behandling ikke er tilgængelige, og de potentielle fordele ved linezolid eller intravenøs methylenblåt behandling vurderes at opveje risikoen for serotonergt syndrom hos en bestemt patient, bør Anafranil stoppes omgående, og linezolid eller intravenøs methylenblåt kan administreres. Patienten skal overvåges for symptomer på serotonergt syndrom i to uger eller indtil 24 timer efter den sidste dosis linezolid eller intravenøs methylenblåt, alt efter hvad der kommer først. Behandling med Anafranil kan genoptages 24 timer efter den sidste dosis linezolid eller intravenøs methylenblåt (se ADVARSLER ).
Risikoen ved at administrere methylenblåt ad ikke-intravenøse veje (såsom orale tabletter eller ved lokal injektion) eller i intravenøse doser meget lavere end 1 mg/kg med Anafranil 50 mg er uklar. Lægen bør ikke desto mindre være opmærksom på muligheden for opståede symptomer på serotonergt syndrom ved sådan brug (se ADVARSLER ).
HVORDAN LEVERET
Anafranil™ (clomipraminhydrochlorid) kapsler USP
Kapsler 25 mg – elfenbenskrop præget i sort med "M" og melon-gul hætte præget i sort med "ANAFRANIL 25 mg"
Flasker á 30………....………...……….....……… … NDC 0406-9906-03
Kapsler 50 mg – elfenbenskrop præget i sort med "M" og aquablå hætte præget i sort med "ANAFRANIL 50 mg"
Flasker på 30………..………....………...………... ..…NDC 0406-9907-03
Kapsler 75 mg – elfenbenskrop præget i sort med "M" og gul hætte præget i sort med "ANAFRANIL 75 mg"
Flasker á 30………..………...……….....……….. ..…NDC 0406-9908-03
Opbevaring
Opbevares ved 20° til 25°C (68° til 77°F) [se USP kontrolleret rumtemperatur ].
Dispenser i godt lukkede beholdere med børnesikret lukning. Beskyt mod fugt.
Dyretoksikologi
Fosfolipidose og testikelforandringer, almindeligvis forbundet med tricykliske forbindelser, er blevet observeret med Anafranil. I kroniske rotteundersøgelser bestod ændringer relateret til Anafranil 50 mg af systemisk fosfolipidose, ændringer i testiklerne (atrofi, mineralisering) og sekundære ændringer i andet væv. Derudover blev der observeret hjertetrombose og dermatitis/keratitis hos rotter behandlet i 2 år ved doser, der var henholdsvis 24 og 10 gange den maksimalt anbefalede humane daglige dosis (MRHD) på mg/kg-basis og 4 og 1,5 gange MRHD på mg/m²-basis.
Mallinckrodt, mærket "M", Mallinckrodt Pharmaceuticals-logoet, M Â og andre mærker er varemærker tilhørende en Mallinckrodt-virksomhed.
Fremstillet af: Patheon Inc., Whitby, Ontario, Canada, L1N 5Z5 for SpecGx LLC, Webster Groves, MO 63119 USA. Revideret: Marts 2019
BIVIRKNINGER
Almindelig observeret
De mest almindeligt observerede bivirkninger forbundet med brugen af Anafranil 10 mg og ikke set i en tilsvarende hyppighed blandt placebo-behandlede patienter var gastrointestinale lidelser, herunder mundtørhed, forstoppelse, kvalme, dyspepsi og anoreksi; nervesystemets plager, herunder somnolens, tremor, svimmelhed, nervøsitet og myoklonus; genitourinære lidelser, herunder ændret libido, ejakulationssvigt, impotens og vandladningsforstyrrelser; og andre diverse klager, herunder træthed, svedtendens, øget appetit, vægtøgning og synsforandringer.
Fører til seponering af behandling
Ca. 20 % af 3616 patienter, som fik Anafranil i amerikanske præmarketing kliniske forsøg, afbrød behandlingen på grund af en bivirkning. Cirka halvdelen af de patienter, der seponerede (9 % af det samlede antal) havde flere klager, hvoraf ingen kunne klassificeres som primære. Hvor en primær årsag til seponering kunne identificeres, afbrød de fleste patienter på grund af nervesystemplager (5,4%), primært somnolens. Den næsthyppigste årsag til seponering var fordøjelsessystemets plager (1,3 %), primært opkastning og kvalme.
Der var ingen tilsyneladende sammenhæng mellem bivirkningerne og forhøjede plasmakoncentrationer af lægemiddel.
Forekomst i kontrollerede kliniske forsøg
Følgende tabel opregner bivirkninger, der forekom med en forekomst på 1 % eller mere blandt patienter med OCD, som fik Anafranil 10 mg i placebokontrollerede kliniske studier for voksne eller pædiatriske. Hyppighederne blev opnået fra poolede data fra kliniske forsøg, der involverede enten voksne, der fik Anafranil (N=322) eller placebo (N=319) eller børn behandlet med Anafranil (N=46) eller placebo (N=44). Den ordinerende læge skal være opmærksom på, at disse tal ikke kan bruges til at forudsige forekomsten af bivirkninger i løbet af sædvanlig lægepraksis, hvor patientkarakteristika og andre faktorer adskiller sig fra dem, der var fremherskende i de kliniske forsøg. Tilsvarende kan de nævnte frekvenser ikke sammenlignes med tal opnået fra andre kliniske undersøgelser, der involverer forskellige behandlinger, anvendelser og efterforskere. De citerede tal giver imidlertid lægen et grundlag for at estimere det relative bidrag fra lægemiddel- og ikke-lægemiddelfaktorer til forekomsten af bivirkninger i de undersøgte populationer.
Forekomst af behandlingsfremspringende bivirkninger i placebokontrollerede kliniske forsøg (procentdel af patienter, der rapporterer hændelse)
Andre hændelser observeret under præmarketing-evalueringen af Anafranil
Under kliniske forsøg i USA blev flere doser Anafranil 50 mg administreret til ca. 3600 forsøgspersoner. Uheldige hændelser forbundet med denne eksponering blev registreret af kliniske efterforskere ved hjælp af terminologi efter eget valg. Det er derfor ikke muligt at give et meningsfuldt skøn over andelen af individer, der oplever uønskede hændelser, uden først at gruppere lignende typer af uheldige hændelser i et mindre antal standardiserede hændelseskategorier.
de efterfølgende tabeller er en ændret terminologiordbog fra Verdenssundhedsorganisationen blevet brugt til at klassificere rapporterede uønskede hændelser. De præsenterede frekvenser repræsenterer derfor andelen af de 3525 individer, der blev eksponeret for Anafranil, som oplevede en hændelse af den type, der er nævnt ved mindst én lejlighed, mens de fik Anafranil. Alle hændelser er inkluderet undtagen dem, der allerede er anført i den foregående tabel, dem, der er rapporteret i termer, der er så generelle, at de er uinformative, og dem, hvor en forbindelse med stoffet var fjern. Det er vigtigt at understrege, at selvom de rapporterede hændelser opstod under behandling med Anafranil, var de ikke nødvendigvis forårsaget af det.
Hændelser er yderligere kategoriseret efter kropssystem og listet i rækkefølge efter faldende frekvens ifølge følgende definitioner: hyppige bivirkninger er dem, der forekommer ved en eller flere lejligheder hos mindst 1/100 patienter; sjældne bivirkninger er dem, der forekommer hos 1/100 til 1/1000 patienter; sjældne hændelser er dem, der forekommer hos mindre end 1/1000 patienter.
Kroppen som helhed - Sjælden - generelt ødem, øget modtagelighed for infektion, utilpashed. Sjælden - afhængig ødem, abstinenssyndrom.
Kardiovaskulære system - Sjælden - unormalt EKG, arytmi, bradykardi, hjertestop, ekstrasystoler, bleghed. Sjælden - aneurisme, atrieflimren, bundtgrenblok, hjertesvigt, hjerneblødning, hjerteblokering, myokardieinfarkt, myokardieiskæmi, perifer iskæmi, tromboflebitis, vasospasme, ventrikulær takykardi.
Fordøjelsessystemet - Sjælden - unormal leverfunktion, blod i afføringen, colitis, duodenitis, mavesår, gastritis, gastroøsofageal refluks, tandkødsbetændelse, glossitis, hæmorider, hepatitis, øget spyt, irritabel tyktarm, mavesår, rektal blødning, ulceration i tungen,. Sjælden - cheilitis, kronisk enteritis, misfarvet afføring, gastrisk dilatation, tandkødsblødning, hikke, intestinal obstruktion, oral/pharyngealt ødem, paralytisk ileus, spytkirtelforstørrelse.
Endokrine system - Sjælden - hypothyroidisme. Sjælden - struma, gynækomasti, hyperthyroidisme.
Hemisk og lymfesystem - Sjælden - lymfadenopati. Sjælden - leukemreaktion, lymfomlignende lidelse, marvsdepression.
Metabolisk og ernæringsforstyrrelse - Sjælden - dehydrering, diabetes mellitus, gigt, hyperkolesterolæmi, hyperglykæmi, hyperurikæmi, hypokaliæmi. Sjælden - fedtintolerance, glykosuri.
Muskuloskeletale system - Sjælden - artrose. Sjælden - dystoni, eksostose, lupus erythematosus udslæt, blå mærker, myopati, myositis, polyarteritis nodosa, torticollis.
Nervesystem - Hyppig - unormal tænkning, svimmelhed. Sjældent - unormal koordination, unormal EEG, unormal gang, apati, ataksi, koma, kramper, delirium, vrangforestillinger, dyskinesi, dysfoni, encefalopati, eufori, ekstrapyramidal lidelse, hallucinationer, fjendtlighed, hyperkinesi, hypnagogiske hallucinationer, benkrampe-hallucinationer, benreaktion. , neuralgi, paranoia, fobisk lidelse, psykose, føleforstyrrelser, somnambulisme, stimulering, selvmordstanker, selvmordsforsøg, tænderskæren. Sjælden - antikolinergt syndrom, afasi, apraksi, katalepsi, kolinergt syndrom, choreoathetosis, generaliseret spasmer, hemiparese, hyperæstesi, hyperrefleksi, hypoæstesi, illusion, nedsat impulskontrol, ubeslutsomhed, mutisme, neuromusisk reaktion, neuropatisk nervesygdom, ocu nysmotorisk krise , stupor, selvmord.
Åndedrætsorganerne - Sjælden - bronkitis, hyperventilation, øget sputum, lungebetændelse. Sjælden - cyanose, hæmoptyse, hypoventilation, laryngismus.
Hud og vedhæng - Sjælden - alopeci, cellulitis, cyste, eksem, erytematøst udslæt, genital pruritus, makulopapulært udslæt, lysfølsomhedsreaktion, psoriasis, pustulært udslæt, misfarvning af huden. Sjælden - chloasma, folliculitis, hypertrichosis, piloerektion, seborrhea, hudhypertrofi, hudsår.
Særlige sanser - Sjælden - unormal akkommodation, døvhed, diplopi, ørepine, øjensmerter, fremmedlegemefornemmelse, hyperakusis, parosmi, fotofobi, skleritis, smagstab. Sjælden - blepharitis, kromatopsi, konjunktival blødning, exophthalmos, glaukom, keratitis, labyrintlidelse, natteblindhed, nethindelidelse, strabismus, synsfeltdefekt.
Urogenitale system - Sjælden - endometriose, epididymitis, hæmaturi, nocturi, oliguri, ovariecyste, perineal smerte, polyuri, prostatasygdom, renal calculus, nyresmerter, urinrørsforstyrrelser, urininkontinens, livmoderblødning, vaginal blødning. Sjælden - albuminuri, anorgasmi, brystforstørrelse, brystfibroadenose, cervikal dysplasi, endometriehyperplasi, for tidlig ejakulation, pyelonefritis, pyuri, nyrecyste, uterinbetændelse, vulvalidelse.
Postmarketing oplevelse
Følgende bivirkning er blevet rapporteret under brug af Anafranil efter godkendelse. Fordi denne reaktion rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt at estimere hyppigheden pålideligt.
Øjenlidelser - Vinkellukkende glaukom.
Forstyrrelser i immunsystemet - Lægemiddeludslæt med eosinofili og systemiske symptomer (DRESS).
Metabolisme og ernæringsforstyrrelser - Hyponatriæmi.
Endokrine lidelser - Syndrom af uhensigtsmæssig antidiuretisk hormonsekretion (SIADH).
DRUGSINTERAKTIONER
Risikoen ved at bruge Anafranil i kombination med andre lægemidler er ikke blevet systematisk evalueret. I betragtning af Anafranils primære CNS-virkninger tilrådes forsigtighed ved brug af det samtidig med andre CNS-aktive lægemidler (se PATIENT INFORMATION ). Anafranil bør ikke anvendes sammen med MAO-hæmmere (se KONTRAINDIKATIONER ).
Tæt overvågning og omhyggelig justering af dosis er påkrævet, når Anafranil administreres sammen med antikolinerge eller sympatomimetika.
Adskillige tricykliske antidepressiva er blevet rapporteret at blokere de farmakologiske virkninger af guanethidin, clonidin eller lignende midler, og en sådan virkning kan forventes med CMI på grund af dens strukturelle lighed med andre tricykliske antidepressiva.
Plasmakoncentrationen af CMI er blevet rapporteret at være øget ved samtidig administration af haloperidol; plasmaniveauer af flere nært beslægtede tricykliske antidepressiva er blevet rapporteret at blive øget ved samtidig administration af methylphenidat eller leverenzyminhibitorer (f.eks. cimetidin, fluoxetin) og faldet ved samtidig administration af leverenzyminducere (f.eks. barbiturater, phenytoin) og en sådan effekt kan også forventes med CMI. Administration af CMI er blevet rapporteret at øge plasmaniveauerne af phenobarbital, hvis det gives samtidig (se KLINISK FARMAKOLOGI , Interaktioner ).
Lægemidler metaboliseret af P450 2D6
Den biokemiske aktivitet af lægemidlets metaboliserende isozym cytochrom P450 2D6 (debrisoquinhydroxylase) er reduceret i en undergruppe af den kaukasiske befolkning (ca. 7% til 10% af kaukasiere er såkaldte "dårlige metabolisatorer"); pålidelige skøn over forekomsten af reduceret P450 2D6 isozymaktivitet blandt asiatiske, afrikanske og andre populationer er endnu ikke tilgængelige. Dårlige metabolisatorer har højere end forventet plasmakoncentrationer af tricykliske antidepressiva (TCA'er), når de gives sædvanlige doser. Afhængigt af fraktionen af lægemidlet, der metaboliseres af P450 2D6, kan stigningen i plasmakoncentration være lille eller ret stor (8 gange stigning i plasma AUC af TCA). Derudover hæmmer visse lægemidler aktiviteten af dette isozym og får normale metabolisatorer til at ligne dårlige metabolisatorer. Et individ, der er stabilt på en given dosis af TCA, kan blive brat toksisk, når det gives et af disse hæmmende lægemidler som samtidig behandling. De lægemidler, der hæmmer cytochrom P450 2D6, omfatter nogle, der ikke metaboliseres af enzymet (quinidin; cimetidin) og mange, der er substrater for P450 2D6 (mange andre antidepressiva, phenothiaziner og Type 1C antiarytmika propafenon og flecainid). Mens alle de selektive serotoningenoptagelseshæmmere (SSRI'er), f.eks. fluoxetin, sertralin, paroxetin og fluvoxamin, hæmmer P450 2D6, kan de variere i omfanget af inhibering. Fluvoxamin har også vist sig at hæmme P450 1A2, en isoform, der også er involveret i TCA-metabolisme. I hvilket omfang SSRI-TCA-interaktioner kan give kliniske problemer, vil afhænge af graden af hæmning og farmakokinetikken af det involverede SSRI. Ikke desto mindre er forsigtighed indiceret ved samtidig administration af TCA'er med nogen af SSRI'erne og også ved skift fra den ene klasse til den anden. Af særlig vigtighed skal der gå tilstrækkelig tid, før TCA-behandling påbegyndes hos en patient, der seponeres med fluoxetin, i betragtning af den lange halveringstid af forælderen og den aktive metabolit (mindst 5 uger kan være nødvendigt). Samtidig brug af midler i den tricykliske antidepressive klasse (som omfatter Anafranil) og lægemidler, der kan hæmme cytochrom P450 2D6, kan kræve lavere doser end normalt foreskrevet for enten det tricykliske antidepressivum eller det andet lægemiddel. Desuden kan en øget dosis af tricyklisk antidepressivt middel være påkrævet, når et af disse lægemidler trækkes ud af samtidig behandling. Det er ønskeligt at overvåge TCA-plasmaniveauer, når et middel af den tricykliske antidepressiva-klasse inklusive Anafranil skal administreres sammen med et andet lægemiddel, der vides at være en hæmmer af P450 2D6 (og/eller P450 1A2).
Da Anafranil er stærkt bundet til serumprotein, kan administration af Anafranil til patienter, der tager andre lægemidler, der er stærkt bundet til protein (f.eks. warfarin, digoxin), forårsage en stigning i plasmakoncentrationerne af disse lægemidler, hvilket potentielt kan resultere i bivirkninger. Omvendt kan bivirkninger skyldes fortrængning af proteinbundet Anafranil med andre stærkt bundne lægemidler (se KLINISK FARMAKOLOGI , Fordeling ).
Monoaminoxidasehæmmere (MAO-hæmmere)
(Se KONTRAINDIKATIONER , ADVARSLER , og DOSERING OG ADMINISTRATION .)
Serotonerge lægemidler
(Se KONTRAINDIKATIONER , ADVARSLER , og DOSERING OG ADMINISTRATION .)
Stofmisbrug og afhængighed
Anafranil er ikke blevet systematisk undersøgt hos dyr eller mennesker for dets potentiale for misbrug, tolerance eller fysisk afhængighed. Mens en række abstinenssymptomer er blevet beskrevet i forbindelse med seponering af Anafranil 50 mg (se FORHOLDSREGLER , Abstinenssymptomer ), er der ingen evidens for narkotikasøgende adfærd, bortset fra en enkelt rapport om potentielt Anafranil-misbrug af en patient med en historie med afhængighed af kodein, benzodiazepiner og flere psykoaktive stoffer. Patienten modtog Anafranil for depression og panikanfald og så ud til at blive afhængig efter udskrivning fra hospitalet.
På trods af manglen på beviser, der tyder på et misbrugsansvar for Anafranil i udenlandsk markedsføring, er det ikke muligt at forudsige, i hvilket omfang Anafranil kan blive misbrugt eller misbrugt, når først det er markedsført i USA. Derfor bør læger omhyggeligt vurdere patienterne for en historie med stofmisbrug og følge sådanne patienter tæt.
ADVARSLER
Klinisk forværring og selvmordsrisiko
Patienter med svær depressiv lidelse (MDD), både voksne og pædiatriske, kan opleve forværring af deres depression og/eller fremkomsten af selvmordstanker og -adfærd (suicidalitet) eller usædvanlige ændringer i adfærd, uanset om de tager antidepressiv medicin eller ej, og dette risikoen kan fortsætte, indtil der indtræffer betydelig remission. Selvmord er en kendt risiko for depression og visse andre psykiatriske lidelser, og disse lidelser er i sig selv de stærkeste forudsigere for selvmord. Der har imidlertid været en langvarig bekymring for, at antidepressiva kan have en rolle i at inducere forværring af depression og fremkomsten af suicidalitet hos visse patienter i de tidlige faser af behandlingen. Samlede analyser af kortsigtede placebokontrollerede forsøg med antidepressive lægemidler (SSRI'er og andre) viste, at disse lægemidler øger risikoen for selvmordstanker og -adfærd (suicidalitet) hos børn, unge og unge voksne (i alderen 18 til 24) med svær depression. lidelse (MDD) og andre psykiatriske lidelser. Korttidsundersøgelser viste ikke en stigning i risikoen for suicidalitet med antidepressiva sammenlignet med placebo hos voksne efter 24 år; der var en reduktion med antidepressiva sammenlignet med placebo hos voksne på 65 år og ældre.
De samlede analyser af placebokontrollerede forsøg med børn og unge med MDD, obsessiv-kompulsiv lidelse (OCD) eller andre psykiatriske lidelser omfattede i alt 24 korttidsforsøg med 9 antidepressive lægemidler hos over 4400 patienter. De samlede analyser af placebokontrollerede forsøg med voksne med MDD eller andre psykiatriske lidelser omfattede i alt 295 korttidsforsøg (median varighed på 2 måneder) med 11 antidepressive lægemidler hos over 77.000 patienter. Der var betydelig variation i risikoen for suicidalitet blandt stoffer, men en tendens til en stigning i de yngre patienter for næsten alle undersøgte stoffer. Der var forskelle i den absolutte risiko for suicidalitet på tværs af de forskellige indikationer, med den højeste forekomst af MDD. Risikoforskellene (lægemiddel versus placebo) var dog relativt stabile inden for aldersgrupper og på tværs af indikationer. Disse risikoforskelle (drugplaceboforskel i antallet af tilfælde af suicidalitet pr. 1000 behandlede patienter) er angivet i tabel 1.
Der forekom ingen selvmord i nogen af de pædiatriske forsøg. Der var selvmord i voksenforsøgene, men antallet var ikke tilstrækkeligt til at nå frem til nogen konklusion om lægemiddeleffekt på selvmord.
Det er uvist, om suicidalitetsrisikoen strækker sig til længerevarende brug, dvs. ud over flere måneder. Der er dog væsentlige beviser fra placebokontrollerede vedligeholdelsesforsøg hos voksne med depression, at brugen af antidepressiva kan forsinke tilbagefald af depression.
Alle patienter, der behandles med antidepressiva for enhver indikation, bør overvåges passende og observeres nøje for klinisk forværring, suicidalitet og usædvanlige ændringer i adfærd, især i løbet af de første par måneder af et lægemiddelbehandlingsforløb, eller i tidspunkter med dosisændringer, enten stigninger eller falder.
Følgende symptomer, angst, agitation, panikanfald, søvnløshed, irritabilitet, fjendtlighed, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshed), hypomani og mani er blevet rapporteret hos voksne og pædiatriske patienter, der også behandles med antidepressiva mod svær depressiv lidelse. som for andre indikationer, både psykiatriske og ikke-psykiatriske. Selvom der ikke er etableret en årsagssammenhæng mellem fremkomsten af sådanne symptomer og enten forværring af depression og/eller fremkomsten af selvmordsimpulser, er der bekymring for, at sådanne symptomer kan repræsentere forløbere for ny suicidalitet.
Det bør overvejes at ændre det terapeutiske regime, herunder eventuelt seponering af medicinen, hos patienter, hvis depression er vedvarende værre, eller som oplever ny suicidalitet eller symptomer, der kan være forløbere for forværring af depression eller suicidalitet, især hvis disse symptomer er alvorlige, pludselige i debut, eller var ikke en del af patientens tilstedeværende symptomer.
Familier og pårørende til patienter, der behandles med antidepressiva for svær depressiv lidelse eller andre indikationer, både psykiatriske og ikke-psykiatriske, bør advares om behovet for at overvåge patienter for fremkomsten af agitation, irritabilitet, usædvanlige ændringer i adfærd og de andre symptomer beskrevet ovenfor. , samt fremkomsten af suicidalitet, og at rapportere sådanne symptomer straks til sundhedsudbydere. Sådan overvågning bør omfatte daglig observation af familier og omsorgspersoner. Recepter for clomipraminhydrochlorid bør udskrives for den mindste mængde kapsler i overensstemmelse med god patientbehandling for at reducere risikoen for overdosering.
Screening af patienter for bipolar lidelse
En alvorlig depressiv episode kan være den første præsentation af bipolar lidelse. Det antages generelt (dog ikke etableret i kontrollerede forsøg), at behandling af en sådan episode med et antidepressivum alene kan øge sandsynligheden for udfældning af en blandet/manisk episode hos patienter med risiko for bipolar lidelse. Hvorvidt nogen af de ovenfor beskrevne symptomer repræsenterer en sådan omdannelse er ukendt. Inden behandling med et antidepressivum påbegyndes, bør patienter med depressive symptomer dog screenes tilstrækkeligt for at afgøre, om de har risiko for bipolar lidelse; sådan screening bør omfatte en detaljeret psykiatrisk historie, herunder en familiehistorie med selvmord, bipolar lidelse og depression. Det skal bemærkes, at clomipraminhydrochlorid ikke er godkendt til brug ved behandling af bipolar depression.
Serotonin syndrom
Udvikling af et potentielt livstruende serotonergt syndrom er blevet rapporteret med SNRI og SSRI, inklusive Anafranil 50 mg, alene, men især ved samtidig brug af andre serotonerge lægemidler (inklusive triptaner, tricykliske antidepressiva, fentanyl, lithium, tramadol, tryptofan, perikon) og med lægemidler, der hæmmer metabolismen af serotonin (især MAO-hæmmere, både dem, der er beregnet til at behandle psykiatriske lidelser og også andre, såsom linezolid og intravenøs methylenblåt).
Symptomer på serotonergt syndrom kan omfatte ændringer i mental status (f.eks. agitation, hallucinationer, delirium og koma), autonom ustabilitet (f.eks. takykardi, labilt blodtryk, svimmelhed, diaforese, rødmen, hypertermi), neuromuskulære ændringer (f.eks. tremor, rigiditet, myoklonus, hyperrefleksi, inkoordination), kramper og/eller gastrointestinale symptomer (f.eks. kvalme, opkastning, diarré). Patienter bør overvåges for forekomsten af serotonergt syndrom.
Samtidig brug af Anafranil 10 mg og MAO-hæmmere beregnet til behandling af psykiatriske lidelser er kontraindiceret. Anafranil 50mg bør heller ikke påbegyndes hos en patient, der er i behandling med MAO-hæmmere såsom linezolid eller intravenøs methylenblåt. Alle rapporter med methylenblåt, der gav information om indgivelsesvejen, involverede intravenøs administration i dosisområdet fra 1 mg/kg til 8 mg/kg. Ingen rapporter involverede administration af methylenblåt ad andre veje (såsom orale tabletter eller lokal vævsinjektion) eller ved lavere doser. Der kan være omstændigheder, hvor det er nødvendigt at påbegynde behandling med en MAO-hæmmer såsom linezolid eller intravenøs methylenblåt hos en patient, der tager Anafranil. Anafranil bør seponeres, før behandling med MAO-hæmmere påbegyndes (se KONTRAINDIKATIONER og DOSERING OG ADMINISTRATION ).
Hvis samtidig brug af Anafranil 10mg med andre serotonerge lægemidler, inklusive triptaner, tricykliske antidepressiva, fentanyl, lithium, tramadol, buspiron, tryptofan og perikon er klinisk berettiget, skal patienterne gøres opmærksomme på en potentiel øget risiko for serotonergt syndrom, især under behandlingsstart og dosisstigninger.
Behandling med Anafranil 10 mg og eventuelle samtidige serotonerge midler skal seponeres øjeblikkeligt, hvis ovennævnte hændelser opstår, og understøttende symptomatisk behandling bør påbegyndes.
Vinkel-lukkende glaukom
Pupiludvidelsen, der opstår efter brug af mange antidepressive lægemidler, herunder Anafranil, kan udløse et vinkellukkeangreb hos en patient med anatomisk snævre vinkler, som ikke har en patenteret iridektomi.
Anfald
Under evaluering før markedet blev anfald identificeret som den største risiko ved brug af Anafranil.
Den observerede kumulative forekomst af anfald blandt patienter eksponeret for Anafranil 25 mg i doser op til 300 mg/dag var 0,64 % efter 90 dage, 1,12 % efter 180 dage og 1,45 % efter 365 dage. De kumulative rater korrigerer råprocenten på 0,7 % (25 ud af 3519 patienter) for den variable eksponeringsvarighed i kliniske forsøg.
Selvom dosis ser ud til at være en prædiktor for anfald, er der en forvirring af dosis og varighed af eksponeringen, hvilket gør det vanskeligt uafhængigt at vurdere effekten af begge faktorer alene. Evnen til at forudsige forekomsten af anfald hos forsøgspersoner udsat for doser af CMI på over 250 mg er begrænset, da plasmakoncentrationen af CMI kan være dosisafhængig og kan variere blandt forsøgspersoner, der får den samme dosis. Ikke desto mindre rådes ordinerende læger til at begrænse den daglige dosis til maksimalt 250 mg til voksne og 3 mg/kg (eller 200 mg) til børn og unge (se DOSERING OG ADMINISTRATION ).
Der bør udvises forsigtighed ved administration af Anafranil 50 mg til patienter med en historie med anfald eller andre disponerende faktorer, f.eks. hjerneskade af varierende ætiologi, alkoholisme og samtidig brug med andre lægemidler, der sænker krampetærsklen.
Sjældne rapporter om dødsfald i forbindelse med anfald er blevet rapporteret af udenlandsk postmarketingovervågning, men ikke i amerikanske kliniske forsøg. I nogle af disse tilfælde var Anafranil blevet administreret sammen med andre epileptogene midler; i andre havde de involverede patienter muligvis prædisponerende medicinske tilstande. En årsagssammenhæng mellem behandling med Anafranil 25 mg og disse dødsfald er således ikke blevet fastslået.
Læger bør diskutere risikoen ved at tage Anafranil med patienter, mens de deltager i aktiviteter, hvor pludseligt bevidsthedstab kan resultere i alvorlig skade på patienten eller andre, f.eks. betjening af komplekse maskiner, kørsel, svømning, klatring.
KJOLE
Sjældne tilfælde af lægemiddeludslæt med eosinofili og systemiske symptomer (DRESS) er blevet rapporteret ved brug af clomipramin. I tilfælde af alvorlige akutte reaktioner, såsom DRESS, skal behandlingen med clomipramin afbrydes omgående og passende behandling igangsættes.
FORHOLDSREGLER
Generel
Selvmord
Da depression er et almindeligt associeret træk ved OCD, skal risikoen for selvmord overvejes. Recepter for Anafranil bør udskrives for den mindste mængde kapsler i overensstemmelse med god patientbehandling for at reducere risikoen for overdosering.
Kardiovaskulære effekter
Moderat ortostatisk blodtryksfald og beskeden takykardi blev hver især set hos ca. 20 % af patienterne, der tog Anafranil 10 mg i kliniske forsøg; men patienterne var ofte asymptomatiske. Blandt ca. 1400 patienter, der blev behandlet med CMI i præmarketingerfaringen, og som havde EKG'er, udviklede 1,5 % abnormiteter under behandlingen, sammenlignet med 3,1 % af patienterne, der fik aktive kontrollægemidler, og 0,7 % af patienterne, der fik placebo. De mest almindelige EKG-forandringer var PVC'er, ST-T-bølgeændringer og intraventrikulære ledningsabnormiteter. Disse ændringer var sjældent forbundet med signifikante kliniske symptomer. Ikke desto mindre er forsigtighed nødvendig ved behandling af patienter med kendt kardiovaskulær sygdom, og gradvis dosistitrering anbefales.
Psykose, forvirring og andre neuropsykiatriske fænomener
Patienter behandlet med Anafranil 10 mg er blevet rapporteret at vise en række neuropsykiatriske tegn og symptomer, herunder vrangforestillinger, hallucinationer, psykotiske episoder, forvirring og paranoia. På grund af den ukontrollerede karakter af mange af undersøgelserne er det umuligt at give et præcist skøn over omfanget af risikoen ved behandling med Anafranil. Som med tricykliske antidepressiva, som det er nært beslægtet med, kan Anafranil 25 mg udløse en akut psykotisk episode hos patienter med ikke-erkendt skizofreni.
Mani/hypomani
Under præmarketingtestning af Anafranil 10 mg hos patienter med affektiv lidelse blev hypomani eller mani udløst hos flere patienter. Aktivering af mani eller hypomani er også blevet rapporteret hos en lille del af patienter med affektiv lidelse behandlet med markedsførte tricykliske antidepressiva, som er tæt beslægtet med Anafranil.
Hepatiske ændringer
Under præmarketingtestning blev Anafranil lejlighedsvis forbundet med stigninger i SGOT og SGPT (sammenlagt forekomst på henholdsvis ca. 1 % og 3 %) af potentiel klinisk betydning (dvs. værdier større end 3 gange den øvre normalgrænse). I langt de fleste tilfælde var disse enzymstigninger ikke forbundet med andre kliniske fund, der tydede på leverskade; desuden var ingen gulsot. Sjældne rapporter om mere alvorlige leverskader, nogle dødelige, er blevet registreret i udenlandske erfaringer efter markedsføring. Forsigtighed er indiceret ved behandling af patienter med kendt leversygdom, og periodisk monitorering af leverenzymniveauer anbefales hos sådanne patienter.
Hæmatologiske ændringer
Selvom der ikke blev set nogen tilfælde af alvorlig hæmatologisk toksicitet i præmarketingerfaringen med Anafranil 25 mg, har der været postmarketingrapporter om leukopeni, agranulocytose, trombocytopeni, anæmi og pancytopeni i forbindelse med brug af Anafranil 50 mg. Ligesom det er tilfældet med tricykliske antidepressiva, som Anafranil 25 mg er nært beslægtet med, bør leukocyttal og differentielle blodtal opnås hos patienter, som udvikler feber og ondt i halsen under behandling med Anafranil.
Centralnervesystemet
Mere end 30 tilfælde af hypertermi er blevet registreret af non-domestic postmarketing overvågningssystemer. De fleste tilfælde opstod, når Anafranil blev brugt i kombination med andre lægemidler. Når Anafranil 25 mg og et neuroleptika blev brugt samtidigt, blev tilfældene nogle gange anset for at være eksempler på et malignt neuroleptikasyndrom.
Seksuel dysfunktion
Hyppigheden af seksuel dysfunktion hos mandlige patienter med OCD, som blev behandlet med Anafranil i præmarketingoplevelsen, var markant øget sammenlignet med placebokontroller (dvs. 42 % oplevede ejakulationssvigt og 20 % oplevede impotens sammenlignet med henholdsvis 2,0 % og 2,6 %, i placebogruppen). Cirka 85 % af mændene med seksuel dysfunktion valgte at fortsætte behandlingen.
Hyponatriæmi
Hyponatriæmi er opstået som følge af behandling med clomipramin. I mange tilfælde ser hyponatriæmi ud til at være resultatet af syndromet med uhensigtsmæssig antidiuretisk hormonsekretion (SIADH). Ældre patienter kan have større risiko for at udvikle hyponatriæmi med et serotonergt antidepressivum. Patienter, der tager diuretika, eller som på anden måde er udtømte, kan have større risiko. Seponering af Anafranil hos patienter med symptomatisk hyponatriæmi og passende medicinsk intervention bør iværksættes. Tegn og symptomer på hyponatriæmi omfatter hovedpine, koncentrationsbesvær, hukommelsessvækkelse, forvirring, svaghed og ustabilitet, som kan føre til fald. Mere alvorlige og/eller akutte tilfælde har inkluderet hallucinationer, synkope, krampeanfald, koma, åndedrætsstop og død.
Vægtændringer
kontrollerede undersøgelser af OCD blev vægtøgning rapporteret hos 18 % af patienterne, der fik Anafranil, sammenlignet med 1 % af patienterne, der fik placebo. I disse undersøgelser havde 28 % af patienterne, der fik Anafranil 25 mg, en vægtøgning på mindst 7 % af deres oprindelige kropsvægt sammenlignet med 4 % af patienterne, der fik placebo. Flere patienter havde vægtøgninger på over 25 % af deres oprindelige kropsvægt. Omvendt havde 5 % af patienterne, der fik Anafranil, og 1 %, der fik placebo, vægttab på mindst 7 % af deres oprindelige kropsvægt.
Elektrokonvulsiv terapi
Som med nært beslægtede tricykliske antidepressiva kan samtidig administration af Anafranil og elektrokonvulsiv behandling øge risikoen; en sådan behandling bør begrænses til de patienter, for hvem den er afgørende, da der er begrænset klinisk erfaring.
Kirurgi
Forud for elektiv kirurgi med generel anæstetika, bør behandling med Anafranil 50 mg seponeres, så længe det er klinisk muligt, og anæstesilægen bør underrettes.
Brug ved samtidig sygdom
Patienter med betydeligt nedsat nyrefunktion.
Abstinenssymptomer
En række abstinenssymptomer er blevet rapporteret i forbindelse med brat seponering af Anafranil 50 mg, herunder svimmelhed, kvalme, opkastning, hovedpine, utilpashed, søvnforstyrrelser, hypertermi og irritabilitet. Derudover kan sådanne patienter opleve en forværring af den psykiatriske status. Selvom abstinensvirkningerne af Anafranil 10 mg ikke er blevet systematisk evalueret i kontrollerede forsøg, er de velkendte med nært beslægtede tricykliske antidepressiva, og det anbefales, at dosis nedtrappes gradvist, og patienten overvåges nøje under seponering (se Stofmisbrug og afhængighed ).
Information til patienter
Ordinerende læger eller andre sundhedsprofessionelle bør informere patienter, deres familier og deres pårørende om fordele og risici forbundet med behandling med clomipraminhydrochlorid og bør rådgive dem om dens passende brug. En patientmedicineringsvejledning om "Antidepressiv medicin, depression og andre alvorlige psykiske sygdomme og selvmordstanker eller -handlinger" er tilgængelig for clomipraminhydrochlorid. Den ordinerende læge eller sundhedspersonalet bør instruere patienter, deres familier og deres pårørende i at læse medicinvejledningen og skal hjælpe dem med at forstå dens indhold. Patienterne skal have mulighed for at diskutere indholdet af medicinvejledningen og få svar på de spørgsmål, de måtte have. Hele teksten til medicinvejledningen er genoptrykt i slutningen af dette dokument.
Patienter bør informeres om følgende problemer og bedes om at advare deres ordinerende læge, hvis disse opstår, mens de tager clomipraminhydrochlorid.
Klinisk forværring og selvmordsrisiko
Patienter, deres familier og deres pårørende bør opmuntres til at være opmærksomme på fremkomsten af angst, agitation, panikanfald, søvnløshed, irritabilitet, fjendtlighed, aggressivitet, impulsivitet, akatisi (psykomotorisk rastløshed), hypomani, mani, andre usædvanlige ændringer i adfærd. , forværring af depression og selvmordstanker, især tidligt under antidepressiv behandling, og når dosis justeres op eller ned. Familier og pårørende til patienter bør rådes til at se efter forekomsten af sådanne symptomer på daglig basis, da ændringer kan være pludselige. Sådanne symptomer bør indberettes til patientens ordinerende læge eller sundhedspersonale, især hvis de er alvorlige, pludseligt opståede eller ikke var en del af patientens symptomer. Symptomer som disse kan være forbundet med en øget risiko for selvmordstanker og -adfærd og indikerer behov for meget tæt overvågning og muligvis ændringer i medicinen.
Læger rådes til at diskutere følgende problemer med patienter, som de ordinerer Anafranil til:
- Risikoen for anfald (se ADVARSLER );
- Den relativt høje forekomst af seksuel dysfunktion blandt mænd (se Seksuel dysfunktion );
- Da Anafranil 50mg kan svække de mentale og/eller fysiske evner, der kræves til udførelse af komplekse opgaver, og da Anafranil 25mg er forbundet med en risiko for anfald, bør patienter advares om udførelsen af komplekse og farlige opgaver (se ADVARSLER );
- Patienter bør advares om samtidig brug af alkohol, barbiturater eller andre CNS-depressiva, da Anafranil 50 mg kan overdrive deres reaktion på disse lægemidler;
- Patienter skal underrette deres læge, hvis de bliver gravide eller har til hensigt at blive gravide under behandlingen;
- Patienter skal underrette deres læge, hvis de ammer.
Patienter skal informeres om, at indtagelse af Anafranil kan forårsage mild pupiludvidelse, som hos følsomme personer kan føre til en episode med vinkel-lukkende glaukom. Eksisterende glaukom er næsten altid åbenvinklet glaukom, fordi vinkel-lukkende glaukom, når diagnosticeret, kan behandles definitivt med iridektomi. Åbenvinklet glaukom er ikke en risikofaktor for lukkevinklet glaukom. Patienter kan ønske at blive undersøgt for at afgøre, om de er modtagelige for vinkellukning, og have en profylaktisk procedure (f.eks. iridektomi), hvis de er modtagelige.
Karcinogenese, mutagenese, svækkelse af fertilitet
Der blev ikke fundet tegn på carcinogenicitet i to 2-årige bioassays i rotter ved doser op til 100 mg/kg, hvilket er 24 og 4 gange den maksimale anbefalede humane daglige dosis (MRHD) på henholdsvis mg/kg og mg/m² basis. , eller i et 2-årigt bioassay i mus i doser op til 80 mg/kg, hvilket er 20 og 1,5 gange MRHD på henholdsvis mg/kg og mg/m² basis.
reproduktionsundersøgelser blev der ikke fundet nogen effekt på fertiliteten hos rotter givet op til 24 mg/kg, hvilket er 6 gange og omtrent lig med MRHD på henholdsvis mg/kg og mg/m² basis.
Graviditetskategori C
Der blev ikke observeret teratogene effekter i undersøgelser udført på rotter og mus ved doser op til 100 mg/kg, hvilket er 24 gange den maksimale anbefalede daglige dosis til mennesker (MRHD) på mg/kg-basis og 4 gange (rotter) og 2 gange ( mus) MRHD på mg/m²-basis. Små uspecifikke embryo-/føtotoksiske virkninger blev set hos afkom fra behandlede rotter givet 50 og 100 mg/kg og af behandlede mus givet 100 mg/kg.
Der er ingen tilstrækkelige eller velkontrollerede undersøgelser af gravide kvinder. Abstinenssymptomer, herunder nervøsitet, rysten og anfald, er blevet rapporteret hos nyfødte, hvis mødre havde taget Anafranil 50 mg indtil fødslen. Anafranil 10 mg bør kun anvendes under graviditet, hvis den potentielle fordel opvejer den potentielle risiko for fosteret.
Ammende mødre
Anafranil er fundet i modermælk. På grund af risikoen for bivirkninger bør der tages en beslutning om, hvorvidt amningen skal afbrydes eller lægemidlet skal seponeres, under hensyntagen til lægemidlets betydning for moderen.
Pædiatrisk brug
Sikkerhed og effektivitet i den pædiatriske population, bortset fra pædiatriske patienter med OCD, er ikke blevet fastlagt (se KASSE ADVARSEL og ADVARSLER , Klinisk forværring og selvmordsrisiko ). Enhver, der overvejer at bruge Anafranil til et barn eller en teenager, skal balancere de potentielle risici med det kliniske behov.
I et kontrolleret klinisk forsøg med børn og unge (10 til 17 år) fik 46 ambulante patienter Anafranil 50 mg i op til 8 uger. Derudover har 150 unge patienter modtaget Anafranil 10 mg i åbne protokoller i perioder fra flere måneder til flere år. Af de 196 undersøgte unge var 50 13 år eller derunder, og 146 var 14 til 17 år. Bivirkningsprofilen i denne aldersgruppe (se BIVIRKNINGER ) svarer til det, der er observeret hos voksne.
De eventuelle risici, der kan være forbundet med Anafranils udvidede brug hos børn og unge med OCD, er ikke blevet systematisk vurderet. Evidensen, der understøtter konklusionen om, at Anafranil 50 mg er sikkert til brug hos børn og unge, stammer fra relativt kortsigtede kliniske undersøgelser og fra ekstrapolering af erfaringer med voksne patienter. Især er der ingen undersøgelser, der direkte evaluerer virkningerne af langtidsbrug af Anafranil 25 mg på vækst, udvikling og modning af børn og unge. Selvom der ikke er noget, der tyder på, at Anafranil 10 mg påvirker vækst, udvikling eller modning negativt, er fraværet af sådanne fund ikke tilstrækkeligt til at udelukke et potentiale for sådanne effekter ved kronisk brug.
Sikkerheden og effektiviteten hos pædiatriske patienter under 10 år er ikke fastlagt. Derfor kan der ikke gives specifikke anbefalinger for brugen af Anafranil til pædiatriske patienter under 10 år.
Geriatrisk brug
Kliniske undersøgelser af Anafranil 50 mg inkluderede ikke et tilstrækkeligt antal forsøgspersoner på 65 år og derover til at afgøre, om de reagerer anderledes end yngre forsøgspersoner; 152 patienter på mindst 60 år, der deltog i forskellige amerikanske kliniske forsøg, fik Anafranil i perioder på flere måneder til flere år. Ingen usædvanlige aldersrelaterede bivirkninger blev identificeret i denne population. Andre rapporterede kliniske erfaringer har ikke identificeret forskelle i respons mellem ældre og yngre patienter. Generelt bør dosisvalg for en ældre patient være forsigtigt, sædvanligvis begyndende i den lave ende af doseringsområdet, hvilket afspejler den større hyppighed af nedsat lever-, nyre- eller hjertefunktion og af samtidig sygdom eller anden lægemiddelbehandling.
Anafranil er blevet forbundet med tilfælde af klinisk signifikant hyponatriæmi. Ældre patienter kan have større risiko for denne bivirkning (se FORHOLDSREGLER , Hyponatriæmi ).
OVERDOSIS
Dødsfald kan forekomme som følge af overdosering med denne klasse af lægemidler. Indtagelse af flere lægemidler (herunder alkohol) er almindelig ved bevidst tricyklisk overdosis. Da håndteringen er kompleks og skiftende, anbefales det, at lægen kontakter en giftcentral for løbende information om behandlingen. Tegn og symptomer på toksicitet udvikler sig hurtigt efter tricyklisk overdosis. Derfor er hospitalsovervågning påkrævet hurtigst muligt.
Menneskelig oplevelse
amerikanske kliniske forsøg forekom 2 dødsfald i 12 rapporterede tilfælde af akut overdosering med Anafranil enten alene eller i kombination med andre lægemidler. Et dødsfald involverede en patient, der var mistænkt for at indtage en dosis på 7000 mg. Det andet dødsfald involverede en patient, der var mistænkt for at have indtaget en dosis på 5750 mg. De 10 ikke-dødelige tilfælde involverede doser på op til 5000 mg, ledsaget af plasmaniveauer på op til 1010 ng/ml. Alle 10 patienter kom sig fuldstændigt. Blandt rapporter fra andre lande om overdosis af Anafranil var den laveste dosis forbundet med dødsfald 750 mg. Baseret på rapporter efter markedsføring i Det Forenede Kongerige anses CMI's dødelighed ved overdosis for at svare til den, der er rapporteret for nært beslægtede tricykliske forbindelser, der markedsføres som antidepressiva.
Manifestationer
Tegn og symptomer varierer i sværhedsgrad afhængigt af faktorer såsom mængden af absorberet lægemiddel, patientens alder og den tid, der er gået siden lægemiddelindtagelse. Kritiske manifestationer af overdosering omfatter hjerterytmeforstyrrelser, alvorlig hypotension, kramper og CNS-depression inklusive koma. Ændringer i elektrokardiogrammet, især i QRS-aksen eller -bredden, er klinisk signifikante indikatorer for tricyklisk toksicitet. Andre CNS-manifestationer kan omfatte døsighed, stupor, ataksi, rastløshed, agitation, delirium, svær sved, hyperaktive reflekser, muskelstivhed og athetoide og choreiforme bevægelser. Hjerteabnormiteter kan omfatte takykardi, tegn på kongestiv hjerteinsufficiens og i meget sjældne tilfælde hjertestop. Respirationsdepression, cyanose, shock, opkastning, hyperpyreksi, mydriasis og oliguri eller anuri kan også være til stede.
Ledelse
Få et EKG og påbegynd straks hjerteovervågning. Beskyt patientens luftveje, opret en intravenøs linje, og påbegynd gastrisk dekontaminering. Det er nødvendigt med minimum 6 timers observation med hjertemonitorering og observation for tegn på CNS eller respirationsdepression, hypotension, hjerterytmeforstyrrelser og/eller ledningsblokke og kramper.
Hvis der opstår tegn på toksicitet på noget tidspunkt i denne periode, er udvidet overvågning påkrævet. Der er tilfælde af patienter, der bukker under for fatale dysrytmier sent efter overdosering; disse patienter havde kliniske tegn på signifikant forgiftning før døden, og de fleste modtog utilstrækkelig gastrointestinal dekontaminering. Overvågning af plasmaniveauer af lægemiddel bør ikke vejlede behandlingen af patienten.
Gastrointestinal dekontaminering
Alle patienter, der mistænkes for tricyklisk overdosis, bør modtage gastrointestinal dekontaminering. Dette bør omfatte stor volumen maveskylning efterfulgt af aktivt kul. Hvis bevidstheden er svækket, skal luftvejene sikres før udskylning. Emesis er kontraindiceret.
Kardiovaskulær
En maksimal QRS-varighed på ≥ 0,10 sekunder kan være den bedste indikation på sværhedsgraden af overdoseringen. Intravenøst natriumbicarbonat bør anvendes for at opretholde serum-pH i området 7,45 til 7,55. Hvis pH-responsen er utilstrækkelig, kan hyperventilation også anvendes. Samtidig brug af hyperventilation og natriumbicarbonat bør ske med ekstrem forsigtighed med hyppig pH-overvågning. En pH >7,60 eller en pCO2
sjældne tilfælde kan hemoperfusion være gavnlig ved akut refraktær kardiovaskulær ustabilitet hos patienter med akut toksicitet. Hæmodialyse, peritonealdialyse, udvekslingstransfusioner og forceret diurese er dog generelt blevet rapporteret som ineffektive ved tricyklisk forgiftning.
CNS
Hos patienter med CNS-depression tilrådes tidlig intubation på grund af risikoen for pludselig forværring. Anfald bør kontrolleres med benzodiazepiner, eller hvis disse er ineffektive, andre antikonvulsiva (f.eks. phenobarbital, phenytoin). Physostigmin anbefales ikke undtagen til behandling af livstruende symptomer, der ikke har reageret på andre behandlinger, og da kun i samråd med et giftkontrolcenter.
Psykiatrisk opfølgning
Da overdosering ofte er bevidst, kan patienter forsøge selvmord på andre måder i genopretningsfasen. Psykiatrisk henvisning kan være passende.
Pædiatrisk ledelse
Principperne for håndtering af overdosering af børn og voksne er ens. Det anbefales kraftigt, at lægen kontakter det lokale giftkontrolcenter for specifik pædiatrisk behandling.
KONTRAINDIKATIONER
Anafranil er kontraindiceret hos patienter med en historie med overfølsomhed over for Anafranil 25 mg eller andre tricykliske antidepressiva.
Monoaminoxidasehæmmere (MAO-hæmmere)
Brugen af MAO-hæmmere beregnet til at behandle psykiatriske lidelser med Anafranil eller inden for 14 dage efter ophør med behandlingen med Anafranil er kontraindiceret på grund af en øget risiko for serotonergt syndrom. Brugen af Anafranil 10 mg inden for 14 dage efter ophør med en MAO-hæmmer beregnet til behandling af psykiatriske lidelser er også kontraindiceret (se ADVARSLER og DOSERING OG ADMINISTRATION ).
Start med Anafranil hos en patient, der er i behandling med linezolid eller intravenøs methylenblåt, er også kontraindiceret på grund af en øget risiko for serotonergt syndrom (se ADVARSLER og DOSERING OG ADMINISTRATION ).
Myokardieinfarkt
Anafranil er kontraindiceret i den akutte restitutionsperiode efter et myokardieinfarkt.
KLINISK FARMAKOLOGI
Farmakodynamik
Clomipramin (CMI) formodes at påvirke obsessiv og kompulsiv adfærd gennem dets virkninger på serotonerg neuronal transmission. Den egentlige neurokemiske mekanisme er ukendt, men CMI's evne til at hæmme genoptagelsen af serotonin (5-HT) menes at være vigtig.
Farmakokinetik
Absorption/Biotilgængelighed
CMI fra Anafranil 25mg kapsler er lige så biotilgængelig som CMI fra en opløsning. Biotilgængeligheden af CMI fra kapsler påvirkes ikke signifikant af fødevarer.
et dosisproportionalitetsstudie, der involverede flere CMI-doser, var steady-state plasmakoncentrationer (Css) og area-under-plasma-concentration-time-kurver (AUC) af CMI og CMI's vigtigste aktive metabolit, desmethylclomipramin (DMI), ikke proportionale med dosis over de vurderede områder, dvs. mellem 25 og 100 mg/dag og mellem 25 og 150 mg/dag, selvom Css og AUC er omtrent lineært relateret til dosis mellem 100 og 150 mg/dag. Forholdet mellem dosis og CMI/DMI-koncentrationer ved højere daglige doser er ikke blevet systematisk vurderet, men hvis der er signifikant dosisafhængighed ved doser over 150 mg/dag, er der potentiale for dramatisk højere Css og AUC, selv for patienter doseret inden for anbefalet rækkevidde. Dette kan udgøre en potentiel risiko for nogle patienter (se ADVARSLER og DRUGSINTERAKTIONER ).
Efter en enkelt 50 mg oral dosis forekommer maksimale plasmakoncentrationer af CMI inden for 2 til 6 timer (gennemsnit, 4,7 timer) og varierer fra 56 ng/ml til 154 ng/ml (gennemsnit, 92 ng/ml). Efter flere daglige doser på 150 mg Anafranil 25 mg varierer steady-state maksimale plasmakoncentrationer fra 94 ng/ml til 339 ng/ml (gennemsnit, 218 ng/ml) for CMI og fra 134 ng/ml til 532 ng/ml ( middel, 274 ng/mL) for DMI. Yderligere information fra et studie med stigende dosis af doser op til 250 mg tyder på, at DMI kan udvise ikke-lineær farmakokinetik over det sædvanlige doseringsområde. Ved en dosis af Anafranil 200 mg havde forsøgspersoner, som fik taget en enkelt blodprøve ca. 9 til 22 timer (median 16 timer) efter dosis, plasmakoncentrationer på op til 605 ng/ml for CMI, 781 ng/ml for DMI og 1386 ng/ml for begge.
Fordeling
CMI fordeler sig i cerebrospinalvæske (CSF) og hjerne og i modermælk. DMI fordeler sig også til CSF med et gennemsnitligt CSF/plasma-forhold på 2,6. Proteinbindingen af CMI er ca. 97%, primært til albumin, og er uafhængig af CMI-koncentrationen. Interaktionen mellem CMI og andre stærkt proteinbundne lægemidler er ikke blevet fuldt ud evalueret, men kan være vigtig (se DRUGSINTERAKTIONER ).
Metabolisme
CMI biotransformeres i vid udstrækning til DMI og andre metabolitter og deres glucuronidkonjugater. DMI er farmakologisk aktiv, men dets virkninger på OCD-adfærd er ukendt. Disse metabolitter udskilles i urin og fæces efter galdeliminering. Efter en 25 mg radioaktivt mærket dosis af CMI hos to forsøgspersoner blev henholdsvis 60 % og 51 % af dosis genfundet i urinen og henholdsvis 32 % og 24 % i fæces. I den samme undersøgelse var de kombinerede uringenvindinger af CMI og DMI kun omkring 0,8 % til 1,3 % af den administrerede dosis. CMI inducerer ikke lægemiddelmetaboliserende enzymer, målt ved antipyrinhalveringstid.
Elimination
Bevis for, at Css og AUC for CMI og DMI kan stige uforholdsmæssigt med stigende orale doser, tyder på, at metabolismen af CMI og DMI kan være kapacitetsbegrænset. Denne kendsgerning skal tages i betragtning ved vurdering af estimaterne af de farmakokinetiske parametre, der er præsenteret nedenfor, da disse blev opnået hos personer, der blev udsat for doser på 150 mg. Hvis farmakokinetikken af CMI og DMI er ikke-lineær ved doser over 150 mg, kan deres eliminationshalveringstider forlænges betydeligt ved doser nær den øvre ende af det anbefalede doseringsområde (dvs. 200 mg/dag til 250 mg/dag). Som følge heraf kan CMI og DMI akkumulere, og denne akkumulering kan øge forekomsten af enhver dosis- eller plasmakoncentrationsafhængige bivirkninger, især anfald (se ADVARSLER ).
Efter en dosis på 150 mg varierer halveringstiden for CMI fra 19 timer til 37 timer (gennemsnit, 32 timer), og halveringstiden for DMI varierer fra 54 timer til 77 timer (gennemsnitlig 69 timer). Steady-state-niveauer efter gentagen dosering nås typisk inden for 7 til 14 dage for CMI. Plasmakoncentrationerne af metabolitten overstiger moderlægemidlet ved gentagen dosering. Efter gentagen dosering med 150 mg/dag er akkumuleringsfaktoren for CMI cirka 2,5 og for DMI er 4,6. Det er vigtigt, at det kan tage to uger eller længere at opnå denne grad af akkumulering ved konstant dosering på grund af de relativt lange eliminationshalveringstider for CMI og DMI (se DOSERING OG ADMINISTRATION ). Virkningerne af nedsat lever- og nyrefunktion på dispositionen af Anafranil er ikke blevet fastslået.
Interaktioner
Samtidig administration af haloperidol og CMI øger plasmakoncentrationerne af CMI. Samtidig administration af CMI med phenobarbital øger plasmakoncentrationerne af phenobarbital (se DRUGSINTERAKTIONER ). Yngre forsøgspersoner (18 til 40 år) tolererede CMI bedre og havde signifikant lavere steady-state plasmakoncentrationer sammenlignet med forsøgspersoner over 65 år. Børn under 15 år havde signifikant lavere plasmakoncentration/dosisforhold sammenlignet med voksne. Plasmakoncentrationer af CMI var signifikant lavere hos rygere end hos ikke-rygere.
PATIENTOPLYSNINGER
Anafranil™ (clomipramin hydrochlorid) Kapsler USP
Antidepressiv medicin, depression og andre alvorlige psykiske sygdomme og selvmordstanker eller -handlinger
Læs medicinvejledningen, der følger med dig eller dit familiemedlems antidepressive medicin. Denne medicinvejledning handler kun om risikoen for selvmordstanker og -handlinger med antidepressiv medicin. Tal med din eller dit familiemedlems sundhedsplejerske om:
- alle risici og fordele ved behandling med antidepressiv medicin
- alle behandlingsvalg for depression eller anden alvorlig psykisk sygdom
Hvad er den vigtigste information, jeg bør vide om antidepressiv medicin, depression og andre alvorlige psykiske sygdomme og selvmordstanker eller -handlinger?
1. Antidepressiv medicin kan øge selvmordstanker eller -handlinger hos nogle børn, teenagere og unge voksne inden for de første par måneder af behandlingen.
2. Depression og andre alvorlige psykiske sygdomme er de vigtigste årsager til selvmordstanker og -handlinger. Nogle mennesker kan have en særlig høj risiko for at få selvmordstanker eller -handlinger. Disse omfatter personer, der har (eller har en familiehistorie med) bipolar sygdom (også kaldet maniodepressiv sygdom) eller selvmordstanker eller -handlinger.
3. Hvordan kan jeg holde øje med og forsøge at forhindre selvmordstanker og -handlinger hos mig selv eller et familiemedlem?
- Vær meget opmærksom på ændringer, især pludselige ændringer, i humør, adfærd, tanker eller følelser. Dette er meget vigtigt, når en antidepressiv medicin startes, eller når dosis ændres.
- Ring til sundhedsudbyderen med det samme for at rapportere nye eller pludselige ændringer i humør, adfærd, tanker eller følelser.
- Hold alle opfølgende besøg hos sundhedsplejersken som planlagt. Ring til lægen mellem besøgene efter behov, især hvis du har bekymringer om symptomer.
Ring til en sundhedsudbyder med det samme, hvis du eller dit familiemedlem har nogle af følgende symptomer, især hvis de er nye, værre eller bekymrer dig:
- tanker om selvmord eller døende
- forsøg på at begå selvmord
- ny eller værre depression
- ny eller værre angst
- føler sig meget ophidset eller rastløs
- Angstanfald
- søvnbesvær (søvnløshed)
- ny eller værre irritabilitet
- opfører sig aggressivt, er vred eller voldelig
- handler på farlige impulser
- en ekstrem stigning i aktivitet og tale (mani)
- andre usædvanlige ændringer i adfærd eller humør
Lavt saltniveau (natrium) i blodet. Ældre mennesker kan have større risiko for dette. Symptomer kan omfatte:
- hovedpine
- svaghed eller følelse ustabil
- forvirring, problemer med at koncentrere sig eller tænke eller hukommelsesproblemer
Visuelle problemer
- øjensmerter
- ændringer i synet
- hævelse eller rødme i eller omkring øjet
Kun nogle mennesker er i fare for disse problemer. Det kan være en god idé at gennemgå en øjenundersøgelse for at se, om du er i fare, og få forebyggende behandling, hvis du er det.
Hvem bør ikke tage Anafranil?
Tag ikke Anafranil, hvis du:
- tage en monoaminoxidasehæmmer (MAOI). Spørg din læge eller apotekspersonalet, hvis du ikke er sikker på, om du tager en MAO-hæmmer, inklusive antibiotikummet linezolid.
- Tag ikke en MAO-hæmmer inden for 2 uger efter at have stoppet Anafranil 25mg, medmindre din læge har bedt det om det.
- Start ikke med Anafranil, hvis du stoppede med at tage en MAO-hæmmer inden for de sidste 2 uger, medmindre din læge har bedt dig om det.
Hvad skal jeg ellers vide om antidepressiv medicin?
- Stop aldrig en antidepressiv medicin uden først at tale med en læge. Hvis du pludselig stopper en antidepressiv medicin, kan det forårsage andre symptomer.
- Antidepressiva er medicin, der bruges til at behandle depression og andre sygdomme. Det er vigtigt at diskutere alle risiciene ved behandling af depression og også risiciene ved ikke at behandle den. Patienter og deres familier eller andre pårørende bør diskutere alle behandlingsvalg med sundhedsudbyderen, ikke kun brugen af antidepressiva.
- Antidepressiv medicin har andre bivirkninger. Tal med lægen om bivirkningerne af den medicin, der er ordineret til dig eller dit familiemedlem.
- Antidepressiv medicin kan interagere med anden medicin. Kend alle de lægemidler, du eller dit familiemedlem tager. Hold en liste over alle lægemidler for at vise sundhedsudbyderen. Start ikke med ny medicin uden først at tjekke med din læge.
- Ikke alle antidepressive lægemidler ordineret til børn er FDA godkendt til brug hos børn. Tal med dit barns sundhedsplejerske for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Denne medicinvejledning er godkendt af US Food and Drug Administration.
