Plavix 75mg Clopidogrel Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Plavix 75mg, og hvordan bruges det?
Plavix 75mg er en receptpligtig medicin, der bruges til at behandle symptomer på akut koronarsyndrom såsom slagtilfælde, blodprop eller alvorlige hjerteproblemer efter et hjerteanfald, alvorlige brystsmerter eller kredsløbsproblemer. Plavix 75mg kan bruges alene eller sammen med anden medicin.
Plavix 75mg tilhører en klasse af lægemidler kaldet antiblodplademidler, kardiovaskulære, antiblodplademidler, hæmatologiske.
Det vides ikke, om Plavix er sikkert og effektivt til børn.
Hvad er de mulige bivirkninger af Plavix 75mg?
Plavix 75mg kan forårsage alvorlige bivirkninger, herunder:
- bleg hud,
- let blå mærker,
- lilla pletter under huden eller i munden,
- gulfarvning af din hud eller øjne (gulsot),
- hurtige hjerteslag,
- stakåndet,
- hovedpine,
- feber,
- svaghed,
- træthedsfornemmelse,
- lidt eller ingen vandladning,
- krampeanfald (kramper),
- pludselig følelsesløshed eller svaghed,
- forvirring, og
- problemer med syn eller tale
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Plavix omfatter:
- øget blødning,
- næseblod,
- hovedpine,
- kløe, og
- blå mærker
ADVARSEL
FORMINDET ANTIPLATELET EFFEKT HOS PATIENTER MED TO FUNKTIONSTABSALLELLER AF CYP2C19-GENET
Effektiviteten af Plavix 75 mg skyldes dets antiblodpladeaktivitet, som er afhængig af dets omdannelse til en aktiv metabolit af cytochrom P450 (CYP) systemet, primært CYP2C19 [se ADVARSLER OG FORHOLDSREGLER , KLINISK FARMAKOLOGI ]. Plavix ved anbefalede doser danner mindre af den aktive metabolit og har derfor en reduceret effekt på blodpladeaktivitet hos patienter, der er homozygote for ikke-funktionelle alleler af CYP2C19-genet (kaldet "CYP2C19-fattige metabolisatorer"). Tests er tilgængelige for at identificere patienter, der er CYP2C19-fattige metabolisatorer [se KLINISK FARMAKOLOGI ]. Overvej brug af en anden trombocyt-P2Y12-hæmmer hos patienter identificeret som CYP2C19-fattige metabolisatorer.
BESKRIVELSE
Plavix (clopidogrel bisulfat) er en thienopyridin-klassehæmmer af P2Y12 ADP-blodpladereceptorer. Kemisk er det methyl-(+)-(S)-a-(2-chlorphenyl)-6,7-dihydrothieno[3,2-c]pyridin-5(4H)-acetatsulfat (1:1). Den empiriske formel for clopidogrelbisulfat er C16H16ClNO2S•H2SO4 og dens molekylvægt er 419,9. Strukturformlen er som følger:

Clopidogrel bisulfat er et hvidt til råhvidt pulver. Det er praktisk talt uopløseligt i vand ved neutral pH, men frit opløseligt ved pH 1. Det opløses også frit i methanol, opløses sparsomt i methylenchlorid og er praktisk talt uopløseligt i ethylether. Den har en specifik optisk rotation på omkring +56°.
Plavix til oral administration leveres som enten lyserøde, runde, bikonvekse, prægede, filmovertrukne tabletter indeholdende 97,875 mg clopidogrelbisulfat, som er den molære ækvivalent af 75 mg clopidogrelbase eller lyserøde, aflange, prægede filmovertrukne tabletter indeholdende 391,5 mg af clopidogrel bisulfat, som er den molære ækvivalent af 300 mg clopidogrel base.
Hver tablet indeholder hydrogeneret ricinusolie, hydroxypropylcellulose, mannitol, mikrokrystallinsk cellulose og polyethylenglycol 6000 som inaktive ingredienser. Den lyserøde filmcoating indeholder jernoxid, hypromellose 2910, lactosemonohydrat, titaniumdioxid og triacetin. Tabletterne er poleret med Carnaubavoks.
INDIKATIONER
Akut koronarsyndrom (ACS)
- Plavix 75mg er indiceret til at reducere frekvensen af myokardieinfarkt (MI) og slagtilfælde hos patienter med ikke-ST-segment elevation ACS (ustabil angina [UA]/non-ST-elevation myokardieinfarkt [NSTEMI]), inklusive patienter, som skal behandles medicinsk og dem, der skal behandles med koronar revaskularisering. Plavix 75 mg bør administreres sammen med aspirin.
- Plavix er indiceret til at reducere frekvensen af myokardieinfarkt og slagtilfælde hos patienter med akut ST-elevation myokardieinfarkt (STEMI), som skal behandles medicinsk. Plavix 75 mg bør administreres sammen med aspirin.
Nylig hjerteinfarkt, nyligt slagtilfælde eller etableret perifer arteriel sygdom
Hos patienter med etableret perifer arteriel sygdom eller med en anamnese med nyligt myokardieinfarkt (MI) eller nyligt slagtilfælde er Plavix 75 mg indiceret til at reducere frekvensen af MI og slagtilfælde.
DOSERING OG ADMINISTRATION
Akut koronarsyndrom
Hos patienter, som har brug for en trombocythæmmende virkning inden for timer, påbegyndes Plavix med en enkelt 300 mg oral startdosis og derefter fortsættes med 75 mg én gang dagligt. Påbegyndelse af Plavix 75 mg uden en startdosis vil forsinke etableringen af en trombocythæmmende effekt med flere dage [se KLINISK FARMAKOLOGI og Kliniske Studier ].
Nylig hjerteinfarkt, nyligt slagtilfælde eller etableret perifer arteriel sygdom
75 mg én gang dagligt oralt uden en startdosis [se KLINISK FARMAKOLOGI og Kliniske Studier ].
HVORDAN LEVERET
Doseringsformer og styrker
- 75 mg tabletter: Lyserøde, runde, bikonvekse, filmovertrukne tabletter præget med "75" på den ene side og "1171" på den anden side
- 300 mg tabletter: Pink, aflange, filmovertrukne tabletter præget med "300" på den ene side og "1332" på den anden side
Opbevaring og håndtering
Plavix (clopidogrel bisulfat) 75 mg Tabletterne fås som lyserøde, runde, bikonvekse, filmovertrukne tabletter præget med "75" på den ene side og "1171" på den anden side. Tabletter leveres som følger:
NDC 63653-1171-6 flasker med 30 stk NDC 63653-1171-1 flasker med 90 stk NDC 63653-1171-5 flasker á 500 stk NDC 63653-1171-3 blærer på 100
Plavix (clopidogrel bisulfat) 300 mg Tabletterne fås som lyserøde, aflange filmovertrukne tabletter præget med "300" på den ene side og "1332" på den anden side. Tabletter leveres som følger:
NDC 63653-1332-2 Enhedsdosispakninger med 30 stk
Opbevares ved 25°C (77°F); udflugter tilladt til 15°C-30°C (59°F-86°F) [se USP kontrolleret rumtemperatur ].
Distribueret af: Bristol-Myers Squibb/Sanofi Pharmaceuticals Partnership, Bridgewater, NJ 08807. Revideret: Mar 2021
BIVIRKNINGER
Følgende alvorlige bivirkninger er beskrevet nedenfor og andre steder i mærkningen:
- Blødning [se ADVARSLER OG FORHOLDSREGLER ]
- Trombotisk trombocytopenisk purpura [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring med kliniske forsøg
Fordi kliniske forsøg udføres under vidt forskellige betingelser og varigheder af opfølgning, kan bivirkningsrater observeret i de kliniske forsøg med et lægemiddel ikke direkte sammenlignes med frekvenser i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de frekvenser, der observeres i praksis.
Plavix er blevet evalueret for sikkerhed hos mere end 54.000 patienter, herunder over 21.000 patienter behandlet i et år eller mere. De klinisk vigtige bivirkninger observeret i forsøg, der sammenligner Plavix 75 mg plus aspirin med placebo plus aspirin, og forsøg, der sammenligner Plavix alene med aspirin alene, diskuteres nedenfor.
Blødende
HELBREDE
I CURE var Plavix-brug sammen med aspirin forbundet med en stigning i større blødninger (primært gastrointestinale og på punktursteder) sammenlignet med placebo med aspirin (se tabel 1). Forekomsten af intrakraniel blødning (0,1 %) og dødelig blødning (0,2 %) var den samme i begge grupper. Andre blødningshændelser, der blev rapporteret hyppigere i clopidogrel-gruppen, var epistaxis, hæmaturi og blå mærker.
Den samlede forekomst af blødning er beskrevet i tabel 1.
BEGÅ
I COMMIT blev lignende hyppigheder af større blødninger observeret i Plavix 75 mg- og placebogruppen, som begge også fik aspirin (se tabel 2).
CAPRIE (Plavix vs Aspirin)
CAPRIE forekom gastrointestinale blødninger med en hastighed på 2,0 % hos dem, der tog Plavix 75 mg mod 2,7 % hos dem, der tog aspirin; indlæggelseskrævende blødning forekom hos henholdsvis 0,7 % og 1,1 %. Incidensen af intrakraniel blødning var 0,4 % for Plavix sammenlignet med 0,5 % for aspirin.
Andre blødningshændelser, der blev rapporteret hyppigere i Plavix 75 mg-gruppen, var epistaxis og hæmatom.
Andre uønskede hændelser
I CURE og CHARISMA, som sammenlignede Plavix plus aspirin med aspirin alene, var der ingen forskel i antallet af bivirkninger (bortset fra blødning) mellem Plavix og placebo.
I CAPRIE, som sammenlignede Plavix 75 mg med aspirin, blev kløe hyppigere rapporteret hos dem, der tog Plavix. Ingen anden forskel i antallet af uønskede hændelser (udover blødning) blev rapporteret.
Postmarketing oplevelse
Følgende bivirkninger er blevet identificeret under brug af Plavix efter godkendelse. Fordi disse reaktioner rapporteres frivilligt fra en population af ukendt størrelse, er det ikke altid muligt pålideligt at estimere deres hyppighed eller etablere en årsagssammenhæng til lægemiddeleksponering.
Der er rapporteret blødninger, inklusive dem med dødelig udgang, hos patienter behandlet med Plavix.
- Blod og lymfesystem: Agranulocytose, aplastisk anæmi/pancytopeni, trombotisk trombocytopenisk purpura (TTP), erhvervet hæmofili A
- Gastrointestinale lidelser: Colitis (inklusive ulcerøs eller lymfocytisk colitis), pancreatitis, stomatitis, mave-/duodenalsår, diarré
- Generelle lidelser og tilstand på administrationsstedet: Feber
- Lever og galdevejslidelser: Akut leversvigt, hepatitis (ikke-infektiøs), unormal leverfunktionstest
- Forstyrrelser i immunsystemet: Overfølsomhedsreaktioner, anafylaktoide reaktioner, serumsyge, insulin autoimmunt syndrom, som kan føre til alvorlig hypoglykæmi
- Sygdomme i bevægeapparatet, bindevæv og knogler: Myalgi, artralgi, gigt
- Forstyrrelser i nervesystemet: Smagsforstyrrelser, hovedpine, ageusia
- Psykiatriske lidelser: Forvirring, hallucinationer
- Åndedræts-, thorax- og mediastinumsygdomme: Bronkospasme, interstitiel pneumonitis, eosinofil pneumoni
- Nyre- og urinvejslidelser: Forøgede kreatininniveauer
- Hud- og subkutane vævssygdomme: Makulopapulært, erytematøst eller eksfoliativt udslæt, nældefeber, bulløs dermatitis, eksem, toksisk epidermal nekrolyse, Stevens-Johnsons syndrom, akut generaliseret eksantematøs pustulose (AGEP), angioødem, lægemiddelinduceret overfølsomhedssyndrom, lægemiddeludslæt med systemicinofili (DRESS), erythema multiforme, lichen planus, generaliseret pruritus
- Vaskulære lidelser: Vaskulitis, hypotension
DRUGSINTERAKTIONER
CYP2C19 inducere
Da clopidogrel metaboliseres til dets aktive metabolit delvist af CYP2C19, forventes brug af lægemidler, der inducerer aktiviteten af dette enzym, at resultere i øgede lægemiddelniveauer af den aktive metabolit af clopidogrel.
Rifampin inducerer kraftigt CYP2C19, hvilket resulterer i både et øget niveau af den aktive clopidogrel-metabolit og blodpladehæmning, hvilket især kan forstærke risikoen for blødning. Undgå for en sikkerheds skyld samtidig brug af stærke CYP2C19-inducere [se ADVARSLER OG FORHOLDSREGLER og KLINISK FARMAKOLOGI ].
CYP2C19-hæmmere
Clopidogrel metaboliseres til dets aktive metabolit delvist af CYP2C19. Samtidig brug af lægemidler, der hæmmer aktiviteten af dette enzym, resulterer i reducerede plasmakoncentrationer af den aktive metabolit af clopidogrel og en reduktion i blodpladehæmning [se ADVARSLER OG FORHOLDSREGLER ].
Omeprazol eller Esomeprazol
Undgå samtidig brug af Plavix 75 mg og omeprazol eller esomeprazol. I kliniske undersøgelser har omeprazol vist sig at reducere den trombocythæmmende aktivitet af Plavix 75 mg signifikant, når det gives samtidigt eller med 12 timers mellemrum. En tilsvarende reduktion i trombocythæmmende aktivitet blev observeret med esomeprazol, når det blev givet samtidig med Plavix. Dexlansoprazol, lansoprazol og pantoprazol havde mindre effekt på den blodpladehæmmende aktivitet af Plavix end omeprazol eller esomeprazol [se ADVARSLER OG FORHOLDSREGLER og KLINISK FARMAKOLOGI ].
Opioider
Som med andre orale P2Y12-hæmmere forsinker og reducerer samtidig administration af opioidagonister absorptionen af clopidogrel, formentlig på grund af langsommere mavetømning, hvilket resulterer i reduceret eksponering for dets metabolitter [se KLINISK FARMAKOLOGI ]. Overvej brugen af et parenteralt trombocythæmmende middel til patienter med akut koronarsyndrom, der kræver samtidig administration af morfin eller andre opioidagonister.
Ikke-steroide antiinflammatoriske lægemidler (NSAID'er)
Samtidig administration af Plavix 75 mg og NSAID'er øger risikoen for gastrointestinal blødning.
Warfarin (CYP2C9 substrater)
Selvom administration af clopidogrel 75 mg dagligt ikke ændrede farmakokinetikken af S-warfarin (et CYP2C9-substrat) eller INR hos patienter, der fik langvarig warfarinbehandling, øger samtidig administration af Plavix 75 mg og warfarin risikoen for blødning på grund af uafhængige virkninger på hæmostase.
Ved høje koncentrationer in vitro hæmmer clopidogrel imidlertid CYP2C9.
SSRI og SNRI
Da selektive serotoningenoptagelseshæmmere (SSRI'er) og serotonin-noradrenalin-genoptagelseshæmmere (SNRI'er) påvirker trombocytaktiveringen, kan samtidig administration af SSRI'er og SNRI'er med clopidogrel øge risikoen for blødning.
Repaglinid (CYP2C8-substrater)
Acyl-β-glucuronid-metabolitten af clopidogrel er en stærk hæmmer af CYP2C8. Plavix 75 mg kan øge den systemiske eksponering for lægemidler, der primært elimineres af CYP2C8, og derved kræve dosisjustering og passende monitorering.
Plavix øgede repaglinideksponeringen med 3,9 gange til 5,1 gange [se KLINISK FARMAKOLOGI ]. Undgå samtidig brug af repaglinid med Plavix. Hvis samtidig brug ikke kan undgås, påbegynd repaglinid med 0,5 mg før hvert måltid og overskrid ikke en samlet daglig dosis på 4 mg. Øget frekvens af glukosemonitorering kan være nødvendig ved samtidig brug.
ADVARSLER
Inkluderet som en del af FORHOLDSREGLER afsnit.
FORHOLDSREGLER
Nedsat trombocythæmmende aktivitet hos patienter med nedsat CYP2C19-funktion
Clopidogrel er et prodrug. Hæmning af trombocytaggregation af clopidogrel opnås gennem en aktiv metabolit. Metabolismen af clopidogrel til dets aktive metabolit kan forringes af genetiske variationer i CYP2C19 [se KASSET ADVARSEL ].
Metabolismen af clopidogrel kan også forringes af lægemidler, der hæmmer CYP2C19, såsom omeprazol eller esomeprazol. Undgå samtidig brug af Plavix og omeprazol eller esomeprazol, da begge dele signifikant reducerer Plavix's antiblodpladeaktivitet [se DRUGSINTERAKTIONER ].
Generel risiko for blødning
P2Y12-hæmmere (Thienopyridiner), inklusive Plavix, øger risikoen for blødning.
P2Y12-hæmmere (Thienopyridiner), hæmmer blodpladeaggregation i blodpladens levetid (7-10 dage). Da halveringstiden for clopidogrels aktive metabolit er kort, kan det være muligt at genoprette hæmostasen ved at administrere eksogene blodplader; trombocyttransfusioner inden for 4 timer efter startdosis eller 2 timer efter vedligeholdelsesdosis kan dog være mindre effektive.
Brug af lægemidler, der inducerer aktiviteten af CYP2C19, forventes at resultere i øgede lægemiddelniveauer af den aktive metabolit af clopidogrel og kan forstærke blødningsrisikoen. Undgå for en sikkerheds skyld samtidig brug af stærke CYP2C19-inducere [se DRUGSINTERAKTIONER og KLINISK FARMAKOLOGI ].
Seponering af Plavix
Seponering af Plavix øger risikoen for kardiovaskulære hændelser. Hvis Plavix midlertidigt skal seponeres (f.eks. for at behandle blødning eller til operation med stor blødningsrisiko), genstartes så hurtigt som muligt. Hvis det er muligt, afbrydes behandlingen med Plavix i fem dage før en sådan operation. Genoptag Plavix 75 mg, så snart hæmostase er opnået.
Trombotisk trombocytopenisk purpura (TTP)
TTP, nogle gange dødelig, er blevet rapporteret efter brug af Plavix 75 mg, nogle gange efter en kort eksponering ( BIVIRKNINGER ].
Krydsreaktivitet blandt thienopyridiner
Overfølsomhed inklusive udslæt, angioødem eller hæmatologisk reaktion er blevet rapporteret hos patienter, der får Plavix 75 mg, inklusive patienter med en historie med overfølsomhed eller hæmatologisk reaktion over for andre thienopyridiner [se KONTRAINDIKATIONER og BIVIRKNINGER ].
Patientrådgivningsinformation
Råd patienter til at læse FDA godkendt patientmærkning ( Medicinvejledning ).
Afbrydelse
Rådgive patienter om ikke at seponere Plavix uden først at have diskuteret det med den sundhedsplejerske, der har ordineret det [se ADVARSLER OG FORHOLDSREGLER ].
Blødende
Rådgiv patienterne, at de:
- vil lettere få blå mærker og bløde
- vil tage længere tid end normalt at stoppe blødningen
- skal rapportere enhver uventet, langvarig eller kraftig blødning eller blod i deres afføring eller urin [se ADVARSLER OG FORHOLDSREGLER ]
Trombotisk trombocytopenisk purpura
Instruer patienterne i at søge omgående lægehjælp, hvis de oplever symptomer på TTP, som ikke ellers kan forklares [se ADVARSLER OG FORHOLDSREGLER ].
Invasive procedurer
Rådgive patienter om at informere læger og tandlæger om, at de tager Plavix før enhver operation eller tandbehandling [se ADVARSLER OG FORHOLDSREGLER ].
Protonpumpehæmmere
Råd til patienter om ikke at tage omeprazol eller esomeprazol, mens de tager Plavix. Dexlansoprazol, lansoprazol og pantoprazol havde mindre udtalt effekt på den blodpladehæmmende aktivitet af Plavix 75 mg end omeprazol eller esomeprazol [se DRUGSINTERAKTIONER ].
Ikke-klinisk toksikologi
Karcinogenese, mutagenese, svækkelse af fertilitet
Der var ingen tegn på tumorigenicitet, når clopidogrel blev administreret i 78 uger til mus og 104 uger til rotter i doser på op til 77 mg/kg pr. dag, hvilket gav plasmaeksponeringer >25 gange større end hos mennesker ved den anbefalede daglige dosis på 75 mg.
Clopidogrel var ikke genotoksisk i fire in vitro-test (Ames-test, DNA-reparationstest i rottehepatocytter, genmutationsanalyse i kinesisk hamsterfibroblaster og metafase-kromosomanalyse af humane lymfocytter) og i én in vivo-test (mikronukleustest ad oral vej i mus).
Clopidogrel viste sig ikke at have nogen effekt på fertiliteten hos han- og hunrotter behandlet før parring og gennem hele drægtighedsperioden ved orale doser op til 400 mg/kg pr. dag (52 gange den anbefalede humane dosis på mg/m²-basis).
Brug i specifikke populationer
Graviditet
Risikooversigt
Tilgængelige data fra tilfælde rapporteret i publiceret litteratur og postmarketingovervågning med brug af clopidogrel hos gravide kvinder har ikke identificeret nogen lægemiddelrelaterede risici for alvorlige fødselsdefekter eller abort [se Data ].Der er risici for den gravide kvinde og foster forbundet med myokardieinfarkt og slagtilfælde [se Kliniske overvejelser ]. Der blev ikke observeret tegn på føtotoksicitet, når clopidogrel blev administreret til drægtige rotter og kaniner under organogenese i doser svarende til 65 og 78 gange den anbefalede daglige humane dosis [se Data ].
Den estimerede baggrundsrisiko for alvorlige fødselsdefekter og abort for de angivne populationer er ukendt. Alle graviditeter har en baggrundsrisiko for fødselsdefekter, tab eller andre ugunstige udfald. I den generelle befolkning i USA er den estimerede baggrundsrisiko for alvorlige fødselsdefekter og abort i klinisk anerkendte graviditeter henholdsvis 2 % til 4 % og 15 % til 20 %.
Kliniske overvejelser
Sygdomsassocieret moder- og/eller embryo-/fosterrisiko
Myokardieinfarkt og slagtilfælde er medicinske nødsituationer. Terapi til den gravide kvinde bør ikke tilbageholdes på grund af potentielle bekymringer vedrørende virkningerne af clopidogrel på fosteret.
Arbejde eller levering
Brug af clopidogrel under fødslen eller fødslen vil øge risikoen for moderblødning og blødning. Undgå neuraksial blokade under brug af clopidogrel på grund af risikoen for spinal hæmatom. Når det er muligt, afbryd behandlingen med clopidogrel 5 til 7 dage før fødsel, fødsel eller neuraksial blokade.
Data
Menneskelige data
De tilgængelige data fra offentliggjorte case-rapporter over to årtiers postmarketingbrug har ikke identificeret en sammenhæng med brug af clopidogrel under graviditet og alvorlige fødselsdefekter, abort eller uønskede føtale resultater.
Dyredata
Embryo-føtale udviklingstoksikologiske undersøgelser blev udført på drægtige rotter og kaniner med doser op til henholdsvis 500 og 300 mg/kg/dag administreret under organogenese. Disse doser, svarende til henholdsvis 65 og 78 gange den anbefalede daglige humane dosis, på mg/m²-basis, viste ingen tegn på nedsat fertilitet eller føtotoksicitet på grund af clopidogrel.
Amning
Risikooversigt
Der er ingen data om tilstedeværelsen af clopidogrel i modermælk eller virkningerne på mælkeproduktionen. Der er ikke observeret bivirkninger på ammede spædbørn ved brug af clopidogrel hos moderen under amning i et lille antal tilfælde efter markedsføring. Undersøgelser med rotter har vist, at clopidogrel og/eller dets metabolitter er til stede i mælken. Når et lægemiddel er til stede i animalsk mælk, er det sandsynligt, at lægemidlet vil være til stede i human mælk. De udviklingsmæssige og sundhedsmæssige fordele ved amning bør overvejes sammen med moderens kliniske behov for PLAVIX og eventuelle negative virkninger på det ammede spædbarn fra PLAVIX 75 mg eller fra underliggende moderens tilstand.
Pædiatrisk brug
Sikkerhed og effektivitet i pædiatriske populationer er ikke blevet fastlagt.
Et randomiseret, placebo-kontrolleret forsøg (CLARINET) viste ikke en klinisk fordel ved clopidogrel hos nyfødte og spædbørn med cyanotisk medfødt hjertesygdom pallieret med en systemisk-til-pulmonal arteriel shunt. Mulige faktorer, der bidrog til dette resultat, var dosis af clopidogrel, samtidig administration af aspirin og den sene påbegyndelse af behandlingen efter shuntpalliation. Det kan ikke udelukkes, at et forsøg med et andet design vil påvise en klinisk fordel i denne patientpopulation.
Geriatrisk brug
Af det samlede antal forsøgspersoner i de CAPRIE- og CURE-kontrollerede kliniske undersøgelser var ca. 50 % af patienterne behandlet med Plavix 65 år og ældre, og 15 % var 75 år og ældre. I COMMIT var ca. 58 % af patienterne behandlet med Plavix 75 mg 60 år og ældre, hvoraf 26 % var 70 år og ældre.
Den observerede risiko for blødningshændelser med Plavix 75 mg plus aspirin versus placebo plus aspirin efter alderskategori er angivet i tabel 1 og tabel 2 for henholdsvis CURE og COMMIT forsøgene [se BIVIRKNINGER ]. Dosisjustering er ikke nødvendig hos ældre patienter.
Nedsat nyrefunktion
Erfaringen er begrænset hos patienter med svært og moderat nedsat nyrefunktion [se KLINISK FARMAKOLOGI ].
Nedsat leverfunktion
Dosisjustering er ikke nødvendig hos patienter med nedsat leverfunktion [se KLINISK FARMAKOLOGI ].
OVERDOSIS
Plavix hæmning af blodplader er irreversibel og vil vare i hele blodpladens levetid. Overdosering efter administration af clopidogrel kan resultere i blødningskomplikationer. En enkelt oral dosis clopidogrel på 1500 eller 2000 mg/kg var dødelig for mus og rotter og ved 3000 mg/kg for bavianer. Symptomer på akut toksicitet var opkastning, udmattelse, åndedrætsbesvær og gastrointestinal blødning hos dyr.
Baseret på biologisk plausibilitet kan blodpladetransfusion genoprette størkningsevnen.
KONTRAINDIKATIONER
Aktiv blødning
Plavix er kontraindiceret til patienter med aktiv patologisk blødning, såsom mavesår eller intrakraniel blødning.
Overfølsomhed
Plavix 75 mg er kontraindiceret til patienter med overfølsomhed (f.eks. anafylaksi) over for clopidogrel eller en hvilken som helst komponent i produktet [se BIVIRKNINGER ].
KLINISK FARMAKOLOGI
Handlingsmekanisme
Clopidogrel er en hæmmer af trombocytaktivering og -aggregering gennem den irreversible binding af dets aktive metabolit til P2Y12-klassen af ADP-receptorer på blodplader.
Farmakodynamik
Clopidogrel skal metaboliseres af CYP450-enzymer for at producere den aktive metabolit, der hæmmer trombocytaggregation. Den aktive metabolit af clopidogrel hæmmer selektivt bindingen af adenosindiphosphat (ADP) til dets trombocyt-P2Y12-receptor og den efterfølgende ADP-medierede aktivering af glycoprotein GPIIb/IIIa-komplekset og hæmmer derved trombocytaggregation. Denne handling er irreversibel. Som følge heraf påvirkes blodplader, der udsættes for clopidogrels aktive metabolit, i resten af deres levetid (ca. 7 til 10 dage). Blodpladeaggregering induceret af andre agonister end ADP inhiberes også ved at blokere amplifikationen af blodpladeaktivering af frigivet ADP.
Dosisafhængig hæmning af trombocytaggregation kan ses 2 timer efter enkelt orale doser af Plavix. Gentagne doser på 75 mg Plavix pr. dag hæmmer ADP-induceret trombocytaggregation den første dag, og hæmningen når steady state mellem dag 3 og dag 7. Ved steady state var det gennemsnitlige hæmningsniveau observeret med en dosis på 75 mg Plavix pr. dag. mellem 40 % og 60 %. Trombocytaggregation og blødningstid vender gradvist tilbage til baseline-værdierne, efter behandlingen er afbrudt, generelt efter ca. 5 dage.
Geriatriske patienter
Ældre (≥75 år) og unge raske forsøgspersoner havde lignende virkninger på trombocytaggregation.
Patienter med nedsat nyrefunktion
Efter gentagne doser på 75 mg Plavix 75 mg dagligt udviste patienter med svært nedsat nyrefunktion (kreatininclearance fra 5 til 15 ml/min) og moderat nedsat nyrefunktion (kreatininclearance fra 30 til 60 ml/min) lav (25 %) hæmning af ADP-induceret blodpladeaggregation.
Patienter med nedsat leverfunktion
Efter gentagne doser på 75 mg Plavix dagligt i 10 dage hos patienter med svær leverinsufficiens var hæmningen af ADP-induceret trombocytaggregation lig den, der blev observeret hos raske forsøgspersoner.
Køn
I en lille undersøgelse, der sammenlignede mænd og kvinder, blev der observeret mindre hæmning af ADP-induceret blodpladeaggregation hos kvinder.
Farmakokinetik
Clopidogrel er et prodrug og metaboliseres til en farmakologisk aktiv metabolit og inaktive metabolitter.
Absorption
Efter enkelte og gentagne orale doser på 75 mg dagligt absorberes clopidogrel hurtigt. Absorptionen er mindst 50 % baseret på urinudskillelse af clopidogrel metabolitter.
Effekt af mad
Plavix kan indgives med eller uden mad. I en undersøgelse med raske mandlige forsøgspersoner, hvor Plavix 75 mg dagligt blev givet sammen med en standardmorgenmad, blev den gennemsnitlige hæmning af ADP-induceret trombocytaggregation reduceret med mindre end 9 %. Den aktive metabolit AUC0-24 var uændret i nærvær af mad, mens der var et fald på 57 % i den aktive metabolit Cmax. Lignende resultater blev observeret, når en Plavix 300 mg startdosis blev administreret sammen med en fedtrig morgenmad.
Metabolisme
Clopidogrel metaboliseres i vid udstrækning via to hovedmetaboliske veje: én medieret af esteraser og fører til hydrolyse til et inaktivt carboxylsyrederivat (85 % af cirkulerende metabolitter) og én medieret af multiple cytokrom P450-enzymer. Cytokromer oxiderer først clopidogrel til en 2-oxo-clopidogrel mellemmetabolit. Efterfølgende metabolisering af 2-oxoclopidogrel-mellemmetabolitten resulterer i dannelse af den aktive metabolit, et thiolderivat af clopidogrel. Den aktive metabolit dannes hovedsageligt af CYP2C19 med bidrag fra flere andre CYP-enzymer, herunder CYP1A2, CYP2B6 og CYP3A. Den aktive thiolmetabolit binder sig hurtigt og irreversibelt til blodpladereceptorer og hæmmer således trombocytaggregation i blodpladens levetid.
Cmax for den aktive metabolit er dobbelt så høj efter en enkelt 300 mg clopidogrel-startdosis, som efter fire dages vedligeholdelsesdosis på 75 mg. Cmax forekommer ca. 30 til 60 minutter efter dosering. I dosisområdet 75 til 300 mg afviger farmakokinetikken af den aktive metabolit fra dosisproportionaliteten: 4 gange dosis resulterer i henholdsvis 2,0 og 2,7 gange Cmax og AUC.
Elimination
Efter en oral dosis af 14C-mærket clopidogrel til mennesker blev ca. 50 % af den samlede radioaktivitet udskilt i urinen og ca. 46 % i fæces i løbet af 5 dage efter dosering. Efter en enkelt oral dosis på 75 mg har clopidogrel en halveringstid på ca. 6 timer. Halveringstiden af den aktive metabolit er ca. 30 minutter.
Lægemiddelinteraktioner
Virkning af andre lægemidler på Plavix
Clopidogrel metaboliseres til dets aktive metabolit delvist af CYP2C19.
CYP2C19 inducere
Samtidig brug af stærke induktorer af CYP2C19 resulterer i øget plasmakoncentration af den aktive metabolit af clopidogrel og en stigning i trombocythæmning.
Rifampin: Samtidig administration af rifampin 300 mg to gange dagligt i 7 dage med 600 mg startdosis af clopidogrel hos raske voksne øgede den gennemsnitlige AUC og Cmax for clopidogrels thiolmetabolitter med 3,8 gange. Den gennemsnitlige hæmning af trombocytaggregation 4 timer efter dosis var 34 % højere i nærvær af rifampin sammenlignet med clopidogrel administreret alene.
CYP2C19-hæmmere
Samtidig brug af visse hæmmere af dette enzym resulterer i reducerede plasmakoncentrationer af den aktive metabolit af clopidogrel og en reduktion i blodpladehæmning.
Protonpumpehæmmere (PPI)
Effekten af protonpumpehæmmere (PPI) på den systemiske eksponering for den aktive clopidogrel-metabolit efter multiple doser af Plavix 75 mg evalueret i dedikerede lægemiddelinteraktionsstudier er vist i figur 1.
Figur 1: Eksponering for Clopidogrel Active Metabolite efter multiple doser af Plavix 75 mg alene eller med protonpumpehæmmere (PPI'er)
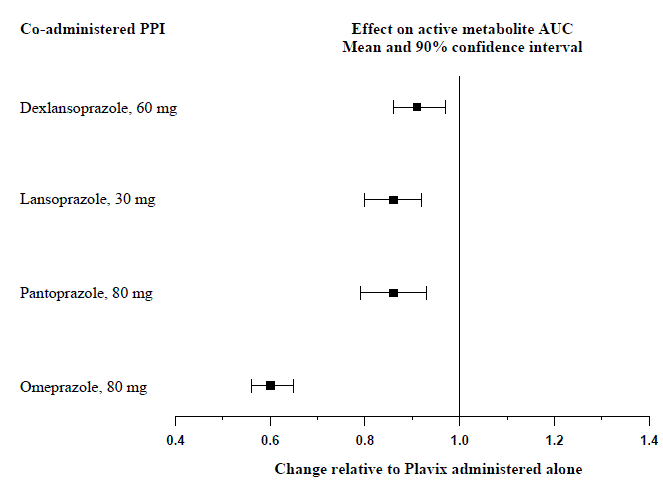
Farmakodynamiske og farmakokinetiske parametre målt i disse undersøgelser viste, at interaktionen var højest med omeprazol og mindst med dexlansoprazol.
Opioider
Samtidig administration af 5 mg intravenøs morfin med 600 mg startdosis clopidogrel hos raske voksne reducerede AUC og Cmax for clopidogrels thiolmetabolitter med 34 %. Gennemsnitlig trombocytaggregation var højere i op til 2 til 4 timer ved samtidig administration af morfin.
Effekt af Plavix 75mg på andre lægemidler
In vitro undersøgelser har vist, at glucuronidmetabolitten af clopidogrel er en stærk hæmmer af CYP2C8. Samtidig administration af repaglinid og Plavix øgede den systemiske eksponering for repaglinid (AUC0-∞) med 5,1 gange efter startdosis (300 mg) og 3,9 gange på dag 3 af vedligeholdelsesdosis (75 mg) af Plavix [se DRUGSINTERAKTIONER ].
Farmakogenomi
CYP2C19 er involveret i dannelsen af både den aktive metabolit og 2-oxo-clopidogrel mellemmetabolit. Clopidogrels aktive metabolits farmakokinetik og trombocythæmmende virkning, målt ved ex vivo blodpladeaggregeringsassays, er forskellige afhængigt af CYP2C19-genotype. Patienter, der er homozygote for ikke-funktionelle alleler af CYP2C19-genet, kaldes "CYP2C19-fattige metabolisatorer." Ca. 2 % af hvide og 4 % af sorte patienter er dårlige metabolisatorer; forekomsten af dårligt stofskifte er højere hos asiatiske patienter (f.eks. 14 % af kineserne). Tests er tilgængelige for at identificere patienter, der er CYP2C19-fattige metabolisatorer.
Et crossover-studie med 40 raske forsøgspersoner, 10 hver i de fire CYP2C19-metabolisatorgrupper, evaluerede farmakokinetiske og trombocythæmmende responser med 300 mg efterfulgt af 75 mg dagligt og 600 mg efterfulgt af 150 mg dagligt, hver i alt i 5 dage. Nedsat eksponering for aktiv metabolit og nedsat hæmning af blodpladeaggregation blev observeret hos de dårlige metabolisatorer sammenlignet med de andre grupper.
Kliniske Studier
Akut koronarsyndrom
HELBREDE
CURE-studiet omfattede 12.562 patienter med ACS uden ST-elevation (UA eller NSTEMI) og præsenterede inden for 24 timer efter indtræden af den seneste episode af brystsmerter eller symptomer, der er i overensstemmelse med iskæmi. Patienterne skulle have enten EKG-forandringer forenelige med ny iskæmi (uden ST-elevation) eller forhøjede hjerteenzymer eller troponin I eller T til mindst det dobbelte af den øvre normalgrænse.
Patienterne blev randomiseret til at modtage Plavix (300 mg startdosis efterfulgt af 75 mg én gang dagligt) eller placebo og blev behandlet i op til et år. Patienterne fik også aspirin (75-325 mg én gang dagligt) og andre standardbehandlinger såsom heparin. Anvendelse af GPIIb/IIIa-hæmmere var ikke tilladt i tre dage før randomisering.
Patientpopulationen var stort set hvid (82 %) og omfattede 38 % kvinder og 52 % alder ≥65 år. Kun omkring 20 % af patienterne gennemgik revaskularisering under den indledende hospitalsindlæggelse, og få gennemgik ny eller akut revaskularisering.
Antallet af patienter, der oplevede det primære resultat (CV-død, MI eller slagtilfælde) var 582 (9,3 %) i den Plavix-behandlede gruppe og 719 (11,4 %) i den placebo-behandlede gruppe, en relativ risikoreduktion på 20 % (95). % CI på 10%-28%; p
Det meste af fordelene ved Plavix indtraf i de første to måneder, men forskellen fra placebo blev opretholdt gennem hele forsøget (op til 12 måneder) (se figur 2).
Figur 2: Kardiovaskulær død, myokardieinfarkt og slagtilfælde i CURE-undersøgelsen
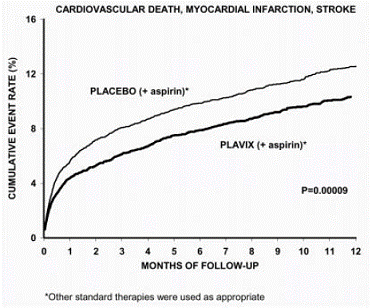
Effekten af Plavix 75mg afveg ikke signifikant i forskellige undergrupper, som vist i figur 3. Fordelene forbundet med Plavix 75mg var uafhængige af brugen af andre akutte og langsigtede kardiovaskulære behandlinger, herunder heparin/LMWH, intravenøst glycoprotein IIb/IIIa (GPIIb/IIIa) hæmmere, lipidsænkende lægemidler, betablokkere og ACE-hæmmere. Effekten af Plavix blev observeret uafhængigt af dosis af aspirin (75-325 mg én gang dagligt). Brug af orale antikoagulantia, non-study antiblodplademedicin og kroniske NSAID'er var ikke tilladt i CURE.
Figur 3: Fareforhold for patientbaselinekarakteristika og samtidig medicin/interventioner under undersøgelsen til CURE-undersøgelsen
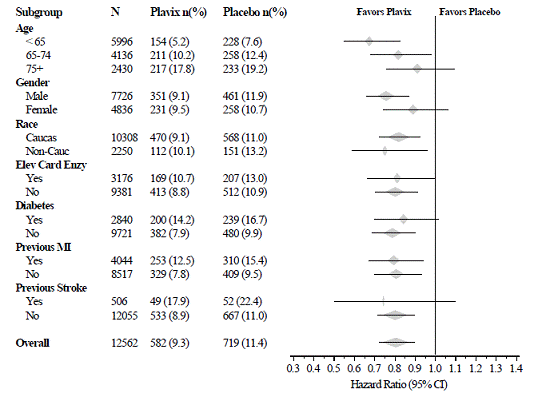
Figur 3: Fareforhold for patientbaselinekarakteristika og samtidig medicin/interventioner under undersøgelsen til CURE-undersøgelsen (fortsat)
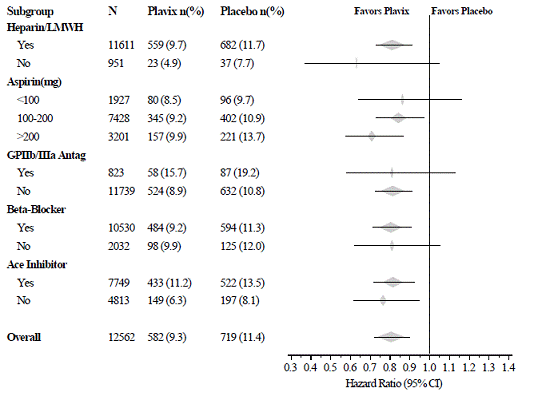
Brugen af Plavix i CURE var forbundet med et fald i brugen af trombolytisk behandling (71 patienter [1,1 %] i Plavix 75 mg-gruppen, 126 patienter [2,0 %] i placebogruppen; relativ risikoreduktion på 43 %), og GPIIb/IIIa-hæmmere (369 patienter [5,9 %] i Plavix 75 mg-gruppen, 454 patienter [7,2 %] i placebogruppen, relativ risikoreduktion på 18 %). Brugen af Plavix 75 mg i CURE påvirkede ikke antallet af patienter behandlet med CABG eller PCI (med eller uden stenting) (2253 patienter [36,0 %] i Plavix 75 mg-gruppen, 2324 patienter [36,9 %] i placebogruppen; risikoreduktion på 4,0 pct.
BEGÅ
Hos patienter med STEMI blev sikkerheden og effekten af Plavix evalueret i den randomiserede, placebokontrollerede, dobbeltblinde undersøgelse, COMMIT. COMMIT omfattede 45.852 patienter, der viste sig inden for 24 timer efter begyndelsen af symptomerne på myokardieinfarkt med understøttende EKG-abnormaliteter (dvs. ST-elevation, ST-depression eller venstre bundt-grenblok). Patienterne blev randomiseret til at modtage Plavix (75 mg én gang dagligt) eller placebo i kombination med aspirin (162 mg dagligt), i 28 dage eller indtil hospitalsudskrivning, alt efter hvad der kom først.
De primære endepunkter var død af enhver årsag og den første forekomst af re-infarkt, slagtilfælde eller død.
Patientpopulationen var 28 % kvinder og 58 % alder ≥60 år (26 % alder ≥70 år). Femoghalvtreds procent (55%) af patienterne fik trombolytika, og kun 3% gennemgik PCI.
Som vist i tabel 5 og figur 4 og figur 5 nedenfor reducerede Plavix signifikant den relative risiko for død af enhver årsag med 7 % (p=0,029) og den relative risiko for kombinationen af reinfarkt, slagtilfælde eller død med 9 % ( p=0,002).
Figur 4: Kumulative hændelsesrater for dødsfald i COMMIT-undersøgelsen*
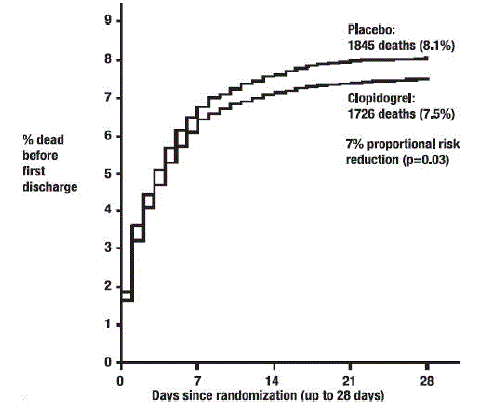
Figur 5: Kumulative hændelsesrater for det kombinerede endepunkt-re-infarkt, slagtilfælde eller død i COMMIT-undersøgelsen*
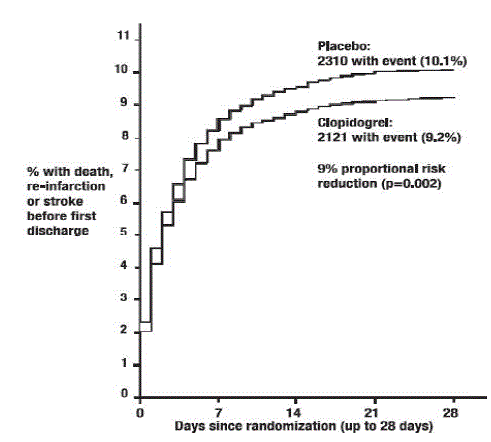
Effekten af Plavix 75 mg afveg ikke signifikant i forskellige forudspecificerede undergrupper som vist i figur 6. Effekten var også ens i ikke-præspecificerede undergrupper, inklusive dem baseret på infarktplacering, Killip-klasse eller tidligere MI-historie. Sådanne undergruppeanalyser bør fortolkes med varsomhed.
Figur 6: Effekter af at tilføje Plavix 75 mg til aspirin på det kombinerede primære endepunkt på tværs af baseline og samtidige medicinundergrupper for COMMIT-undersøgelsen
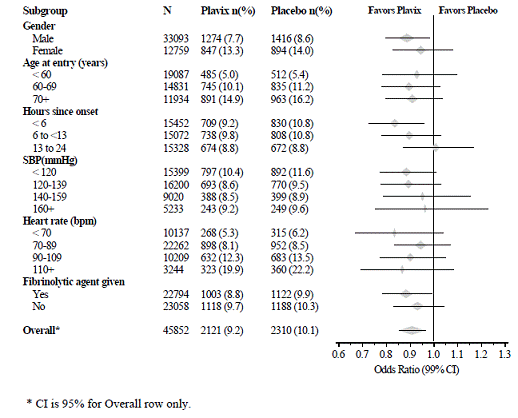
Nyligt myokardieinfarkt, nyligt slagtilfælde eller etableret perifer arteriel sygdom
CAPRIE
CAPRIE-studiet var et 19.185-patienter, 304-center, internationalt, randomiseret, dobbeltblindt, parallelgruppestudie, der sammenlignede Plavix (75 mg dagligt) med aspirin (325 mg dagligt). For at være berettiget til at blive optaget, skulle patienterne have: 1) nyere historie med myokardieinfarkt (inden for 35 dage); 2) nylige historier om iskæmisk slagtilfælde (inden for 6 måneder) med mindst en uge med resterende neurologiske tegn; og/eller 3) etableret perifer arteriel sygdom (PAD). Patienterne modtog randomiseret behandling i gennemsnitligt 1,6 år (maksimalt 3 år).
Forsøgets primære resultat var tiden til den første forekomst af nyt iskæmisk slagtilfælde (fatalt eller ej), nyt myokardieinfarkt (fatalt eller ej) eller anden vaskulær død. Dødsfald, der ikke let kan tilskrives ikke-vaskulære årsager, blev alle klassificeret som vaskulære.
Som vist i tabel 6 var Plavix forbundet med en lavere forekomst af udfaldshændelser, primært hjerteinfarkt. Den samlede relative risikoreduktion (9,8 % vs. 10,6 %) var 8,7 %, p=0,045. Lignende resultater blev opnået, når mortalitet af alle årsager og slagtilfælde af alle årsager blev talt i stedet for vaskulær dødelighed og iskæmiske slagtilfælde (risikoreduktion 6,9%). Hos patienter, der overlevede et apopleksi eller myokardieinfarkt i undersøgelsen, var forekomsten af efterfølgende hændelser lavere i Plavix 75 mg-gruppen.
Kurverne, der viser den samlede hændelsesrate, er vist i figur 7. Hændelseskurverne adskilte sig tidligt og fortsatte med at divergere over den 3-årige opfølgningsperiode.
Figur 7: Fatale eller ikke-dødelige vaskulære hændelser i CAPRIE-undersøgelsen
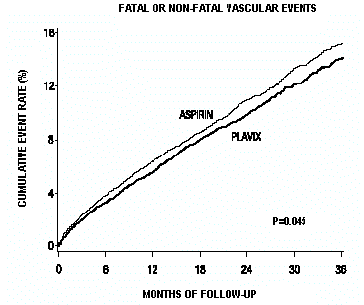
Den statistiske signifikans, der favoriserer Plavix 75 mg frem for aspirin, var marginal (p=0,045). Men fordi aspirin i sig selv er effektivt til at reducere kardiovaskulære hændelser hos patienter med nyligt myokardieinfarkt eller slagtilfælde, er effekten af Plavix 75 mg betydelig.
CAPRIE-forsøget inkluderede en befolkning, der havde nyligt MI, nyligt slagtilfælde eller PAD. Effektiviteten af Plavix 75 mg i forhold til aspirin var heterogen på tværs af disse undergrupper (p=0,043) (se figur 8). Ikke desto mindre kan denne forskel være en tilfældig forekomst, fordi CAPRIE-studiet ikke var designet til at evaluere den relative fordel af Plavix 75 mg i forhold til aspirin i de individuelle patientundergrupper. Fordelen var mest tydelig hos patienter, der blev indskrevet på grund af perifer arteriel sygdom og mindre tydelig hos patienter med slagtilfælde. Hos patienter, der blev inkluderet i forsøget udelukkende på grundlag af et nyligt myokardieinfarkt, var Plavix 75 mg ikke numerisk overlegen i forhold til aspirin.
Figur 8: Hazard Ratio og 95 % CI efter baseline undergrupper i CAPRIE-undersøgelsen
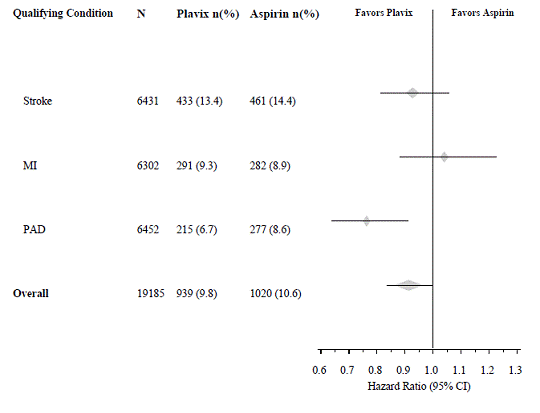
Ingen påvist fordel ved Plavix 75mg plus aspirin hos patienter med flere risikofaktorer eller etableret vaskulær sygdom
KARISMA
CHARISMA-studiet var et randomiseret, dobbeltblindt, parallelgruppestudie med 15.603 forsøgspersoner, der sammenlignede Plavix (75 mg dagligt) med placebo til forebyggelse af iskæmiske hændelser hos patienter med vaskulær sygdom eller multiple risikofaktorer for aterosklerose. Alle forsøgspersoner blev behandlet med aspirin 75-162 mg dagligt. Den gennemsnitlige behandlingsvarighed var 23 måneder. Undersøgelsen kunne ikke påvise en reduktion i forekomsten af det primære endepunkt, en sammensætning af CV-død, MI eller slagtilfælde. I alt 534 (6,9 %) patienter i Plavix-gruppen mod 573 (7,4 %) patienter i placebogruppen oplevede en primær udfaldshændelse (p=0,22). Blødning af alle sværhedsgrader var mere almindelig hos forsøgspersonerne randomiseret til Plavix.
PATIENTOPLYSNINGER
Plavix® (PLAV-iks) (clopidogrel bisulfat) tabletter
Læs denne medicinvejledning, før du begynder at tage Plavix, og hver gang du får genopfyldning. Der kan være nye oplysninger. Denne medicinvejledning træder ikke i stedet for at tale med din læge om din medicinske tilstand eller din behandling.
Hvad er den vigtigste information, jeg bør vide om Plavix 75mg?
1. Plavix virker muligvis ikke så godt hos personer, der:
- har visse genetiske faktorer, der påvirker, hvordan kroppen nedbryder Plavix. Din læge kan udføre genetiske tests for at sikre, at Plavix er det rigtige for dig.
- tage visse lægemidler, især omeprazol (Prilosec®) eller esomeprazol (Nexium®). Din læge kan ændre den medicin, du tager mod mavesyreproblemer, mens du tager Plavix.
2. Plavix 75mg kan forårsage blødninger, som kan være alvorlige og nogle gange kan føre til døden. Plavix er et blodfortyndende lægemiddel, der nedsætter risikoen for, at der dannes blodpropper i din krop. Mens du tager Plavix:
- du kan lettere få blå mærker og bløde
- du er mere tilbøjelig til at få næseblod
- det vil tage længere tid for enhver blødning at stoppe
Ring til din læge med det samme, hvis du har nogle af disse tegn eller symptomer på blødning:
- uventet blødning eller blødning, der varer længe
- blod i din urin (lyserød, rød eller brun urin)
- rød eller sort afføring (ligner tjære)
- blå mærker, der opstår uden kendt årsag eller bliver større
- hoste blod eller blodpropper op
- kaste blod op, eller dit opkast ligner kaffegrums
Stop ikke med at tage Plavix 75 mg uden at tale med lægen, som har ordineret det til dig. Personer, der holder op med at tage Plavix 75 mg for tidligt, har en højere risiko for at få et hjerteanfald eller dø. Hvis du skal stoppe med Plavix på grund af blødning, kan din risiko for et hjerteanfald være højere.
Hvad er Plavix 75mg?
Plavix er en receptpligtig medicin, der bruges til at behandle mennesker, der har en af følgende:
- brystsmerter på grund af hjerteproblemer
- dårligt blodomløb i benene (perifer arteriel sygdom)
- et hjerteanfald
- et slagtilfælde
Plavix bruges alene eller sammen med aspirin for at mindske din chance for at få et andet alvorligt problem med dit hjerte eller blodkar, såsom hjerteanfald, slagtilfælde eller blodprop, der kan føre til døden.
Blodplader er blodceller, der hjælper dit blod til at størkne normalt. Plavix 75mg hjælper med at forhindre, at blodplader klæber sammen og danner en blodprop, der kan blokere en arterie.
Det vides ikke, om Plavix 75mg er sikkert og effektivt til børn.
Hvem bør ikke tage Plavix 75mg?
Tag ikke Plavix, hvis du:
- har i øjeblikket en tilstand, der forårsager blødning, såsom et mavesår
- er allergisk over for clopidogrel eller andre indholdsstoffer i Plavix. Se slutningen af denne indlægsseddel for en komplet liste over ingredienser i Plavix.
Hvad skal jeg fortælle min læge, før jeg tager Plavix 75mg?
Inden du tager Plavix, skal du fortælle det til din læge, hvis du:
- har en historie med tarm (gastrointestinale) eller mavesår
- har en historie med blødningsproblemer
- planlægger at blive opereret eller en tandbehandling. Se "Hvordan skal jeg tage Plavix?"
- er gravid eller planlægger at blive gravid. Det vides ikke, om Plavix 75 mg vil skade dit ufødte barn
- ammer eller planlægger at amme. Det vides ikke, om Plavix 75 mg udskilles i din modermælk. Der bør træffes en beslutning med din læge om at undgå eller afbryde amning, når det er nødvendigt at fortsætte med Plavix.
- har haft en allergi eller reaktion på medicin, der bruges til at behandle din sygdom.
Fortæl alle dine læger og din tandlæge, at du tager Plavix. De bør tale med den læge, der har ordineret Plavix 75 mg til dig, før du får foretaget en operation eller invasiv procedure.
Fortæl din læge om al den medicin du tager, herunder receptpligtig, ikke-receptpligtig medicin, vitaminer og naturlægemidler.
Plavix 75 mg kan påvirke den måde, anden medicin virker på, og anden medicin kan påvirke, hvordan Plavix virker. Se "Hvad er den vigtigste information, jeg bør vide om Plavix 75mg?"
Plavix 75 mg kan øge blodniveauet af anden medicin, såsom repaglinid (Prandin®).
Hvis du tager Plavix sammen med visse andre lægemidler, kan det øge din risiko for blødning.
Fortæl det især din læge, hvis du tager:
- aspirin, især hvis du har haft et slagtilfælde. Tal altid med din læge om, hvorvidt du skal tage aspirin sammen med Plavix 75mg for at behandle din tilstand.
- Ikke-steroide antiinflammatoriske lægemidler (NSAID'er). Spørg din læge eller apoteket om en liste over NSAID-medicin, hvis du er i tvivl.
- warfarin (Coumadin®, Jantoven®).
- selektive serotoningenoptagelseshæmmere (SSRI'er) og serotonin-noradrenalin-genoptagelseshæmmere (SNRI'er). Spørg din læge eller apoteket om en liste over SSRI- eller SNRI-medicin, hvis du er i tvivl.
- rifampin (bruges til at behandle alvorlige infektioner)
Kend den medicin du tager. Hold en liste over dem for at vise din læge eller apotek, når du får en ny medicin.
Hvordan skal jeg tage Plavix?
- Tag Plavix nøjagtigt som din læge fortæller dig.
- Du må ikke ændre din dosis eller stoppe med at tage Plavix 75 mg uden først at tale med din læge. Hvis du stopper med Plavix, kan det øge din risiko for hjerteanfald eller slagtilfælde.
- Tag Plavix 75mg med aspirin som instrueret af din læge.
- Hvis du glemmer en dosis, skal du tage Plavix, så snart du husker det. Hvis det næsten er tid til din næste dosis, skal du springe den glemte dosis over. Tag den næste dosis på dit normale tidspunkt. Tag ikke 2 doser Plavix 75 mg på samme tid, medmindre din læge fortæller dig det.
- Hvis du tager for meget Plavix, skal du straks ringe til din læge eller gå til den nærmeste skadestue.
- Tal med din læge om at stoppe din Plavix 75mg, før du skal opereres. Din læge kan fortælle dig, at du skal stoppe med at tage Plavix 75 mg mindst 5 dage før du skal opereres for at undgå overdreven blødning under operationen.
Hvad er de mulige bivirkninger af Plavix?
Plavix 75mg kan forårsage alvorlige bivirkninger, herunder:
- Se "Hvad er den vigtigste information, jeg bør vide om Plavix?"
- Et blodkoagulationsproblem kaldet trombotisk trombocytopenisk purpura (TTP). TTP kan forekomme med Plavix 75 mg, nogle gange efter kort tid (mindre end 2 uger). TTP er et problem med blodpropper, hvor der dannes blodpropper i blodkar; og kan ske overalt i kroppen. TTP skal behandles på et hospital med det samme, fordi det kan forårsage død. Få lægehjælp med det samme, hvis du har nogle af disse symptomer, og de ikke kan forklares med en anden medicinsk tilstand:
- lilla pletter (kaldet purpura) på huden eller i munden (slimhinderne) på grund af blødning under huden
- din hud eller det hvide i dine øjne er gule (gulsot)
- du føler dig træt eller svag
- din hud ser meget bleg ud
- feber
- hurtig puls eller åndenød
- hovedpine
- taleændringer
- forvirring
- koma
- slag
- anfald
- lav mængde urin, eller urin, der er lyserød eller har blod i sig
- smerter i maveområdet (mave).
- kvalme, opkastning eller diarré
- synsforandringer
- vedvarende lavt blodsukkersymptomer
Fortæl det til din læge, hvis du har en bivirkning, som generer dig, eller som ikke forsvinder. Fortæl det til din læge, hvis du udvikler en allergisk reaktion, herunder hudreaktioner, mens du tager Plavix.
Disse er ikke alle de mulige bivirkninger af Plavix. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan skal jeg opbevare Plavix 75mg?
- Opbevar Plavix 75mg ved 59°F til 86°F (15°C til 30°C).
Opbevar Plavix og al medicin utilgængeligt for børn.
Generel information om Plavix
Medicin bruges nogle gange til andre formål end dem, der er angivet i en medicinvejledning. Tag ikke Plavix 75 mg for en tilstand, som det ikke er ordineret til. Giv ikke Plavix til andre mennesker, selvom de har de samme symptomer, som du har. Det kan skade dem.
Denne medicinvejledning opsummerer de vigtigste oplysninger om Plavix. Hvis du vil have mere information, så tal med din læge. Spørg din læge eller apoteket om oplysninger om Plavix, som er skrevet til sundhedspersonale.
For mere information, gå til www.sanofi-aventis.us eller www.bms.com eller ring på 1-800-321-1335.
Hvad er ingredienserne i Plavix 75mg?
Aktiv ingrediens: clopidogrel bisulfat
Inaktive ingredienser:
Tablet: hydrogeneret ricinusolie, hydroxypropylcellulose, mannitol, mikrokrystallinsk cellulose, polyethylenglycol 6000
Filmcoating: jernoxid, hypromellose 2910, lactosemonohydrat, titaniumdioxid, triacetin, carnaubavoks
Denne medicinvejledning er godkendt af US Food and Drug.
