Cordarone 100mg, 50mg Amiodarone Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Cordarone 100mg, og hvordan bruges det?
Cordarone 100mg IV er en receptpligtig medicin, der bruges til at behandle symptomer på uregelmæssig hjerterytme (ventrikulære arytmier).
- Cordarone IV kan bruges alene eller sammen med anden medicin.
- Cordarone 50mg IV tilhører en klasse af lægemidler kaldet Antidysrhythmisc, III.
Hvad er de mulige bivirkninger af Cordarone 100mg?
Cordarone 100mg kan forårsage alvorlige bivirkninger, herunder:
- stakåndet,
- besvimelse,
- hurtige eller uregelmæssige hjerteslag,
- brystsmerter,
- hvæsen, og
- åndedrætsbesvær
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Cordarone 100mg IV omfatter:
- lavt blodtryk (hypotension),
- langsom puls,
- hjertestop,
- kvalme,
- feber,
- kongestiv hjertesvigt,
- unormal hjerterytme,
- kardiogent shock, og
- unormale leverfunktionsprøver
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Cordarone. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ADVARSEL
LUNGE-, LEVER- OG HJERTETOKSICITET
CORDARONE 100mg er kun beregnet til brug hos patienter med de angivne livstruende arytmier, fordi brugen er ledsaget af betydelig toksicitet [se INDIKATIONER OG ANVENDELSE].
CORDARONE kan forårsage pulmonal toksicitet (hypersensitivitetspneumonitis eller interstitiel/alveolær pneumonitis), der har resulteret i klinisk manifest sygdom med hastigheder så høje som 17 % i nogle serier af patienter. Lungetoksicitet har været dødelig omkring 10 % af tiden. Anskaf en baseline røntgenundersøgelse af thorax og lungefunktionstest, inklusive diffusionskapacitet, når CORDARONE 100 mg behandling påbegyndes. Gentag historie, fysisk undersøgelse og røntgen af thorax hver 3. til 6. måned [se ADVARSLER OG FORHOLDSREGLER].
CORDARONE kan forårsage hepatoksicitet, som kan være dødelig. Opnå baseline og periodiske levertransaminaser, og afbryd eller reducer dosis, hvis stigningen overstiger tre gange det normale eller fordobles hos en patient med en forhøjet baseline. Afbryd CORDARONE, hvis patienten oplever tegn eller symptomer på klinisk leverskade [se ADVARSLER OG FORHOLDSREGLER].
CORDARONE kan forværre arytmier. Påbegynd CORDARONE 50 mg i et klinisk miljø, hvor kontinuerlige elektrokardiogrammer og hjerte-genoplivning er tilgængelige [se ADVARSLER OG FORHOLDSREGLER].
BESKRIVELSE
CORDARONE (amiodaron HCl) er et antiarytmisk lægemiddel, tilgængeligt til oral administration som lyserøde tabletter med delekærv indeholdende 200 mg amiodaronhydrochlorid. De tilstedeværende inaktive ingredienser er kolloid siliciumdioxid, lactose, magnesiumstearat, povidon, stivelse og FD&C Red 40. CORDARONE er et benzofuranderivat: 2-butyl-3-benzofuranyl 4-[2-(diethylamino)-ethoxy]- 3, 5-diiodphenylketonhydrochlorid.
Strukturformlen er som følger:
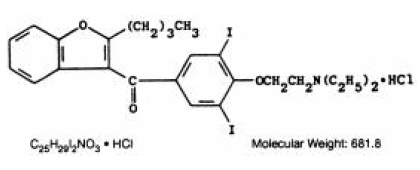
Amiodarone HCl er et hvidt til cremefarvet krystallinsk pulver. Det er let opløseligt i vand, opløseligt i alkohol og frit opløseligt i chloroform. Den indeholder 37,3 vægtprocent jod.
INDIKATIONER
CORDARONE er indiceret til behandling af dokumenteret, livstruende tilbagevendende ventrikelflimmer og livstruende tilbagevendende hæmodynamisk ustabil takykardi hos voksne, som ikke har reageret på tilstrækkelige doser af andre tilgængelige antiarytmika, eller når alternative midler ikke kan tolereres.
DOSERING OG ADMINISTRATION
Dosis skal individualiseres baseret på sværhedsgraden af arytmi og respons. Brug den laveste effektive dosis. Få baseline røntgenbillede af thorax, lungefunktionstest, thyreoideafunktionstest og leveraminotransferaser. Korriger hypokaliæmi, hypomagnesæmi og hypocalcæmi før påbegyndelse af behandling
Anbefalet dosering
Start behandlingen med en belastningsdosering på 800 til 1600 mg/dag, indtil den første terapeutiske respons indtræder (sædvanligvis 1 til 3 uger). Når tilstrækkelig arytmikontrol er opnået, eller hvis bivirkninger bliver fremtrædende, reduceres CORDARONE 50 mg dosis til 600 til 800 mg/dag i en måned og derefter til vedligeholdelsesdosis, sædvanligvis 400 mg/dag.
Administration
Administrer CORDARONE konsekvent med hensyn til måltider [se KLINISK FARMAKOLOGI ]. Administration af CORDARONE i opdelte doser sammen med måltider anbefales til samlede daglige doser på 1000 mg eller højere, eller når der opstår gastrointestinal intolerance.
HVORDAN LEVERET
Doseringsformer og styrker
200 mg tabletter: runde, lyserøde, konvekse tabletter med forhøjet "C" og mærket "200" på den ene side, med bagside delekærv og mærket "WYETH" og "4188".
Opbevaring og håndtering
CORDARONE® (amiodaron HCl) tabletter er tilgængelige i flasker med 60 tabletter som følger:
200 mg , NDC 0008-4188-04, runde, lyserøde tabletter med konveks ansigt med hævet "C" og mærket "200" på den ene side, med delekærv på bagsiden og mærket "WYETH" og "4188".
Opbevares tæt lukket.
Opbevares ved kontrolleret rumtemperatur, 20° til 25°C (68° til 77°F).
Beskyt mod lys.
Dispenser i en lysbestandig, tæt beholder.
Fremstillet af Sanofi Winthrop Industrie, 1, rue de la Vierge, 33440 Ambares, Frankrig. Distribueret af: Wyeth Pharmaceuticals Inc., Et datterselskab af Pfizer Inc., Philadelphia, PA 19101. Revideret: Okt 2018
BIVIRKNINGER
Følgende alvorlige bivirkninger er beskrevet mere detaljeret i andre afsnit af ordinationsinformationen:
- Lungetoksicitet [se ADVARSLER OG FORHOLDSREGLER ]
- Leverskade [se ADVARSLER OG FORHOLDSREGLER ]
- Forværret arytmi [se ADVARSLER OG FORHOLDSREGLER ]
- Synsforstyrrelser og tab af syn [se ADVARSLER OG FORHOLDSREGLER ]
- Skjoldbruskkirtelabnormiteter [se ADVARSLER OG FORHOLDSREGLER ]
- Bradykardi [se ADVARSLER OG FORHOLDSREGLER ]
- Perifer neuropati [se ADVARSLER OG FORHOLDSREGLER ]
- Lysfølsomhed og misfarvning af huden [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring med kliniske forsøg
Fordi kliniske forsøg udføres under vidt forskellige forhold, kan bivirkningsrater observeret i de kliniske forsøg med et lægemiddel ikke direkte sammenlignes med hastigheder i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de frekvenser, der observeres i praksis.
Ved den sædvanlige vedligeholdelsesdosis (400 mg/dag) og derover forårsager CORDARONE 100 mg bivirkninger hos omkring tre fjerdedele af alle patienter, hvilket resulterer i seponering hos 7 til 18 %.
I undersøgelser af næsten 5.000 patienter behandlet i åbne amerikanske undersøgelser og i offentliggjorte rapporter om behandling med CORDARONE omfattede de bivirkninger, der oftest krævede seponering af CORDARONE, pulmonale infiltrater eller fibrose, paroxysmal ventrikulær takykardi, kongestiv hjertesvigt og forhøjede leverenzymer. Andre symptomer, der sjældnere forårsagede seponeringer, omfattede synsforstyrrelser, lysfølsomhed, blå hudmisfarvning, hyperthyroidisme og hypothyroidisme.
Følgende bivirkninger er baseret på en retrospektiv undersøgelse af 241 patienter behandlet i 2 til 1.515 dage (gennemsnitlig 441,3 dage):
Skjoldbruskkirtel
Almindelig: Hypothyroidisme, hyperthyroidisme.
Kardiovaskulær
Almindelig: Kongestiv hjerteinsufficiens, hjertearytmier, SA-knudedysfunktion.
Gastrointestinale
Meget almindelig: Kvalme, opkastning.
Almindelig: Forstoppelse, anoreksi, mavesmerter.
Dermatologisk
Almindelig: Solar dermatitis/lysfølsomhed.
Neurologisk
Almindelig: Ildebefindende og træthed, tremor/unormale ufrivillige bevægelser, manglende koordination, unormal gang/ataksi, svimmelhed, paræstesier, nedsat libido, søvnløshed, hovedpine, søvnforstyrrelser.
Oftalmisk
Almindelig: Synsforstyrrelser.
Hepatisk
Almindelig: Unormale leverfunktionsprøver, uspecifikke leversygdomme.
Åndedræt
Almindelig: Lungebetændelse eller fibrose.
Andet
Almindelig: Rødmen, unormal smag og lugt, ødem, unormal spytsekretion, koagulationsabnormiteter.
Ikke almindelig: Blå hudmisfarvning, udslæt, spontan ekkymose, alopeci, hypotension og hjerteledningsabnormiteter.
Postmarketing oplevelse
Følgende bivirkninger er blevet identificeret under brug af CORDARONE efter godkendelse. Fordi disse reaktioner rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt pålideligt at estimere deres hyppighed eller etablere en årsagssammenhæng til lægemiddeleksponering.
Hæmatologisk hæmolytisk anæmi, aplastisk anæmi, pancytopeni, neutropeni, trombocytopeni, agranulocytose, granulom.
Immun : anafylaktisk/anafylaktoid reaktion (inklusive shock), angioødem.
Neurologisk : pseudotumor cerebri, parkinsonsymptomer såsom akinesi og bradykinesi (nogle gange reversibel med seponering af behandlingen), demyeliniserende polyneuropati.
Psykiatrisk : hallucination, forvirringstilstand, desorientering, delirium.
Hjerte : hypotension (nogle gange dødelig), bihulestop.
Åndedræt : eosinofil lungebetændelse, akut respiratorisk distress-syndrom i postoperative omgivelser, bronkospasme, bronchiolitis obliterans organiserende lungebetændelse, pulmonal alveolær blødning, pleural effusion, pleuritis.
Gastrointestinale : pancreatitis, akut pancreatitis.
Hepatisk : hepatitis, kolestatisk hepatitis, skrumpelever.
Hud- og subkutane vævsforstyrrelser nældefeber, toksisk epidermal nekrolyse (nogle gange dødelig), erythema multiforme, Stevens-Johnsons syndrom, eksfoliativ dermatitis, bulløs dermatitis, lægemiddeludslæt med eosinofili og systemiske symptomer (DRESS), eksem, kløe, hudkræft, lupuslignende syndrom.
Muskuloskeletale : myopati, muskelsvaghed, rabdomyolyse.
Renal : nedsat nyrefunktion, nyreinsufficiens, akut nyresvigt.
Reproduktiv : epididymitis, impotens.
Kroppen som helhed : feber, mundtørhed.
Endokrine og metaboliske : skjoldbruskkirtelknolder/skjoldbruskkirtelkræft, syndrom med uhensigtsmæssig antidiuretisk hormonsekretion (SIADH).
Vaskulær : vaskulitis.
DRUGSINTERAKTIONER
På grund af amiodarons lange halveringstid forventes lægemiddelinteraktioner at vare ved i uger til måneder efter seponering af amiodaron.
Lægemiddelinteraktioner med amiodaron er beskrevet i tabel 1 nedenfor.
ADVARSLER
Inkluderet som en del af FORHOLDSREGLER afsnit.
FORHOLDSREGLER
Vedvarende bivirkninger
På grund af den lange halveringstid for amiodaron (15 til 142 dage) og dets aktive metabolit desethylamiodaron (14 til 75 dage), kan bivirkninger og lægemiddelinteraktioner vare ved i flere uger efter seponering af amiodaron [se KLINISK FARMAKOLOGI ].
Lungetoksicitet
CORDARONE kan forårsage et klinisk syndrom med hoste og progressiv dyspnø ledsaget af funktionelle, radiografiske, galliumscannings- og patologiske data, der stemmer overens med pulmonal toksicitet. Pulmonal toksicitet sekundær til CORDARONE kan skyldes enten indirekte eller direkte toksicitet som repræsenteret ved henholdsvis overfølsomhedspneumonitis (inklusive eosinofil pneumoni) eller interstitiel/alveolær pneumonitis. Hyppigheden af pulmonal toksicitet er blevet rapporteret til at være så høj som 17 % og er dødelig i omkring 10 % af tilfældene. Opnå en baseline røntgenundersøgelse af thorax og lungefunktionstest, inklusive diffusionskapacitet, når CORDARONE 50 mg behandling påbegyndes. Gentag historie, fysisk undersøgelse og røntgen af thorax hver 3. til 6. måned, eller hvis der opstår symptomer. Overvej alternativ antiarytmisk behandling, hvis patienten oplever tegn eller symptomer på pulmonal toksicitet. Prednison 40 til 60 mg/dag nedtrappet over flere uger kan være nyttig til behandling af pulmonal toksicitet.
Adult Respiratory Distress Syndrome (ARDS)
Postoperativt er forekomster af ARDS blevet rapporteret hos patienter, der får CORDARONE-behandling, og som har gennemgået enten hjerte- eller ikke-kardial kirurgi. Selvom patienter normalt reagerer godt på kraftig respiratorisk behandling, har resultatet i sjældne tilfælde været fatalt.
Leverskade
Asymptomatiske forhøjelser af leverenzymniveauer ses hyppigt, men CORDARONE 100mg kan forårsage livstruende leverskade. Histologien har lignet alkoholisk hepatitis eller skrumpelever. Få baseline og periodiske levertransaminaser. Hvis transaminaser overstiger tre gange det normale eller fordobles hos en patient med en forhøjet baseline, skal du afbryde eller reducere dosis af CORDARONE 100 mg, opnå opfølgende test og behandle passende.
Forværret arytmi
CORDARONE 100mg kan forværre den aktuelle arytmi hos omkring 2 til 5 % af patienterne eller forårsage ny ventrikulær fibrillering, uophørlig ventrikulær takykardi, øget modstand mod kardioversion og polymorf ventrikulær takykardi forbundet med QTc-forlængelse (Torsade dees).
Korriger hypokaliæmi, hypomagnesiæmi og hypocalcæmi før påbegyndelse af behandling med CORDARONE, da disse lidelser kan overdrive graden af QTc-forlængelse og øge potentialet for TdP. Vær særlig opmærksom på elektrolyt- og syre-basebalancen hos patienter, der oplever svær eller langvarig diarré eller får medicin, der påvirker elektrolytniveauet, såsom diuretika, afføringsmidler, systemiske kortikosteroider eller amphotericin B.
Synsforstyrrelser og tab af syn
Optisk neuropati og optisk neuritis
Tilfælde af optisk neuropati og optisk neuritis, som sædvanligvis resulterer i synsnedsættelse og nogle gange permanent blindhed, er blevet rapporteret hos patienter behandlet med amiodaron og kan forekomme på ethvert tidspunkt under behandlingen. Hvis der opstår symptomer på synshandicap, såsom ændringer i synsstyrke og fald i perifert syn, skal du overveje at seponere CORDARONE 100 mg og straks henvise til oftalmisk undersøgelse. Regelmæssig oftalmisk undersøgelse, inklusive funduskopi og spaltelampeundersøgelse, anbefales under administration af CORDARONE [se BIVIRKNINGER ].
Hornhinde mikroaflejringer
Korneale mikroaflejringer forekommer hos størstedelen af voksne behandlet med CORDARONE. De er normalt kun synlige ved spaltelampeundersøgelse, men giver anledning til symptomer som visuelle glorier eller sløret syn hos så mange som 10 % af patienterne. Korneale mikroaflejringer er reversible ved reduktion af dosis eller afslutning af behandling. Asymptomatiske mikroaflejringer alene er ikke en grund til at reducere dosis eller afbryde behandlingen [se BIVIRKNINGER ].
Skjoldbruskkirtel abnormiteter
CORDARONE 50mg hæmmer perifer omdannelse af thyroxin (T4) til triiodothyronin (T3) og kan forårsage øgede thyroxinniveauer, nedsatte T3-niveauer og øgede niveauer af inaktivt omvendt T3 (rT3) hos klinisk euthyroidpatienter. CORDARONE 50mg kan forårsage enten hypothyroidisme (rapporteret hos op til 10 % af patienterne) eller hyperthyroidisme (forekommer hos omkring 2 % af patienterne). Overvåg skjoldbruskkirtelfunktionen før behandling og periodisk derefter, især hos ældre patienter og hos enhver patient med tidligere skjoldbruskkirtelknolder, struma eller anden skjoldbruskkirteldysfunktion.
Hyperthyroidisme kan inducere arytmigennembrud. Hvis der opstår nye tegn på arytmi, bør muligheden for hyperthyroidisme overvejes. Antithyroidmedicin, β-adrenerge blokkere, midlertidig kortikosteroidbehandling kan være nødvendig for at behandle symptomerne på hyperthyroidisme. Virkningen af antithyreoidealægemidler kan være forsinket ved amiodaron-induceret thyrotoksikose på grund af betydelige mængder af præformede skjoldbruskkirtelhormoner, der er lagret i kirtlen. Behandling med radioaktivt jod er kontraindiceret på grund af den lave radiojodoptagelse forbundet med amiodaron-induceret hyperthyroidisme. CORDARONE-induceret hyperthyroidisme kan efterfølges af en forbigående periode med hypothyroidisme.
Hypothyroidisme kan være primær eller efter opløsning af forudgående amiodaron-induceret hyperthyroidisme. Alvorlig hypothyroidisme og myxødem koma, nogle gange dødelig, er blevet rapporteret i forbindelse med amiodaronbehandling. Hos nogle klinisk hypothyroid amiodaron-behandlede patienter kan frit thyroxinindeksværdier være normale. Håndter hypothyroidisme ved at reducere dosis af eller afbryde CORDARONE og thyreoideahormontilskud.
Bradykardi
CORDARONE forårsager symptomatisk bradykardi eller sinusstop med undertrykkelse af escape foci hos 2 til 4 % af patienterne. Risikoen øges ved elektrolytiske lidelser eller brug af samtidig antiarytmika eller negative kronotroper [se DRUGSINTERAKTIONER ]. Bradykardi kan kræve en pacemaker til frekvenskontrol.
Postmarketingtilfælde af symptomatisk bradykardi, hvoraf nogle kræver pacemakerindsættelse og mindst én fatal, er blevet rapporteret, når ledipasvir/sofosbuvir eller sofosbuvir med simeprevir blev påbegyndt hos patienter på amiodaron. Bradykardi opstod generelt inden for timer til dage, men i nogle tilfælde optrådte op til 2 uger efter påbegyndelse af antiviral behandling. Bradykardi forsvandt generelt efter seponering af antiviral behandling. Mekanismen for denne effekt er ukendt. Overvåg hjertefrekvens hos patienter, der tager eller for nylig har seponeret amiodaron, når de starter antiviral behandling [se DRUGSINTERAKTIONER ].
Implanterbare hjerteudstyr
Hos patienter med implanterede defibrillatorer eller pacemakere kan kronisk administration af antiarytmiske lægemidler påvirke pacing- eller defibrilleringstærsklerne. Derfor bør pacing- og defibrilleringstærskler vurderes ved begyndelsen af og under amiodaronbehandling.
Føtal toksicitet
CORDARONE kan forårsage fosterskader, når det administreres til en gravid kvinde. Fostereksponering kan øge potentialet for hjerte-, skjoldbruskkirtel-, neuroudviklingsmæssige, neurologiske og vækstpåvirkninger hos nyfødte [se Brug i specifikke populationer ].
Perifer neuropati
Kronisk administration af CORDARONE kan føre til perifer neuropati, som muligvis ikke forsvinder, når CORDARONE seponeres.
Lysfølsomhed og misfarvning af huden
CORDARONE inducerer fotosensibilisering hos omkring 10 % af patienterne; en vis beskyttelse kan gives sol-barriere cremer eller beskyttende tøj. Ved langtidsbehandling kan der forekomme en blågrå misfarvning af den blottede hud. Risikoen kan være øget hos patienter med lys hud eller patienter med overdreven soleksponering. En vis vending af misfarvning kan forekomme ved seponering af lægemidlet.
Kirurgi
Flygtige anæstesimidler
Patienter i behandling med CORDARONE 100 mg kan være mere følsomme over for de myokardiedepressive og ledningseffekter af halogenerede inhalationsanæstetika.
Patientrådgivningsinformation
Råd patienten til at læse den FDA-godkendte patientmærkning ( Medicinvejledning ).
Rådgiv gravide kvinder om den potentielle risiko for et foster. Rådgiv kvinder med reproduktionspotentiale om at informere deres ordinerende læge om en kendt eller formodet graviditet [se Brug i specifikke populationer ].
Rådfør kvinder om, at amning ikke anbefales under behandling med CORDARONE [se Brug i specifikke populationer ].
Rådgive patienter til at undgå grapefrugtjuice og perikon.
Råd patienter til at søge lægehjælp, hvis de oplever tegn og symptomer på pulmonal toksicitet, forværret arytmi, bradykardi, synsnedsættelse eller hypo- og hyperthyroidisme.
Dette produkts etiket er muligvis blevet opdateret. For fuldstændig ordinationsinformation, besøg venligst www.pfizer.com.
Ikke-klinisk toksikologi
Karcinogenese, mutagenese, svækkelse af fertilitet
Amiodaron HCl var forbundet med en statistisk signifikant, dosisrelateret stigning i forekomsten af thyreoidea-tumorer (follikulært adenom og/eller karcinom) hos rotter. Forekomsten af skjoldbruskkirteltumorer var større end kontrollen ved det laveste testede dosisniveau, dvs. 5 mg/kg/dag (ca. 0,08 gange den maksimalt anbefalede humane vedligeholdelsesdosis*).
Mutagenicitetsundersøgelser (Ames, mikronucleus og lysogene test) med CORDARONE var negative.
I et studie, hvor amiodaron HCl blev administreret til han- og hunrotter, begyndende 9 uger før parring, blev der observeret nedsat fertilitet ved et dosisniveau på 90 mg/kg/dag (ca. 1,4 gange den maksimale anbefalede humane vedligeholdelsesdosis*).
*600 mg hos en patient på 60 kg (dosis sammenlignet på basis af kropsoverfladeareal)
Brug i specifikke populationer
Graviditet
Risikooversigt
Tilgængelige data fra postmarketing-rapporter og offentliggjorte case-serier indikerer, at brug af amiodaron hos gravide kvinder kan øge risikoen for føtale bivirkninger, herunder neonatal hypo- og hyperthyroidisme, neonatal bradykardi, neuroudviklingsabnormiteter, præterm fødsel og føtal vækstbegrænsning. Amiodaron og dets metabolit, desethylamiodaron (DEA), krydser placenta. Ubehandlede underliggende arytmier, herunder ventrikulære arytmier, under graviditet udgør en risiko for moderen og fosteret (se Kliniske overvejelser ). I dyreforsøg resulterede administration af amiodaron til kaniner, rotter og mus under organogenese i embryoføtal toksicitet ved doser mindre end den maksimalt anbefalede humane vedligeholdelsesdosis (se Data ). Rådgiv gravide kvinder om den potentielle risiko for et foster.
Den estimerede baggrundsrisiko for alvorlige fødselsdefekter og abort for den angivne population er ukendt. Alle graviditeter har en baggrundsrisiko for fødselsdefekter, tab eller andre ugunstige udfald. I den generelle befolkning i USA er den estimerede baggrundsrisiko for alvorlige fødselsdefekter og abort i klinisk anerkendte graviditeter henholdsvis 2%-4% og 15%-20%.
Kliniske overvejelser
Sygdomsassocieret moder- og eller embryo-/fosterrisiko
Hyppigheden af ventrikulær takykardi er øget og kan være mere symptomatisk under graviditet. Ventrikulære arytmier forekommer oftest hos gravide kvinder med underliggende kardiomyopati, medfødt hjertesygdom, hjerteklapsygdom eller mitralklapprolaps. De fleste takykardiepisoder initieres af ektopiske slag, og forekomsten af arytmiepisoder kan derfor øges under graviditeten på grund af den øgede tilbøjelighed til ektopisk aktivitet. Gennembrudsarytmier kan også forekomme under graviditet, da terapeutiske behandlingsniveauer kan være vanskelige at opretholde på grund af det øgede distributionsvolumen og øget stofskifte i den gravide tilstand.
Fetale/neonatale bivirkninger
Amiodaron og dets metabolit har vist sig at krydse placenta. Uønskede føtale virkninger forbundet med moderbrug af amiodaron under graviditet kan omfatte neonatal bradykardi, QT-forlængelse og periodiske ventrikulære ekstrasystoler, neonatal hypothyroidisme (med eller uden struma) påvist antenatalt eller hos den nyfødte og rapporteret selv efter et par dages eksponering, neonatal hyperthyroxinæmi, neuroudviklingsmæssige abnormiteter uafhængigt af skjoldbruskkirtelfunktionen, herunder taleforsinkelse og vanskeligheder med skriftsprog og aritmetik, forsinket motorisk udvikling og ataksi, ryknystagmus med synkron hovedtitubation, fostervækstbegrænsning og for tidlig fødsel. Overvåg den nyfødte for tegn og symptomer på skjoldbruskkirtelsygdom og hjertearytmier.
Arbejde og levering
Risikoen for arytmier kan øges under veer og fødsel. Patienter, der behandles med CORDARONE, skal overvåges kontinuerligt under fødslen og fødslen [se ADVARSLER OG FORHOLDSREGLER ].
Data
Dyredata
Hos drægtige rotter og kaniner i organogeneseperioden havde amiodaron HCl i doser på 25 mg/kg/dag (henholdsvis ca. 0,4 og 0,9 gange den maksimalt anbefalede humane vedligeholdelsesdosis*) ingen bivirkninger på fosteret. Hos kaninen forårsagede 75 mg/kg/dag (ca. 2,7 gange den maksimalt anbefalede humane vedligeholdelsesdosis*) aborter hos mere end 90 % af dyrene. Hos rotter var doser på 50 mg/kg/dag eller mere forbundet med let forskydning af testiklerne og en øget forekomst af ufuldstændig ossifikation af nogle kranier og digitale knogler; ved 100 mg/kg/dag eller mere blev fosterets kropsvægt reduceret; ved 200 mg/kg/dag var der en øget forekomst af føtal resorption. (Disse doser hos rotter er ca. 0,8, 1,6 og 3,2 gange den maksimale anbefalede humane vedligeholdelsesdosis*) Bivirkninger på føtal vækst og overlevelse blev også observeret i en af to musestammer ved en dosis på 5 mg/kg/dag ( ca. 0,04 gange den maksimalt anbefalede humane vedligeholdelsesdosis*).
*600 mg hos en patient på 60 kg (doser sammenlignet på basis af kropsoverfladeareal)
Amning
Risikooversigt
Amiodaron og en af dets vigtigste metabolitter, DEA, er til stede i modermælk i mellem 3,5 % og 45 % af moderens vægtjusterede dosis af amiodaron. Der er tilfælde af hypothyroidisme og bradykardi hos ammede spædbørn, selvom det er uklart, om disse virkninger skyldes amiodaroneksponering i modermælk. Amning frarådes under behandling med CORDARONE [se ADVARSLER OG FORHOLDSREGLER ].
Hunner og mænd med reproduktionspotentiale
Infertilitet
Baseret på dyrefertilitetsundersøgelser kan CORDARONE reducere kvindelig og mandlig fertilitet. Det vides ikke, om denne effekt er reversibel. [se Ikke-klinisk toksikologi ].
Pædiatrisk brug
Sikkerheden og effektiviteten af CORDARONE hos pædiatriske patienter er ikke blevet fastslået.
Geriatrisk brug
Normale forsøgspersoner over 65 år viser lavere clearance og øget lægemiddelhalveringstid end yngre forsøgspersoner [se KLINISK FARMAKOLOGI ]. Generelt bør dosisvalg for en ældre patient være forsigtigt, sædvanligvis begyndende i den lave ende af doseringsområdet, hvilket afspejler den større hyppighed af nedsat lever-, nyre- eller hjertefunktion og af samtidig sygdom eller anden lægemiddelbehandling.
OVERDOSIS
Der har været tilfælde, nogle dødelige, af CORDARONE 50 mg overdosis.
Overvåg patientens hjerterytme og blodtryk, og hvis der opstår bradykardi, kan en β-adrenerg agonist eller en pacemaker anvendes. Behandl hypotension med utilstrækkelig vævsperfusion med positive inotrope og vasopressormidler. Hverken CORDARONE 50mg eller dets metabolit kan dialyseres.
KONTRAINDIKATIONER
- Kardiogent shock.
- Syg sinus syndrom, anden- eller tredjegrads atrioventrikulær blokering, bradykardi, der fører til synkope uden en fungerende pacemaker.
- Kendt overfølsomhed over for lægemidlet eller nogen af dets komponenter, herunder jod.
KLINISK FARMAKOLOGI
Handlingsmekanisme
Amiodaron betragtes som et klasse III antiarytmisk lægemiddel, men det besidder elektrofysiologiske egenskaber fra alle fire Vaughan Williams klasser. Ligesom klasse I-lægemidler blokerer amiodaron natriumkanaler ved hurtige pacing-frekvenser, og ligesom klasse II-lægemidler udøver amiodaron en ikke-kompetitiv antisympatisk virkning. En af dens vigtigste virkninger, ved langvarig administration, er at forlænge det kardiale handlingspotentiale, en klasse III-effekt. Den negative kronotropiske virkning af amiodaron i knudevæv svarer til virkningen af klasse IV-lægemidler. Ud over at blokere natriumkanaler blokerer amiodaron myokardiale kaliumkanaler, hvilket bidrager til at nedsætte ledningsevnen og forlænge refraktæriteten. Den antisympatiske virkning og blokeringen af calcium- og kaliumkanaler er ansvarlige for de negative dromotrope virkninger på sinusknuden og for sænkning af ledning og forlængelse af refraktæritet i den atrioventrikulære (AV) knude. Dens vasodilatatoriske virkning kan mindske hjertearbejdsbelastningen og følgelig myokardiets iltforbrug.
CORDARONE forlænger varigheden af aktionspotentialet for alle hjertefibre, mens det forårsager minimal reduktion af dV/dt (maksimal opslagshastighed af aktionspotentialet). Den refraktære periode forlænges i alle hjertevæv. CORDARONE øger den kardiale refraktære periode uden at påvirke hvilemembranpotentialet, undtagen i automatiske celler, hvor hældningen af præpotentialet er reduceret, hvilket generelt reducerer automatikken. Disse elektrofysiologiske effekter afspejles i en nedsat sinusrate på 15 til 20 %, øgede PR- og QT-intervaller på omkring 10 %, udviklingen af U-bølger og ændringer i T-bølgekonturen. Disse ændringer bør ikke kræve afbrydelse af CORDARONE 50 mg, da de er tegn på dets farmakologiske virkning, selvom CORDARONE kan forårsage markant sinusbradykardi eller sinusstop og hjerteblokering [se ADVARSLER OG FORHOLDSREGLER ].
Hæmodynamik
dyreforsøg og efter intravenøs administration hos mennesker afslapper CORDARONE 100mg vaskulær glat muskulatur, reducerer perifer vaskulær modstand (efterbelastning) og øger hjerteindekset en smule. Efter oral dosering producerer CORDARONE 100mg imidlertid ingen signifikant ændring i venstre ventrikulær ejektionsfraktion (LVEF), selv hos patienter med deprimeret LVEF. Efter akut intravenøs dosering til mennesker kan CORDARONE 100mg have en mild negativ inotrop effekt.
Farmakodynamik
Der er ingen veletableret sammenhæng mellem plasmakoncentration og effektivitet, men det ser ud til, at koncentrationer meget under 1 mg/L ofte er ineffektive, og at niveauer over 2,5 mg/L generelt ikke er nødvendige. Plasmakoncentrationsmålinger kan bruges til at identificere patienter, hvis niveauer er usædvanligt lave, og som kan have gavn af en dosisforhøjelse eller usædvanlig høj, og som kan have dosisreduktion i håb om at minimere bivirkninger.
Effekter på unormale rytmer ses ikke før 2 til 3 dage og kræver normalt 1 til 3 uger, selv når en startdosis anvendes. Der kan være en fortsat stigning i effekten i længere perioder stadig. Der er evidens for, at virkningstiden er kortere, når der anvendes en loading-dosis regime.
I overensstemmelse med den langsomme eliminationshastighed vedvarer antiarytmiske virkninger i uger eller måneder efter seponering af CORDARONE 50mg, men tidspunktet for tilbagefald er variabelt og uforudsigeligt. Generelt, når lægemidlet genoptages efter tilbagefald af arytmien, etableres kontrol relativt hurtigt sammenlignet med den indledende respons, formentlig fordi vævslagrene ikke var fuldstændigt udtømte.
Farmakokinetik
Absorption
Efter oral administration til mennesker absorberes CORDARONE langsomt og variabelt. Biotilgængeligheden af CORDARONE er ca. 50%. Maksimal plasmakoncentration opnås 3 til 7 timer efter en enkelt dosis. Plasmakoncentrationer ved kronisk dosering på 100 til 600 mg/dag er omtrent dosisproportionale, med en gennemsnitlig stigning på 0,5 mg/L for hver 100 mg/dag. Disse midler omfatter imidlertid betydelig individuel variabilitet.
Mad øger hastigheden og omfanget af absorptionen af CORDARONE. Virkningerne af mad på biotilgængeligheden af CORDARONE er blevet undersøgt hos 30 raske forsøgspersoner, som fik en enkelt dosis på 600 mg umiddelbart efter indtagelse af et fedtrigt måltid og efter en faste natten over. Arealet under plasmakoncentration-tid-kurven (AUC) og den maksimale plasmakoncentration (Cmax) af amiodaron steg med henholdsvis 2,3 (interval 1,7 til 3,6) og 3,8 (interval 2,7 til 4,4) gange i nærvær af mad. Mad øgede også absorptionshastigheden af amiodaron, hvilket reducerede tiden til maksimal plasmakoncentration (Tmax) med 37 %. Den gennemsnitlige AUC og den gennemsnitlige Cmax for hovedmetabolitten af amiodaron, DEA steg med henholdsvis 55% (interval 58 til 101%) og 32% (interval 4 til 84%), men der var ingen ændring i Tmax ved tilstedeværelse af mad.
Fordeling
CORDARONE er stærkt proteinbundet (ca. 96%). CORDARONE har et meget stort, men variabelt distributionsvolumen, i gennemsnit omkring 60 l/kg, på grund af omfattende ophobning på forskellige steder, især fedtvæv og stærkt perfunderede organer, såsom lever, lunge og milt.
En hovedmetabolit af CORDARONE 50mg, DEA, er blevet identificeret hos mennesker; det akkumuleres i endnu højere grad i næsten alle væv. Der er ingen tilgængelige data om aktiviteten af DEA hos mennesker, men hos dyr har det signifikante elektrofysiologiske og antiarytmiske virkninger, der generelt ligner amiodaron selv. DEA's præcise rolle og bidrag til den antiarytmiske aktivitet af oral amiodaron er ikke sikker. Udviklingen af maksimal ventrikulær klasse III-effekt efter oral CORDARONE 100 mg administration hos mennesker korrelerer tættere med DEA-akkumulering over tid end med amiodaron-akkumulering.
Elimination
Efter administration af en enkelt dosis til 12 raske forsøgspersoner udviste CORDARONE multi-kompartmental farmakokinetik med en gennemsnitlig tilsyneladende terminal plasmahalveringstid på 58 dage (interval 15 til 142 dage) for amiodaron og 36 dage (interval 14 til 75 dage) for den aktive metabolit (DEA). Hos patienter har CORDARONE 100 mg efter seponering af kronisk oral behandling vist sig at have en bifasisk elimination med en initial 50 % reduktion af plasmaniveauer efter 2,5 til 10 dage. En meget langsommere terminal plasmaelimineringsfase viser en halveringstid af moderforbindelsen i området fra 26 til 107 dage, med et gennemsnit på ca. 53 dage og de fleste patienter i intervallet 40 til 55 dage. I fravær af en loading-dosis-periode ville steady-state plasmakoncentrationer, ved konstant oral dosering, derfor nås mellem 130 og 535 dage med et gennemsnit på 265 dage. For metabolitten var den gennemsnitlige plasmaelimineringshalveringstid ca. 61 dage. Disse data afspejler sandsynligvis en initial eliminering af lægemiddel fra godt perfunderet væv (halveringstiden på 2,5 til 10 dage), efterfulgt af en terminal fase, der repræsenterer ekstremt langsom eliminering fra dårligt perfunderet vævsrum, såsom fedt.
Den betydelige inter-individuelle variation i begge eliminationsfaser, såvel som usikkerheden med hensyn til, hvilket kompartment der er afgørende for lægemiddeleffekten, kræver opmærksomhed på individuelle responser, når først arytmikontrol er opnået med ladningsdoser, fordi den korrekte vedligeholdelsesdosis bestemmes, delvist. ved eliminationsraterne. Tilpas vedligeholdelsesdoser af CORDARONE [se DOSERING OG ADMINISTRATION ].
Metabolisme
Amiodaron metaboliseres til DEA af cytochrom P450 (CYP) enzymgruppen, specifikt CYP3A og CYP2C8. CYP3A isoenzymet er til stede i både leveren og tarmene. In vitro udviser amiodaron og DEA potentiale til at hæmme CYP2C9, CYP2C19, CYP2D6, CYP3A, CYP2A6, CYP2B6 og CYP2C8. Amiodaron og DEA har også potentiale til at hæmme nogle transportere såsom P-glycoprotein og organisk kationtransporter (OCT2).
Udskillelse
Amiodaron elimineres primært ved hepatisk metabolisme og galdeudskillelse, og der er ubetydelig udskillelse af amiodaron eller DEA i urinen. Hverken amiodaron eller DEA er dialyserbare.
Specifikke populationer
Effekt af alder
Normale forsøgspersoner over 65 år viser lavere clearance (ca. 100 ml/time/kg) end yngre forsøgspersoner (ca. 150 ml/time/kg) og en stigning i t½ fra ca. 20 til 47 dage.
Nedsat nyrefunktion
Nedsat nyrefunktion påvirker ikke farmakokinetikken af amiodaron eller DEA.
Nedsat leverfunktion
Efter en enkelt dosis af intravenøs amiodaron til cirrosepatienter ses signifikant lavere Cmax og gennemsnitlige koncentrationsværdier for DEA, men gennemsnitlige amiodaronniveauer er uændrede.
Hjertesygdom
Hos patienter med svær venstre ventrikulær dysfunktion ændres amiodarons farmakokinetik ikke signifikant, men den terminale elimination t½ af DEA er forlænget.
Selvom der ikke er defineret nogen dosisjustering for patienter med nyre-, lever- eller hjerteabnormiteter under kronisk behandling med oral amiodaron, er tæt klinisk monitorering forsigtig for ældre patienter og dem med alvorlig venstre ventrikel dysfunktion.
Lægemiddelinteraktioner
Virkninger af andre midler på amiodaron
Grapefrugtjuice: Grapefrugtjuice givet til raske frivillige øgede amiodaron AUC med 50 % og Cmax med 84 % og reducerede DEA til ikke-kvantificerbare koncentrationer.
Cimetidin hæmmer CYP3A og kan øge serumamiodaronniveauet.
Kolestyramin reducerer den enterohepatiske cirkulation af amiodaron og øger derved dets eliminering. Dette resulterer i reducerede amiodaron-serumniveauer og halveringstid.
Virkninger af amiodaron på midler
CYP3A substrater
Amiodaron taget samtidig med quinidin øger quinidinserumkoncentrationen med 33 % efter to dage. Amiodaron taget samtidig med procainamid i mindre end syv dage øger plasmakoncentrationerne af procainamid og n-acetylprocainamid med henholdsvis 55 % og 33 %.
Loratadin, et ikke-sederende antihistamin, metaboliseres primært af CYP3A, og dets metabolisme kan hæmmes af amiodaron.
Metabolismen af lidocain kan hæmmes af amiodaron.
Cyclophosphamid er et prodrug, der metaboliseres af CYP450 inklusive CYP3A til en aktiv metabolit. Metabolismen af cyclophosphamid kan hæmmes af amiodaron.
Clopidogrel, et inaktivt thienopyridin-prodrug, metaboliseres i leveren af CYP3A til en aktiv metabolit. En potentiel interaktion mellem clopidogrel og amiodaron, der resulterer i ineffektiv hæmning af trombocytaggregation, er blevet rapporteret.
Macrolid/Ketolide Antibiotika
Amiodaron kan hæmme metabolismen af makrolid/ketolid-antibiotika (undtagen azithromycin) og systemiske azol-svampemidler.
P-glycoprotein substrater
Amiodaron taget samtidig med digoxin øger serumdigoxinkoncentrationen med 70 % efter en dag.
Dabigatran etexilat, når det tages samtidig med oral amiodaron, kan resultere i forhøjet serumkoncentration af dabigatran.
Dextromethorphan er et substrat for både CYP2D6 og CYP3A. Amiodaron hæmmer CYP2D6. Kronisk (> 2 uger) oral administration af amiodaron svækker metabolismen af dextromethorphan kan føre til øgede serumkoncentrationer.
PATIENTOPLYSNINGER
CORDARONE® (KOR-DU-RON) (amiodaron) tabletter
Hvad er den vigtigste information, jeg bør vide om CORDARONE 50mg?
CORDARONE kan forårsage alvorlige bivirkninger, der kan føre til døden, herunder:
- lungeproblemer
- leverproblemer
- forværring af hjerteslagsproblemer
Ring til din læge eller få lægehjælp med det samme, hvis du har nogle af følgende symptomer under behandling med CORDARONE:
- vejrtrækningsbesvær, hvæsende vejrtrækning, åndenød, hostende brystsmerter, opspytning af blod eller feber
- kvalme eller opkastning, brun eller mørkfarvet urin, føler sig mere træt end normalt, gulfarvning af din hud eller det hvide i øjnene (gulsot) eller smerter i det øverste højre side af maven
- hjertet banker, springer et slag over, slår hurtigt eller langsomt, føler dig svimmel, eller hvis du besvimer
- synsproblemer, herunder sløret syn, se glorier, eller dine øjne bliver følsomme over for lys. Du bør have regelmæssige øjenundersøgelser før og under behandlingen med CORDARONE.
CORDARONE bør startes på et hospital, så din medicinske tilstand kan overvåges nøje.
CORDARONE bør kun bruges til at behandle personer, der er blevet diagnosticeret med livstruende hjerteslagsproblemer kaldet ventrikulære arytmier, når andre behandlinger ikke virkede, eller du ikke kan tolerere dem.
CORDARONE 50mg kan forårsage andre alvorlige bivirkninger. Se "Hvad er de mulige bivirkninger af CORDARONE 100mg?" Hvis du får alvorlige bivirkninger under behandlingen, skal du muligvis stoppe med CORDARONE, få ændret din dosis eller få medicinsk behandling. Tal med din læge, før du holder op med at tage CORDARONE.
Du kan stadig få bivirkninger, efter du er stoppet med CORDARONE, fordi medicinen forbliver i din krop i flere måneder efter behandlingen er stoppet.
Du bør have regelmæssig kontrol, blodprøver, røntgenbilleder af thorax før og under behandling med CORDARONE 100mg for at tjekke for alvorlige bivirkninger. Du bør også have lungefunktionstest, før du starter behandling med CORDARONE.
Hvad er CORDARONE?
CORDARONE er en receptpligtig medicin, der bruges til at behandle mennesker, der er blevet diagnosticeret med livstruende hjerteslagsproblemer kaldet ventrikulære arytmier, når andre behandlinger ikke virkede, eller du ikke kan tolerere dem. Det vides ikke, om CORDARONE er sikkert og effektivt til børn.
Hvem bør ikke tage CORDARONE 100mg?
Tag ikke CORDARONE 100 mg, hvis du:
- har et alvorligt hjerteproblem kaldet kardiogent shock
- har visse typer af hjertesygdommen kaldet hjerteblokade, med eller uden langsom puls
- har en langsom puls med svimmelhed eller svimmelhed, og du ikke har en indopereret pacemaker
- er allergisk over for amiodaron, jod eller et af de øvrige indholdsstoffer i CORDARONE. Se slutningen af denne medicinvejledning for en komplet liste over ingredienser i CORDARONE.
Inden du tager CORDARONE 100mg, skal du fortælle din læge om alle dine medicinske tilstande, inklusive hvis du:
- har lunge- eller vejrtrækningsproblemer
- har leverproblemer
- har eller haft problemer med skjoldbruskkirtlen
- har en langsom puls eller blodtryksproblemer
- har diarré eller har haft diarré i længere tid
- har fået at vide, at du har lave niveauer af kalium, magnesium eller calcium i dit blod
- har en implanteret pacemaker eller defribrillator
- hvis du planlægger at blive opereret med generel anæstesi
- er gravid eller planlægger at blive gravid. CORDARONE kan skade dit ufødte barn. Fortæl det straks til din læge, hvis du bliver gravid under behandling med CORDARONE. CORDARONE 100mg kan blive i din krop i flere måneder efter behandlingen er stoppet.
- ammer eller planlægger at amme. CORDARONE 100mg kan passere over i din modermælk og kan skade din baby. Du bør ikke amme, mens du tager CORDARONE. CORDARONE kan forblive i din krop i flere måneder efter behandlingen er stoppet. Tal med din læge om den bedste måde at fodre din baby på i denne tid.
Fortæl din sundhedsudbyder om al den medicin, du tager, inklusive receptpligtig og håndkøbsmedicin, vitaminer og naturlægemidler. CORDARONE 50mg og visse andre lægemidler kan påvirke hinanden og forårsage alvorlige bivirkninger. Du kan bede din apotek om en liste over lægemidler, der interagerer med CORDARONE.
Hvordan skal jeg tage CORDARONE?
- Når du bliver udskrevet fra hospitalet, skal du tage CORDARONE nøjagtigt, som din læge siger, at du skal tage det.
- Din læge vil fortælle dig, hvor meget CORDARONE du skal tage, og hvornår du skal tage det.
- Din læge kan ændre din dosis af CORDARONE 50mg efter behov, hvis din hjerterytme er kontrolleret, eller hvis du har visse bivirkninger. Din læge bør overvåge dig omhyggeligt, når din dosis af CORDARONE 50mg bliver ændret.
- Tag din dosis CORDARONE på samme måde hver gang, enten med eller uden mad.
- Hvis du tager for meget CORDARONE 100mg, skal du straks ringe til din læge eller gå til den nærmeste skadestue. Hvis du glemmer en dosis, skal du vente og tage din næste dosis på dit normale tidspunkt. Tag ikke to doser på samme tid. Fortsæt med din næste regelmæssige planlagte dosis.
Hvad skal jeg undgå, mens jeg tager CORDARONE?
- Undgå at drikke grapefrugtjuice under behandling med CORDARONE. At drikke grapefrugtjuice med CORDARONE 50mg kan øge mængden af CORDARONE i dit blod, og dette kan føre til bivirkninger.
- CORDARONE 100mg kan gøre din hud følsom over for sollys. Du kan få alvorlig solskoldning. Brug solcreme og brug en hat og tøj, der dækker din hud for at hjælpe med at beskytte dig, hvis du skal være i sollys. Tal med din læge, hvis du bliver solskoldet. Se "Hudproblemer" i afsnittet Medicinvejledning "Hvad er de mulige bivirkninger af CORDARONE?" under.
Hvad er de mulige bivirkninger af CORDARONE?
CORADARONE kan forårsage alvorlige bivirkninger, herunder:
- Se "Hvad er den vigtigste information, jeg bør vide om CORDARONE?"
- Nerveproblemer. CORDARONE 100mg kan give nerveproblemer. Ring til din læge, hvis du udvikler symptomer på nerveproblemer, herunder: en følelse af "pinde og nåle" eller følelsesløshed i dine hænder, ben eller fødder, muskelsvaghed, ukontrollerede bevægelser, dårlig koordination eller problemer med at gå.
- Hudproblemer. CORDARONE kan få din hud til at være mere følsom over for solen eller få en blågrå farve. Folk, der har lys hud eller folk, der har meget soleksponering, kan være mere udsatte for disse hudproblemer. Noget af den blågrå hudfarve kan vende tilbage til normal efter ophør med CORDARONE.
- Skjoldbruskkirtel problemer. CORDARONE kan forårsage, at du enten har nedsat skjoldbruskkirtelfunktion (hypothyroidisme), som nogle gange kan være alvorlig, eller en overaktiv skjoldbruskkirtel (hyperthyroidisme), som kan være alvorlig.
- Hvis du udvikler nedsat skjoldbruskkirtelfunktion under behandling med CORDARONE, skal din læge muligvis reducere din dosis eller stoppe din behandling med CORDARONE og eventuelt ordinere medicin til at erstatte dit skjoldbruskkirtelhormon.
- En overaktiv skjoldbruskkirtel kan få dig til at producere for meget skjoldbruskkirtelhormon. Du kan få unormale hjerteslag, selv mens du får CORDARONE. Din læge kan ordinere visse lægemidler til behandling af din overaktive skjoldbruskkirtel. Ring til din læge, hvis du får unormale hjerteslag under behandlingen med CORDARONE. Det kan betyde, at du har en overaktiv skjoldbruskkirtel.
- Din læge bør foretage tests for at kontrollere din skjoldbruskkirtelfunktion, før du starter og under behandlingen med CORDARONE.
- Ring til din læge, hvis du udvikler nogle af følgende symptomer på et skjoldbruskkirtelproblem under behandling med CORDARONE:
- svaghed
- vægttab eller vægtøgning
- varme- eller kuldeintolerance
- hår udtynding
- svedtendens
- ændringer i dine menstruationer
- hævelse af din nakke (struma)
- nervøsitet
- irritabilitet
- rastløshed
- nedsat koncentration
- føler sig deprimeret (hos ældre)
- rysten
De mest almindelige bivirkninger af CORDARONE omfatter:
- lungeproblemer
- hjerteslagsproblemer
- hjerteproblemer
- leverproblemer
CORDARONE 50mg kan påvirke fertiliteten hos mænd og kvinder. Det vides ikke, om virkningerne er reversible. Tal med din læge, hvis du har bekymringer om fertilitet.
Disse er ikke alle de mulige bivirkninger af CORDARONE. For mere information, spørg din læge eller apotek.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan skal jeg opbevare CORDARONE?
- Opbevar CORDARONE 100mg ved stuetemperatur mellem 20° til 25°C (68° til 77°F).
- Opbevar CORDARONE i en tæt lukket beholder, og hold CORDARONE 50 mg væk fra lyset.
Opbevar CORDARONE 50mg og al medicin utilgængeligt for børn.
Generel information om sikker og effektiv brug af CORDARONE
Lægemidler ordineres nogle gange til andre formål end dem, der er anført i en medicinvejledning. Brug ikke CORDARONE til en tilstand, som det ikke er ordineret til. Giv ikke CORDARONE til andre mennesker, selvom de har de samme symptomer, som du har. Det kan skade dem. Du kan bede din apoteker eller sundhedsudbyder om oplysninger om CORDARONE, som er skrevet til sundhedspersonale.
Hvad er ingredienserne i CORDARONE 100mg?
Aktiv ingrediens: amiodaron HCl
Inaktive ingredienser: kolloid siliciumdioxid, lactose, magnesiumstearat, povidon, stivelse og FD&C Red 40.
Denne medicinvejledning er godkendt af US Food and Drug Administration.
