Cardizem 30mg, 60mg, 90mg, 120mg, 180mg Diltiazem Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Cardizem 120mg, og hvordan bruges det?
Cardizem er en receptpligtig medicin, der bruges til at behandle symptomerne på brystsmerter (angina), forhøjet blodtryk (hypertension) samt visse hjerterytmeforstyrrelser såsom farligt hurtige hjerteslag (paroksysmal supraventrikulær takykardi) og atrieflimren/fladder. Cardizem kan bruges alene eller sammen med anden medicin.
Cardizem tilhører en klasse af lægemidler kaldet Antidysrhythmics, IV; Calciumkanalblokkere; Calciumkanalblokkere, ikke-dihydropyridin.
Hvad er de mulige bivirkninger af Cardizem 120mg?
Cardizem kan forårsage alvorlige bivirkninger, herunder:
- brystsmerter,
- langsomme hjerteslag,
- bankende hjerteslag eller flagrende i dit bryst,
- svimmelhed,
- hævelse,
- hurtig vægtøgning, og
- følelse af åndenød
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Cardizem omfatter:
- hævelse,
- svimmelhed,
- svaghed,
- hovedpine,
- kvalme, og
- udslæt
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Cardizem. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
CARDIZEM® (diltiazemhydrochlorid) er en cellulær calciumion-influxhæmmer (langsom kanalblokker eller calciumantagonist). Kemisk er diltiazemhydrochlorid 1,5-benzothiazepin-4(5H)-on, 3-(acetyloxy)-5-[2-(dimethylamino)ethyl]-2,3-dihydro-2-(4-methoxyphenyl)-, monohydrochlorid,(+)-cis-. Den kemiske struktur er:
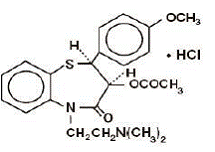
Diltiazem hydrochlorid er et hvidt til råhvidt krystallinsk pulver med en bitter smag. Det er opløseligt i vand, methanol og chloroform. Det har en molekylvægt på 450,98. Hver tablet CARDIZEM 60 mg indeholder 30 mg, 60 mg, 90 mg eller 120 mg diltiazemhydrochlorid.
Indeholder også: kolloid siliciumdioxid, D&C Yellow #10 Aluminium Lake, FD&C Blue #1 Aluminium Lake (30 mg og 90 mg), FD&C Yellow #6 Aluminium Lake (60 mg og 120 mg), hydroxypropylcellulose, hypromellose, lactose, magnesium stearat, methylparaben, mikrokrystallinsk cellulose og polyethylenglycol.
Til oral administration.
INDIKATIONER
CARDIZEM 120mg er indiceret til behandling af kronisk stabil angina og angina på grund af kranspulsårespasmer.
DOSERING OG ADMINISTRATION
Anstrengende Angina Pectoris på grund af aterosklerotisk koronararteriesygdom eller Angina Pectoris i hvile på grund af koronararteriespasme
Dosis skal tilpasses den enkelte patients behov. Startende med 30 mg fire gange dagligt, før måltider og ved sengetid, bør dosis øges gradvist (givet i opdelte doser tre eller fire gange dagligt) med 1 til 2 dages intervaller, indtil optimal respons opnås. Selvom individuelle patienter kan reagere på ethvert dosisniveau, ser det gennemsnitlige optimale dosisinterval ud til at være 180 til 360 mg/dag. Der er ingen tilgængelige data vedrørende dosiskrav til patienter med nedsat nyre- eller leverfunktion. Hvis lægemidlet skal anvendes til sådanne patienter, skal titreringen udføres med særlig forsigtighed.
Samtidig brug med andre kardiovaskulære midler
Swallow Cardizem tabletter hele; du må ikke dele, knuse eller tygge tabletterne.
HVORDAN LEVERET
CARDIZEM 30 mg tabletter leveres i flasker med 100 stk. NDC 0187-0771-47) og 500 ( NDC 0187-0771-55). Hver lysegrøn, rund tablet er indgraveret med MARION på den ene side og 1771 på den anden.
CARDIZEM 60 mg tabletter med delekærv leveres i flasker med 100 stk. NDC 0187-0772-47). Hver lysegul, rund tablet er indgraveret med MARION på den ene side og 1772 på den anden.
CARDIZEM 90 mg tabletter med delekærv leveres i flasker med 100 stk. NDC 0187-0791-47). Hver grøn, aflang tablet er indgraveret med CARDIZEM på den ene side og 90 mg på den anden.
CARDIZEM 120 mg tabletter med delekærv leveres i flasker med 100 stk. NDC 0187-0792-47). Hver lysegul, kapselformet tablet er indgraveret med CARDIZEM på den ene side og 120 mg på den anden.
Opbevares ved 25°C (77°); udflugter tilladt til 15-30°C (59-86°) [se USP kontrolleret rumtemperatur ].
Undgå for høj luftfugtighed.
Distribueret af: Valeant Pharmaceuticals North America LLC Bridgewater, NJ 08807 USA. Lavet i Canada. Revideret. 14/11
BIVIRKNINGER
Alvorlige bivirkninger har været sjældne i undersøgelser udført til dato, men det skal erkendes, at patienter med nedsat ventrikulær funktion og hjerteledningsabnormaliteter normalt er blevet udelukket.
I hjemlige placebokontrollerede angina-forsøg var forekomsten af bivirkninger rapporteret under CARDIZEM-behandling ikke større end rapporteret under placebobehandling.
Det følgende repræsenterer hændelser observeret i kliniske undersøgelser af anginapatienter. I mange tilfælde er forholdet til CARDIZEM ikke blevet fastslået. De mest almindelige forekomster fra disse undersøgelser, såvel som deres præsentationsfrekvens, er ødem (2,4 %), hovedpine (2,1 %), kvalme (1,9 %), svimmelhed (1,5 %), udslæt (1,3 %) og asteni (1,2 %). %). Derudover blev følgende hændelser rapporteret sjældent (mindre end 1 %):
Kardiovaskulær
Angina, arytmi, AV-blok (første grad), AV-blok (anden eller tredje grad – se ADVARSLER , Hjerteledning ), bradykardi, grenblok, kongestiv hjertesvigt, EKG-abnormitet, rødmen, hypotension, hjertebanken, synkope, takykardi, ventrikulære ekstrasystoler.
Nervesystem
Unormale drømme, hukommelsestab, depression, gangabnormitet, hallucinationer, søvnløshed, nervøsitet, paræstesi, personlighedsændring, somnolens, tremor.
Gastrointestinale
Anoreksi, forstoppelse, diarré, dysgeusi, dyspepsi, milde forhøjelser af alkalisk fosfatase, SGOT, SGPT og LDH (se ADVARSLER , Akut leverskade ), tørst, opkastning, vægtstigning.
Dermatologisk
Petekkier, lysfølsomhed, pruritus, nældefeber.
Andet
Amblyopi, CPK-forhøjelse, mundtørhed, dyspnø, næseblod, øjenirritation, hyperglykæmi, hyperurikæmi, impotens, muskelkramper, tilstoppet næse, nocturi, osteoartikulær smerte, polyuri, seksuelle vanskeligheder, tinnitus.
Følgende postmarketing-hændelser er sjældent blevet rapporteret hos patienter, der får CARDIZEM: akut generaliseret eksantematøs pustulose, allergiske reaktioner, alopeci, angioødem (inklusive ansigts- eller periorbitalt ødem), asystoli, erythema multiforme (inklusive Stevens-Johnlyssons syndrom), ekstrakroamidersyndrom, , gingival hyperplasi, hæmolytisk anæmi, øget blødningstid, leukopeni, lysfølsomhed (herunder lichenoid keratose og hyperpigmentering ved soleksponerede hudområder), purpura, retinopati, myopati og trombocytopeni. Der er observeret tilfælde af generaliseret udslæt, nogle karakteriseret som leukocytoklastisk vaskulitis. Derudover er hændelser såsom myokardieinfarkt blevet observeret, som ikke umiddelbart kan skelnes fra sygdommens naturlige historie hos disse patienter. En endelig årsag og virkning sammenhæng mellem disse hændelser og CARDIZEM-behandling kan endnu ikke fastslås. Eksfoliativ dermatitis (påvist ved genudsættelse) er også blevet rapporteret.
DRUGSINTERAKTIONER
På grund af potentialet for additive virkninger er forsigtighed og omhyggelig titrering berettiget hos patienter, der får CARDIZEM 180 mg samtidig med midler, der vides at påvirke hjertets kontraktilitet og/eller ledning (se ADVARSLER ).
Farmakologiske undersøgelser tyder på, at der kan være additive virkninger ved at forlænge AV-ledning ved brug af betablokkere eller digitalis samtidig med CARDIZEM (se ADVARSLER ).
Som med alle lægemidler skal der udvises forsigtighed ved behandling af patienter med flere lægemidler. Diltiazem er både et substrat og en hæmmer af cytochrom P-450 3A4 enzymsystemet. Andre lægemidler, der er specifikke substrater, inhibitorer eller inducere af dette enzymsystem, kan have en betydelig indvirkning på effektiviteten og bivirkningsprofilen af diltiazem. Patienter, der tager andre lægemidler, der er substrater for CYP450 3A4, især patienter med nedsat nyre- og/eller leverfunktion, kan kræve dosisjustering, når man starter eller stopper samtidig indgift af diltiazem for at opretholde optimale terapeutiske blodniveauer.
Bedøvelsesmidler
Nedsættelsen af hjertets kontraktilitet, ledningsevne og automatik såvel som den vaskulære udvidelse i forbindelse med anæstetika kan forstærkes af calciumkanalblokkere. Ved samtidig brug bør anæstetika og calciumblokkere titreres omhyggeligt.
Benzodiazepiner
Undersøgelser viste, at diltiazem øgede AUC for midazolam og triazolam med 3 til 4 gange og Cmax med 2 gange sammenlignet med placebo. Eliminationshalveringstiden for midazolam og triazolam øgedes også (1,5 til 2,5 gange) under samtidig administration med diltiazem. Disse farmakokinetiske virkninger, der ses under samtidig administration af diltiazem, kan resultere i øgede kliniske virkninger (f.eks. forlænget sedation) af både midazolam og triazolam.
Beta-blokkere
Kontrollerede og ukontrollerede indenlandske undersøgelser tyder på, at samtidig brug af CARDIZEM 180 mg og betablokkere normalt tolereres godt. Tilgængelige data er imidlertid ikke tilstrækkelige til at forudsige virkningerne af samtidig behandling, især hos patienter med venstre ventrikulær dysfunktion eller hjerteledningsabnormiteter.
Administration af CARDIZEM (diltiazem hydrochlorid) samtidig med propranolol hos fem normale frivillige resulterede i øgede propranololniveauer hos alle forsøgspersoner, og biotilgængeligheden af propranolol blev øget med ca. 50 %. In vitro synes propranolol at blive fortrængt fra dets bindingssteder af diltiazem. Hvis kombinationsbehandling påbegyndes eller seponeres i forbindelse med propranolol, kan en justering af propranololdosis være berettiget (se ADVARSLER ).
Buspiron
Hos ni raske forsøgspersoner øgede diltiazem den gennemsnitlige buspiron AUC 5,5 gange og Cmax 4,1 gange signifikant sammenlignet med placebo. T½ og Tmax for buspiron var ikke signifikant påvirket af diltiazem. Forstærkede effekter og øget toksicitet af buspiron kan være mulig ved samtidig administration med diltiazem. Efterfølgende dosisjusteringer kan være nødvendige under samtidig administration og bør være baseret på klinisk vurdering.

Carbamazepin
Samtidig administration af diltiazem og carbamazepin er blevet rapporteret at resultere i forhøjede serumniveauer af carbamazepin (40 % til 72 % stigning), hvilket resulterer i toksicitet i nogle tilfælde. Patienter, der får disse lægemidler samtidigt, bør overvåges for en potentiel lægemiddelinteraktion.
Cimetidin
En undersøgelse med seks raske frivillige har vist en signifikant stigning i maksimale diltiazem-plasmaniveauer (58 %) og area-under-kurven (53 %) efter en 1-uges behandling med cimetidin på 1200 mg dagligt og en enkelt dosis af diltiazem 60 mg. Ranitidin producerede mindre, ikke-signifikante stigninger. Virkningen kan medieres af cimetidins kendte hæmning af hepatisk cytochrom P-450, det enzymsystem, der er ansvarlig for first-pass metabolismen af diltiazem. Patienter, der i øjeblikket får diltiazem-behandling, bør overvåges nøje for en ændring i farmakologisk effekt, når behandlingen med cimetidin påbegyndes og seponeres. En justering af diltiazemdosis kan være berettiget.
Clonidin
Sinusbradykardi, der resulterer i hospitalsindlæggelse og pacemakerindsættelse, er blevet rapporteret i forbindelse med brug af clonidin samtidig med diltiazem. Overvåg hjertefrekvens hos patienter, der samtidig får diltiazem og clonidin.
Cyclosporin
En farmakokinetisk interaktion mellem diltiazem og cyclosporin er blevet observeret under undersøgelser med nyre- og hjertetransplanterede patienter. Hos nyre- og hjertetransplanterede patienter var en reduktion af cyclosporin-daldosis varierende fra 15 % til 48 % nødvendig for at opretholde koncentrationer svarende til dem, der blev set før tilsætning af diltiazem. Hvis disse midler skal administreres samtidigt, bør ciclosporinkoncentrationerne monitoreres, især når diltiazembehandling påbegyndes, justeres eller seponeres. Virkningen af cyclosporin på plasmakoncentrationer af diltiazem er ikke blevet evalueret.
Digitalis
Administration af CARDIZEM 180 mg med digoxin til 24 raske mandlige forsøgspersoner øgede plasmadigoxinkoncentrationerne med ca. 20 %. En anden efterforsker fandt ingen stigning i digoxinniveauer hos 12 patienter med koronararteriesygdom. Da der har været modstridende resultater med hensyn til virkningen af digoxinniveauer, anbefales det, at digoxinniveauer overvåges, når behandlingen med CARDIZEM 60 mg påbegyndes, justeres og seponeres for at undgå mulig over- eller underdigitalisering (se ADVARSLER ).
Quinidin
Diltiazem øger signifikant AUC (0→infin;) af quinidin med 51 %, T½ med 36 % og reducerer dets CLoral med 33 %. Overvågning for quinidin-bivirkninger kan være berettiget, og dosis justeres i overensstemmelse hermed.
Rifampin
Samtidig administration af rifampin og diltiazem sænkede plasmakoncentrationerne af diltiazem til upåviselige niveauer. Samtidig administration af diltiazem med rifampin eller enhver kendt CYP3A4-inducer bør undgås, når det er muligt, og alternativ behandling bør overvejes.
Statiner
Diltiazem er en hæmmer af CYP3A4 og har vist sig at øge AUC signifikant for nogle statiner. Risikoen for myopati og rabdomyolyse med statiner metaboliseret af CYP3A4 kan øges ved samtidig brug af diltiazem. Når det er muligt, skal du bruge et ikke-CYP3A4-metaboliseret statin sammen med diltiazem; ellers bør dosisjusteringer for både diltiazem og statinet overvejes sammen med tæt monitorering for tegn og symptomer på statinrelaterede bivirkninger.
et cross-over-studie med raske frivillige (N=10) resulterede samtidig administration af en enkelt 20 mg dosis simvastatin i slutningen af et 14-dages regime med 120 mg 2D diltiazem SR i en 5-fold stigning i den gennemsnitlige simvastatin AUC versus simvastatin alene. Forsøgspersoner med øget gennemsnitlig steady-state eksponering for diltiazem viste en større fold stigning i simvastatin eksponering. Computerbaserede simuleringer viste, at der ved en daglig dosis på 480 mg diltiazem kan forventes en 8- til 9 gange gennemsnitlig stigning i simvastatin AUC. Hvis samtidig administration af simvastatin og diltiazem er påkrævet, skal de daglige doser af simvastatin begrænses til 10 mg og diltiazem til 240 mg.
et randomiseret, åbent, 4-vejs cross-over-studie med ti forsøgspersoner, resulterede samtidig administration af diltiazem (120 mg Diltiazem SR i 2 uger) med en enkelt dosis på 20 mg lovastatin i en 3- til 4-fold stigning. i gennemsnitlig lovastatin AUC og Cmax versus lovastatin alene. I samme undersøgelse var der ingen signifikant ændring i 20 mg enkeltdosis pravastatin AUC og Cmax under samtidig administration af diltiazem. Diltiazem plasmaniveauer blev ikke signifikant påvirket af lovastatin eller pravastatin.
ADVARSLER
FORHOLDSREGLER
Generel
CARDIZEM (diltiazem hydrochlorid) metaboliseres i vid udstrækning i leveren og udskilles af nyrerne og i galden. Som med ethvert lægemiddel givet over længere perioder, bør laboratorieparametre for nyre- og leverfunktion monitoreres med regelmæssige intervaller. Lægemidlet bør anvendes med forsigtighed til patienter med nedsat nyre- eller leverfunktion. I subakutte og kroniske hunde- og rottestudier designet til at producere toksicitet, var høje doser af diltiazem forbundet med leverskade. I særlige subakutte leverundersøgelser var orale doser på 125 mg/kg og højere hos rotter forbundet med histologiske forandringer i leveren, som var reversible, da lægemidlet blev seponeret. Hos hunde var doser på 20 mg/kg også forbundet med leverforandringer; disse ændringer var dog reversible ved fortsat dosering. Dermatologiske hændelser (se BIVIRKNINGER kan være forbigående og kan forsvinde på trods af fortsat brug af CARDIZEM. Imidlertid er hududbrud, der udvikler sig til erythema multiforme og/eller eksfoliativ dermatitis, også sjældent blevet rapporteret. Hvis en dermatologisk reaktion fortsætter, bør lægemidlet seponeres.
Karcinogenese, mutagenese, svækkelse af fertilitet
Et 24-måneders studie med rotter og et 21-måneders studie med mus viste ingen tegn på carcinogenicitet. Der var heller ingen mutagen respons i in vitro bakterielle test. Der blev ikke observeret nogen iboende effekt på fertiliteten hos rotter.
Graviditet
Kategori C
Reproduktionsundersøgelser er blevet udført på mus, rotter og kaniner. Administration af doser fra fem til ti gange større (på mg/kg basis) end den daglige anbefalede terapeutiske dosis har resulteret i embryo- og fosterdødelighed. Disse doser er i nogle undersøgelser blevet rapporteret at forårsage skeletabnormiteter. I de perinatale/postnatale undersøgelser var der en vis reduktion i tidlige individuelle hvalpevægte og overlevelsesrater. Der var en øget forekomst af dødfødsler ved doser på 20 gange den humane dosis eller mere.
Der er ingen velkontrollerede undersøgelser af gravide kvinder; Brug derfor kun CARDIZEM til gravide kvinder, hvis den potentielle fordel opvejer den potentielle risiko for fosteret.
Ammende mødre
Diltiazem udskilles i modermælk. En rapport tyder på, at koncentrationer i modermælk kan nærme sig serumniveauer. Hvis brug af CARDIZEM anses for at være nødvendig, bør en alternativ metode til spædbørnsernæring anvendes.
Pædiatrisk brug
Sikkerhed og effektivitet hos pædiatriske patienter er ikke blevet fastslået.
Geriatrisk brug
Kliniske undersøgelser af diltiazem omfattede ikke et tilstrækkeligt antal forsøgspersoner på 65 år og derover til at afgøre, om de reagerer anderledes end yngre forsøgspersoner. Andre rapporterede kliniske erfaringer har ikke identificeret forskelle i respons mellem ældre og yngre patienter. Generelt bør dosisvalg for en ældre patient være forsigtigt, sædvanligvis begyndende i den lave ende af doseringsområdet, hvilket afspejler den større hyppighed af nedsat lever-, nyre- eller hjertefunktion og af samtidig sygdom eller anden lægemiddelbehandling.
OVERDOSIS
De orale LD50'er hos mus og rotter varierer fra henholdsvis 415 til 740 mg/kg og fra 560 til 810 mg/kg. De intravenøse LD50'er hos disse arter var henholdsvis 60 og 38 mg/kg. Den orale LD50 hos hunde anses for at være over 50 mg/kg, mens dødelighed blev set hos aber ved 360 mg/kg.
Den toksiske dosis hos mennesker kendes ikke. På grund af omfattende stofskifte kan blodniveauer efter en standarddosis diltiazem variere over tidoblet, hvilket begrænser nytten af blodniveauer i tilfælde af overdosis.
Der har været rapporter om overdosering af diltiazem i mængder fra
Hændelser observeret efter overdosering af diltiazem omfattede bradykardi, hypotension, hjerteblokade og hjertesvigt. De fleste indberetninger om overdosering beskrev en understøttende medicinsk foranstaltning og/eller lægemiddelbehandling. Bradykardi reagerede ofte positivt på atropin, ligesom hjerteblokade gjorde, selvom hjertestimulering også ofte blev brugt til at behandle hjerteblokade. Væsker og vasopressorer blev brugt til at opretholde blodtrykket, og i tilfælde af hjertesvigt blev der givet inotrope midler. Derudover fik nogle patienter behandling med ventilatorisk støtte, maveskylning, aktivt kul og/eller intravenøs calcium.
Effektiviteten af intravenøs calciumadministration til at vende de farmakologiske virkninger af diltiazem-overdosis har været inkonsekvent. I nogle få rapporterede tilfælde blev overdosering med calciumkanalblokkere forbundet med hypotension og bradykardi, som oprindeligt var refraktær over for atropin, mere responsiv over for atropin, efter at patienterne fik intravenøs calcium. I nogle tilfælde er intravenøst calcium blevet administreret (1 g calciumchlorid eller 3 g calciumgluconat) over 5 minutter og gentaget hvert 10. til 20. minut efter behov. Calciumgluconat er også blevet administreret som en kontinuerlig infusion med en hastighed på 2 g pr. time i 10 timer. Infusioner af calcium i 24 timer eller mere kan være påkrævet. Patienter bør overvåges for tegn på hypercalcæmi.
tilfælde af overdosering eller overdrevet respons bør passende støttende foranstaltninger anvendes ud over gastrointestinal dekontaminering. Diltiazem ser ikke ud til at blive fjernet ved peritoneal eller hæmodialyse. Begrænsede data tyder på, at plasmaferese eller kulhæmoperfusion kan fremskynde eliminering af diltiazem efter overdosering. Baseret på de kendte farmakologiske virkninger af diltiazem og/eller rapporterede kliniske erfaringer, kan følgende foranstaltninger overvejes:
Bradykardi: Administrer atropin (0,60 til 1,0 mg). Hvis der ikke er nogen reaktion på vagal blokade, administreres isoproterenol med forsigtighed.
AV-blok i høj grad: Behandl som for bradykardi ovenfor. Fast højgrads AV-blok bør behandles med hjertestimulering.
Hjertesvigt: Administrer inotrope midler (isoproterenol, dopamin eller dobutamin) og diuretika.
Hypotension: Vasopressorer (f.eks. dopamin eller noradrenalin).
Faktisk behandling og dosering bør afhænge af sværhedsgraden af den kliniske situation og den behandlende læges vurdering og erfaring.
KONTRAINDIKATIONER
CARDIZEM er kontraindiceret til (1) patienter med syg sinus-syndrom undtagen ved tilstedeværelse af en fungerende ventrikulær pacemaker, (2) patienter med anden- eller tredjegrads AV-blok, undtagen ved tilstedeværelse af en fungerende ventrikulær pacemaker, (3) patienter med hypotension (mindre end 90 mm Hg systolisk), (4) patienter, der har udvist overfølsomhed over for lægemidlet, og (5) patienter med akut myokardieinfarkt og lungekongestion dokumenteret ved røntgen ved indlæggelsen.
KLINISK FARMAKOLOGI
De terapeutiske fordele opnået med CARDIZEM 180mg menes at være relateret til dets evne til at hæmme tilstrømningen af calciumioner under membrandepolarisering af hjerte- og vaskulær glat muskulatur.
Virkningsmekanismer
Selvom præcise mekanismer for dets antianginale virkning stadig er ved at blive afgrænset, menes CARDIZEM 120mg at virke på følgende måder:
dyremodeller interfererer diltiazem med den langsomme indadgående (depolariserende) strøm i exciterbart væv. Det forårsager excitation-kontraktionsafkobling i forskellige myokardievæv uden ændringer i konfigurationen af aktionspotentialet. Diltiazem frembringer afslapning af den glatte muskulatur i koronar vaskulær og udvidelse af både store og små kranspulsårer ved lægemiddelniveauer, som forårsager ringe eller ingen negativ inotrop effekt. De resulterende stigninger i koronar blodgennemstrømning (epicardie og subendokardie) forekommer i iskæmiske og ikke-iskæmiske modeller og er ledsaget af dosisafhængige fald i systemisk blodtryk og fald i perifer modstand.
Hæmodynamiske og elektrofysiologiske effekter
Som andre calciumantagonister nedsætter diltiazem sinoatrial og atrioventrikulær ledning i isolerede væv og har en negativ inotrop effekt i isolerede præparater. Hos det intakte dyr kan forlængelse af AH-intervallet ses ved højere doser.
Hos mennesker forhindrer diltiazem spontane og ergonovin-provokerede kranspulsårer. Det forårsager et fald i perifer vaskulær modstand og et beskedent fald i blodtrykket, og i træningstoleranceundersøgelser hos patienter med iskæmisk hjertesygdom reducerer det puls-blodtryksproduktet for enhver given arbejdsbyrde. Undersøgelser til dato, primært hos patienter med god ventrikulær funktion, har ikke afsløret tegn på en negativ inotrop effekt; Hjertevolumen, ejektionsfraktion og venstre ventrikel end-diastolisk tryk er ikke blevet påvirket. Der er endnu få data om interaktionen mellem diltiazem og betablokkere. Hvilepuls er normalt uændret eller svagt reduceret af diltiazem.
Intravenøs diltiazem i doser på 20 mg forlænger AH-ledningstiden og AV-knudefunktionelle og effektive refraktære perioder med ca. 20%. I en undersøgelse, der involverede enkelt orale doser på 300 mg CARDIZEM 60 mg i seks normale frivillige, var den gennemsnitlige maksimale PR-forlængelse 14 % uden tilfælde af større end førstegrads AV-blok. Diltiazem-associeret forlængelse af AH-intervallet er ikke mere udtalt hos patienter med førstegrads hjerteblokade. Hos patienter med syg sinus-syndrom forlænger diltiazem sinuscykluslængden betydeligt (op til 50 % i nogle tilfælde).
Kronisk oral administration af CARDIZEM i doser på op til 240 mg/dag har resulteret i små stigninger i PR-intervallet, men har normalt ikke givet unormal forlængelse.
Farmakokinetik og metabolisme
Diltiazem absorberes godt fra mave-tarmkanalen og er genstand for en omfattende first-pass effekt, hvilket giver en absolut biotilgængelighed (sammenlignet med intravenøs dosering) på omkring 40 %. CARDIZEM gennemgår omfattende metabolisme, hvor 2% til 4% af det uændrede lægemiddel vises i urinen. In vitro bindingsundersøgelser viser, at CARDIZEM 90 mg er 70 % til 80 % bundet til plasmaproteiner. Konkurrerende in vitro ligandbindingsundersøgelser har også vist, at CARDIZEM 120 mg-binding ikke ændres af terapeutiske koncentrationer af digoxin, hydrochlorthiazid, phenylbutazon, propranolol, salicylsyre eller warfarin. Plasmaelimineringshalveringstiden efter enkelt- eller multipel lægemiddeladministration er ca. 3,0 til 4,5 timer. Desacetyldiltiazem er også til stede i plasmaet i niveauer på 10% til 20% af moderlægemidlet og er 25% til 50% så potent som en koronar vasodilator som diltiazem. Minimum terapeutiske plasmaniveauer af CARDIZEM 120 mg ser ud til at være i området 50 til 200 ng/ml. Der er en afvigelse fra linearitet, når dosisstyrkerne øges. En undersøgelse, der sammenlignede patienter med normal leverfunktion med patienter med cirrose, fandt en stigning i halveringstid og en stigning på 69 % i AUC (areal-under-plasmakoncentration vs tidskurve) hos patienter med nedsat leverfunktion. En enkelt undersøgelse med ni patienter med alvorligt nedsat nyrefunktion viste ingen forskel i den farmakokinetiske profil af diltiazem sammenlignet med patienter med normal nyrefunktion.
CARDIZEM 120mg tabletter . Diltiazem absorberes fra tabletformuleringen til ca. 98 % af en referenceopløsning. Enkelte orale doser på 30 til 120 mg CARDIZEM 30 mg tabletter resulterer i påviselige plasmaniveauer inden for 30 til 60 minutter og maksimale plasmaniveauer 2 til 4 timer efter lægemiddeladministration. Da dosis af CARDIZEM 120 mg tabletter øges fra en daglig dosis på 120 mg (30 mg dagligt) til 240 mg (60 mg dagligt) dagligt, er der en stigning i arealet under kurven på 2,3 gange. Når dosis øges fra 240 mg til 360 mg dagligt, er der en stigning i arealet under kurven på 1,8 gange.
PATIENTOPLYSNINGER
Swallow Cardizem tabletter hele; ikke flække, knuse eller tygge. Medicinen i Cardizem 180mg er formuleret til at frigive langsomt.
