Precose 25mg, 50mg Acarbose Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Precose 50mg, og hvordan bruges det?
Precose (acarbosetabletter) er en oral alfa-glucosidasehæmmer, der bruges til at behandle type 2-diabetes. Precose 50mg bruges nogle gange i kombination med insulin eller anden diabetesmedicin, du tager gennem munden. Precose 25mg er tilgængelig i generisk form.
Hvad er bivirkninger af Precose 25mg?
Almindelige bivirkninger af Precose omfatter:
- diarré,
- gas,
- oppustethed,
- dårlig mave, eller
- mavesmerter i de første par uger af behandlingen, da din krop tilpasser sig denne medicin, men som regel forbedres med tiden.
Andre bivirkninger af Precose 50mg omfatter hududslæt eller kløe. Fortæl det til din læge, hvis du har sjældne, men meget alvorlige bivirkninger af Precose 25mg, herunder:
- usædvanlig træthed,
- vedvarende kvalme eller opkastning,
- stærke mave- eller mavesmerter,
- rektal blødning,
- gulne øjne eller hud, eller
- mørk urin.
BESKRIVELSE
PRECOSE® (acarbosetabletter) er en oral alfa-glucosidasehæmmer til brug ved behandling af type 2 diabetes mellitus. Acarbose er et oligosaccharid, som er opnået fra fermenteringsprocesser af en mikroorganisme, Actinoplanes utahensis, og er kemisk kendt som O-4,6-dideoxy4-[[(1S,4R,5S,6S)-4,5,6-trihydroxy- 3-(hydroxymethyl)-2-cyclohexen-1-yl]amino]a-D-glucopyranosyl-(1-→4)-O-a-D-glucopyranosyl-(1-→4)-D-glucose. Det er et hvidt til råhvidt pulver med en molekylvægt på 645,6. Acarbose er opløseligt i vand og har en pKa på 5,1. Dens empiriske formel er C25H43NO18 og dens kemiske struktur er som følger:
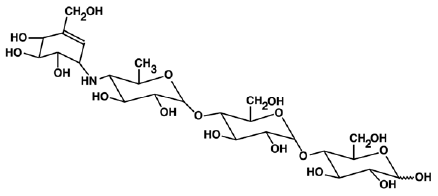
PRECOSE 50 mg er tilgængelig som 25 mg, 50 mg og 100 mg tabletter til oral brug. De inaktive ingredienser er stivelse, mikrokrystallinsk cellulose, magnesiumstearat og kolloid siliciumdioxid.
INDIKATIONER
PRECOSE er indiceret som et supplement til diæt og motion for at forbedre den glykæmiske kontrol hos voksne med type 2-diabetes mellitus.
DOSERING OG ADMINISTRATION
Der er ingen fast dosisregime til behandling af diabetes mellitus med PRECOSE eller noget andet farmakologisk middel. Dosis af PRECOSE 25 mg skal individualiseres på basis af både effektivitet og tolerance, mens den maksimalt anbefalede dosis på 100 mg ikke overskrides. PRECOSE bør tages tre gange dagligt ved starten (med den første bid) af hvert hovedmåltid.
PRECOSE bør startes med en lav dosis med gradvis dosisoptrapning som beskrevet nedenfor, både for at reducere gastrointestinale bivirkninger og for at muliggøre identifikation af den minimumsdosis, der kræves for tilstrækkelig glykæmisk kontrol af patienten. Hvis den foreskrevne diæt ikke overholdes, kan tarmbivirkningerne forstærkes. Hvis der opstår stærkt belastende symptomer på trods af overholdelse af den foreskrevne diabetiske diæt, skal lægen konsulteres og dosis reduceres midlertidigt eller permanent.
Under behandlingsstart og dosistitrering (se nedenfor), kan en times postprandial plasmaglucose anvendes til at bestemme det terapeutiske respons på PRECOSE og identificere den minimale effektive dosis for patienten. Derefter skal glykosyleret hæmoglobin måles med intervaller på ca. tre måneder. Det terapeutiske mål bør være at sænke både postprandiale plasmaglucose- og glykosyleret hæmoglobinniveauer til normalt eller næsten normalt ved at bruge den laveste effektive dosis af PRECOSE, enten som monoterapi eller i kombination med sulfonylurinstoffer, insulin eller metformin.
Startdosering
Den anbefalede startdosis af PRECOSE 25 mg er 25 mg givet oralt tre gange dagligt ved starten (med den første bid) af hvert hovedmåltid. Nogle patienter kan dog have gavn af mere gradvis dosistitrering for at minimere gastrointestinale bivirkninger. Dette kan opnås ved at påbegynde behandling med 25 mg én gang dagligt og efterfølgende øge administrationshyppigheden for at opnå 25 mg tid.
Vedligeholdelsesdosering
Når en dosis på 25 mg tid er nået, skal dosis af PRECOSE 50 mg justeres med 4-8 ugers intervaller baseret på en time postprandial glucose eller glykosyleret hæmoglobinniveau og tolerance. Doseringen kan øges fra 25 mg tid til 50 mg tid. Nogle patienter kan drage fordel af yderligere at øge dosis til 100 mg tid. Vedligeholdelsesdosis varierer fra 50 mg tid til 100 mg tid, men da patienter med lav kropsvægt kan have øget risiko for forhøjede serumtransaminaser, bør kun patienter med kropsvægt > 60 kg overvejes for dosistitrering over 50 mg tid (se FORHOLDSREGLER ). Hvis der ikke observeres yderligere reduktion i postprandiale glukose- eller glykosyleret hæmoglobinniveau ved titrering til 100 mg tid, bør det overvejes at sænke dosis. Når en effektiv og tolereret dosis er etableret, bør den opretholdes.
Maksimal dosis
Den maksimalt anbefalede dosis til patienter ≤ 60 kg er 50 mg tid Den maksimalt anbefalede dosis til patienter > 60 kg er 100 mg tid.
Patienter, der får sulfonylurinstoffer eller insulin
Sulfonylurinstofmidler eller insulin kan forårsage hypoglykæmi. PRECOSE givet i kombination med et sulfonylurinstof eller insulin vil forårsage en yderligere sænkning af blodsukkeret og kan øge risikoen for hypoglykæmi. Hvis der opstår hypoglykæmi, skal der foretages passende justeringer i doseringen af disse midler.
HVORDAN LEVERET
PRECOSE fås som 25 mg, 50 mg eller 100 mg runde tabletter uden delekærv. Hver tabletstyrke er hvid til gulfarvet. 25 mg tabletten er kodet med ordet "PRECOSE" på den ene side og "25" på den anden side. 50 mg tabletten er kodet med ordet "PRECOSE" og "50" på samme side. 100 mg tabletten er kodet med ordene "PRECOSE" og "100" på samme side. PRECOSE fås i flasker med 100 og 50 mg styrke i enhedsdosispakninger med 100 stk.
Må ikke opbevares over 25°C (77°F). Beskyt mod fugt. For flasker skal beholderen holdes tæt lukket.
Bayer HealthCare Pharmaceuticals Inc. Wayne, NJ 07470. Fremstillet i Tyskland. 11/11
BIVIRKNINGER
Fordøjelsessystemet
Gastrointestinale symptomer er de mest almindelige reaktioner på PRECOSE. I amerikanske placebokontrollerede forsøg var forekomsten af mavesmerter, diarré og flatulens henholdsvis 19 %, 31 % og 74 % hos 1255 patienter behandlet med PRECOSE 50-300 mg tre gange, mens den tilsvarende forekomst var 9 %, 12 % og 29 % af 999 placebobehandlede patienter.
et etårigt sikkerhedsstudie, hvor patienterne førte dagbog over gastrointestinale symptomer, havde mavesmerter og diarré tendens til at vende tilbage til niveauerne før behandlingen over tid, og hyppigheden og intensiteten af flatulens havde en tendens til at aftage med tiden. De øgede symptomer i mave-tarmkanalen hos patienter behandlet med PRECOSE 50 mg er en manifestation af virkningsmekanismen af PRECOSE og er relateret til tilstedeværelsen af ufordøjet kulhydrat i den nedre mave-tarmkanal.
Hvis den foreskrevne diæt ikke overholdes, kan tarmbivirkningerne forstærkes. Hvis der opstår stærkt belastende symptomer på trods af overholdelse af den foreskrevne diabetiske diæt, skal lægen konsulteres og dosis reduceres midlertidigt eller permanent.
Forhøjede serumtransaminaseniveauer
Se FORHOLDSREGLER .
Andre unormale laboratoriefund
Små reduktioner i hæmatokrit forekom oftere hos PRECOSE-behandlede patienter end hos placebobehandlede patienter, men var ikke forbundet med reduktioner i hæmoglobin. Lavt serum-calcium og lave plasma-vitamin B6-niveauer var forbundet med PRECOSE 50 mg behandling, men menes at være enten falsk eller uden klinisk betydning.
Rapporter om uønskede hændelser efter markedsføring
Yderligere bivirkninger rapporteret fra verdensomspændende postmarketing-erfaringer omfatter fulminant hepatitis med dødelig udgang, overfølsomme hudreaktioner (for eksempel udslæt, erytem, exanthema og uticaria), ødem, ileus/subileus, gulsot og/eller hepatitis og associeret leverskade, trombocytopeni og pneumatose cystoides intestinalis (se FORHOLDSREGLER ).
Pneumatosis Cystoides Intestinalis
Der har været sjældne rapporter efter markedsføring om pneumatosis cystoides intestinalis forbundet med brugen af alfa-glucosidasehæmmere, inklusive Precose. Pneumatosis cystoides intestinalis kan vise sig med symptomer på diarré, slimudslip, rektal blødning og forstoppelse. Komplikationer kan omfatte pneumoperitoneum, volvulus, intestinal obstruktion, intussusception, intestinal blødning og intestinal perforation. Hvis der er mistanke om pneumatosis cystoides intestinalis, skal du seponere Precose 25 mg og udføre den passende billeddiagnostik.
DRUGSINTERAKTIONER
Visse lægemidler har tendens til at producere hyperglykæmi og kan føre til tab af blodsukkerkontrol. Disse lægemidler omfatter thiazider og andre diuretika, kortikosteroider, phenothiaziner, skjoldbruskkirtelprodukter, østrogener, orale præventionsmidler, phenytoin, nikotinsyre, sympatomimetika, calciumkanal-blokerende lægemidler og isoniazid. Når sådanne lægemidler administreres til en patient, der får PRECOSE 25 mg, skal patienten observeres nøje for tab af blodsukkerkontrol. Når sådanne lægemidler seponeres fra patienter, der får PRECOSE 50 mg i kombination med sulfonylurinstoffer eller insulin, skal patienterne observeres nøje for tegn på hypoglykæmi.
Patienter, der får sulfonylurinstoffer eller insulin: Sulfonylurinstoffer eller insulin kan forårsage hypoglykæmi. PRECOSE 25 mg givet i kombination med et sulfonylurinstof eller insulin kan forårsage en yderligere sænkning af blodsukkeret og kan øge risikoen for hypoglykæmi. Hvis der opstår hypoglykæmi, skal der foretages passende justeringer i doseringen af disse midler. Meget sjældent er individuelle tilfælde af hypoglykæmisk shock blevet rapporteret hos patienter, der får PRECOSE-behandling i kombination med sulfonylurinstoffer og/eller insulin.
Intestinale adsorbenter (f.eks. trækul) og fordøjelsesenzympræparater, der indeholder kulhydratspaltende enzymer (f.eks. amylase, pancreatin) kan reducere virkningen af PRECOSE og bør ikke tages samtidig.
PRECOSE 25 mg har vist sig at ændre biotilgængeligheden af digoxin, når de administreres samtidigt, hvilket kan kræve digoxindosisjustering. (Se KLINISK FARMAKOLOGI , Lægemiddel-lægemiddelinteraktioner .)
ADVARSLER
Ingen oplysninger angivet
FORHOLDSREGLER
Generel
Makrovaskulære resultater
Der har ikke været kliniske undersøgelser, der har fastslået endegyldige beviser for makrovaskulær risikoreduktion med PRECOSE 25 mg eller noget andet antidiabetisk lægemiddel.
Hypoglykæmi
På grund af dets virkningsmekanisme bør PRECOSE, når det administreres alene, ikke forårsage hypoglykæmi i fastende eller postprandial tilstand. Sulfonylurinstofmidler eller insulin kan forårsage hypoglykæmi. Fordi PRECOSE 50 mg givet i kombination med et sulfonylurinstof eller insulin vil forårsage en yderligere sænkning af blodsukkeret, kan det øge risikoen for hypoglykæmi. Hypoglykæmi forekommer ikke hos patienter, der får metformin alene under normale brugsforhold, og der blev ikke observeret en øget forekomst af hypoglykæmi hos patienter, når PRECOSE 50 mg blev tilføjet til metforminbehandling.
Oral glucose (dextrose), hvis absorption ikke hæmmes af PRECOSE, bør anvendes i stedet for saccharose (rørsukker) til behandling af mild til moderat hypoglykæmi. Saccharose, hvis hydrolyse til glucose og fructose hæmmes af PRECOSE, er uegnet til hurtig korrektion af hypoglykæmi. Alvorlig hypoglykæmi kan kræve brug af enten intravenøs glucoseinfusion eller glukagoninjektion.
Forhøjede serumtransaminaseniveauer
langtidsundersøgelser (op til 12 måneder, og inklusive PRECOSE 25 mg doser op til 300 mg tid) udført i USA, var behandlingsfremkaldte forhøjelser af serumtransaminaser (AST og/eller ALAT) over den øvre normalgrænse (ULN) ), større end 1,8 gange ULN og mere end 3 gange ULN forekom hos henholdsvis 14 %, 6 % og 3 % af PRECOSE-behandlede patienter sammenlignet med henholdsvis 7 %, 2 % og 1 %. af placebo-behandlede patienter. Selvom disse forskelle mellem behandlinger var statistisk signifikante, var disse forhøjelser asymptomatiske, reversible, mere almindelige hos kvinder og var generelt ikke forbundet med andre tegn på leverdysfunktion. Derudover så disse serumtransaminaseforhøjelser ud til at være dosisrelaterede. I amerikanske undersøgelser inklusive PRECOSE 50 mg doser op til den maksimalt godkendte dosis på 100 mg tid, var behandlingsfremkaldte stigninger af ASAT og/eller ALAT på et hvilket som helst niveau af sværhedsgrad ens mellem PRECOSE-behandlede patienter og placebo-behandlede patienter (p ≥ 0,496) .
ca. 3 millioner patientårs international postmarketing-erfaring med PRECOSE 50 mg, er der rapporteret 62 tilfælde af serumtransaminaseforhøjelser > 500 IE/L (hvoraf 29 var forbundet med gulsot). Enogfyrre af disse 62 patienter modtog behandling med 100 mg tid eller mere, og 33 ud af 45 patienter, for hvem vægten blev rapporteret, vejede
Tab af kontrol over blodsukkeret
Når diabetespatienter udsættes for stress såsom feber, traumer, infektion eller operation, kan der opstå et midlertidigt tab af kontrol over blodsukkeret. På sådanne tidspunkter kan midlertidig insulinbehandling være nødvendig.
Laboratorieprøver
Terapeutisk respons på PRECOSE bør overvåges ved periodiske blodsukkermålinger. Måling af glykosyleret hæmoglobinniveauer anbefales til overvågning af langsigtet glykæmisk kontrol.
PRECOSE 25 mg, især ved doser over 50 mg dagligt, kan give anledning til forhøjede serumtransaminaser og i sjældne tilfælde hyperbilirubinæmi. Det anbefales, at serumtransaminaseniveauer kontrolleres hver 3. måned i løbet af det første behandlingsår med PRECOSE og periodisk derefter. Hvis forhøjede transaminaser observeres, kan en reduktion i dosis eller seponering af behandlingen være indiceret, især hvis forhøjelserne varer ved.
Nedsat nyrefunktion
Plasmakoncentrationer af PRECOSE hos frivillige med nedsat nyrefunktion var proportionalt øget i forhold til graden af nyreinsufficiens. Langtids kliniske forsøg med diabetespatienter med signifikant nyreinsufficiens (serumkreatinin > 2,0 mg/dL) er ikke blevet udført. Derfor frarådes behandling af disse patienter med PRECOSE 50 mg.
Karcinogenese, mutagenese og svækkelse af fertilitet
Otte carcinogenicitetsundersøgelser blev udført med acarbose. Seks undersøgelser blev udført på rotter (to stammer, Sprague-Dawley og Wistar), og to undersøgelser blev udført på hamstere.
det første rottestudie modtog Sprague-Dawley-rotter acarbose i foder i høje doser (op til ca. 500 mg/kg legemsvægt) i 104 uger. Acarbosebehandling resulterede i en signifikant stigning i forekomsten af nyretumorer (adenomer og adenokarcinomer) og benigne Leydig-celletumorer. Denne undersøgelse blev gentaget med et lignende resultat. Yderligere undersøgelser blev udført for at adskille direkte kræftfremkaldende virkninger af acarbose fra indirekte virkninger som følge af kulhydratunderernæring induceret af de store doser acarbose, der blev anvendt i undersøgelserne. I en undersøgelse med Sprague-Dawley-rotter blev acarbose blandet med foder, men kulhydratmangel blev forhindret ved tilsætning af glukose til kosten.

en 26-måneders undersøgelse af Sprague-Dawley-rotter blev acarbose indgivet ved daglig postprandial sonde for at undgå de farmakologiske virkninger af lægemidlet. I begge disse undersøgelser forekom den øgede forekomst af nyretumorer fundet i de oprindelige undersøgelser ikke. Acarbose blev også givet i føde og ved postprandial sondeernæring i to separate undersøgelser med Wistar-rotter. Ingen øget forekomst af nyretumorer blev fundet i nogen af disse Wistar-rotteundersøgelser. I to fodringsundersøgelser af hamstere, med og uden glukosetilskud, var der heller ingen tegn på carcinogenicitet.
Acarbose inducerede ikke nogen DNA-skade in vitro i CHO kromosomafvigelsesassayet, bakteriel mutagenese (Ames) assay eller et DNA-bindingsassay. In vivo blev der ikke påvist nogen DNA-beskadigelse i den dominerende letale test i hanmus eller musemikronkernetesten.
Fertilitetsundersøgelser udført på rotter efter oral administration havde ingen uønsket effekt på fertiliteten eller på den generelle evne til at reproducere.
Graviditet
Teratogene virkninger: Graviditetskategori B.
Sikkerheden af PRECOSE hos gravide kvinder er ikke blevet fastslået. Reproduktionsundersøgelser er blevet udført på rotter i doser på op til 480 mg/kg (svarende til 9 gange eksponeringen hos mennesker, baseret på lægemiddelniveauer i blodet) og har ikke afsløret tegn på nedsat fertilitet eller skade på fosteret på grund af acarbose. Hos kaniner kan reduceret moderens vægtøgning, sandsynligvis et resultat af den farmakodynamiske aktivitet af høje doser acarbose i tarmene, have været skyld i en let stigning i antallet af embryonale tab. Imidlertid viste kaniner, der fik 160 mg/kg acarbose (svarende til 10 gange dosis til mennesker, baseret på kropsoverfladeareal) ingen tegn på embryotoksicitet, og der var ingen tegn på teratogenicitet ved en dosis på 32 gange dosis til mennesker (baseret på krop overfladeareal). Der er dog ingen tilstrækkelige og velkontrollerede undersøgelser af PRECOSE 25mg hos gravide kvinder. Da reproduktionsstudier på dyr ikke altid er forudsigelige for den menneskelige reaktion, bør dette lægemiddel kun anvendes under graviditet, hvis det er klart nødvendigt. Fordi aktuelle oplysninger kraftigt tyder på, at unormale blodsukkerniveauer under graviditet er forbundet med en højere forekomst af medfødte anomalier samt øget neonatal morbiditet og dødelighed, anbefaler de fleste eksperter, at insulin anvendes under graviditeten for at opretholde blodsukkerniveauet så tæt på det normale som muligt. .
Ammende mødre
En lille mængde radioaktivitet er fundet i mælken fra diegivende rotter efter administration af radioaktivt mærket acarbose. Det vides ikke, om dette lægemiddel udskilles i modermælk. Da mange lægemidler udskilles i modermælk, bør PRECOSE 25 mg ikke administreres til en ammende kvinde.
Pædiatrisk brug
Sikkerhed og effektivitet af PRECOSE 25 mg hos pædiatriske patienter er ikke blevet fastslået.
Geriatrisk brug
Af det samlede antal forsøgspersoner i kliniske studier med PRECOSE 25 mg i USA var 27 % 65 og derover, mens 4 % var 75 og derover. Der blev ikke observeret nogen overordnede forskelle i sikkerhed og effektivitet mellem disse forsøgspersoner og yngre forsøgspersoner. Det gennemsnitlige steady-state areal under kurven (AUC) og maksimale koncentrationer af acarbose var ca. 1,5 gange højere hos ældre sammenlignet med unge frivillige; disse forskelle var dog ikke statistisk signifikante.
OVERDOSIS
modsætning til sulfonylurinstoffer eller insulin vil en overdosis af PRECOSE ikke resultere i hypoglykæmi. En overdosis kan resultere i forbigående stigninger i flatulens, diarré og abdominalt ubehag, som kort tid aftager. I tilfælde af overdosering bør patienten ikke have drikkevarer eller måltider, der indeholder kulhydrater (polysaccharider, oligosaccharider og disaccharider) i de næste 4-6 timer.
KONTRAINDIKATIONER
PRECOSE 25mg er kontraindiceret til patienter med kendt overfølsomhed over for lægemidlet. Precose 25mg er kontraindiceret til patienter med diabetisk ketoacidose eller cirrhose. PRECOSE 25mg er også kontraindiceret hos patienter med inflammatorisk tarmsygdom, colonulceration, delvis tarmobstruktion eller hos patienter, der er disponeret for tarmobstruktion. Derudover er PRECOSE kontraindiceret til patienter, som har kroniske tarmsygdomme forbundet med markante forstyrrelser i fordøjelsen eller absorptionen og hos patienter, der har tilstande, der kan forværres som følge af øget gasdannelse i tarmen.
KLINISK FARMAKOLOGI
Acarbose er et komplekst oligosaccharid, der forsinker fordøjelsen af indtagne kulhydrater, hvilket resulterer i en mindre stigning i blodsukkerkoncentrationen efter måltider. Som en konsekvens af reduktion af plasmaglukose reducerer PRECOSE niveauet af glykosyleret hæmoglobin hos patienter med type 2-diabetes mellitus. Systemisk ikke-enzymatisk proteinglykosylering, som afspejlet af niveauer af glycosyleret hæmoglobin, er en funktion af den gennemsnitlige blodsukkerkoncentration over tid.
Virkningsmekanisme
modsætning til sulfonylurinstoffer øger PRECOSE 50mg ikke insulinsekretion. Den antihyperglykæmiske virkning af acarbose er resultatet af en kompetitiv, reversibel hæmning af alfa-amylase i bugspytkirtlen og membranbundne tarm-alfa-glucosidhydrolase-enzymer. Bugspytkirtel-alfa-amylase hydrolyserer komplekse stivelser til oligosaccharider i tyndtarmens lumen, mens de membranbundne tarm-alfa-glucosidaser hydrolyserer oligosaccharider, trisaccharider og disaccharider til glucose og andre monosaccharider i tyndtarmskanten. Hos diabetespatienter resulterer denne enzymhæmning i en forsinket glucoseabsorption og en sænkning af postprandial hyperglykæmi.
Fordi dets virkningsmekanisme er anderledes, er virkningen af PRECOSE til at forbedre den glykæmiske kontrol additiv til virkningen af sulfonylurinstoffer, insulin eller metformin, når de bruges i kombination. Derudover mindsker PRECOSE 50mg de insulinotrope og vægtforøgende virkninger af sulfonylurinstoffer.
Acarbose har ingen hæmmende aktivitet mod laktase og forventes derfor ikke at inducere laktoseintolerans.
Farmakokinetik
Absorption
et studie med 6 raske mænd blev mindre end 2 % af en oral dosis acarbose absorberet som aktivt lægemiddel, mens ca. 35 % af den samlede radioaktivitet fra en 14C-mærket oral dosis blev absorberet. I gennemsnit blev 51 % af en oral dosis udskilt i fæces som uabsorberet lægemiddelrelateret radioaktivitet inden for 96 timer efter indtagelse. Fordi acarbose virker lokalt i mave-tarmkanalen, er denne lave systemiske biotilgængelighed af moderforbindelsen terapeutisk ønsket. Efter oral dosering af raske frivillige med 14C-mærket acarbose blev maksimale plasmakoncentrationer af radioaktivitet opnået 14-24 timer efter dosering, mens maksimale plasmakoncentrationer af aktivt lægemiddel blev opnået efter ca. 1 time. Den forsinkede absorption af acarbose-relateret radioaktivitet afspejler absorptionen af metabolitter, der kan dannes af enten tarmbakterier eller intestinal enzymatisk hydrolyse.
Metabolisme
Acarbose metaboliseres udelukkende i mave-tarmkanalen, primært af tarmbakterier, men også af fordøjelsesenzymer. En brøkdel af disse metabolitter (ca. 34 % af dosis) blev absorberet og efterfølgende udskilt i urinen. Mindst 13 metabolitter er blevet separeret kromatografisk fra urinprøver. De vigtigste metabolitter er blevet identificeret som 4-methylpyrogallol-derivater (det vil sige sulfat-, methyl- og glucuronidkonjugater). Én metabolit (dannet ved spaltning af et glucosemolekyle fra acarbose) har også alfa-glucosidasehæmmende aktivitet. Denne metabolit, sammen med moderforbindelsen, udvundet fra urinen, udgør mindre end 2 % af den samlede administrerede dosis.
Udskillelse
Den del af acarbose, der absorberes som intakt lægemiddel, udskilles næsten fuldstændigt af nyrerne. Når acarbose blev givet intravenøst, blev 89 % af dosis genfundet i urinen som aktivt lægemiddel inden for 48 timer. I modsætning hertil blev mindre end 2 % af en oral dosis genfundet i urinen som aktivt (det vil sige moderstof og aktiv metabolit) lægemiddel. Dette er i overensstemmelse med den lave biotilgængelighed af moderlægemidlet. Halveringstiden for plasmaeliminering af acarboseaktivitet er ca. 2 timer hos raske frivillige. Som følge heraf forekommer lægemiddelakkumulering ikke ved oral dosering tre gange om dagen (tid).
Særlige Populationer
Det gennemsnitlige steady-state areal under kurven (AUC) og maksimale koncentrationer af acarbose var ca. 1,5 gange højere hos ældre sammenlignet med unge frivillige; disse forskelle var dog ikke statistisk signifikante. Patienter med svært nedsat nyrefunktion (Clcr
Lægemiddel-lægemiddelinteraktioner
Undersøgelser med raske frivillige har vist, at PRECOSE ikke har nogen effekt på hverken farmakokinetikken eller farmakodynamikken af nifedipin, propranolol eller ranitidin. PRECOSE interfererede ikke med absorptionen eller dispositionen af sulfonylurinstofglyburid hos diabetespatienter. PRECOSE kan påvirke digoxins biotilgængelighed og kan kræve dosisjustering af digoxin med 16 % (90 % konfidensinterval: 8-23 %), sænke middel Cmax for digoxin med 26 % (90 % konfidensinterval: 16-34 %) og reducere gennemsnitlig dal koncentrationer af digoxin med 9 % (90 % konfidensgrænse: 19 % fald til 2 % stigning). (Se FORHOLDSREGLER: DRUGSINTERAKTIONER .)
Mængden af metformin, der blev absorberet, mens du tog PRECOSE, var bioækvivalent med den mængde, der blev absorberet, når du tog placebo, som angivet af plasma-AUC-værdierne. Det maksimale plasmaniveau af metformin blev dog reduceret med ca. 20 %, når man tog PRECOSE på grund af en lille forsinkelse i absorptionen af metformin. Der er ringe om nogen klinisk signifikant interaktion mellem PRECOSE og metformin.
Kliniske forsøg
Klinisk erfaring fra dosisfindende undersøgelser i type 2-diabetes mellitus-patienter, der kun er i diætbehandling
Resultater fra seks kontrollerede, fastdosis-monoterapiundersøgelser af PRECOSE til behandling af type 2-diabetes mellitus, der involverede 769 PRECOSE-behandlede patienter, blev kombineret og et vægtet gennemsnit af forskellen fra placebo i den gennemsnitlige ændring fra baseline i glycosyleret hæmoglobin ( HbA1c) blev beregnet for hvert dosisniveau som vist nedenfor:
Selvom undersøgelser brugte en maksimal dosis på 200 eller 300 mg tid, er den maksimalt anbefalede dosis for patienter 60 kg er 100 mg tid
Resultater fra disse seks monoterapiundersøgelser med faste doser blev også kombineret for at udlede et vægtet gennemsnit af forskellen fra placebo i gennemsnitlig ændring fra baseline for en time postprandiale plasmaglucoseniveauer som vist i følgende figur:
figur 1 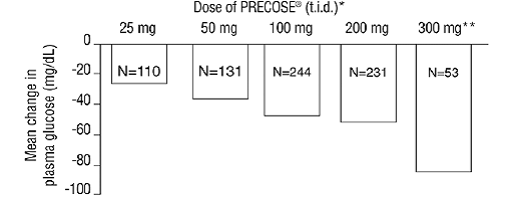
* PRECOSE 50 mg var statistisk signifikant forskellig fra placebo ved alle doser med hensyn til effekt på en time postprandial plasmaglucose. ** 300 mg tid PRECOSE 50 mg kur var bedre end lavere doser, men der var ingen statistisk signifikante forskelle fra 50 til 200 mg tid
Klinisk erfaring hos patienter med type 2 diabetes mellitus i monoterapi eller i kombination med sulfonylurinstoffer, metformin eller insulin
PRECOSE blev undersøgt som monoterapi og som kombinationsterapi til sulfonylurinstof-, metformin- eller insulinbehandling. Behandlingseffekterne på HbA1c-niveauer og en-times postprandiale glukoseniveauer er opsummeret for fire placebokontrollerede, dobbeltblindede, randomiserede undersøgelser udført i USA i henholdsvis tabel 2 og 3. De placebo-subtraherede behandlingsforskelle, som er opsummeret nedenfor, var statistisk signifikante for begge variabler i alle disse undersøgelser.
Undersøgelse 1 (n=109) involverede patienter i baggrundsbehandling udelukkende med diæt. Den gennemsnitlige effekt af tilføjelsen af PRECOSE til diætbehandling var en ændring i HbA1c på -0,78 % og en forbedring af en time postprandial glucose på -74,4 mg/dL.
I undersøgelse 2 (n=137) var den gennemsnitlige effekt af tilføjelsen af PRECOSE 25 mg til maksimal sulfonylurinstofbehandling en ændring i HbA1c på -0,54 % og en forbedring af en time postprandial glucose på -33,5 mg/dL.
undersøgelse 3 (n=147) var den gennemsnitlige effekt af tilføjelsen af PRECOSE 50 mg til maksimal metforminbehandling en ændring i HbA1c på -0,65 % og en forbedring af en time postprandial glucose på -34,3 mg/dL.
Undersøgelse 4 (n=145) viste, at PRECOSE tilsat patienter i baggrundsbehandling med insulin resulterede i en gennemsnitlig ændring i HbA1c på -0,69 % og en forbedring af en time postprandial glucose på -36,0 mg/dL.
Et etårigt studie af PRECOSE som monoterapi eller i kombination med sulfonylurinstof, metformin eller insulinbehandling blev udført i Canada, hvor 316 patienter blev inkluderet i den primære effektanalyse (figur 2). I diæt-, sulfonylurinstof- og metformingrupperne var det gennemsnitlige fald i HbA1c produceret ved tilsætning af PRECOSE 50 mg statistisk signifikant efter seks måneder, og denne effekt var vedvarende efter et år. Hos de PRECOSE-behandlede patienter på insulin var der en statistisk signifikant reduktion i HbA1c efter seks måneder og en tendens til en reduktion efter et år.
Figur 2 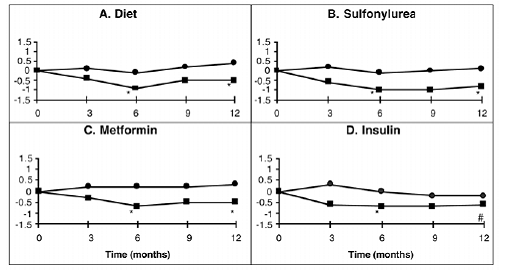
Figur 2: Virkninger af PRECOSE (III) og Placebo (III) på gennemsnitlig ændring i HbA1c-niveauer fra baseline gennem et et-årigt studie hos patienter med type 2-diabetes mellitus, når det anvendes i kombination med: (A) diæt alene; (B) sulfonylurinstof; (C) metformin; eller (D) insulin. Behandlingsforskelle efter 6 og 12 måneder blev testet: * p
PATIENTOPLYSNINGER
Patienterne skal fortælles, at de skal tage PRECOSE 50 mg oralt tre gange dagligt ved starten (med den første bid) af hvert hovedmåltid. Det er vigtigt, at patienterne fortsætter med at følge kostvejledningen, et regelmæssigt træningsprogram og regelmæssig test af urin og/eller blodsukker.
PRECOSE i sig selv forårsager ikke hypoglykæmi, selv når det administreres til patienter i fastende tilstand. Sulfonylurinstofmedicin og insulin kan dog sænke blodsukkerniveauet nok til at forårsage symptomer eller nogle gange livstruende hypoglykæmi. Fordi PRECOSE givet i kombination med et sulfonylurinstof eller insulin vil forårsage en yderligere sænkning af blodsukkeret, kan det øge det hypoglykæmiske potentiale af disse midler. Hypoglykæmi forekommer ikke hos patienter, der får metformin alene under normale brugsforhold, og der blev ikke observeret en øget forekomst af hypoglykæmi hos patienter, når PRECOSE blev tilføjet til metforminbehandling. Risikoen for hypoglykæmi, dens symptomer og behandling og tilstande, der disponerer for dets udvikling, bør forstås godt af patienter og ansvarlige familiemedlemmer. Fordi PRECOSE 50 mg forhindrer nedbrydning af spisesukker, bør patienter have en let tilgængelig kilde til glukose (dextrose, D-glukose) til at behandle symptomer på lavt blodsukker, når de tager PRECOSE i kombination med et sulfonylurinstof eller insulin.
Hvis der opstår bivirkninger med PRECOSE, udvikles de normalt i løbet af de første par uger af behandlingen. De er oftest milde til moderate gastrointestinale virkninger, såsom flatulens, diarré eller ubehag i maven, og aftager generelt i hyppighed og intensitet med tiden.
