Mobic 7.5mg, 15mg Meloxicam Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Mobic 15mg, og hvordan bruges det?
Mobic 7.5mg er en receptpligtig ikke-steroid antiinflammatorisk medicin, der bruges til at behandle symptomerne på slidgigt, leddegigt og moderate til svære smerter. Mobic 7,5 mg kan bruges alene eller sammen med anden medicin.
Mobic er et ikke-steroidt antiinflammatorisk lægemiddel (NSAID).
Det vides ikke, om Mobic er sikkert og effektivt til børn, der vejer mindre end 132 lbs (60 kg).
Hvad er de mulige bivirkninger af Mobic 7.5mg?
- enhver form for hududslæt,
- stakåndet,
- hævelse,
- hurtig vægtøgning,
- blodig eller tjæreagtig afføring,
- hoste blod eller opkast, der ligner kaffegrums,
- kvalme,
- smerter i øvre mave,
- kløe,
- træthedsfornemmelse,
- influenzalignende symptomer,
- mistet appetiten,
- mørk urin,
- lerfarvede afføring,
- gulfarvning af øjne eller hud (gulsot),
- bleg hud,
- træthed,
- svimmelhed,
- kolde hænder eller fødder,
- lidt eller ingen vandladning, og
- hævelse i fødder eller ankler
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Mobic 15mg omfatter:
- mavesmerter,
- kvalme,
- opkastning,
- halsbrand,
- diarré,
- forstoppelse,
- gas,
- svimmelhed, og
- forkølelses- eller influenzasymptomer
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Mobic. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
ADVARSEL
RISIKO FOR ALVORLIG Hjerte- og kardiovaskulære hændelser
Kardiovaskulære trombotiske hændelser
- Ikke-steroide antiinflammatoriske lægemidler (NSAID'er) forårsager en øget risiko for alvorlige kardiovaskulære trombotiske hændelser, herunder myokardieinfarkt og slagtilfælde, som kan være dødelige. Denne risiko kan opstå tidligt i behandlingen og kan stige med varigheden af brugen [se ADVARSLER OG FORHOLDSREGLER].
- MOBIC 7,5 mg er kontraindiceret i forbindelse med koronararterie bypass-operationer (CABG) [se KONTRAINDIKATIONER og ADVARSLER OG FORHOLDSREGLER].
Gastrointestinal blødning, ulceration og perforation
- NSAID'er forårsager en øget risiko for alvorlige gastrointestinale (GI) bivirkninger, herunder blødning, ulceration og perforering af maven eller tarmene, som kan være dødelige. Disse hændelser kan opstå når som helst under brug og uden advarselssymptomer. Ældre patienter og patienter med en tidligere anamnese med mavesår og/eller GI-blødning har større risiko for alvorlige GI-hændelser [se ADVARSLER OG FORHOLDSREGLER].
BESKRIVELSE
MOBIC (meloxicam) er et ikke-steroidt antiinflammatorisk lægemiddel (NSAID). Hver pastelgul MOBIC 15 mg tablet indeholder 7,5 mg eller 15 mg meloxicam til oral administration. Meloxicam er kemisk betegnet som 4-hydroxy-2-methyl-N-(5methyl2thiazolyl)-2H-1,2-benzothiazin-3-carboxamid-1,1-dioxid. Molekylvægten er 351,4. Dens empiriske formel er C14H13N3O4S2 og den har følgende strukturformel:
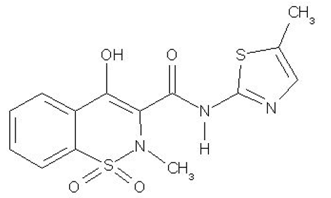
Meloxicam er et pastelgult fast stof, praktisk talt uopløseligt i vand, med højere opløselighed observeret i stærke syrer og baser. Det er meget lidt opløseligt i methanol. Meloxicam har en tilsyneladende fordelingskoefficient (log P)app = 0,1 i n-oktanol/buffer pH 7,4. Meloxicam har pKa-værdier på 1,1 og 4,2.
MOBIC 15mg fås som en tablet til oral administration indeholdende 7,5 mg eller 15 mg meloxicam.
De inaktive ingredienser i MOBIC 15 mg tabletter omfatter kolloid siliciumdioxid, crospovidon, lactosemonohydrat, magnesiumstearat, mikrokrystallinsk cellulose, povidon og natriumcitratdihydrat.
INDIKATIONER
Slidgigt (OA)
MOBIC er indiceret til lindring af tegn og symptomer på slidgigt [se Kliniske Studier
Reumatoid arthritis (RA)
MOBIC er indiceret til lindring af tegn og symptomer på reumatoid arthritis [se Kliniske Studier ].
Juvenil Reumatoid Arthritis (JRA) Pauciartikulært og polyartikulært forløb
MOBIC 7,5 mg er indiceret til lindring af tegn og symptomer på pauciartikulært eller polyartikulært forløb Juvenil Reumatoid Arthritis hos patienter, der vejer ≥60 kg [se DOSERING OG ADMINISTRATION og Kliniske Studier ].
DOSERING OG ADMINISTRATION
Generelle doseringsanvisninger
Overvej omhyggeligt de potentielle fordele og risici ved MOBIC og andre behandlingsmuligheder, før du beslutter dig for at bruge MOBIC. Brug den laveste effektive dosis i den korteste varighed i overensstemmelse med individuelle patientbehandlingsmål [se ADVARSLER OG FORHOLDSREGLER ].
Efter at have observeret responsen på den indledende behandling med MOBIC, justeres dosis, så den passer til den enkelte patients behov.
Hos voksne er den maksimalt anbefalede daglige orale dosis af MOBIC 15 mg uanset formulering. Hos patienter med hæmodialyse anbefales en maksimal daglig dosis på 7,5 mg [se Brug i specifikke populationer og KLINISK FARMAKOLOGI
MOBIC kan tages uden hensyntagen til tidspunktet for måltider.
Slidgigt
Til lindring af tegn og symptomer på slidgigt er den anbefalede orale start- og vedligeholdelsesdosis af MOBIC 7,5 mg én gang dagligt. Nogle patienter kan få yderligere fordele ved at øge dosis til 15 mg én gang dagligt.
Rheumatoid arthritis
Til lindring af tegn og symptomer på leddegigt er den anbefalede orale start- og vedligeholdelsesdosis af MOBIC 7,5 mg 7,5 mg én gang dagligt. Nogle patienter kan få yderligere fordele ved at øge dosis til 15 mg én gang dagligt.
Juvenil Reumatoid Arthritis (JRA) Pauciartikulært og polyartikulært forløb
Til behandling af juvenil reumatoid arthritis er den anbefalede orale dosis MOBIC 7,5 mg 7,5 mg én gang dagligt til børn, der vejer ≥60 kg. Der var ingen yderligere fordel påvist ved at øge dosis over 7,5 mg i kliniske forsøg.
MOBIC tabletter bør ikke anvendes til børn, der vejer
Nedsat nyrefunktion
Det anbefales ikke at bruge MOBIC 15 mg til personer med svært nedsat nyrefunktion.
Hos patienter i hæmodialyse er den maksimale dosis af MOBIC 7,5 mg dagligt [se KLINISK FARMAKOLOGI ].
Ikke-udskiftelighed med andre formuleringer af Meloxicam
MOBIC-tabletter har ikke vist tilsvarende systemisk eksponering for andre godkendte formuleringer af oral meloxicam. Derfor kan MOBIC 7,5 mg tabletter ikke udskiftes med andre formuleringer af oralt meloxicamprodukt, selvom den samlede milligramstyrke er den samme. Udskift ikke lignende dosisstyrker af MOBIC 7,5 mg tabletter med andre formuleringer af oralt meloxicamprodukt.
HVORDAN LEVERET
Doseringsformer og styrker
MOBIC (meloxicam) tabletter:
- 7,5 mg: pastelgul, rund, bikonveks, uovertrukket tablet indeholdende meloxicam 7,5 mg. Imponeret med Boehringer Ingelheim-logoet på den ene side og bogstavet "M" på den anden.
- 15 mg: pastelgul, aflang, bikonveks, uovertrukket tablet indeholdende meloxicam 15 mg. Imponeret med tabletkoden "15" på den ene side og bogstavet "M" på den anden.
Opbevaring og håndtering
MOBIK fås som en pastelgul, rund, bikonveks, uovertrukket tablet indeholdende meloxicam 7,5 mg eller som en pastelgul, aflang, bikonveks, uovertrukket tablet indeholdende meloxicam 15 mg. 7,5 mg tabletten er præget med Boehringer Ingelheim-logoet på den ene side og bogstavet "M" på den anden side. Tabletten på 15 mg er præget med tabletkoden "15" på den ene side og bogstavet "M" på den anden side.
MOBIC (meloxicam) tabletter 7,5 mg: NDC 0597-0029-01; 100 flasker
MOBIC (meloxicam) tabletter 15 mg: NDC 0597-0030-01; 100 flasker
Opbevaring
Opbevares ved 20°C til 25°C (68°F til 77°F); udflugter tilladt til 15°C til 30°C (59°F til 86°F) [se USP kontrolleret rumtemperatur ]. Opbevar MOBIC-tabletter på et tørt sted.
Dispenser tabletterne i en tæt beholder.
Opbevar dette og al medicin utilgængeligt for børn.
Distribueret af: Boehringer Ingelheim Pharmaceuticals, Inc. Ridgefield, CT 06877 USA. Revideret: april 2021
BIVIRKNINGER
Følgende bivirkninger er beskrevet mere detaljeret i andre afsnit af mærkningen:
- Kardiovaskulære trombotiske hændelser [se KASSET ADVARSEL og ADVARSLER OG FORHOLDSREGLER ]
- GI-blødning, ulceration og perforation [se KASSET ADVARSEL og ADVARSLER OG FORHOLDSREGLER ]
- Hepatotoksicitet [se ADVARSLER OG FORHOLDSREGLER ]
- Hypertension [se ADVARSLER OG FORHOLDSREGLER ]
- Hjertesvigt og ødem [se ADVARSLER OG FORHOLDSREGLER ]
- Nyretoksicitet og hyperkaliæmi [se ADVARSLER OG FORHOLDSREGLER ]
- Anafylaktiske reaktioner [se ADVARSLER OG FORHOLDSREGLER ]
- Alvorlige hudreaktioner [se ADVARSLER OG FORHOLDSREGLER ]
- Lægemiddelreaktion med eosinofili og systemiske symptomer (DRESS) [se ADVARSLER OG FORHOLDSREGLER ]
- Fostertoksicitet [se ADVARSLER OG FORHOLDSREGLER ]
- Hæmatologisk toksicitet [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring med kliniske forsøg
Fordi kliniske forsøg udføres under vidt forskellige forhold, kan bivirkningsrater observeret i de kliniske forsøg med et lægemiddel ikke direkte sammenlignes med hastigheder i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de frekvenser, der observeres i praksis.
Voksne
Slidgigt og reumatoid arthritis
MOBIC fase 2/3 kliniske forsøgsdatabase omfatter 10.122 OA-patienter og 1012 RA-patienter behandlet med MOBIC 7,5 mg/dag, 3505 OA-patienter og 1351 RA-patienter behandlet med MOBIC 15 mg/dag. MOBIC i disse doser blev administreret til 661 patienter i mindst 6 måneder og til 312 patienter i mindst et år. Ca. 10.500 af disse patienter blev behandlet i ti placebo- og/eller aktiv-kontrollerede slidgigt-forsøg, og 2363 af disse patienter blev behandlet i ti placebo- og/eller aktiv-kontrollerede reumatoid arthritis-forsøg. Gastrointestinale (GI) bivirkninger var de hyppigst rapporterede bivirkninger i alle behandlingsgrupper på tværs af MOBIC 15 mg forsøg.
Et 12-ugers multicenter, dobbeltblindt, randomiseret forsøg blev udført med patienter med slidgigt i knæet eller hoften for at sammenligne effektiviteten og sikkerheden af MOBIC 7,5 mg med placebo og med en aktiv kontrol. To 12-ugers multicenter, dobbeltblindede, randomiserede forsøg blev udført med patienter med reumatoid arthritis for at sammenligne effektiviteten og sikkerheden af MOBIC med placebo.
Tabel 1a viser uønskede hændelser, der forekom i ≥2 % af MOBIC-behandlingsgrupperne i et 12-ugers placebo- og aktivt kontrolleret slidgigtforsøg.
Tabel 1b viser uønskede hændelser, der forekom i ≥2 % af MOBIC 7,5 mg-behandlingsgrupperne i to 12-ugers placebokontrollerede reumatoid arthritis forsøg.
De uønskede hændelser, der forekom med MOBIC 15 mg hos ≥2 % af patienterne behandlet kortvarigt (4 til 6 uger) og langvarigt (6 måneder) i aktivt kontrollerede slidgigtforsøg er vist i tabel 2.
Højere doser af MOBIC (22,5 mg og mere) er blevet forbundet med en øget risiko for alvorlige GI-hændelser; derfor bør den daglige dosis af MOBIC 15 mg ikke overstige 15 mg.
Pædiatri
Pauciartikulært og polyartikulært forløb Juvenil Reumatoid Arthritis (JRA)
Tre hundrede og syvogfirs patienter med pauciartikulært og polyartikulært JRA blev eksponeret for MOBIC 15 mg med doser fra 0,125 til 0,375 mg/kg pr. dag i tre kliniske forsøg. Disse undersøgelser bestod af to 12-ugers multicenter, dobbeltblindede, randomiserede forsøg (et med en 12-ugers åben forlængelse og en med en 40-ugers forlængelse) og et 1-årigt åbent PK-studie. De bivirkninger, der blev observeret i disse pædiatriske undersøgelser med MOBIC 15 mg, svarede til de kliniske forsøg med voksne, selvom der var forskelle i hyppighed. Især de følgende mest almindelige bivirkninger, mavesmerter, opkastning, diarré, hovedpine og pyreksi, var mere almindelige hos pædiatrien end i de voksne forsøg. Udslæt blev rapporteret hos syv (
Det følgende er en liste over bivirkninger, der forekommer hos
Kroppen som helhed: allergisk reaktion, ansigtsødem, træthed, feber, hedeture, utilpashed, synkope, vægttab, vægtstigning
Kardiovaskulær: angina pectoris, hjertesvigt, hypertension, hypotension, myokardieinfarkt, vaskulitis
Centrale og perifere nervesystem: kramper, paræstesi, tremor, svimmelhed
Gastrointestinale : colitis, mundtørhed, sår på tolvfingertarmen, udbrud, esophagitis, mavesår, gastritis, gastroøsofageal refluks, gastrointestinal blødning, hæmatemese, hæmoragisk sår på tolvfingertarmen, hæmoragisk mavesår, intestinal perforeret, mavebetændelse, perforeret mavebetændelse, perforeret mavebetændelse, perforeret melena, ulcerativ
Puls og rytme: arytmi, hjertebanken, takykardi
Hæmatologisk: leukopeni, purpura, trombocytopeni
Lever og galdesystem: ALT øget, AST øget, bilirubinæmi, GGT øget, hepatitis
Metabolisk og ernæringsmæssig : dehydrering
Psykiatrisk : unormal drøm, angst, øget appetit, forvirring, depression, nervøsitet, somnolens
Åndedræt: astma, bronkospasme, dyspnø
Hud og vedhæng: alopeci, angioødem, bulløst udbrud, lysfølsomhedsreaktion, pruritus, øget svedtendens, nældefeber
Særlige sanser: unormalt syn, conjunctivitis, smagsforstyrrelser, tinnitus
Urinsystemet: albuminuri, BUN øget, kreatinin øget, hæmaturi, nyresvigt
Postmarketing oplevelse
Følgende bivirkninger er blevet identificeret under brug af MOBIC efter godkendelse. Fordi disse reaktioner rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt pålideligt at estimere deres hyppighed eller etablere en årsagssammenhæng til lægemiddeleksponering. Beslutninger om, hvorvidt en uønsket hændelse fra spontane indberetninger skal inkluderes i mærkningen, er typisk baseret på en eller flere af følgende faktorer: (1) hændelsens alvor, (2) antallet af indberetninger eller (3) styrken af årsagssammenhængen til medicin. Bivirkninger rapporteret i verdensomspændende erfaring efter markedsføring eller litteraturen omfatter: akut urinretention; agranulocytose; ændringer i humør (såsom humørforhøjelse); anafylaktiske reaktioner inklusive shock; erythema multiforme; eksfoliativ dermatitis; interstitiel nefritis; gulsot; leversvigt; Stevens Johnson syndrom; toksisk epidermal nekrolyse, og infertilitet kvinde.
DRUGSINTERAKTIONER
Se tabel 3 for klinisk signifikante lægemiddelinteraktioner med meloxicam. Se også ADVARSLER OG FORHOLDSREGLER og KLINISK FARMAKOLOGI .
ADVARSLER
Inkluderet som en del af FORHOLDSREGLER afsnit.
FORHOLDSREGLER
Kardiovaskulære trombotiske hændelser
Kliniske forsøg med flere COX-2 selektive og ikke-selektive NSAID'er af op til tre års varighed har vist en øget risiko for alvorlige kardiovaskulære (CV) trombotiske hændelser, herunder myokardieinfarkt (MI) og slagtilfælde, som kan være fatale. Baseret på tilgængelige data er det uklart, at risikoen for CV-trombotiske hændelser er ens for alle NSAID'er. Den relative stigning i alvorlige CV-trombotiske hændelser over baseline forårsaget af NSAID-brug synes at være ens hos dem med og uden kendt CV-sygdom eller risikofaktorer for CV-sygdom. Patienter med kendt CV-sygdom eller risikofaktorer havde dog en højere absolut forekomst af overskydende alvorlige CV-trombotiske hændelser på grund af deres øgede baseline-rate. Nogle observationsstudier viste, at denne øgede risiko for alvorlige CV-trombotiske hændelser begyndte allerede i de første uger af behandlingen. Stigningen i CV-trombotisk risiko er blevet observeret mest konsekvent ved højere doser.
For at minimere den potentielle risiko for en uønsket CV-hændelse hos NSAID-behandlede patienter skal du bruge den laveste effektive dosis i den kortest mulige varighed. Læger og patienter bør forblive opmærksomme på udviklingen af sådanne hændelser under hele behandlingsforløbet, selv i fravær af tidligere CV-symptomer. Patienter bør informeres om symptomerne på alvorlige CV-hændelser og de skridt, der skal tages, hvis de opstår.
Der er ingen konsekvent evidens for, at samtidig brug af aspirin mindsker den øgede risiko for alvorlige CV-trombotiske hændelser forbundet med NSAID-brug. Samtidig brug af aspirin og et NSAID, såsom meloxicam, øger risikoen for alvorlige gastrointestinale (GI) hændelser [se ADVARSLER OG FORHOLDSREGLER ].
Status Post Koronararterie Bypass Graft (CABG) kirurgi
To store, kontrollerede kliniske forsøg med et COX-2-selektivt NSAID til behandling af smerte i de første 10-14 dage efter CABG-operation fandt en øget forekomst af myokardieinfarkt og slagtilfælde. NSAID'er er kontraindiceret i forbindelse med CABG [se KONTRAINDIKATIONER ].
Post-MI-patienter
Observationsundersøgelser udført i det danske folkeregister har vist, at patienter behandlet med NSAID i post-MI-perioden havde øget risiko for reinfarkt, CV-relateret død og dødelighed af alle årsager begyndende i den første uge af behandlingen. I denne samme kohorte var forekomsten af dødsfald i det første år efter MI 20 pr. 100 personår hos NSAID-behandlede patienter sammenlignet med 12 pr. 100 personår hos ikke-NSAID-eksponerede patienter. Selvom den absolutte dødsrate faldt noget efter det første år efter MI, var den øgede relative risiko for død hos NSAID-brugere ved i mindst de næste fire års opfølgning.
Undgå brugen af MOBIC 15mg hos patienter med nylig MI, medmindre fordelene forventes at opveje risikoen for tilbagevendende CV-trombotiske hændelser. Hvis MOBIC 15mg anvendes til patienter med nylig MI, skal patienter overvåges for tegn på hjerteiskæmi.
Gastrointestinal blødning, ulceration og perforering
NSAID'er, herunder meloxicam, kan forårsage alvorlige gastrointestinale (GI) bivirkninger, herunder betændelse, blødning, ulceration og perforering af spiserøret, maven, tyndtarmen eller tyktarmen, hvilket kan være dødeligt. Disse alvorlige bivirkninger kan forekomme til enhver tid, med eller uden advarselssymptomer, hos patienter behandlet med NSAID'er. Kun én ud af fem patienter, som udvikler en alvorlig øvre GI-bivirkning under NSAID-behandling, er symptomatisk. Øvre mavesår, grov blødning eller perforation forårsaget af NSAID'er forekom hos ca. 1 % af patienterne behandlet i 3-6 måneder og hos ca. 2 % til 4 % af patienterne behandlet i et år. Selv kortvarig NSAID-behandling er dog ikke uden risiko.
Risikofaktorer for GI-blødning, ulceration og perforering
Patienter med en tidligere anamnese med mavesår og/eller GI-blødning, som brugte NSAID'er, havde en større end 10 gange øget risiko for at udvikle GI-blødning sammenlignet med patienter uden disse risikofaktorer. Andre faktorer, der øger risikoen for GI-blødning hos patienter behandlet med NSAID'er, omfatter længere varighed af NSAID-behandling; samtidig brug af orale kortikosteroider, aspirin, antikoagulantia eller selektive serotoningenoptagshæmmere (SSRI'er); rygning; brug af alkohol; ældre alder; og dårlig generel sundhedstilstand. De fleste postmarketingrapporter om fatale gastrointestinale hændelser forekom hos ældre eller svækkede patienter. Derudover har patienter med fremskreden leversygdom og/eller koagulopati øget risiko for GI-blødning.
Strategier til at minimere GI-risici hos NSAID-behandlede patienter
- Brug den laveste effektive dosis i den kortest mulige varighed.
- Undgå administration af mere end ét NSAID ad gangen.
- Undgå brug til patienter med højere risiko, medmindre fordelene forventes at opveje den øgede risiko for blødning. For sådanne patienter, såvel som dem med aktiv gastrointestinale blødning, bør du overveje alternative behandlinger, bortset fra NSAID'er.
- Vær opmærksom på tegn og symptomer på GI-ulceration og blødning under NSAID-behandling.
- Hvis der er mistanke om en alvorlig GI-bivirkning, påbegynd omgående evaluering og behandling og afbryd MOBIC 15mg, indtil en alvorlig GI-bivirkning er udelukket.
- Ved samtidig brug af lavdosis aspirin til hjerteprofylakse skal patienterne overvåges tættere for tegn på GI-blødning [se DRUGSINTERAKTIONER ].
Hepatotoksicitet
Forhøjelser af ALAT eller ASAT (tre eller flere gange den øvre grænse for normal [ULN]) er blevet rapporteret hos ca. 1 % af NSAID-behandlede patienter i kliniske forsøg. Derudover er der rapporteret sjældne, nogle gange fatale, tilfælde af alvorlig leverskade, herunder fulminant hepatitis, levernekrose og leversvigt.
Forhøjelser af ALAT eller ASAT (mindre end tre gange ULN) kan forekomme hos op til 15 % af patienter, der behandles med NSAID, inklusive meloxicam.
Informer patienterne om advarselstegn og symptomer på hepatotoksicitet (f.eks. kvalme, træthed, sløvhed, diarré, kløe, gulsot, ømhed i højre øvre kvadrant og "influenzalignende" symptomer). Hvis der udvikles kliniske tegn og symptomer, der er forenelige med leversygdom, eller hvis systemiske manifestationer opstår (f.eks. eosinofili, udslæt osv.), skal du straks afbryde MOBIC og udføre en klinisk evaluering af patienten [se Brug i specifikke populationer og KLINISK FARMAKOLOGI ].
Forhøjet blodtryk
NSAID'er, inklusive MOBIC, kan føre til ny opstået eller forværring af allerede eksisterende hypertension, som begge kan bidrage til den øgede forekomst af CV-hændelser. Patienter, der tager angiotensin-konverterende enzym (ACE)-hæmmere, thiaziddiuretika eller loop-diuretika, kan have nedsat respons på disse behandlinger, når de tager NSAID'er [se DRUGSINTERAKTIONER ].
Overvåg blodtrykket (BP) under påbegyndelse af NSAID-behandling og under hele behandlingsforløbet.
Hjertesvigt og ødem
Coxib og traditionelle NSAID Trialists' Collaboration meta-analyse af randomiserede kontrollerede undersøgelser viste en ca. to gange stigning i hospitalsindlæggelser for hjertesvigt hos COX-2 selektivt behandlede patienter og ikke-selektive NSAID-behandlede patienter sammenlignet med placebo-behandlede patienter. I et dansk folkeregisterundersøgelse af patienter med hjertesvigt øgede NSAID-brug risikoen for MI, hospitalsindlæggelse for hjertesvigt og død.
Derudover er væskeretention og ødem blevet observeret hos nogle patienter behandlet med NSAID'er. Brug af meloxicam kan sløve CV-virkningerne af flere terapeutiske midler, der bruges til at behandle disse medicinske tilstande (f.eks. diuretika, ACE-hæmmere eller angiotensinreceptorblokkere [ARB'er]) [se DRUGSINTERAKTIONER ].
Undgå brugen af MOBIC 15mg til patienter med alvorligt hjertesvigt, medmindre fordelene forventes at opveje risikoen for forværring af hjertesvigt. Hvis MOBIC anvendes til patienter med alvorligt hjertesvigt, overvåg patienterne for tegn på forværret hjertesvigt.
Nyretoksicitet og hyperkaliæmi
Renal toksicitet
Langvarig administration af NSAID'er, inklusive MOBIC, har resulteret i nyrepapillær nekrose, nyreinsufficiens, akut nyresvigt og anden nyreskade.
Renal toksicitet er også set hos patienter, hvor renale prostaglandiner har en kompenserende rolle i opretholdelsen af renal perfusion. Hos disse patienter kan administration af et NSAID forårsage en dosisafhængig reduktion i prostaglandindannelsen og sekundært i renal blodgennemstrømning, hvilket kan fremkalde åbenlys nyreinsufficiens. Patienter med størst risiko for denne reaktion er dem med nedsat nyrefunktion, dehydrering, hypovolæmi, hjertesvigt, leverdysfunktion, dem, der tager diuretika og ACE-hæmmere eller ARB'er, og ældre. Seponering af NSAID-behandling efterfølges sædvanligvis af genopretning til forbehandlingstilstanden.
De renale virkninger af MOBIC kan fremskynde udviklingen af nyreinsufficiens hos patienter med allerede eksisterende nyresygdom. Da nogle MOBIC-metabolitter udskilles af nyrerne, overvåg patienterne for tegn på forværret nyrefunktion.
Korrekt volumenstatus hos dehydrerede eller hypovolæmiske patienter før påbegyndelse af MOBIC. Overvåg nyrefunktionen hos patienter med nedsat nyre- eller leverfunktion, hjertesvigt, dehydrering eller hypovolæmi under brug af MOBIC [se DRUGSINTERAKTIONER ].
Der er ingen tilgængelig information fra kontrollerede kliniske undersøgelser vedrørende brugen af MOBIC 15mg hos patienter med fremskreden nyresygdom. Undgå brugen af MOBIC 7,5 mg til patienter med fremskreden nyresygdom, medmindre fordelene forventes at opveje risikoen for forværring af nyrefunktionen. Hvis MOBIC anvendes til patienter med fremskreden nyresygdom, overvåg patienterne for tegn på forværret nyrefunktion [se KLINISK FARMAKOLOGI ].
Hyperkaliæmi
Stigninger i serumkaliumkoncentrationen, inklusive hyperkaliæmi, er blevet rapporteret ved brug af NSAID'er, selv hos nogle patienter uden nedsat nyrefunktion. Hos patienter med normal nyrefunktion er disse virkninger blevet tilskrevet en tilstand af hyporeninemisk-hypoaldosteronisme.
Anafylaktiske reaktioner
Meloxicam er blevet forbundet med anafylaktiske reaktioner hos patienter med og uden kendt overfølsomhed over for meloxicam og hos patienter med aspirinfølsom astma [se KONTRAINDIKATIONER og ADVARSLER OG FORHOLDSREGLER ].
Søg akut hjælp, hvis der opstår en anafylaktisk reaktion.
Forværring af astma relateret til aspirinfølsomhed
En subpopulation af patienter med astma kan have aspirinfølsom astma, som kan omfatte kronisk rhinosinusitis kompliceret af næsepolypper; alvorlig, potentielt dødelig bronkospasme; og/eller intolerance over for aspirin og andre NSAID'er. Fordi krydsreaktivitet mellem aspirin og andre NSAID'er er blevet rapporteret hos sådanne aspirinfølsomme patienter, er MOBIC kontraindiceret hos patienter med denne form for aspirinfølsomhed [se KONTRAINDIKATIONER ]. Når MOBIC 15 mg anvendes til patienter med allerede eksisterende astma (uden kendt aspirinfølsomhed), overvåg patienterne for ændringer i tegn og symptomer på astma.
Alvorlige hudreaktioner
NSAID'er, herunder meloxicam, kan forårsage alvorlige hudbivirkninger såsom eksfoliativ dermatitis, Stevens-Johnsons syndrom (SJS) og toksisk epidermal nekrolyse (TEN), som kan være dødelig. Disse alvorlige hændelser kan forekomme uden varsel. Informer patienterne om tegn og symptomer på alvorlige hudreaktioner og om at afbryde brugen af MOBIC ved den første forekomst af hududslæt eller andre tegn på overfølsomhed. MOBIC er kontraindiceret hos patienter med tidligere alvorlige hudreaktioner på NSAID'er [se KONTRAINDIKATIONER ].
Lægemiddelreaktion med eosinofili og systemiske symptomer (DRESS)
Lægemiddelreaktion med eosinofili og systemiske symptomer (DRESS) er blevet rapporteret hos patienter, der tager NSAID'er såsom MOBIC. Nogle af disse hændelser har været dødelige eller livstruende. DRESS viser sig typisk, men ikke udelukkende, med feber, udslæt, lymfadenopati og/eller hævelse i ansigtet. Andre kliniske manifestationer kan omfatte hepatitis, nefritis, hæmatologiske abnormiteter, myocarditis eller myositis. Nogle gange kan symptomer på DRESS minde om en akut virusinfektion. Eosinofili er ofte til stede. Fordi denne lidelse er variabel i sin præsentation, kan andre organsystemer, der ikke er nævnt her, være involveret. Det er vigtigt at bemærke, at tidlige manifestationer af overfølsomhed, såsom feber eller lymfadenopati, kan være til stede, selvom udslæt ikke er tydeligt. Hvis sådanne tegn eller symptomer er til stede, skal du afbryde MOBIC og straks evaluere patienten.
Føtal toksicitet
For tidlig lukning af føtal ductus arteriosus
Undgå brug af NSAID'er, inklusive MOBIC, hos gravide kvinder ved ca. 30 ugers graviditet og senere. NSAID'er, inklusive MOBIC, øger risikoen for for tidlig lukning af føtal ductus arteriosus ved omtrent denne svangerskabsalder.
Oligohydramnios/neonatal nyreinsufficiens
Brug af NSAID'er, inklusive MOBIC 15 mg, ved ca. 20 ugers svangerskab eller senere i graviditeten kan forårsage føtal nyreinsufficiens, hvilket fører til oligohydramnios og i nogle tilfælde neonatal nyreinsufficiens. Disse uønskede resultater ses i gennemsnit efter dage til ugers behandling, selvom oligohydramnios sjældent er blevet rapporteret så snart som 48 timer efter NSAID-start. Oligohydramnios er ofte, men ikke altid, reversibel med seponering af behandlingen. Komplikationer af forlænget oligohydramnios kan for eksempel omfatte lemmerkontrakturer og forsinket lungemodning. I nogle tilfælde efter markedsføring af nedsat nyrefunktion hos nyfødte var invasive procedurer såsom udvekslingstransfusion eller dialyse påkrævet.
Hvis NSAID-behandling er nødvendig mellem ca. 20 uger og 30 ugers svangerskab, skal MOBIC-brug begrænses til den lavest mulige effektive dosis og kortest mulige varighed. Overvej ultralydsovervågning af fostervand, hvis MOBIC 15mg-behandling strækker sig ud over 48 timer. Afbryd MOBIC 15 mg, hvis der opstår oligohydramnios, og følg op i henhold til klinisk praksis [se Brug i specifikke populationer ].
Hæmatologisk toksicitet
Anæmi er forekommet hos NSAID-behandlede patienter. Dette kan skyldes okkult eller groft blodtab, væskeophobning eller en ufuldstændigt beskrevet effekt på erytropoiese. Hvis en patient behandlet med MOBIC har tegn eller symptomer på anæmi, skal du overvåge hæmoglobin eller hæmatokrit.
NSAID'er, inklusive MOBIC 7,5 mg, kan øge risikoen for blødningshændelser. Komorbide tilstande såsom koagulationsforstyrrelser eller samtidig brug af warfarin, andre antikoagulantia, trombocythæmmende midler (f.eks. aspirin), serotoningenoptagelseshæmmere (SSRI'er) og serotonin-noradrenalin-genoptagelseshæmmere (SNRI'er) kan øge denne risiko. Overvåg disse patienter for tegn på blødning [se DRUGSINTERAKTIONER ].
Maskering af betændelse og feber
Den farmakologiske aktivitet af MOBIC 15 mg til at reducere inflammation og muligvis feber, kan mindske anvendeligheden af diagnostiske tegn til at påvise infektioner.
Laboratorieovervågning
Da alvorlig GI-blødning, levertoksicitet og nyreskade kan forekomme uden advarselssymptomer eller tegn, bør du overveje at overvåge patienter i langvarig NSAID-behandling med en CBC og en kemiprofil med jævne mellemrum [se ADVARSLER OG FORHOLDSREGLER ].
Patientrådgivningsinformation
Råd patienten til at læse den FDA-godkendte patientmærkning ( Medicinvejledning ), der følger med hver udleveret recept.
Informer patienter, familier eller deres pårørende om følgende information, før behandling med et NSAID påbegyndes og med jævne mellemrum i løbet af den igangværende behandling.
Kardiovaskulære trombotiske hændelser
Rådgiv patienterne om at være opmærksomme på symptomer på kardiovaskulære trombotiske hændelser, herunder brystsmerter, åndenød, svaghed eller sløret tale, og at rapportere alle disse symptomer til deres læge med det samme [se ADVARSLER OG FORHOLDSREGLER ].
Gastrointestinal blødning, ulceration og perforering
Rådgive patienter om at rapportere symptomer på ulcerationer og blødninger, herunder epigastriske smerter, dyspepsi, melena og hæmatemese til deres læge. I forbindelse med samtidig brug af lavdosis aspirin til hjerteprofylakse, informere patienterne om den øgede risiko for tegn og symptomer på GI-blødning [se ADVARSLER OG FORHOLDSREGLER ].
Hepatotoksicitet
Informer patienterne om advarselstegn og symptomer på hepatotoksicitet (f.eks. kvalme, træthed, sløvhed, diarré, kløe, gulsot, ømhed i højre øvre kvadrant og "influenzalignende" symptomer). Hvis disse opstår, instruer patienterne i at stoppe MOBIC 7,5 mg og søge øjeblikkelig medicinsk behandling [se ADVARSLER OG FORHOLDSREGLER ].
Hjertesvigt og ødem
Rådgiv patienterne om at være opmærksomme på symptomer på kongestiv hjertesvigt, herunder åndenød, uforklarlig vægtøgning eller ødem, og at kontakte deres læge, hvis sådanne symptomer opstår [se ADVARSLER OG FORHOLDSREGLER ].
Anafylaktiske reaktioner
Informer patienterne om tegn på en anafylaktisk reaktion (f.eks. åndedrætsbesvær, hævelse af ansigt eller hals). Instruer patienterne i at søge øjeblikkelig nødhjælp, hvis disse opstår [se KONTRAINDIKATIONER og ADVARSLER OG FORHOLDSREGLER ].
Alvorlige hudreaktioner, inklusive DRESS
Rådgiv patienter om at stoppe med at tage MOBIC øjeblikkeligt, hvis de udvikler nogen form for udslæt eller feber, og at kontakte deres læge så hurtigt som muligt [se ADVARSLER OG FORHOLDSREGLER ].
Kvindelig fertilitet
Informer kvinder med reproduktionspotentiale, som ønsker graviditet, at NSAID'er, inklusive MOBIC 7,5 mg, kan være forbundet med en reversibel forsinkelse i ægløsning [se Brug i specifikke populationer ].
Føtal toksicitet
Informer gravide kvinder om at undgå brug af MOBIC 15mg og andre NSAID'er fra 30. svangerskabsuge på grund af risikoen for for tidlig lukning af føtal ductus arteriosus. Hvis behandling med MOBIC 15 mg er nødvendig for en gravid kvinde mellem ca. 20 og 30 ugers graviditet, skal du rådgive hende om, at hun muligvis skal overvåges for oligohydramnios, hvis behandlingen fortsætter i mere end 48 timer [se ADVARSLER OG FORHOLDSREGLER og Brug i specifikke populationer ].
Undgå samtidig brug af NSAID'er
Informer patienterne om, at samtidig brug af MOBIC 15 mg og andre NSAID'er eller salicylater (f.eks. diflunisal, salsalat) ikke anbefales på grund af den øgede risiko for gastrointestinal toksicitet og ringe eller ingen stigning i effektivitet [se ADVARSLER OG FORHOLDSREGLER og DRUGSINTERAKTIONER ]. Advarer patienter om, at NSAID'er kan være til stede i "håndkøbsmedicin" til behandling af forkølelse, feber eller søvnløshed.
Brug af NSAID'er og lavdosis aspirin
Informer patienterne om ikke at bruge lavdosis aspirin samtidig med MOBIC 7,5 mg, før de taler med deres læge [se DRUGSINTERAKTIONER ].
For aktuelle ordinationsoplysninger skal du scanne koden eller ringe til Boehringer Ingelheim Pharmaceuticals, Inc. på 1-800-542-6257.
Ikke-klinisk toksikologi
Karcinogenese, mutagenese, svækkelse af fertilitet
Karcinogenese
Der var ingen stigning i tumorincidens i langtidskarcinogenicitetsundersøgelser hos rotter (104 uger) og mus (99 uger), der fik meloxicam i orale doser op til 0,8 mg/kg/dag hos rotter og op til 8,0 mg/kg/dag i mus (op til henholdsvis 0,5 og 2,6 gange den maksimalt anbefalede humane dosis [MRHD] på 15 mg/dag MOBIC 7,5 mg baseret på kropsoverfladeareal [BSA] sammenligning).
Mutagenese
Meloxicam var ikke mutagent i et Ames-assay eller klastogent i et kromosomafvigelsesassay med humane lymfocytter og en in vivo mikronukleustest i museknoglemarv.
Forringelse af fertilitet
Meloxicam svækkede ikke han- og hunfrugtbarheden hos rotter ved orale doser op til 9 mg/kg/dag hos hanner og 5 mg/kg/dag hos hunner (hhv. op til 5,8 og 3,2 gange større end MRHD baseret på BSA sammenligning).
Brug i specifikke populationer
Graviditet
Risikooversigt
Brug af NSAID'er, inklusive MOBIC, kan forårsage for tidlig lukning af føtal ductus arteriosus og føtal nyreinsufficiens, hvilket fører til oligohydramnios og i nogle tilfælde neonatal nyreinsufficiens. På grund af disse risici skal du begrænse dosis og varighed af MOBIC-brug mellem ca. 20 og 30 uger af graviditeten, og undgå brug af MOBIC ved ca. 30 uger af graviditeten og senere i graviditeten (se Kliniske overvejelser , Data ).
For tidlig lukning af føtal ductus arteriosus
Brug af NSAID'er, inklusive MOBIC 15 mg, ved ca. 30 ugers graviditet eller senere i graviditeten øger risikoen for for tidlig lukning af fosterets ductus arteriosus.
Oligohydramnios/neonatal nyreinsufficiens
Brug af NSAID'er ved omkring 20 ugers graviditet eller senere i graviditeten har været forbundet med tilfælde af føtal nyreinsufficiens, der fører til oligohydramnios og i nogle tilfælde neonatal nyreinsufficiens.
Data fra observationsstudier vedrørende potentielle embryoføtale risici ved brug af NSAID hos kvinder i graviditetens første eller andet trimester er ikke konklusive.
I dyrereproduktionsstudier blev embryoføtal død observeret hos rotter og kaniner behandlet i organogeneseperioden med meloxicam i orale doser svarende til 0,65- og 6,5 gange den maksimale anbefalede humane dosis (MRHD) af MOBIC. Øget forekomst af septale hjertedefekter blev observeret hos kaniner behandlet under hele embryogenese med meloxicam i en oral dosis svarende til 78 gange MRHD. I præ- og postnatale reproduktionsundersøgelser var der en øget forekomst af dystoci, forsinket fødsel og nedsat afkoms overlevelse ved 0,08 gange MRHD af meloxicam. Der blev ikke observeret teratogene virkninger hos rotter og kaniner behandlet med meloxicam under organogenese ved en oral dosis svarende til 2,6 og 26 gange MRHD [se Data ].
Baseret på dyredata har prostaglandiner vist sig at have en vigtig rolle i endometrievaskulær permeabilitet, blastocystimplantation og decidualisering. I dyreforsøg resulterede administration af prostaglandinsyntesehæmmere såsom meloxicam i øget præ- og postimplantationstab. Prostaglandiner har også vist sig at have en vigtig rolle i fosterets nyreudvikling. I publicerede dyreforsøg er prostaglandinsyntesehæmmere blevet rapporteret at hæmme nyreudviklingen, når de administreres i klinisk relevante doser.
Den estimerede baggrundsrisiko for alvorlige fødselsdefekter og abort for de(n) angivne population(er) er ukendt. Alle graviditeter har en baggrundsrisiko for fødselsdefekter, tab eller andre ugunstige udfald. I den generelle befolkning i USA er den estimerede baggrundsrisiko for alvorlige fødselsdefekter og abort i klinisk anerkendte graviditeter henholdsvis 2 % til 4 % og 15 % til 20 %.
Kliniske overvejelser
Fetale/neonatale bivirkninger
For tidlig lukning af føtal ductus arteriosus
Undgå brug af NSAID'er hos kvinder ved ca. 30. svangerskabsuge og senere i graviditeten, da NSAID'er, inklusive MOBIC 7,5 mg, kan forårsage for tidlig lukning af føtal ductus arteriosus (se Data ).
Oligohydramnios/neonatal nyreinsufficiens
Hvis et NSAID er nødvendigt ved ca. 20 ugers graviditet eller senere i graviditeten, skal du begrænse brugen til den laveste effektive dosis og kortest mulige varighed. Hvis MOBIC 15 mg-behandling strækker sig ud over 48 timer, skal du overveje at monitorere med ultralyd for oligohydramnios. Hvis der opstår oligohydramnios, skal du seponere MOBIC 7,5 mg og følge op i henhold til klinisk praksis (se Data ).
Arbejde eller levering
Der er ingen undersøgelser af virkningerne af MOBIC 7,5 mg under fødsel eller fødsel. I dyreforsøg hæmmer NSAID'er, inklusive meloxicam, prostaglandinsyntesen, forårsager forsinket fødsel og øger forekomsten af dødfødsler.
Data
Menneskelige data
For tidlig lukning af føtal ductus arteriosus
Publiceret litteratur rapporterer, at brugen af NSAID'er ved ca. 30 ugers graviditet og senere i graviditeten kan forårsage for tidlig lukning af føtal ductus arteriosus.
Oligohydramnios/neonatal nyreinsufficiens
Publicerede undersøgelser og postmarketingrapporter beskriver moderbrug af NSAID ved ca. 20 ugers svangerskab eller senere i graviditeten forbundet med føtal nyreinsufficiens, der fører til oligohydramnios og i nogle tilfælde neonatal nyreinsufficiens. Disse uønskede resultater ses i gennemsnit efter dage til ugers behandling, selvom oligohydramnios sjældent er blevet rapporteret så snart som 48 timer efter NSAID-start. I mange tilfælde, men ikke alle, var faldet i fostervand forbigående og reversibelt med ophør af lægemidlet. Der har været et begrænset antal case-rapporter af moderbrug af NSAID og neonatal nyreinsufficiens uden oligohydramnios, hvoraf nogle var irreversible. Nogle tilfælde af neonatal nyredysfunktion krævede behandling med invasive procedurer, såsom udvekslingstransfusion eller dialyse.
Metodiske begrænsninger af disse postmarketing undersøgelser og rapporter omfatter mangel på en kontrolgruppe; begrænset information om dosis, varighed og tidspunkt for lægemiddeleksponering; og samtidig brug af anden medicin. Disse begrænsninger udelukker etablering af et pålideligt estimat af risikoen for uønskede føtale og neonatale resultater ved brug af NSAID hos moderen. Da de offentliggjorte sikkerhedsdata om neonatale udfald hovedsageligt involverede præmature spædbørn, er generaliserbarheden af visse rapporterede risici for fuldbårne spædbørn, der er udsat for NSAID'er gennem moderbrug, usikker.
Dyredata
Meloxicam var ikke teratogent, når det blev administreret til gravide rotter under føtal organogenese ved orale doser op til 4 mg/kg/dag (2,6 gange højere end MRHD på 15 mg MOBIC baseret på BSA-sammenligning). Administration af meloxicam til gravide kaniner under hele embryogenese frembragte en øget forekomst af septumdefekter i hjertet ved en oral dosis på 60 mg/kg/dag (78 gange højere end MRHD baseret på BSA-sammenligning). Niveauet uden effekt var 20 mg/kg/dag (26 gange højere end MRHD baseret på BSA-konvertering). Hos rotter og kaniner forekom embryodødelighed ved orale meloxicamdoser på henholdsvis 1 mg/kg/dag og 5 mg/kg/dag (henholdsvis 0,65- og 6,5 gange større end MRHD baseret på BSA-sammenligning), når det blev administreret gennem hele organogenesen .
Oral administration af meloxicam til gravide rotter under sen drægtighed gennem laktation øgede forekomsten af dystoci, forsinket fødsel og nedsatte afkoms overlevelse ved meloxicamdoser på 0,125 mg/kg/dag eller mere (0,08 gange MRHD baseret på BSA-sammenligning).
Amning
Risikooversigt
Der er ingen humane data tilgængelige om, hvorvidt meloxicam er til stede i modermælk, eller om virkningen på ammede spædbørn eller på mælkeproduktionen. De udviklingsmæssige og sundhedsmæssige fordele ved amning bør overvejes sammen med moderens kliniske behov for MOBIC og eventuelle negative virkninger på det ammede spædbarn fra MOBIC 15 mg eller fra den underliggende moderens tilstand.
Data
Dyredata
Meloxicam var til stede i mælken hos diegivende rotter i koncentrationer, der var højere end i plasma.
Hunner og mænd med reproduktionspotentiale
Infertilitet
Kvinder
Baseret på virkningsmekanismen kan brugen af prostaglandin-medierede NSAID'er, inklusive MOBIC, forsinke eller forhindre brud på ovariefollikler, hvilket er blevet forbundet med reversibel infertilitet hos nogle kvinder. Publicerede dyreforsøg har vist, at administration af prostaglandinsyntesehæmmere har potentialet til at forstyrre prostaglandin-medieret follikulær ruptur, der er nødvendig for ægløsning. Små undersøgelser af kvinder behandlet med NSAID'er har også vist en reversibel forsinkelse i ægløsning. Overvej seponering af NSAID'er, inklusive MOBIC, hos kvinder, der har svært ved at blive gravide, eller som er under undersøgelse af infertilitet.
Pædiatrisk brug
Sikkerheden og effektiviteten af meloxicam hos pædiatriske JRA-patienter fra 2 til 17 år er blevet evalueret i tre kliniske forsøg [se DOSERING OG ADMINISTRATION , BIVIRKNINGER og Kliniske Studier ].
Geriatrisk brug
Ældre patienter, sammenlignet med yngre patienter, har større risiko for NSAID-associerede alvorlige kardiovaskulære, gastrointestinale og/eller renale bivirkninger. Hvis den forventede fordel for den ældre patient opvejer disse potentielle risici, skal du begynde at dosere i den lave ende af doseringsområdet og overvåge patienterne for bivirkninger [se ADVARSLER OG FORHOLDSREGLER ].
Nedsat leverfunktion
Dosisjustering er ikke nødvendig hos patienter med let til moderat nedsat leverfunktion. Patienter med svært nedsat leverfunktion er ikke blevet tilstrækkeligt undersøgt. Da meloxicam metaboliseres betydeligt i leveren, og der kan forekomme levertoksicitet, skal meloxicam anvendes med forsigtighed til patienter med nedsat leverfunktion [se ADVARSLER OG FORHOLDSREGLER og KLINISK FARMAKOLOGI ].
Nedsat nyrefunktion
Dosisjustering er ikke nødvendig hos patienter med let til moderat nedsat nyrefunktion. Patienter med svært nedsat nyrefunktion er ikke blevet undersøgt. Anvendelse af MOBIC 7,5 mg til forsøgspersoner med svært nedsat nyrefunktion anbefales ikke. Hos patienter i hæmodialyse bør meloxicam ikke overstige 7,5 mg dagligt. Meloxicam kan ikke dialyseres [se DOSERING OG ADMINISTRATION og KLINISK FARMAKOLOGI ].
OVERDOSIS
Symptomer efter akutte NSAID-overdoseringer har typisk været begrænset til sløvhed, døsighed, kvalme, opkastning og epigastriske smerter, som generelt har været reversible med støttende behandling. Der er opstået gastrointestinal blødning. Hypertension, akut nyresvigt, respirationsdepression og koma er forekommet, men var sjældne [se ADVARSLER OG FORHOLDSREGLER ].
Håndter patienter med symptomatisk og understøttende behandling efter en NSAID-overdosering. Der er ingen specifikke modgifte. Overvej emeser og/eller aktivt kul (60 til 100 gram hos voksne, 1 til 2 gram pr. kg kropsvægt hos pædiatriske patienter) og/eller osmotisk katarsis hos symptomatiske patienter, der ses inden for fire timer efter indtagelse eller hos patienter med en stor overdosering ( 5 til 10 gange den anbefalede dosis). Tvungen diurese, alkalinisering af urin, hæmodialyse eller hemoperfusion er muligvis ikke nyttige på grund af høj proteinbinding.
Der er begrænset erfaring med overdosering af meloxicam. Kolestyramin er kendt for at fremskynde clearance af meloxicam. Accelereret fjernelse af meloxicam med 4 g orale doser cholestyramin givet tre gange dagligt blev påvist i et klinisk forsøg. Administration af kolestyramin kan være nyttig efter en overdosering.
For yderligere information om overdoseringsbehandling, ring til et giftkontrolcenter (1-800-222-1222).
KONTRAINDIKATIONER
MOBIC 15mg er kontraindiceret til følgende patienter:
- Kendt overfølsomhed (f.eks. anafylaktiske reaktioner og alvorlige hudreaktioner) over for meloxicam eller andre komponenter i lægemidlet [se ADVARSLER OG FORHOLDSREGLER ]
- Anamnese med astma, nældefeber eller andre allergiske reaktioner efter indtagelse af aspirin eller andre NSAID'er. Alvorlige, nogle gange fatale, anafylaktiske reaktioner på NSAID'er er blevet rapporteret hos sådanne patienter [se ADVARSLER OG FORHOLDSREGLER ]
- I forbindelse med koronar bypass-operation (CABG) [se ADVARSLER OG FORHOLDSREGLER ]
KLINISK FARMAKOLOGI
Handlingsmekanisme
Meloxicam har smertestillende, anti-inflammatoriske og antipyretiske egenskaber.
Virkningsmekanismen for MOBIC, ligesom andre NSAID'er, er ikke fuldstændigt forstået, men involverer hæmning af cyclooxygenase (COX-1 og COX-2).
Meloxicam er en potent hæmmer af prostaglandinsyntese in vitro. Meloxicam-koncentrationer opnået under behandlingen har fremkaldt in vivo-effekter. Prostaglandiner sensibiliserer afferente nerver og forstærker virkningen af bradykinin til at inducere smerte i dyremodeller. Prostaglandiner er mediatorer af inflammation. Da meloxicam er en hæmmer af prostaglandinsyntese, kan dets virkningsmåde skyldes et fald i prostaglandiner i perifere væv.
Farmakokinetik
Absorption
Den absolutte biotilgængelighed af meloxicamkapsler var 89 % efter en enkelt oral dosis på 30 mg sammenlignet med 30 mg IV bolusinjektion. Efter enkelte intravenøse doser blev dosisproportional farmakokinetik vist i området fra 5 mg til 60 mg. Efter flere orale doser var farmakokinetikken af meloxicamkapsler dosisproportional over intervallet 7,5 mg til 15 mg. Gennemsnitlig C blev opnået inden for fire til fem timer efter, at en 7,5 mg meloxicam-tablet blev taget under fastende forhold, hvilket indikerer en forlænget lægemiddelabsorption. Ved multiple doseringer blev steady-state-koncentrationer nået på dag 5. En anden meloxicam-koncentrationstoppe forekommer omkring 12 til 14 timer efter dosis, hvilket tyder på recirkulering af galde.
Meloxicam oral suspensionsdoser på 7,5 mg/5 ml og 15 mg/10 ml har vist sig at være bioækvivalente med henholdsvis meloxicam 7,5 mg og 15 mg kapsler. Meloxicam kapsler har vist sig at være bioækvivalente med MOBIC 7,5 mg tabletter.
Mad og syreneutraliserende virkninger
Administration af meloxicamkapsler efter en morgenmad med højt fedtindhold (75 g fedt) resulterede i, at de gennemsnitlige maksimale lægemiddelniveauer (dvs. Cmax) blev øget med ca. 22 %, mens absorptionsgraden (AUC) var uændret. Tiden til maksimal koncentration (Tmax) blev opnået mellem 5 og 6 timer. Til sammenligning blev hverken AUC- eller Cmax-værdierne for meloxicamsuspension påvirket efter et tilsvarende fedtrigt måltid, mens gennemsnitlige Tmax-værdier blev øget til ca. 7 timer. Der blev ikke påvist nogen farmakokinetisk interaktion ved samtidig administration af antacida. Baseret på disse resultater kan MOBIC 15 mg administreres uden hensyntagen til timing af måltider eller samtidig administration af antacida.
Fordeling
Det gennemsnitlige distributionsvolumen (Vss) af meloxicam er ca. 10 l. Meloxicam er ~99,4% bundet til humane plasmaproteiner (primært albumin) inden for det terapeutiske dosisområde. Fraktionen af proteinbinding er uafhængig af lægemiddelkoncentration over det klinisk relevante koncentrationsområde, men falder til ~99% hos patienter med nyresygdom. Meloxicam penetration i humane røde blodlegemer efter oral dosering er mindre end 10 %. Efter en radioaktivt mærket dosis var over 90 % af radioaktiviteten påvist i plasma til stede som uændret meloxicam.
Meloxicamkoncentrationer i ledvæske varierer efter en enkelt oral dosis fra 40 % til 50 % af koncentrationerne i plasma. Den frie fraktion i ledvæske er 2,5 gange højere end i plasma på grund af det lavere albuminindhold i ledvæske sammenlignet med plasma. Betydningen af denne penetration er ukendt.
Elimination
Metabolisme
Meloxicam metaboliseres i vid udstrækning i leveren. Meloxicammetabolitter omfatter 5'-carboxymeloxicam (60 % af dosis), fra P-450-medieret metabolisme dannet ved oxidation af en mellemmetabolit 5'-hydroxymethylmeloxicam, som også udskilles i mindre grad (9 % af dosis) ). In vitro undersøgelser indikerer, at CYP2C9 (cytochrom P450 metaboliserende enzym) spiller en vigtig rolle i denne metaboliske vej med et mindre bidrag fra CYP3A4 isozymet. Patienternes peroxidaseaktivitet er sandsynligvis ansvarlig for de to andre metabolitter, som tegner sig for henholdsvis 16 % og 4 % af den administrerede dosis. Alle fire metabolitter vides ikke at have nogen in vivo farmakologisk aktivitet.
Udskillelse
Udskillelse af meloxicam sker overvejende i form af metabolitter og sker i samme grad i urin og afføring. Kun spor af den uændrede moderforbindelse udskilles i urinen (0,2%) og fæces (1,6%). Omfanget af urinudskillelsen blev bekræftet for umærkede multiple 7,5 mg doser: 0,5 %, 6 % og 13 % af dosis blev fundet i urinen i form af meloxicam, og 5'-hydroxymethyl og 5' -carboxy metabolitter, henholdsvis. Der er betydelig galde- og/eller enteral sekretion af lægemidlet. Dette blev påvist, når oral administration af cholestyramin efter en enkelt IV-dosis af meloxicam reducerede AUC for meloxicam med 50 %.
Den gennemsnitlige eliminationshalveringstid (t1/2) varierer fra 15 timer til 20 timer. Eliminationshalveringstiden er konstant på tværs af dosisniveauer, hvilket indikerer lineær metabolisme inden for det terapeutiske dosisområde. Plasmaclearance varierer fra 7 til 9 ml/min.
Specifikke populationer
Pædiatrisk
Efter indgivelse af en enkelt (0,25 mg/kg) dosis og efter opnåelse af steady state (0,375 mg/kg/dag) var der en generel tendens til ca. 30 % lavere eksponering hos yngre patienter (2 til 6 år) sammenlignet med de ældre. patienter (7 til 16 år). De ældre patienter havde meloxicameksponeringer svarende til (enkeltdosis) eller let reduceret (steady state) som hos voksne patienter, når de brugte AUC-værdier normaliseret til en dosis på 0,25 mg/kg [se DOSERING OG ADMINISTRATION ]. Den gennemsnitlige (SD) eliminationshalveringstid for meloxicam var 15,2 (10,1) og 13,0 timer (3,0) for henholdsvis 2-6-årige patienter og 7-16-årige patienter.
I en kovariat analyse var anvendelse af populationsfarmakokinetik kropsvægt, men ikke alder, den enkelte forudsigende kovariat for forskelle i meloxicams tilsyneladende orale plasmaclearance. De kropsvægtnormaliserede tilsyneladende orale clearance-værdier var tilstrækkelige forudsigere for meloxicameksponering hos pædiatriske patienter.
Farmakokinetikken af MOBIC hos pædiatriske patienter under 2 år er ikke blevet undersøgt.
Geriatrisk
Ældre mænd (≥65 år) udviste meloxicam-plasmakoncentrationer og steady-state farmakokinetik svarende til unge mænd. Ældre kvinder (≥65 år) havde en 47 % højere AUCss og 32 % højere Cmax,ss sammenlignet med yngre kvinder (≤55 år) efter normalisering af kropsvægt. På trods af de øgede samlede koncentrationer hos ældre kvinder var bivirkningsprofilen sammenlignelig for begge ældre patientpopulationer. En mindre fri fraktion blev fundet hos ældre kvindelige patienter sammenlignet med ældre mandlige patienter.
Køn
Unge hunner udviste lidt lavere plasmakoncentrationer i forhold til unge hanner. Efter enkeltdoser på 7,5 mg MOBIC var den gennemsnitlige eliminationshalveringstid 19,5 timer for den kvindelige gruppe sammenlignet med 23,4 timer for den mandlige gruppe. Ved steady state var dataene ens (17,9 timer mod 21,4 timer). Denne farmakokinetiske forskel på grund af køn er sandsynligvis af ringe klinisk betydning. Der var linearitet i farmakokinetikken og ingen mærkbar forskel i Cmax eller Tmax på tværs af køn.
Nedsat leverfunktion
Efter en enkelt dosis på 15 mg meloxicam var der ingen markant forskel i plasmakoncentrationer hos patienter med let (Child-Pugh Klasse I) eller moderat (Child-Pugh Klasse II) nedsat leverfunktion sammenlignet med raske frivillige. Meloxicams proteinbinding blev ikke påvirket af nedsat leverfunktion. Dosisjustering er ikke nødvendig hos patienter med let til moderat nedsat leverfunktion. Patienter med svært nedsat leverfunktion (Child-Pugh klasse III) er ikke blevet tilstrækkeligt undersøgt [se ADVARSLER OG FORHOLDSREGLER og Brug i specifikke populationer ].
Nedsat nyrefunktion
Meloxicams farmakokinetik er blevet undersøgt hos personer med let og moderat nedsat nyrefunktion. De samlede plasmakoncentrationer af meloxicam faldt, og den totale clearance af meloxicam steg med graden af nedsat nyrefunktion, mens frie AUC-værdier var ens i alle grupper. Den højere meloxicam-clearance hos personer med nedsat nyrefunktion kan skyldes øget andel af ubundet meloxicam, som er tilgængelig for levermetabolisme og efterfølgende udskillelse. Dosisjustering er ikke nødvendig hos patienter med let til moderat nedsat nyrefunktion. Patienter med svært nedsat nyrefunktion er ikke blevet tilstrækkeligt undersøgt. Anvendelse af MOBIC til personer med svært nedsat nyrefunktion anbefales ikke [se DOSERING OG ADMINISTRATION , ADVARSLER OG FORHOLDSREGLER og Brug i specifikke populationer ].
Hæmodialyse
Efter en enkelt dosis meloxicam var de frie Cmax-plasmakoncentrationer højere hos patienter med nyresvigt i kronisk hæmodialyse (1 % fri fraktion) sammenlignet med raske frivillige (0,3 % fri fraktion). Hæmodialyse sænkede ikke den totale lægemiddelkoncentration i plasma; derfor er yderligere doser ikke nødvendige efter hæmodialyse. Meloxicam kan ikke dialyseres [se DOSERING OG ADMINISTRATION og Brug i specifikke populationer ].
Lægemiddelinteraktionsstudier
Aspirin
Når NSAID'er blev administreret sammen med aspirin, blev proteinbindingen af NSAID'er reduceret, selvom clearance af frit NSAID ikke blev ændret. Når MOBIC 15 mg administreres sammen med aspirin (1000 mg tre gange dagligt) til raske frivillige, havde det en tendens til at øge AUC (10%) og C (24%) af meloxicam. Den kliniske betydning af denne interaktion er ikke kendt. Se tabel 3 for klinisk signifikante lægemiddelinteraktioner af NSAID'er med aspirin [se DRUGSINTERAKTIONER ].
Kolestyramin
Forbehandling i fire dage med kolestyramin øgede clearance af meloxicam signifikant med 50 %. Dette resulterede i et fald i t1/2, fra 19,2 timer til 12,5 timer, og en reduktion på 35 % i AUC. Dette tyder på eksistensen af en recirkulationsvej for meloxicam i mave-tarmkanalen. Den kliniske relevans af denne interaktion er ikke fastlagt.
Cimetidin
Samtidig administration af 200 mg cimetidin fire gange dagligt ændrede ikke enkeltdosisfarmakokinetikken for 30 mg meloxicam.
Digoxin
Meloxicam 15 mg én gang dagligt i 7 dage ændrede ikke plasmakoncentrationsprofilen af digoxin efter administration af β-acetyldigoxin i 7 dage ved kliniske doser. In vitro-test fandt ingen proteinbindende lægemiddelinteraktion mellem digoxin og meloxicam.
Lithium
en undersøgelse udført med raske forsøgspersoner blev den gennemsnitlige præ-dosis lithiumkoncentration og AUC øget med 21 % hos forsøgspersoner, der fik lithiumdoser i området fra 804 til 1072 mg to gange dagligt med meloxicam 15 mg dagligt hver dag sammenlignet med forsøgspersoner, der fik lithium alene [se DRUGSINTERAKTIONER ].
Methotrexat
En undersøgelse med 13 patienter med reumatoid arthritis (RA) evaluerede virkningerne af flere doser meloxicam på farmakokinetikken af methotrexat taget en gang om ugen. Meloxicam havde ikke en signifikant effekt på farmakokinetikken af enkeltdoser af methotrexat. In vitro fortrængte methotrexat ikke meloxicam fra dets humane serumbindingssteder [se DRUGSINTERAKTIONER ].
Warfarin
Virkningen af meloxicam på den antikoagulerende virkning af warfarin blev undersøgt hos en gruppe raske forsøgspersoner, der fik daglige doser af warfarin, som producerede en INR (International Normalized Ratio) mellem 1,2 og 1,8. Hos disse forsøgspersoner ændrede meloxicam ikke warfarins farmakokinetik og den gennemsnitlige antikoagulerende effekt af warfarin som bestemt ved protrombintid. Et individ viste dog en stigning i INR fra 1,5 til 2,1. Der bør udvises forsigtighed ved administration af MOBIC 15mg med warfarin, da patienter på warfarin kan opleve ændringer i INR og en øget risiko for blødningskomplikationer, når en ny medicin introduceres [se DRUGSINTERAKTIONER ].
Kliniske Studier
Slidgigt og reumatoid arthritis
Brugen af MOBIC 15 mg til behandling af tegn og symptomer på slidgigt i knæ og hofte blev evalueret i et 12-ugers, dobbeltblindt, kontrolleret forsøg. MOBIC (3,75 mg, 7,5 mg og 15 mg dagligt) blev sammenlignet med placebo. De fire primære endepunkter var investigators globale vurdering, patientens globale vurdering, patientens smertevurdering og total WOMAC-score (et selvadministreret spørgeskema, der omhandler smerte, funktion og stivhed). Patienter på MOBIC 7,5 mg dagligt og MOBIC 15 mg dagligt viste signifikant forbedring i hvert af disse endepunkter sammenlignet med placebo.
Brugen af MOBIC til håndtering af tegn og symptomer på slidgigt blev evalueret i seks dobbeltblindede, aktivt kontrollerede forsøg uden for USA med en varighed på fra 4 uger til 6 måneder. I disse forsøg var effekten af MOBIC, i doser på 7,5 mg/dag og 15 mg/dag, sammenlignelig med piroxicam 20 mg/dag og diclofenac SR 100 mg/dag og i overensstemmelse med den effekt, der blev set i det amerikanske forsøg.
Brugen af MOBIC 7,5 mg til behandling af tegn og symptomer på leddegigt blev evalueret i et 12-ugers, dobbeltblindt, kontrolleret multinationalt forsøg. MOBIC (7,5 mg, 15 mg og 22,5 mg dagligt) blev sammenlignet med placebo. Det primære endepunkt i denne undersøgelse var ACR20-responsraten, et sammensat mål for kliniske, laboratoriemæssige og funktionelle mål for RA-respons. Patienter, der modtog MOBIC 7,5 mg og 15 mg dagligt, viste signifikant forbedring i det primære endepunkt sammenlignet med placebo. Der blev ikke observeret nogen trinvis fordel med en dosis på 22,5 mg sammenlignet med en dosis på 15 mg.
Juvenil Reumatoid Arthritis (JRA) Pauciartikulært og polyartikulært forløb
Anvendelsen af MOBIC 7,5 mg til behandling af tegn og symptomer på pauciartikulært eller polyartikulært Juvenil Reumatoid Arthritis hos patienter på 2 år og ældre blev evalueret i to 12-ugers, dobbeltblindede, parallelarmede, aktivt kontrollerede forsøg .
Begge undersøgelser omfattede tre arme: naproxen og to doser meloxicam. I begge undersøgelser begyndte doseringen af meloxicam ved 0,125 mg/kg/dag (7,5 mg maksimum) eller 0,25 mg/kg/dag (maks. 15 mg), og naproxen-dosering begyndte ved 10 mg/kg/dag. En undersøgelse brugte disse doser gennem hele den 12-ugers doseringsperiode, mens den anden inkorporerede en titrering efter 4 uger til doser på 0,25 mg/kg/dag og 0,375 mg/kg/dag (maksimalt 22,5 mg) meloxicam og 15 mg/kg /dag af naproxen.
Effektanalysen brugte ACR Pediatric 30 responder-definitionen, en sammensætning af forældre- og investigatorvurderinger, tællinger af aktive led og led med begrænset bevægelsesområde og erytrocytsedimentationshastighed. Andelen af respondere var ens i alle tre grupper i begge undersøgelser, og der blev ikke observeret nogen forskel mellem meloxicamdosisgrupperne.
PATIENTOPLYSNINGER
Medicinvejledning til ikke-steroide antiinflammatoriske lægemidler (NSAID'er)
Hvad er den vigtigste information, jeg bør vide om medicin kaldet ikke-steroide antiinflammatoriske lægemidler (NSAID'er)?
NSAID'er kan forårsage alvorlige bivirkninger, herunder:
- Øget risiko for et hjerteanfald eller slagtilfælde, der kan føre til døden. Denne risiko kan opstå tidligt i behandlingen og kan øge:
- med stigende doser af NSAID'er
- ved længere brug af NSAID
Tag ikke NSAID'er lige før eller efter en hjerteoperation kaldet "koronararterie bypassgraft (CABG)."
Undgå at tage NSAID'er efter et nyligt hjerteanfald, medmindre din læge fortæller dig det. Du kan have en øget risiko for endnu et hjerteanfald, hvis du tager NSAID'er efter et nyligt hjerteanfald.
- Øget risiko for blødning, sår og rifter (perforering) af spiserøret (rør der fører fra munden til maven), mave og tarme:
- når som helst under brug
- uden advarselssymptomer
- der kan forårsage død
Risikoen for at få et sår eller blødning øges med:
- tidligere historie med mavesår, eller mave- eller tarmblødninger ved brug af NSAID'er
- tager medicin kaldet "kortikosteroider", "antikoagulantia", "SSRI" eller "SNRI" stigende doser af NSAID'er
- længere brug af NSAID
- rygning
- drikke alkohol
- ældre alder
- dårligt helbred
- fremskreden leversygdom
- blødningsproblemer
NSAID bør kun anvendes:
- præcis som foreskrevet
- ved den lavest mulige dosis til din behandling
- for den kortest nødvendige tid
Hvad er NSAID'er?
NSAID'er bruges til at behandle smerter og rødme, hævelse og varme (betændelse) fra medicinske tilstande såsom forskellige typer gigt, menstruationssmerter og andre typer kortvarige smerter.
Hvem bør ikke tage NSAID'er?
Tag ikke NSAID'er:
- hvis du har haft et astmaanfald, nældefeber eller anden allergisk reaktion med aspirin eller andre NSAID'er.
- lige før eller efter en bypassoperation.
Inden du tager NSAID'er, skal du fortælle din læge om alle dine medicinske tilstande, herunder hvis du:
- har lever- eller nyreproblemer
- har forhøjet blodtryk
- har astma
- er gravid eller planlægger at blive gravid. Hvis du tager NSAID'er omkring 20 uger af graviditeten eller senere, kan det skade dit ufødte barn. Hvis du har brug for at tage NSAID'er i mere end 2 dage, når du er mellem 20 og 30 uger af graviditeten, skal din læge muligvis overvåge mængden af væske i din livmoder omkring din baby. Du bør ikke tage NSAID'er efter omkring 30 ugers graviditet.
- ammer eller planlægger at amme.
Fortæl din sundhedsudbyder om al den medicin, du tager, inklusive receptpligtig eller håndkøbsmedicin, vitaminer eller naturlægemidler. NSAID'er og nogle andre lægemidler kan interagere med hinanden og forårsage alvorlige bivirkninger. Begynd ikke at tage ny medicin uden først at tale med din læge.
Hvad er de mulige bivirkninger af NSAID'er?
NSAID'er kan forårsage alvorlige bivirkninger, herunder:
Se "Hvad er den vigtigste information, jeg bør vide om medicin kaldet ikke-steroide antiinflammatoriske lægemidler (NSAID'er)?"
- nyt eller værre forhøjet blodtryk
- hjertefejl
- leverproblemer inklusive leversvigt
- nyreproblemer, herunder nyresvigt
- lavt antal røde blodlegemer (anæmi)
- livstruende hudreaktioner
- livstruende allergiske reaktioner
Andre bivirkninger af NSAID'er omfatter: mavesmerter, forstoppelse, diarré, gas, halsbrand, kvalme, opkastning og svimmelhed.
Få akut hjælp med det samme, hvis du får nogle af følgende symptomer:
- åndenød eller åndedrætsbesvær
- brystsmerter
- svaghed i en del eller side af din krop
- utydelig tale
- hævelse af ansigt eller hals
Stop med at tage dit NSAID og ring til din læge med det samme, hvis du får nogle af følgende symptomer:
- kvalme
- mere træt eller svagere end normalt
- diarré
- kløe
- din hud eller øjne ser gule ud
- fordøjelsesbesvær eller mavesmerter
- influenzalignende symptomer
- opkast blod
- der er blod i din afføring, eller den er sort og klistret som tjære
- usædvanlig vægtøgning
- hududslæt eller blærer med feber
- hævelse af arme, ben, hænder og fødder
Hvis du tager for meget af dit NSAID, skal du kontakte din læge eller få lægehjælp med det samme.
Disse er ikke alle de mulige bivirkninger af NSAID'er. For mere information, spørg din læge eller apotek om NSAID'er.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Andre oplysninger om NSAID'er:
- Aspirin er et NSAID, men det øger ikke chancen for et hjerteanfald. Aspirin kan forårsage blødninger i hjernen, maven og tarmene. Aspirin kan også forårsage sår i maven og tarmene.
- Nogle NSAID'er sælges i lavere doser uden recept (håndkøb). Tal med din læge, før du bruger NSAID'er i mere end 10 dage.
Generel information om sikker og effektiv brug af NSAID'er
Lægemidler ordineres nogle gange til andre formål end dem, der er anført i en medicinvejledning. Brug ikke NSAID til en tilstand, som det ikke er ordineret til. Giv ikke NSAID til andre mennesker, selvom de har de samme symptomer, som du har. Det kan skade dem.
Hvis du ønsker mere information om NSAID'er, så tal med din læge. Du kan bede din apoteker eller sundhedsplejerske om oplysninger om NSAID'er, der er skrevet til sundhedspersonale.
Denne medicinvejledning er godkendt af US Food and Drug Administration.
