Medicin mod kolesterol: Lipitor 10mg, 20mg, 40mg Atorvastatin Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er Lipitor 40mg, og hvordan bruges det?
Lipitor 10mg er en receptpligtig medicin, der bruges til at sænke blodniveauet af "dårligt" kolesterol (low-density lipoprotein eller LDL), til at øge niveauet af "gode" kolesterol (high-density lipoprotein eller HDL) og til at sænke triglycerider og behandle symptomerne på forhøjet kolesterol (hyperlipidæmi) og for at sænke risikoen for slagtilfælde, hjerteanfald eller andre hjertekomplikationer. Lipitor 40mg kan bruges alene eller sammen med anden medicin.
Lipitor 10mg tilhører en klasse af lægemidler kaldet lipidsænkende midler, statiner, HMG-CoA-reduktasehæmmere.
Det vides ikke, om Lipitor 10mg er sikkert og effektivt til børn under 10 år.
Hvad er de mulige bivirkninger af Lipitor?
Lipitor 10mg kan forårsage alvorlige bivirkninger, herunder:
- smerte eller svie, når du tisser,
- smerter i øvre mave,
- svaghed,
- træthedsfornemmelse,
- mistet appetiten,
- mørk urin,
- gulfarvning af huden eller øjnene (gulsot),
- lidt eller ingen vandladning,
- hævelse i dine fødder eller ankler, og
- forpustet
Få lægehjælp med det samme, hvis du har nogle af symptomerne nævnt ovenfor.
De mest almindelige bivirkninger af Lipitor omfatter:
- ledsmerter,
- tilstoppet næse,
- ondt i halsen,
- diarré, og
- smerter i dine arme eller ben
Fortæl det til lægen, hvis du har en bivirkning, der generer dig, eller som ikke forsvinder.
Disse er ikke alle de mulige bivirkninger af Lipitor. Spørg din læge eller apotek for mere information.
Ring til din læge for lægehjælp om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
BESKRIVELSE
LIPITOR er et syntetisk lipidsænkende middel. Atorvastatin er en hæmmer af 3-hydroxy-3-methylglutaryl-coenzym A (HMG-CoA) reduktase. Dette enzym katalyserer omdannelsen af HMG-CoA til mevalonat, et tidligt andrat-begrænsende trin i kolesterolbiosyntesen.
Atorvastatin calcium er [R-(R*, R*)]-2-(4-fluorphenyl)-β, δ-dihydroxy-5-(1-methylethyl)-3-phenyl-4-[(phenylamino)carbonyl]- 1Hpyrrol-1-heptansyre, calciumsalt (2:1)trihydrat. Den empiriske formel for atorvastatin-calcium er (C33H34FN2O5)2Ca•3H2O og dens molekylvægt er 1209,42. Dens strukturformel er:
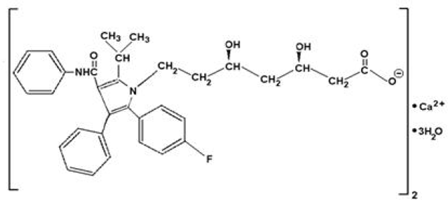
Atorvastatin calcium er et hvidt til råhvidt krystallinsk pulver, der er uopløseligt i vandige opløsninger med pH 4 og derunder. Atorvastatin calcium er meget lidt opløseligt i destilleret vand, pH 7,4 fosfatbuffer og acetonitril; let opløselig i ethanol; og frit opløselig i methanol.
LIPITOR-tabletter til oral administration indeholder 10, 20, 40 eller 80 mg atorvastatin og følgende inaktive ingredienser: calciumcarbonat, USP; candelilla voks,FCC; croscarmellosenatrium, NF; hydroxypropylcellulose, NF; lactosemonohydrat, NF; magnesiumstearat, NF; mikrokrystallinsk cellulose, NF; Opadry White YS-1-7040(hypromellose, polyethylenglycol, talkum, titaniumdioxid); polysorbat 80, NF; simeticonemulsion.
INDIKATIONER
Terapi med lipidændrende midler bør kun være en komponent i multipel risikofaktorintervention hos personer med signifikant øget risiko for aterosklerotisk vaskulær sygdom på grund af hyperkolesterolæmi. Lægemiddelbehandling anbefales som et supplement til diæt, når responsen på en diæt begrænset i mættet fedt og kolesterol og andre ikke-farmakologiske foranstaltninger alene har været utilstrækkelig. Hos patienter med CHD eller flere risikofaktorer for CHD, kan LIPITOR 20 mg startes samtidigt med diæt.
Forebyggelse af hjerte-kar-sygdomme hos voksne
Hos voksne patienter uden klinisk tydelig koronar hjertesygdom, men med flere risikofaktorer for koronar hjertesygdom såsom alder, rygning, hypertension, lavt HDL-C eller en familiehistorie med tidlig koronar hjertesygdom, er LIPITOR 10mg indiceret til:
- Reducer risikoen for myokardieinfarkt
- Reducer risikoen for slagtilfælde
- Reducer risikoen for revaskulariseringsprocedurer og angina
Hos voksne patienter med type 2-diabetes og uden klinisk tydelig koronar hjertesygdom, men med flere risikofaktorer for koronar hjertesygdom såsom retinopati, albuminuri, rygning eller hypertension, er LIPITOR indiceret til:
- Reducer risikoen for myokardieinfarkt
- Reducer risikoen for slagtilfælde
Hos voksne patienter med klinisk tydelig koronar hjertesygdom er LIPITOR 20 mg indiceret til:
- Reducer risikoen for ikke-dødelig myokardieinfarkt
- Reducer risikoen for fatalt og ikke-dødeligt slagtilfælde
- Reducer risikoen for revaskulariseringsprocedurer
- Reducer risikoen for hospitalsindlæggelse for CHF
- Reducer risikoen for angina
Hyperlipidæmi
LIPITOR 20mg er indiceret:
- Som et supplement til diæt for at reducere forhøjede total-C, LDL-C, apo B og TG niveauer og for at øge HDL-C hos voksne patienter med primær hyperkolesterolæmi (heterozygot familiær og ikke-familiær) og blandet dyslipidæmi (Fredrickson Type IIa og IIb) ;
- Som et supplement til diæt til behandling af voksne patienter med forhøjede serum-TG-niveauer (Fredrickson Type IV);
- Til behandling af voksne patienter med primær dysbetalipoproteinæmi (Fredrickson Type III), som ikke reagerer tilstrækkeligt på kosten;
- At reducere total-C og LDL-C hos patienter med homozygot familiær hyperkolesterolæmi (HoFH) som et supplement til andre lipidsænkende behandlinger (f.eks. LDL-aferese), eller hvis sådanne behandlinger ikke er tilgængelige;
- Som et supplement til diæt for at reducere total-C, LDL-C og apo B-niveauer hos pædiatriske patienter i alderen 10 år til 17 år med heterozygot familiær hyperkolesterolæmi (HeFH), hvis følgende resultater er efter et tilstrækkeligt forsøg med diætterapi. til stede:
- der er en positiv familiehistorie med for tidlig hjertekarsygdom eller
- to eller flere andre CVD-risikofaktorer er til stede hos den pædiatriske patient
Brugsbegrænsninger
LIPITOR 40mg er ikke blevet undersøgt under tilstande, hvor den største lipoproteinabnormitet er forhøjelse af chylomikroner (Fredrickson Type I og V).
DOSERING OG ADMINISTRATION
Hyperlipidæmi og blandet dyslipidæmi
Den anbefalede startdosis af LIPITOR 10 mg er 10 eller 20 mg én gang dagligt. Patienter, som kræver en stor reduktion af LDL-C (mere end 45%), kan startes med 40 mg én gang dagligt. Dosisområdet for LIPITOR er 10 til 80 mg én gang dagligt. LIPITOR 10 mg kan administreres som en enkelt dosis på ethvert tidspunkt af dagen, med eller uden mad. Startdosis og vedligeholdelsesdoser af LIPITOR bør individualiseres i henhold til patientkarakteristika, såsom mål for behandlingen og respons. Efter initiering og/eller efter titrering af LIPITOR 10 mg, bør lipidniveauer analyseres inden for 2 til 4 uger og dosis justeres i overensstemmelse hermed.
Heterozygot familiær hyperkolesterolæmi hos pædiatriske patienter (10 år til 17 år)
Den anbefalede startdosis af LIPITOR 10 mg er 10 mg/dag; det sædvanlige dosisområde er 10 til 20 mg oralt én gang dagligt [se Kliniske Studier ]. Doser bør individualiseres i henhold til det anbefalede mål for behandlingen [se INDIKATIONER OG BRUG og KLINISK FARMAKOLOGI ]. Justeringer bør foretages med intervaller på 4 uger eller mere.
Homozygot familiær hyperkolesterolæmi
Doseringen af LIPITOR 20 mg til patienter med HoFH er 10 til 80 mg dagligt. LIPITOR 20 mg bør anvendes som et supplement til andre lipidsænkende behandlinger (f.eks. LDL-aferese) hos disse patienter, eller hvis sådanne behandlinger ikke er tilgængelige.
Samtidig lipidsænkende terapi
LIPITOR 20mg kan bruges sammen med galdesyreharpikser. Kombinationen af HMG-CoA-reduktasehæmmere (statiner) og fibrater bør generelt anvendes med forsigtighed [se ADVARSLER OG FORHOLDSREGLER og DRUGSINTERAKTIONER ].
Dosering hos patienter med nedsat nyrefunktion
Nyresygdom påvirker ikke plasmakoncentrationerne eller LDL-C-reduktionen af LIPITOR; Dosisjustering hos patienter med nedsat nyrefunktion er derfor ikke nødvendig [se ADVARSLER OG FORHOLDSREGLER og KLINISK FARMAKOLOGI ].
Dosering hos patienter, der tager Cyclosporin, Clarithromycin, Itraconazol, Letermovir eller visse proteasehæmmere
Hos patienter, der tager ciclosporin eller HIV-proteasehæmmeren tipranavir plus ritonavir eller hepatitis C-virus (HCV) proteasehæmmeren glecaprevir plus pibrentasvir eller letermovir, når de administreres sammen med ciclosporin, bør behandling med LIPITOR 40 mg undgås. Hos patienter med HIV, der tager lopinavir plus ritonavir, skal du bruge den laveste nødvendige dosis af LIPITOR. Hos patienter, der tager clarithromycin, itraconazol, elbasvir plus grazoprevir, eller hos patienter med HIV, der tager en kombination af saquinavir plus ritonavir, darunavir plus ritonavir, fosamprenavir, fosamprenavir plus ritonavir eller letermovir, bør behandling med LIPITOR begrænses til 20 mg, og passende klinisk vurdering er anbefales for at sikre, at den laveste nødvendige dosis af LIPITOR 20mg anvendes. Hos patienter, der tager HIV-proteasehæmmeren, bør nelfinavir-behandling med LIPITOR 10 mg begrænses til 40 mg [se ADVARSLER OG FORHOLDSREGLER og DRUGSINTERAKTIONER ].
HVORDAN LEVERET
Doseringsformer og styrker
LIPITOR tabletter er hvide elliptiske, filmovertrukne og fås i fire styrker (se tabel 1).
Opbevaring og håndtering
10 mg tabletter (10 mg atorvastatin): kodet "PD 155" på den ene side og "10" på den anden side.
NDC 0071-0155-23 flasker á 90 NDC 0071-0155-40 10 x 10 enhedsdosisblister
20 mg tabletter (20 mg atorvastatin): kodet "PD 156" på den ene side og "20" på den anden side.
NDC 0071-0156-23 flasker á 90 stk NDC 0071-0156-40 10 x 10 enhedsdosisblister
40 mg tabletter (40 mg atorvastatin): kodet "PD 157" på den ene side og "40" på den anden.
NDC 0071-0157-23 flasker á 90 stk NDC 0071-0157-40 10 x 10 enhedsdosisblister
80 mg tabletter (80 mg atorvastatin): kodet "PD 158" på den ene side og "80" på den anden side.
NDC 0071-0158-23 flasker á 90 stk NDC 0071-0158-73 flasker á 500 NDC 0071-0158-92 8 x 8 enhedsdosisblister
Opbevaring
Opbevares ved kontrolleret stuetemperatur 20 – 25°C (68 – 77°F) [se USP].
Distribueret af: Parke-Davis, Division of Pfizer Inc., NY, NY 10017. Revideret: Aug 2021
BIVIRKNINGER
Følgende alvorlige bivirkninger er beskrevet mere detaljeret i andre sektioner af etiketten:
- Myopati og rabdomyolyse [se ADVARSLER OG FORHOLDSREGLER ]
- Leverenzymabnormiteter [se ADVARSLER OG FORHOLDSREGLER ]
Erfaring med kliniske forsøg
Fordi kliniske forsøg udføres under vidt forskellige forhold, kan de bivirkninger, der er observeret i de kliniske forsøg med et lægemiddel, ikke direkte sammenlignes med hastigheder i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de hastigheder, der observeres i praksis.
LIPITORs placebokontrollerede kliniske forsøgsdatabase med 16.066 patienter (8755 LIPITOR vs. 7311 placebo; aldersgruppe 10-93 år, 39 % kvinder, 91 % kaukasiere, 3 % sorte, 2 % asiater, 4 % andre) med en median behandlingsvarighed på 53 uger, 9,7 % af patienterne på LIPITOR 10 mg og 9,5 % af patienterne på placebo seponerede på grund af bivirkninger uanset årsagssammenhæng. De fem mest almindelige bivirkninger hos patienter behandlet med LIPITOR 20 mg, som førte til afbrydelse af behandlingen og forekom med en højere hastighed end placebo, var: myalgi (0,7 %), diarré (0,5 %), kvalme (0,4 %), stigning i alaninaminotransferase (0,4 %). %) og hepatisk enzymstigning (0,4 %).
De hyppigst rapporterede bivirkninger (incidens ≥ 2 % og større end placebo) uanset årsagssammenhæng hos patienter behandlet med LIPITOR i placebokontrollerede forsøg (n=8755) var: nasopharyngitis (8,3 %), artralgi (6,9 %), diarré ( 6,8 %), smerter i ekstremiteter (6,0 %) og urinvejsinfektion (5,7 %).
Tabel 2 opsummerer hyppigheden af kliniske bivirkninger, uanset årsagssammenhæng, rapporteret i ≥ 2 % og med en højere frekvens end placebo hos patienter behandlet med LIPITOR (n=8755), fra sytten placebokontrollerede forsøg.
Andre bivirkninger rapporteret i placebokontrollerede undersøgelser omfatter:
Kroppen som helhed: utilpashed, pyreksi; Fordøjelsessystemet: abdominal ubehag, udbrud, flatulens, hepatitis, kolestase; Muskuloskeletale system: muskuloskeletale smerter, muskeltræthed, nakkesmerter, ledhævelse; Metabolisk og ernæringssystem: stigning i transaminaser, unormal leverfunktionstest, stigning i alkalisk phosphatase i blodet, stigning i kreatinfosphokinase, hyperglykæmi; Nervesystem: mareridt; Åndedrætsorganerne: epistaxis; Hud og vedhæng: nældefeber; Særlige sanser: sløret syn, tinnitus; Urogenital system: hvide blodlegemer urin positiv.
Anglo-Scandinavian Cardiac Outcomes Trial (ASCOT)
I ASCOT [se Kliniske Studier involverer 10.305 deltagere (aldersinterval 40-80 år, 19 % kvinder; 94,6 % kaukasiere, 2,6 % afrikanere, 1,5 % sydasiater, 1,3 % blandet/andet) behandlet med LIPITOR 10 mg dagligt (n=5.168) eller placebo (n) =5.137), var sikkerheds- og tolerabilitetsprofilen for gruppen behandlet med LIPITOR 10 mg sammenlignelig med den for gruppen behandlet med placebo under en median på 3,3 års opfølgning.
Collaborative Atorvastatin Diabetes Study (CARDS)
I KORT [se Kliniske Studier ] involverer 2.838 forsøgspersoner (aldersinterval 39-77 år, 32 % kvinder; 94,3 % kaukasiere, 2,4 % sydasiater, 2,3 % afro-caribien, 1,0 % andet) med type 2-diabetes behandlet med LIPITOR 10 mg dagligt (n=1.428) eller placebo (n=1.410), var der ingen forskel i den samlede hyppighed af bivirkninger eller alvorlige bivirkninger mellem behandlingsgrupperne under en median opfølgning på 3,9 år. Ingen tilfælde af rabdomyolyse blev rapporteret.
Treating To New Targets Study (TNT)
I TNT [se Kliniske Studier involverer 10.001 forsøgspersoner (aldersinterval 29-78 år, 19 % kvinder; 94,1 % kaukasiere, 2,9 % sorte, 1,0 % asiater, 2,0 % andre) med klinisk tydelig CHD behandlet med LIPITOR 10 mg dagligt (n=5006) eller LIPITOR mg dagligt (n=4995), var der flere alvorlige bivirkninger og seponeringer på grund af bivirkninger i højdosis atorvastatin-gruppen (henholdsvis 92, 1,8 %; 497, 9,9 %) sammenlignet med lavdosis-gruppen (69 1,4 %, henholdsvis 404, 8,1 %) under en medianopfølgning på 4,9 år. Vedvarende transaminasestigninger (≥3 x ULN to gange inden for 4-10 dage) forekom hos 62 (1,3 %) individer med atorvastatin 80 mg og hos ni (0,2 %) individer med atorvastatin 10 mg. Forhøjelser af CK (≥ 10 x ULN) var generelt lave, men var højere i gruppen med højdosis atorvastatin (13, 0,3 %) sammenlignet med lavdosis atorvastatin-gruppen (6, 0,1 %).
Inkrementelt fald i endepunkter gennem aggressiv lipidsænkende undersøgelse (IDEAL)
I IDEAL [se Kliniske Studier involverer 8.888 forsøgspersoner (aldersinterval 26-80 år, 19 % kvinder; 99,3 % kaukasiere, 0,4 % asiater, 0,3 % sorte, 0,04 % andre) behandlet med LIPITOR 80 mg/dag (n=4439) eller simvastatin 20-40 mg dagligt (n=4449), var der ingen forskel i den samlede hyppighed af bivirkninger eller alvorlige bivirkninger mellem behandlingsgrupperne under en median opfølgning på 4,8 år.
Forebyggelse af slagtilfælde ved aggressiv reduktion af kolesterolniveauer (SPARCL)
SPARCL, der involverede 4731 forsøgspersoner (aldersinterval 21-92 år, 40 % kvinder; 93,3 % kaukasiere, 3,0 % sorte, 0,6 % asiater, 3,1 % andre) uden klinisk tydelig CHD, men med et slagtilfælde eller forbigående iskæmisk anfald (TIA) inden for tidligere 6 måneder behandlet med LIPITOR 80 mg (n=2365) eller placebo (n=2366) i en median opfølgning på 4,9 år, var der en højere forekomst af vedvarende levertransaminasestigninger (≥ 3 x ULN to gange inden for 4-10 måneder) dage) i atorvastatingruppen (0,9 %) sammenlignet med placebo (0,1 %). Forhøjelser af CK (>10 x ULN) var sjældne, men var højere i atorvastatingruppen (0,1 %) sammenlignet med placebo (0,0 %). Diabetes blev rapporteret som en bivirkning hos 144 forsøgspersoner (6,1 %) i atorvastatingruppen og 89 forsøgspersoner (3,8 %) i placebogruppen [se ADVARSLER OG FORHOLDSREGLER ].
en post-hoc analyse reducerede LIPITOR 80 mg forekomsten af iskæmisk slagtilfælde (218/2365, 9,2% vs. 274/2366, 11,6%) og øgede forekomsten af hæmoragisk slagtilfælde (55/2365, 2,3% vs. 33/) 2366, 1,4%) sammenlignet med placebo. Hyppigheden af fatalt hæmoragisk slagtilfælde var ens mellem grupperne (17 LIPITOR 40 mg vs. 18 placebo). Forekomsten af ikke-dødelige hæmoragiske slagtilfælde var signifikant større i atorvastatin-gruppen (38 ikke-dødelige hæmoragiske slagtilfælde) sammenlignet med placebogruppen (16 ikke-dødelige hæmoragiske slagtilfælde). Forsøgspersoner, der deltog i undersøgelsen med et hæmoragisk slagtilfælde, så ud til at have øget risiko for hæmoragisk slagtilfælde [7 (16 %) LIPITOR vs. 2 (4 %) placebo].
Der var ingen signifikante forskelle mellem behandlingsgrupperne for dødelighed af alle årsager: 216 (9,1 %) i LIPITOR 80 mg/dag-gruppen mod 211 (8,9 %) i placebogruppen. Andelene af forsøgspersoner, der oplevede kardiovaskulær død, var numerisk mindre i LIPITOR 80 mg-gruppen (3,3 %) end i placebo-gruppen (4,1 %). Andelene af forsøgspersoner, der oplevede ikke-kardiovaskulær død, var numerisk større i LIPITOR 80 mg-gruppen (5,0 %) end i placebo-gruppen (4,0 %).
Bivirkninger fra kliniske undersøgelser af LIPITOR 20mg hos pædiatriske patienter
I en 26-ugers kontrolleret undersøgelse af drenge og postmenarkalske piger med HeFH (i alderen 10 år til 17 år) (n=140, 31 % kvinder; 92 % kaukasiere, 1,6 % sorte, 1,6 % asiater, 4,8 % andre) og tolerabilitetsprofilen for LIPITOR 10 til 20 mg dagligt, som et supplement til diæt for at reducere totalt kolesterol, LDL-C og apo B-niveauer, svarede generelt til placebo [se Brug i særlige populationer og Kliniske Studier ].
Postmarketing oplevelse
Følgende bivirkninger er blevet identificeret under brug af LIPITOR efter godkendelse. Fordi disse reaktioner rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt pålideligt at estimere deres hyppighed eller etablere en årsagssammenhæng til lægemiddeleksponering.
Bivirkninger forbundet med LIPITOR-behandling rapporteret siden markedsintroduktionen, som ikke er anført ovenfor, uanset årsagsvurdering, omfatter følgende: anafylaksi, angioneurotisk ødem, bulløst udslæt (herunder erythema multiforme, Stevens-Johnsons syndrom og toksisk epidermal nekroyolyse), rhabdomomisk nekroyolyse , myositis, træthed, seneruptur, fatalt og ikke-fatalt leversvigt, svimmelhed, depression, perifer neuropati, pancreatitis og interstitiel lungesygdom.
Der har været sjældne rapporter om immunmedieret nekrotiserende myopati forbundet med statinbrug [se ADVARSLER OG FORHOLDSREGLER ].
Der har været sjældne postmarketingrapporter om kognitiv svækkelse (f.eks. hukommelsestab, glemsomhed, hukommelsestab, hukommelsessvækkelse, forvirring) forbundet med statinbrug. Disse kognitive problemer er blevet rapporteret for alle statiner. Indberetningerne er generelt ikke-seriøse og reversible ved seponering af statin med varierende tidspunkter til symptomdebut (1 dag til år) og symptomopløsning (median på 3 uger).
DRUGSINTERAKTIONER
Lægemiddelinteraktioner, der kan øge risikoen for myopati og rabdomyolyse med LIPITOR
LIPITOR er et substrat for CYP3A4 og transportører (f.eks. OATP1B1/1B3, P-gp eller BCRP). LIPITOR-plasmaniveauer kan øges signifikant ved samtidig administration af CYP3A4-hæmmere og transportører. Tabel 3 indeholder en liste over lægemidler, der kan øge eksponeringen for Lipitor og kan øge risikoen for myopati og rhabdomyolyse, når de bruges samtidig, og instruktioner til at forebygge eller håndtere dem [se ADVARSLER OG FORHOLDSREGLER og KLINISK FARMAKOLOGI ].
Lægemiddelinteraktioner, der kan mindske eksponeringen for LIPITOR
Tabel 4 viser lægemiddelinteraktioner, der kan reducere eksponeringen for LIPITOR 20 mg, og instruktioner til at forebygge eller håndtere dem.
LIPITOR 20mg Virkninger på andre stoffer
Tabel 5 viser LIPITORs effekt på andre lægemidler og instruktioner til at forebygge eller håndtere dem.
ADVARSLER
Inkluderet som en del af FORHOLDSREGLER afsnit.
FORHOLDSREGLER
Myopati og rabdomyolyse
LIPITOR 10 mg kan forårsage myopati (muskelsmerter, ømhed eller svaghed med kreatinkinase (CK) over ti gange den øvre grænse for normalen) og rabdomyolyse (med eller uden akut nyresvigt sekundært til myoglobinuri). Sjældne dødsfald er opstået som følge af rabdomyolyse med statinbrug, inklusive LIPITOR.
Risikofaktorer for myopati
Risikofaktorer for myopati omfatter alder 65 år eller derover, ukontrolleret hypothyroidisme, nedsat nyrefunktion, samtidig brug med visse andre lægemidler og højere LIPITOR-dosis [se DRUGSINTERAKTIONER ].
Trin til at forebygge eller reducere risikoen for myopati og rabdomyolyse
LIPITOR-eksponering kan øges af lægemiddelinteraktioner på grund af hæmning af cytochrom P450-enzym 3A4 (CYP3A4) og/eller transportører (f.eks. brystkræftresistent protein [BCRP], organisk aniontransporterende polypeptid [OATP1B1/OATP1B3] og P-glycoprotein [P] -gp]), hvilket resulterer i en øget risiko for myopati og rabdomyolyse. Samtidig brug af cyclosporin, gemfibrozil, tipranavir plus ritonavir eller glecaprevir plus pibrentasvir med LIPITOR anbefales ikke. LIPITOR 40 mg dosisændringer anbefales til patienter, der tager visse antivirale, azol-svampemidler eller makrolidantibiotika [se DOSERING OG ADMINISTRATION ]. Tilfælde af myopati/rhabdomyolyse er blevet rapporteret med atorvastatin givet sammen med lipidmodificerende doser (>1 gram/dag) af niacin, fibrater, colchicin og ledipasvir plus sofosbuvir. Overvej om fordelene ved brug af disse produkter opvejer den øgede risiko for myopati og rhabdomyolyse [se DRUGSINTERAKTIONER ].
Samtidig indtagelse af store mængder, mere end 1,2 liter dagligt, grapefrugtjuice anbefales ikke til patienter, der tager LIPITOR [se DRUGSINTERAKTIONER ].
Seponer LIPITOR, hvis der opstår markant forhøjede CK-niveauer, eller der er diagnosticeret eller mistanke om myopati. Muskelsymptomer og CK-stigninger kan forsvinde, hvis LIPITOR seponeres. Seponer midlertidigt LIPITOR 40 mg hos patienter, der oplever en akut eller alvorlig tilstand med høj risiko for at udvikle nyresvigt sekundært til rhabdomyolyse (f.eks. sepsis; shock; svær hypovolæmi; større operation; traumer; svære metaboliske, endokrine eller elektrolytforstyrrelser; eller ukontrolleret epilepsi) .
Informer patienterne om risikoen for myopati og rabdomyolyse, når du starter eller øger LIPITOR-doseringen. Instruer patienterne i omgående at rapportere enhver uforklarlig muskelsmerte, ømhed eller svaghed, især hvis de ledsages af utilpashed eller feber.
Immun-medieret nekrotiserende myopati
Der har været sjældne rapporter om immunmedieret nekrotiserende myopati (IMNM), en autoimmun myopati, forbundet med statinbrug. IMNM er karakteriseret ved: proksimal muskelsvaghed og forhøjet serumkreatinkinase, som fortsætter på trods af seponering af statinbehandling; positivt anti-HMG CoA-reduktase-antistof; muskelbiopsi, der viser nekrotiserende myopati; og forbedring med immunsuppressive midler. Yderligere neuromuskulær og serologisk test kan være nødvendig. Behandling med immunsuppressive midler kan være nødvendig. Overvej nøje risikoen for IMNM før påbegyndelse af et andet statin. Hvis behandlingen påbegyndes med et andet statin, skal du overvåge for tegn og symptomer på IMNM.
Leverdysfunktion
Statiner er ligesom nogle andre lipidsænkende behandlinger blevet forbundet med biokemiske abnormiteter i leverfunktionen. Vedvarende forhøjelser (>3 gange den øvre grænse for normal [ULN], der forekommer ved 2 eller flere lejligheder) i serumtransaminaser forekom hos 0,7 % af patienterne, som fik LIPITOR i kliniske forsøg. Forekomsten af disse abnormiteter var 0,2 %, 0,2 %, 0,6 % og 2,3 % for henholdsvis 10, 20, 40 og 80 mg.
En patient i kliniske forsøg udviklede gulsot. Forøgelser i leverfunktionstests (LFT) hos andre patienter var ikke forbundet med gulsot eller andre kliniske tegn eller symptomer. Efter dosisreduktion, lægemiddelafbrydelse eller seponering vendte transaminaseniveauer tilbage til eller nær førbehandlingsniveauer uden følgesygdomme. Atten ud af 30 patienter med vedvarende LFT-stigninger fortsatte behandlingen med en reduceret dosis LIPITOR.
Det anbefales, at leverenzymtest udføres før påbegyndelse af behandling med LIPITOR 40 mg og gentages som klinisk indiceret. Der har været sjældne rapporter efter markedsføring om fatalt og ikke-fatalt leversvigt hos patienter, der tager statiner, inklusive atorvastatin. Hvis der opstår alvorlig leverskade med kliniske symptomer og/eller hyperbilirubinæmi eller gulsot under behandling med LIPITOR 10 mg, afbrydes behandlingen omgående. Hvis en alternativ ætiologi ikke findes, skal du ikke genstarte LIPITOR.
LIPITOR 10mg bør anvendes med forsigtighed til patienter, der indtager betydelige mængder alkohol og/eller har tidligere haft leversygdomme. Aktiv leversygdom eller uforklarlige vedvarende transaminasestigninger er kontraindikationer for brugen af LIPITOR [se KONTRAINDIKATIONER ].
Endokrin funktion
Stigninger i HbA1c og fastende serumglukoseniveauer er blevet rapporteret med HMG-CoA-reduktasehæmmere, inklusive LIPITOR.
Statiner interfererer med kolesterolsyntesen og kan teoretisk gøre produktionen af binyre- og/eller gonadale steroider sløve. Kliniske undersøgelser har vist, at LIPITOR 20 mg ikke reducerer basal plasmakortisolkoncentration eller forringer binyrereserven. Effekten af statiner på mandlig fertilitet er ikke blevet undersøgt hos et tilstrækkeligt antal patienter. Virkningerne, hvis nogen, på hypofyse-gonadeaksen hos præmenopausale kvinder er ukendte. Der bør udvises forsigtighed, hvis et statin administreres samtidig med lægemidler, der kan nedsætte niveauet eller aktiviteten af endogene steroidhormoner, såsom ketoconazol, spironolacton og cimetidin.
CNS toksicitet
Hjerneblødning blev set hos en hunhund behandlet i 3 måneder med 120 mg/kg/dag. Hjerneblødning og optisk nervevakuolation blev set hos en anden hunhund, der blev aflivet i døende tilstand efter 11 ugers eskalerende doser op til 280 mg/kg/dag. Dosis på 120 mg/kg resulterede i en systemisk eksponering på ca. 16 gange det humane plasmaareal-under-kurven (AUC, 0–24 timer) baseret på den maksimale humane dosis på 80 mg/dag. En enkelt tonisk kramper blev set hos hver af 2 hanhunde (en behandlet med 10 mg/kg/dag og en med 120 mg/kg/dag) i en 2-årig undersøgelse. Der er ikke observeret CNS-læsioner hos mus efter kronisk behandling i op til 2 år ved doser op til 400 mg/kg/dag eller hos rotter ved doser op til 100 mg/kg/dag. Disse doser var 6 til 11 gange (mus) og 8 til 16 gange (rotte) den humane AUC (0–24) baseret på den maksimalt anbefalede humane dosis på 80 mg/dag.
CNS vaskulære læsioner, karakteriseret ved perivaskulær blødning, ødem og mononukleær celleinfiltration af perivaskulære rum, er blevet observeret hos hunde behandlet med andre medlemmer af denne klasse. Et kemisk lignende lægemiddel i denne klasse producerede optisk nervedegeneration (Wallerian degeneration af retinogene fibre) hos klinisk normale hunde på en dosisafhængig måde ved en dosis, der producerede plasma-lægemiddelniveauer omkring 30 gange højere end det gennemsnitlige lægemiddelniveau hos mennesker, der tog det højeste anbefalet dosis.
Brug hos patienter med nyligt slagtilfælde eller TIA
en post-hoc analyse af SPARCL-undersøgelsen til forebyggelse af slagtilfælde ved aggressiv reduktion i kolesterolniveauer (SPARCL), hvor LIPITOR 80 mg vs. placebo blev administreret til 4.731 forsøgspersoner uden CHD, som havde et slagtilfælde eller TIA inden for de foregående 6 måneder, var en højere forekomst af hæmoragisk slagtilfælde blev set i LIPITOR 80 mg-gruppen sammenlignet med placebo (55, 2,3 % atorvastatin vs. 33, 1,4 % placebo; HR: 1,68, 95 % CI: 1,09, 2,59; p=0,0168). Hyppigheden af fatalt hæmoragisk slagtilfælde var ens på tværs af behandlingsgrupperne (17 vs. 18 for henholdsvis atorvastatin- og placebogrupperne). Hyppigheden af ikke-dødelig hæmoragisk slagtilfælde var signifikant højere i atorvastatin-gruppen (38, 1,6 %) sammenlignet med placebo-gruppen (16, 0,7 %).
Nogle baseline-karakteristika, herunder hæmoragisk og lakunarisk slagtilfælde ved undersøgelsens start, var forbundet med en højere forekomst af hæmoragisk slagtilfælde i atorvastatingruppen [se BIVIRKNINGER ].
Patientrådgivningsinformation
Råd patienten til at læse den FDA-godkendte patientmærkning ( PATIENTOPLYSNINGER ).
Patienter, der tager LIPITOR 10mg, bør informeres om, at kolesterol er en kronisk tilstand, og de bør følge deres medicin sammen med deres nationale kolesteroluddannelsesprogram (NCEP) anbefalede diæt, et regelmæssigt træningsprogram efter behov og periodisk test af et fastende lipidpanel for at bestemme målopfyldelse.
Patienter bør informeres om stoffer, de ikke bør tage samtidig med atorvastatin [se ADVARSLER OG FORHOLDSREGLER]. Patienter bør også rådes til at informere andet sundhedspersonale, der ordinerer en ny medicin, om, at de tager LIPITOR.
Muskelsmerter
Alle patienter, der starter behandling med LIPITOR, skal informeres om risikoen for myopati og informeres om straks at rapportere enhver uforklarlig muskelsmerte, ømhed eller svaghed, især hvis de ledsages af utilpashed eller feber, eller hvis disse muskeltegn eller symptomer varer ved efter seponering af LIPITOR. Risikoen for dette er øget, når du tager visse typer medicin eller indtager større mængder (>1 liter) grapefrugtjuice. De bør diskutere al medicin, både receptpligtig og i håndkøb, med deres sundhedspersonale.
Leverenzymer
Det anbefales, at leverenzymtest udføres før påbegyndelse af LIPITOR 40 mg, og hvis der opstår tegn eller symptomer på leverskade. Alle patienter, der behandles med LIPITOR, bør rådes til omgående at rapportere alle symptomer, der kan indikere leverskade, herunder træthed, anoreksi, ubehag i højre øvre abdominal, mørk urin eller gulsot.
Embryofetal toksicitet
Rådgive kvinder om reproduktionspotentiale om risikoen for et foster, om at bruge effektiv prævention under behandlingen og at informere deres læge om en kendt eller formodet graviditet [se KONTRAINDIKATIONER og Brug i specifikke populationer ].
Amning
Advis kvinder til ikke at amme under behandling med LIPITOR [se KONTRAINDIKATIONER og Brug i specifikke populationer ].
Dette produkts mærkning er muligvis blevet opdateret. Besøg www.pfizer.com for at få de seneste ordinationsoplysninger.
Ikke-klinisk toksikologi
Karcinogenese, mutagenese, svækkelse af fertilitet
I et 2-årigt carcinogenicitetsstudie i rotter ved dosisniveauer på 10, 30 og 100 mg/kg/dag blev der fundet 2 sjældne tumorer i muskler hos højdosis hunner: hos den ene var der et rhabdomyosarkom og i en anden, der var et fibrosarkom. Denne dosis repræsenterer en plasma AUC (0–24) værdi på ca. 16 gange den gennemsnitlige humane plasma lægemiddel eksponering efter en 80 mg oral dosis.
Et 2-årigt carcinogenicitetsstudie i mus givet 100, 200 eller 400 mg/kg/dag resulterede i en signifikant stigning i leveradenomer hos højdosis hanner og levercarcinomer hos højdosis hunner. Disse fund forekom ved plasma-AUC-værdier (0–24) på ca. 6 gange den gennemsnitlige humane plasmalægemiddeleksponering efter en oral dosis på 80 mg.
In vitro var atorvastatin ikke mutagent eller klastogent i følgende test med og uden metabolisk aktivering: Ames-testen med Salmonella typhimurium og Escherichia coli, HGPRT-forward-mutationsanalysen i kinesisk hamster-lungeceller og kromosomafvigelsesanalysen i kinesisk hamster-lungeceller . Atorvastatin var negativt i in vivo muse mikronukleustest.
Hos hunrotter forårsagede atorvastatin i doser op til 225 mg/kg (56 gange den humane eksponering) ingen negative virkninger på fertiliteten. Undersøgelser med hanrotter udført i doser på op til 175 mg/kg (15 gange den humane eksponering) gav ingen ændringer i fertiliteten. Der var aplasi og aspermi i epididymis hos 2 ud af 10 rotter behandlet med 100 mg/kg/dag atorvastatin i 3 måneder (16 gange den humane AUC ved 80 mg dosis); testikelvægten var signifikant lavere ved 30 og 100 mg/kg, og epididymalvægten var lavere ved 100 mg/kg. Hanrotter, der fik 100 mg/kg/dag i 11 uger før parring, havde nedsat sædmotilitet, koncentration af sædceller i hovedet og øget unormal sæd. Atorvastatin forårsagede ingen bivirkninger på sædparametre eller reproduktionsorganhistopatologi hos hunde, der fik doser på 10, 40 eller 120 mg/kg i to år.
Brug i specifikke populationer
Graviditet
Risikooversigt
LIPITOR 10mg er kontraindiceret til brug hos gravide kvinder, da sikkerheden hos gravide kvinder ikke er blevet fastslået, og der ikke er nogen åbenlys fordel ved lipidsænkende medicin under graviditet. Fordi HMG-CoA-reduktasehæmmere nedsætter kolesterolsyntesen og muligvis syntesen af andre biologisk aktive stoffer afledt af kolesterol, kan LIPITOR forårsage fosterskader, når det administreres til en gravid kvinde. LIPITOR 40mg bør seponeres, så snart graviditet er erkendt [se KONTRAINDIKATIONER ]. Begrænsede offentliggjorte data om brugen af atorvastatin er utilstrækkelige til at bestemme en lægemiddelassocieret risiko for alvorlige medfødte misdannelser eller abort. I reproduktionsstudier på dyr med rotter og kaniner var der ingen tegn på embryo-føtal toksicitet eller medfødte misdannelser ved doser op til henholdsvis 30 og 20 gange den menneskelige eksponering ved den maksimalt anbefalede humane dosis (MRHD) på 80 mg baseret på krop overfladeareal (mg/m ). Hos rotter, der fik atorvastatin under drægtighed og diegivning, blev der observeret nedsat postnatal vækst og udvikling ved doser ≥ 6 gange MRHD (se Data ).
Den estimerede baggrundsrisiko for alvorlige fødselsdefekter og abort for den angivne population er ukendt. I den generelle befolkning i USA er den estimerede baggrundsrisiko for alvorlige fødselsdefekter og abort i klinisk anerkendte graviditeter henholdsvis 2–4 % og 15–20 %.
Data
Menneskelige data
Begrænsede publicerede data om atorvastatin-calcium fra observationsstudier, metaanalyser og case-rapporter har ikke vist en øget risiko for større medfødte misdannelser eller abort. Sjældne rapporter om medfødte anomalier er modtaget efter intrauterin eksponering for andre HMGCoA-reduktasehæmmere. I en gennemgang af ca. 100 prospektivt fulgte graviditeter hos kvinder udsat for simvastatin eller lovastatin oversteg forekomsten af medfødte anomalier, spontane aborter og føtale dødsfald/dødfødsler ikke, hvad man kunne forvente i den generelle befolkning. Antallet af tilfælde er tilstrækkeligt til at udelukke en ≥3 til 4 gange stigning i medfødte anomalier i forhold til baggrundsincidensen. I 89 % af de prospektivt fulgte graviditeter blev lægemiddelbehandling påbegyndt før graviditeten og blev afbrudt på et tidspunkt i første trimester, da graviditet blev identificeret.
Dyredata
Atorvastatin krydser rotteplacenta og når et niveau i føtal lever svarende til niveauet i moderens plasma. Atorvastatin blev givet til gravide rotter og kaniner under organogenese i orale doser op til henholdsvis 300 mg/kg/dag og 100 mg/kg/dag. Atorvastatin var ikke teratogent hos rotter ved doser op til 300 mg/kg/dag eller hos kaniner ved doser op til 100 mg/kg/dag. Disse doser resulterede i multipla på ca. 30 gange (rotte) eller 20 gange (kanin) den menneskelige eksponering ved MRHD baseret på overfladeareal (mg/m ). Hos rotter resulterede den maternelle toksiske dosis på 300 mg/kg i øget postimplantationstab og nedsat føtal kropsvægt. Ved de maternelt toksiske doser på 50 og 100 mg/kg/dag hos kaniner var der øget postimplantationstab, og ved 100 mg/kg/dag faldt føtal kropsvægt.
en undersøgelse med drægtige rotter, der fik 20, 100 eller 225 mg/kg/dag fra drægtighedsdag 7 til og med diegivningsdag 20 (fravænning), var der nedsat overlevelse ved fødslen, postnatal dag 4, fravænning og post-fravænning hos hvalpe af mødre doseret med 225 mg/kg/dag, en dosis, hvor der blev observeret maternel toksicitet. Hvalpens kropsvægt blev reduceret gennem postnatal dag 21 med 100 mg/kg/dag og gennem postnatal dag 91 med 225 mg/kg/dag. Udviklingen af hvalpe blev forsinket (rotarods ydeevne ved 100 mg/kg/dag og akustisk forskrækkelse ved 225 mg/kg/dag; løs hoven og øjenåbning ved 225 mg/kg/dag). Disse doser svarer til 6 gange (100 mg/kg) og 22 gange (225 mg/kg) den humane eksponering ved MRHD, baseret på AUC.
Amning
Risikooversigt
Brug af LIPITOR 40 mg er kontraindiceret under amning [se KONTRAINDIKATIONER ]. Der er ingen tilgængelig information om lægemidlets virkning på det ammede spædbarn eller lægemidlets virkning på mælkeproduktionen. Det vides ikke, om atorvastatin er til stede i modermælk, men det er vist, at et andet lægemiddel i denne klasse passerer over i modermælk, og atorvastatin er til stede i rottemælk. På grund af risikoen for alvorlige bivirkninger hos et ammet spædbarn, skal du rådgive kvinder om, at amning ikke anbefales under behandling med LIPITOR.
Hunner og mænd med reproduktionspotentiale
Svangerskabsforebyggelse
LIPITOR kan forårsage fosterskader, når det administreres til en gravid kvinde. Rådgiv kvinder med reproduktionspotentiale til at bruge effektiv prævention under behandling med LIPITOR [se Brug i specifikke populationer ].
Pædiatrisk brug
Heterozygot familiær hyperkolesterolæmi (HeFH)
Sikkerheden og effektiviteten af LIPITOR 20 mg er blevet fastslået hos pædiatriske patienter i alderen 10 år til 17 år, med HeFH som et supplement til diæt for at reducere totalt kolesterol, LDL-C og apo B-niveauer efter en tilstrækkelig diætforsøg. terapi, er følgende til stede:
- LDL-C ≥ 190 mg/dL, eller
- LDL-C ≥ 160 mg/dL og
- en positiv familiehistorie med FH eller for tidlig hjerte-kar-sygdom hos en første- eller andengradsslægtning, eller
- to eller flere andre CVD-risikofaktorer er til stede.
Brug af LIPITOR 20mg til denne indikation understøttes af beviser fra [se DOSERING OG ADMINISTRATION , BIVIRKNINGER , KLINISK FARMAKOLOGI , og Kliniske Studier ]:
- Et placebokontrolleret klinisk forsøg af 6 måneders varighed med 187 drenge og postmenarkalske piger i alderen 10 år til 17 år. Patienter behandlet med 10 mg eller 20 mg dagligt LIPITOR havde en bivirkningsprofil, der generelt svarede til den for patienter behandlet med placebo. I denne begrænsede kontrollerede undersøgelse var der ingen signifikant effekt på vækst eller seksuel modning hos drenge eller på menstruationscykluslængde hos piger.
- Et treårigt åbent ukontrolleret forsøg, der omfattede 163 pædiatriske patienter i alderen 10 til 15 år med HeFH, som blev titreret for at opnå et mål for LDL-C
Rådgiv postmenarkalske piger om præventionsanbefalinger, hvis det er relevant for patienten [se Brug i specifikke populationer ].
Den langsigtede effekt af LIPITOR-behandling påbegyndt i barndommen for at reducere morbiditet og dødelighed i voksenalderen er ikke blevet fastlagt.
Sikkerheden og effekten af LIPITOR 10 mg er ikke blevet fastslået hos pædiatriske patienter under 10 år med HeFH.
Homozygot familiær hyperkolesterolæmi (HoFH)
Klinisk effekt af LIPITOR 20 mg med doser op til 80 mg/dag i 1 år blev evalueret i et ukontrolleret studie af patienter med HoFH, inklusive 8 pædiatriske patienter [se Kliniske Studier ].
Geriatrisk brug
Af de 39.828 patienter, der fik LIPITOR 40 mg i kliniske undersøgelser, var 15.813 (40 %) ≥65 år og 2.800 (7 %) var ≥75 år. Der blev ikke observeret nogen overordnede forskelle i sikkerhed eller effektivitet mellem disse forsøgspersoner og yngre forsøgspersoner, og anden rapporteret klinisk erfaring har ikke identificeret forskelle i respons mellem ældre og yngre patienter, men større følsomhed hos nogle ældre voksne kan ikke udelukkes. Da høj alder (≥65 år) er en disponerende faktor for myopati, bør LIPITOR ordineres med forsigtighed til ældre.
Nedsat leverfunktion
Lipitor er kontraindiceret hos patienter med aktiv leversygdom, som kan omfatte uforklarlige vedvarende stigninger i levertransaminaseniveauer [se KONTRAINDIKATIONER og KLINISK FARMAKOLOGI ].
OVERDOSIS
Der er ingen specifik behandling for overdosering af LIPITOR. I tilfælde af en overdosis bør patienten behandles symptomatisk, og støttende foranstaltninger skal iværksættes efter behov. På grund af omfattende lægemiddelbinding til plasmaproteiner forventes hæmodialyse ikke at øge LIPITOR 20 mg clearance signifikant.
KONTRAINDIKATIONER
- Aktiv leversygdom, som kan omfatte uforklarlige vedvarende stigninger i hepatiske transaminaseniveauer
- Overfølsomhed over for enhver komponent i denne medicin
- Graviditet [se Brug i specifikke populationer].
- Amning [se Brug i specifikke populationer].
KLINISK FARMAKOLOGI
Handlingsmekanisme
LIPITOR 20mg er en selektiv, kompetitiv hæmmer af HMG-CoA-reduktase, det hastighedsbegrænsende enzym, der omdanner 3-hydroxy-3-methylglutaryl-coenzym A til mevalonat, en forløber for steroler, herunder kolesterol. I dyremodeller sænker LIPITOR 40 mg plasmakolesterol- og lipoproteinniveauer ved at hæmme HMG-CoA-reduktase og kolesterolsyntese i leveren og ved at øge antallet af hepatiske LDL-receptorer på celleoverfladen for at øge optagelsen og katabolismen af LDL; LIPITOR reducerer også LDL-produktionen og antallet af LDL-partikler.
Farmakodynamik
LIPITOR, såvel som nogle af dets metabolitter, er farmakologisk aktive hos mennesker. Leveren er det primære virkningssted og det primære sted for kolesterolsyntese og LDL-clearance. Lægemiddeldosering, snarere end systemisk lægemiddelkoncentration, korrelerer bedre med LDL-C-reduktion. Individualisering af lægemiddeldosering bør baseres på terapeutisk respons [se DOSERING OG ADMINISTRATION ].
Farmakokinetik
Absorption
LIPITOR absorberes hurtigt efter oral administration; maksimale plasmakoncentrationer forekommer inden for 1 til 2 timer. Omfanget af absorption stiger proportionalt med LIPITOR-dosis. Den absolutte biotilgængelighed af atorvastatin (moderlægemiddel) er ca. 14 %, og den systemiske tilgængelighed af HMG-CoA-reduktasehæmmende aktivitet er ca. 30 %. Den lave systemiske tilgængelighed tilskrives præsystemisk clearance i gastrointestinal mucosa og/eller hepatisk first-pass metabolisme. Selvom mad nedsætter hastigheden og omfanget af lægemiddelabsorption med henholdsvis ca. 25 % og 9 %, som vurderet ved Cmax og AUC, er LDL-C-reduktionen ens, uanset om LIPITOR 40 mg gives med eller uden mad. Plasma LIPITOR 20 mg koncentrationer er lavere (ca. 30 % for Cmax og AUC) efter lægemiddeladministration om aftenen sammenlignet med morgen. LDL-C-reduktionen er dog den samme uanset tidspunktet på dagen for lægemiddeladministration [se DOSERING OG ADMINISTRATION ].
Fordeling
Gennemsnitlig distributionsvolumen af LIPITOR 20 mg er ca. 381 liter. LIPITOR 20mg er ≥98% bundet til plasmaproteiner. Et blod/plasma-forhold på ca. 0,25 indikerer dårlig lægemiddelpenetration i røde blodlegemer. Baseret på observationer hos rotter udskilles LIPITOR 10 mg sandsynligvis i modermælk [se KONTRAINDIKATIONER og Brug i specifikke populationer ].
Metabolisme
LIPITOR 20mg metaboliseres i vid udstrækning til orto- og parahydroxylerede derivater og forskellige beta-oxidationsprodukter. In vitro-hæmning af HMG-CoA-reduktase af ortho- og parahydroxylerede metabolitter svarer til hæmningen af LIPITOR. Ca. 70 % af den cirkulerende hæmmende aktivitet for HMG-CoA-reduktase tilskrives aktive metabolitter. In vitro undersøgelser tyder på vigtigheden af LIPITOR 40mg metabolisme af cytochrom P450 3A4, i overensstemmelse med øgede plasmakoncentrationer af LIPITOR 20mg hos mennesker efter samtidig administration med erythromycin, en kendt hæmmer af dette isozym [se DRUGSINTERAKTIONER ]. Hos dyr gennemgår ortho-hydroxymetabolitten yderligere glukuronidering.
Udskillelse
LIPITOR 20mg og dets metabolitter elimineres primært i galden efter hepatisk og/eller ekstrahepatisk metabolisme; dog ser lægemidlet ikke ud til at gennemgå enterohepatisk recirkulation. Gennemsnitlig plasmaelimineringshalveringstid for LIPITOR hos mennesker er ca. 14 timer, men halveringstiden af hæmmende aktivitet for HMG-CoA-reduktase er 20 til 30 timer på grund af bidraget fra aktive metabolitter. Mindre end 2 % af en dosis LIPITOR genfindes i urinen efter oral administration.
Specifikke populationer
Geriatrisk
Plasmakoncentrationer af LIPITOR er højere (ca. 40 % for Cmax og 30 % for AUC) hos raske ældre forsøgspersoner (alder ≥65 år) end hos unge voksne. Kliniske data tyder på en større grad af LDL-sænkning ved enhver dosis af lægemiddel hos den ældre patientpopulation sammenlignet med yngre voksne [se Brug i specifikke populationer ].
Pædiatrisk
Tilsyneladende oral clearance af atorvastatin hos pædiatriske forsøgspersoner så ud til at svare til den hos voksne, når den blev skaleret allometrisk efter kropsvægt, da kropsvægten var den eneste signifikante kovariat i atorvastatinpopulationens farmakokinetiske model med data inklusive pædiatriske HeFH-patienter (i alderen 10 år til 17 år, n=29) i et åbent, 8-ugers studie.
Køn
Plasmakoncentrationer af LIPITOR 40 mg hos kvinder adskiller sig fra dem hos mænd (ca. 20 % højere for Cmax og 10 % lavere for AUC); der er dog ingen klinisk signifikant forskel i LDL-C-reduktion med LIPITOR 10 mg mellem mænd og kvinder.
Nedsat nyrefunktion
Nyresygdom har ingen indflydelse på plasmakoncentrationerne eller LDL-C-reduktionen af LIPITOR; Dosisjustering hos patienter med nedsat nyrefunktion er derfor ikke nødvendig [se DOSERING OG ADMINISTRATION og ADVARSLER OG FORHOLDSREGLER ].
Hæmodialyse
Mens undersøgelser ikke er blevet udført på patienter med nyresygdom i slutstadiet, forventes hæmodialyse ikke at øge clearance af LIPITOR 10 mg signifikant, da lægemidlet er udstrakt bundet til plasmaproteiner.
Nedsat leverfunktion
Hos patienter med kronisk alkoholisk leversygdom er plasmakoncentrationerne af LIPITOR markant forhøjede. Cmax og AUC er hver 4 gange større hos patienter med Childs-Pugh A sygdom. Cmax og AUC er henholdsvis ca. 16 gange og 11 gange øget hos patienter med Childs-Pugh B sygdom [se KONTRAINDIKATIONER ].
Lægemiddelinteraktionsstudier
Atorvastatin er et substrat for de hepatiske transportører, OATP1B1 og OATP1B3 transporter. Metabolitter af atorvastatin er substrater for OATP1B1. Atorvastatin er også identificeret som et substrat for effluxtransportøren BCRP, hvilket kan begrænse den intestinale absorption og biliær clearance af atorvastatin.
TABEL 6: Effekt af samtidig administrerede lægemidler på farmakokinetikken af atorvastatin
TABEL 7: Effekt af Atorvastatin på farmakokinetikken af samtidig administrerede lægemidler
LIPITOR havde ingen klinisk signifikant effekt på protrombintiden, når det blev givet til patienter i kronisk warfarinbehandling.
Kliniske Studier
Forebyggelse af hjerte-kar-sygdomme
Anglo-Scandinavian Cardiac Outcomes Trial (ASCOT) blev effekten af LIPITOR 10 mg på fatal og ikke-dødelig koronar hjertesygdom vurderet hos 10.305 hypertensive patienter i alderen 40-80 år (gennemsnit af 63 år) uden tidligere myokardie. infarkt og med TC-niveauer ≤251 mg/dL (6,5 mmol/L). Derudover havde alle patienter mindst 3 af følgende kardiovaskulære risikofaktorer: mandligt køn (81,1%), alder >55 år (84,5%), rygning (33,2%), diabetes (24,3%), historie med CHD i en første- grad relativ (26%), TC:HDL >6 (14,3%), perifer vaskulær sygdom (5,1%), venstre ventrikel hypertrofi (14,4%), tidligere cerebrovaskulær hændelse (9,8%), specifik EKG-abnormitet (14,3%), proteinuri /albuminuri (62,4%). I dette dobbeltblindede, placebokontrollerede studie blev patienterne behandlet med antihypertensiv terapi (mål BP
Effekten af 10 mg/dag af LIPITOR på lipidniveauer svarede til den, der er set i tidligere kliniske forsøg.
LIPITOR reducerede signifikant hyppigheden af koronare hændelser [enten fatal koronar hjertesygdom (46 hændelser i placebogruppen vs. 40 hændelser i LIPITOR 40 mg-gruppen) eller ikke-dødelig MI (108 hændelser i placebogruppen vs. 60 hændelser i LIPITOR-gruppen) 20 mg gruppe)] med en relativ risikoreduktion på 36 % [(baseret på forekomster på 1,9 % for LIPITOR 40 mg vs. 3,0 % for placebo), p=0,0005 (se figur 1)]. Risikoreduktionen var konsistent uanset alder, rygestatus, fedme eller tilstedeværelse af nyreinsufficiens. Effekten af LIPITOR blev set uanset baseline LDL-niveauer. På grund af det lille antal begivenheder var resultaterne for kvinder ikke entydige.
Figur 1: Effekt af LIPITOR 10 mg/dag på kumulativ forekomst af ikke-fatalt myokardieinfarkt eller koronar hjertesygdomsdød (i ASCOT-LLA)
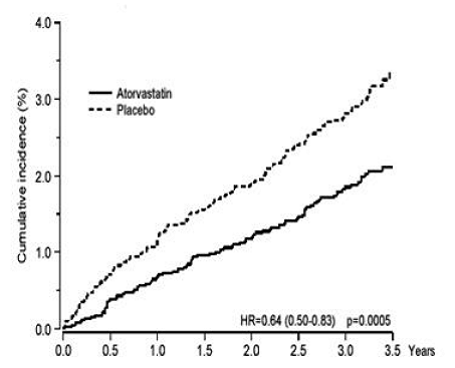
LIPITOR 40 mg reducerede også signifikant den relative risiko for revaskulariseringsprocedurer med 42 % (hyppighed på 1,4 % for LIPITOR 20 mg og 2,5 % for placebo). Selvom reduktionen af fatale og ikke-dødelige slagtilfælde ikke nåede et foruddefineret signifikansniveau (p=0,01), blev der observeret en gunstig tendens med en 26 % relativ risikoreduktion (hyppighed på 1,7 % for LIPITOR og 2,3 % for placebo). . Der var ingen signifikant forskel mellem behandlingsgrupperne for dødsfald på grund af kardiovaskulære årsager (p=0,51) eller ikke-kardiovaskulære årsager (p=0,17).
Collaborative Atorvastatin Diabetes Study (CARDS) blev effekten af LIPITOR på kardiovaskulær sygdom (CVD) endepunkter vurderet hos 2838 forsøgspersoner (94 % hvide, 68 % mænd), i alderen 40-75 år med type 2-diabetes baseret på WHO-kriterier, uden tidligere kardiovaskulær sygdom og med LDL ≤ 160 mg/dL og TG ≤ 600 mg/dL. Ud over diabetes havde forsøgspersoner 1 eller flere af følgende risikofaktorer: nuværende rygning (23 %), hypertension (80 %), retinopati (30 %) eller mikroalbuminuri (9 %) eller makroalbuminuri (3 %). Ingen forsøgspersoner i hæmodialyse blev inkluderet i undersøgelsen. I dette multicenter, placebokontrollerede, dobbeltblindede kliniske forsøg blev forsøgspersoner tilfældigt fordelt til enten LIPITOR 10 mg daglig (1429) eller placebo (1411) i et 1:1-forhold og blev fulgt i en medianvarighed på 3,9 år. Det primære endepunkt var forekomsten af enhver af de større kardiovaskulære hændelser: myokardieinfarkt, akut CHD-død, ustabil angina, koronar revaskularisering eller slagtilfælde. Den primære analyse var tiden til den første forekomst af det primære endepunkt.
Baselinekarakteristika for forsøgspersoner var: gennemsnitsalder på 62 år, gennemsnitlig HbA 7,7%; median LDL-C 120 mg/dL; median TC 207 mg/dL; median TG 151 mg/dL; median HDL-C 52 mg/dL.
Effekten af LIPITOR 10 mg/dag på lipidniveauer svarede til den, der er set i tidligere kliniske forsøg.
LIPITOR reducerede signifikant hyppigheden af større kardiovaskulære hændelser (primære endepunkthændelser) (83 hændelser i LIPITOR-gruppen vs. 127 hændelser i placebogruppen) med en relativ risikoreduktion på 37 %, HR 0,63, 95 % CI (0,48, 0,83) (p=0,001) (se figur 2). En effekt af LIPITOR blev set uanset alder, køn eller baseline lipidniveauer.
LIPITOR 20 mg reducerede signifikant risikoen for slagtilfælde med 48 % (21 hændelser i LIPITOR 10 mg-gruppen vs. 39 hændelser i placebogruppen), HR 0,52, 95 % CI (0,31, 0,89) (p=0,016) og reducerede risikoen for MI med 42 % (38 hændelser i LIPITOR-gruppen vs. 64 hændelser i placebogruppen), HR 0,58, 95,1 % CI (0,39, 0,86) (p=0,007). Der var ingen signifikant forskel mellem behandlingsgrupperne for angina, revaskulariseringsprocedurer og akut CHD-død.
Der var 61 dødsfald i LIPITOR-gruppen mod 82 dødsfald i placebogruppen (HR 0,73, p=0,059).
Figur 2: Effekt af LIPITOR 10 mg/dag på tid til forekomst af større kardiovaskulær hændelse (myokardieinfarkt, akut CHD død, ustabil angina, koronar revaskularisering eller slagtilfælde) i CARDS
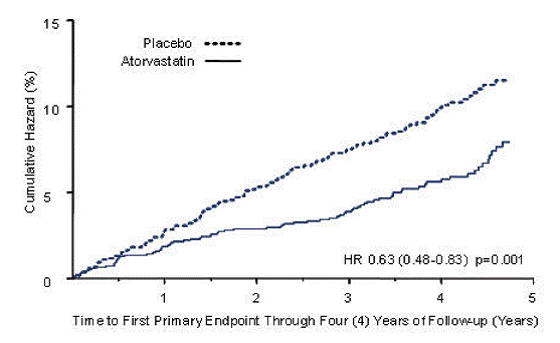
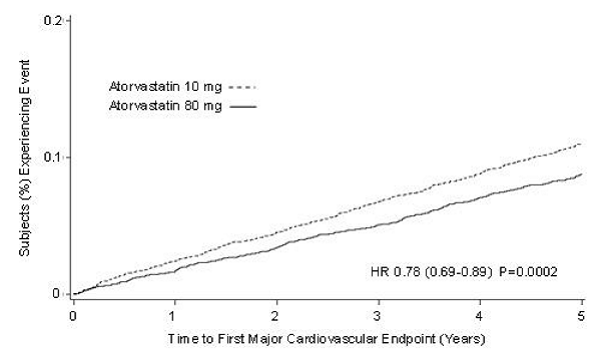
Treating to New Targets-studiet (TNT) blev effekten af LIPITOR 80 mg/dag vs. LIPITOR 10 mg/dag på reduktionen af kardiovaskulære hændelser vurderet hos 10.001 forsøgspersoner (94 % hvide, 81 % mænd, 38 % ≥65 år) med klinisk tydelig koronar hjertesygdom, som havde opnået et mål for LDL-C-niveau
Behandling med LIPITOR 80 mg/dag reducerede signifikant frekvensen af MCVE (434 hændelser i 80 mg/dag-gruppen vs. 548 hændelser i 10 mg/dag-gruppen) med en relativ risikoreduktion på 22 %, HR 0,78, 95 % CI (0,69, 0,89), p=0,0002 (se figur 3 og tabel 9). Den samlede risikoreduktion var konsistent uanset alder (
Figur 3: Effekt af LIPITOR 80 mg/dag vs. 10 mg/dag på tid til forekomst af større kardiovaskulære hændelser (TNT)
TABEL 8: Oversigt over effektivitetsresultater i TNT
Af de hændelser, der omfattede det primære effektmål, reducerede behandling med LIPITOR 80 mg/dag signifikant frekvensen af ikke-dødelig, ikke-procedurerelateret MI og fatalt og ikke-dødeligt slagtilfælde, men ikke CHD-død eller genoplivet hjertestop (tabel 8). Af de foruddefinerede sekundære endepunkter reducerede behandling med LIPITOR 80 mg/dag signifikant hastigheden af koronar revaskularisering, angina og hospitalsindlæggelse for hjertesvigt, men ikke perifer vaskulær sygdom. Reduktionen i frekvensen af CHF med hospitalsindlæggelse blev kun observeret hos de 8 % af patienterne med en tidligere historie med CHF.
Der var ingen signifikant forskel mellem behandlingsgrupperne for dødelighed af alle årsager (tabel 8). Andelene af forsøgspersoner, der oplevede kardiovaskulær død, inklusive komponenterne af CHD-død og fatalt slagtilfælde, var numerisk mindre i LIPITOR 80 mg-gruppen end i LIPITOR 10 mg-behandlingsgruppen. Andelene af forsøgspersoner, der oplevede ikke-kardiovaskulær død, var numerisk større i LIPITOR 80 mg-gruppen end i LIPITOR 10 mg-behandlingsgruppen.
det inkrementelle fald i endepunkter gennem aggressiv lipidsænkende undersøgelse (IDEAL) blev behandling med LIPITOR 80 mg/dag sammenlignet med behandling med simvastatin 20–40 mg/dag hos 8.888 forsøgspersoner op til 80 år med en historie med CHD til vurdere, om reduktion i CV-risiko kunne opnås. Patienterne var hovedsageligt mænd (81 %), hvide (99 %) med en gennemsnitsalder på 61,7 år og en gennemsnitlig LDL-C på 121,5 mg/dL ved randomisering; 76 % var i statinbehandling. I dette prospektive, randomiserede, åbne, blindede endepunkt (PROBE) forsøg uden indkøringsperiode blev forsøgspersoner fulgt i en median varighed på 4,8 år. De gennemsnitlige LDL-C, TC, TG, HDL og non-HDL kolesterolniveauer i uge 12 var 78, 145, 115, 45 og 100 mg/dL under behandling med 80 mg LIPITOR 40 mg og 105, 179, 142, 47 og 132 mg/dL under behandling med 20-40 mg simvastatin.
Der var ingen signifikant forskel mellem behandlingsgrupperne for det primære endepunkt, frekvensen af første større koronar hændelse (fatal CHD, nonfatal MI og genoplivet hjertestop): 411 (9,3 %) i LIPITOR 80 mg/dag-gruppen vs. 463 (10,4%) i simvastatin 20-40 mg/dag-gruppen, HR 0,89, 95% CI (0,78, 1,01), p=0,07.
Der var ingen signifikante forskelle mellem behandlingsgrupperne for dødelighed af alle årsager: 366 (8,2 %) i LIPITOR 80 mg/dag-gruppen mod 374 (8,4 %) i simvastatin 20-40 mg/dag-gruppen. Andelene af forsøgspersoner, der oplevede CV- eller ikke-CV-dødsfald, var ens for LIPITOR 80 mg-gruppen og simvastatin 20-40 mg-gruppen.
Hyperlipidæmi og blandet dyslipidæmi
LIPITOR reducerer total-C, LDL-C, VLDL-C, apo B og TG og øger HDL-C hos patienter med hyperlipidæmi (heterozygot familiær og ikke-familiær) og blandet dyslipidæmi (Fredrickson Type IIa og IIb). Terapeutisk respons ses inden for 2 uger, og maksimal respons opnås normalt inden for 4 uger og opretholdes under kronisk behandling.
LIPITOR er effektiv i en lang række patientpopulationer med hyperlipidæmi, med og uden hypertriglyceridæmi, hos mænd og kvinder og hos ældre.
I to multicenter, placebo-kontrollerede, dosis-respons undersøgelser hos patienter med hyperlipidæmi, LIPITOR givet som en enkelt dosis over 6 uger, reducerede total-C, LDL-C, apo B og TG signifikant. (Samlede resultater er angivet i tabel 9.)
TABEL 9: Dosisrespons hos patienter med primær hyperlipidæmi (justeret gennemsnitlig %-ændring fra baseline)*
Hos patienter med Fredrickson Type IIa og IIb hyperlipoproteinæmi samlet fra 24 kontrollerede forsøg var median (25. Â og 75. Â percentil) procentvise ændringer fra baseline i HDL-C for LIPITOR 10, 20, 40 og 80 mg 6,4 (-1,4, 14), 8,7 (0, 17), 7,8 (0, 16) og 5,1 (-2,7, 15). Derudover viste analyse af de samlede data konsistente og signifikante fald i total-C, LDL-C, TG, total-C/HDL-C og LDLC/HDL-C.
I tre multicenter, dobbeltblindede undersøgelser af patienter med hyperlipidæmi, blev LIPITOR sammenlignet med andre statiner. Efter randomisering blev patienterne behandlet i 16 uger med enten LIPITOR 10 mg dagligt eller en fast dosis af sammenligningsmidlet (tabel 10).
TABEL 10: Gennemsnitlig procentvis ændring fra baseline ved slutpunkt (dobbeltblindede, randomiserede, aktivt kontrollerede forsøg)
Indvirkningen på de kliniske resultater af forskellene i lipidændrende virkninger mellem behandlinger vist i tabel 10 kendes ikke. Tabel 10 indeholder ikke data, der sammenligner virkningerne af LIPITOR 10 mg og højere doser af lovastatin, pravastatin og simvastatin. Lægemidlerne sammenlignet i undersøgelserne opsummeret i tabellen er ikke nødvendigvis udskiftelige.
Hypertriglyceridæmi
Responsen på LIPITOR hos 64 patienter med isoleret hypertriglyceridæmi (Fredrickson Type IV) behandlet på tværs af flere kliniske forsøg er vist i tabellen nedenfor (tabel 11). For de LIPITOR-behandlede patienter var median (min, max) baseline TG-niveau 565 (267-1502).
TABEL 11: Kombinerede patienter med isoleret forhøjet TG: Median (min, max) procentvis ændring fra baseline
Dysbetalipoproteinæmi
Resultaterne af et åbent krydsningsstudie af 16 patienter (genotyper: 14 apo E2/E2 og 2 apo E3/E2) med dysbetalipoproteinæmi (Fredrickson Type III) er vist i nedenstående tabel (tabel 12).
TABEL 12: Open-label crossover-undersøgelse af 16 patienter med dysbetalipoproteinæmi (Fredrickson Type III)
Homozygot familiær hyperkolesterolæmi
I et studie uden en samtidig kontrolgruppe fik 29 patienter i alderen 6 år til 37 år med HoFH maksimale daglige doser på 20 til 80 mg LIPITOR. Den gennemsnitlige LDL-C-reduktion i denne undersøgelse var 18 %. Femogtyve patienter med en reduktion i LDL-C havde et gennemsnitligt respons på 20 % (interval fra 7 % til 53 %, median på 24 %); de resterende 4 patienter havde 7 % til 24 % stigninger i LDL-C. Fem af de 29 patienter havde fraværende LDL-receptorfunktion. Af disse havde 2 patienter også en portacaval-shunt og havde ingen signifikant reduktion i LDL-C. De resterende 3 receptornegative patienter havde en gennemsnitlig LDL-C-reduktion på 22 %.
Heterozygot familiær hyperkolesterolæmi hos pædiatriske patienter
et dobbeltblindt, placebokontrolleret studie efterfulgt af en åben fase blev 187 drenge og postmenarkalske piger i alderen 10 år til 17 år (gennemsnitsalder 14,1 år) med heterozygot familiær hyperkolesterolæmi (HeFH) eller svær hyperkolesterolæmi. randomiseret til LIPITOR (n=140) eller placebo (n=47) i 26 uger og fik derefter alle LIPITOR 40 mg i 26 uger. Inkludering i undersøgelsen krævede 1) et baseline LDL-C niveau ≥ 190 mg/dL eller 2) et baseline LDL-C niveau ≥ 160 mg/dL og positiv familiehistorie med FH eller dokumenteret for tidlig hjertekarsygdom i en første eller anden grad i forhold. Den gennemsnitlige baseline LDL-C-værdi var 218,6 mg/dL (interval: 138,5–385,0 mg/dL) i LIPITOR-gruppen sammenlignet med 230,0 mg/dL (interval: 160,0–324,5 mg/dL) i placebogruppen . Dosis af LIPITOR (en gang dagligt) var 10 mg i de første 4 uger og optitreret til 20 mg, hvis LDL-C-niveauet var > 130 mg/dL. Antallet af LIPITOR-behandlede patienter, som krævede optitrering til 20 mg efter uge 4 i den dobbeltblinde fase, var 78 (55,7%).
LIPITOR 10 mg reducerede signifikant plasmaniveauer af total-C, LDL-C, triglycerider og apolipoprotein B i løbet af den 26-ugers dobbeltblinde fase (se tabel 13).
TABEL 13: Lipidændrende virkninger af LIPITOR hos unge drenge og piger med heterozygot familiær hyperkolesterolæmi eller svær hyperkolesterolæmi (gennemsnitlig procentvis ændring fra baseline ved endepunkt i intention-to-treat population)
Den gennemsnitlige opnåede LDL-C-værdi var 130,7 mg/dL (interval: 70,0–242,0 mg/dL) i LIPITOR 10 mg-gruppen sammenlignet med 228,5 mg/dL (interval: 152,0–385,0 mg/dL) i placebo gruppe i den 26-ugers dobbeltblinde fase.
Atorvastatin blev også undersøgt i et treårigt åbent, ukontrolleret forsøg, der omfattede 163 patienter med HeFH, som var 10 år til 15 år gamle (82 drenge og 81 piger). Alle patienter havde en klinisk diagnose af HeFH bekræftet ved genetisk analyse (hvis ikke allerede bekræftet af familiens historie). Cirka 98 % var kaukasiske, og mindre end 1 % var sorte eller asiatiske. Gennemsnitlig LDL-C ved baseline var 232 mg/dL. Startdosis atorvastatin var 10 mg én gang dagligt, og doserne blev justeret for at nå et mål på
Den langsigtede effekt af LIPITOR 20 mg behandling i barndommen til at reducere morbiditet og dødelighed i voksenalderen er ikke blevet fastlagt.
PATIENTOPLYSNINGER
LIPITOR® atorvastatin calcium tabletter (LIP-ih-tore))
Læs patientinformationen, der følger med LIPITOR 20mg, før du begynder at tage den, og hver gang du får en genopfyldning. Der kan være nye oplysninger. Denne indlægsseddel træder ikke i stedet for at tale med din læge om din tilstand eller behandling.
Spørg din læge eller apoteket, hvis du har spørgsmål om LIPITOR.
Hvad er LIPITOR?
LIPITOR er en receptpligtig medicin, der sænker kolesterol i dit blod. Det sænker LDL-C ("dårligt" kolesterol) og triglycerider i dit blod. Det kan også hæve dit HDL-C ("gode" kolesterol). LIPITOR er til voksne og børn over 10 år, hvis kolesterol ikke falder nok med motion og en fedtfattig kost alene.
LIPITOR kan sænke risikoen for hjerteanfald, slagtilfælde, visse typer hjertekirurgi og brystsmerter hos patienter, der har hjertesygdomme eller risikofaktorer for hjertesygdom, såsom:
- alder, rygning, forhøjet blodtryk, lavt HDL-C, hjertesygdomme i familien.
LIPITOR 20mg kan sænke risikoen for hjerteanfald eller slagtilfælde hos patienter med diabetes og risikofaktorer som:
- øjenproblemer, nyreproblemer, rygning eller forhøjet blodtryk.
LIPITOR 40mg begynder at virke efter ca. 2 uger.
Hvad er kolesterol?
Kolesterol og triglycerider er fedtstoffer, der dannes i din krop. De findes også i fødevarer. Du har brug for noget kolesterol for et godt helbred, men for meget er ikke godt for dig. Kolesterol og triglycerider kan tilstoppe dine blodkar. Det er især vigtigt at sænke dit kolesteroltal, hvis du har hjertesygdomme, ryger, har diabetes eller forhøjet blodtryk, er ældre, eller hvis hjertesygdomme starter tidligt i din familie.
Hvem bør ikke tage LIPITOR 40mg?
Tag ikke LIPITOR 10 mg, hvis du:
- er gravid eller tror, du kan være gravid, eller planlægger at blive gravid. LIPITOR kan skade dit ufødte barn. Hvis du bliver gravid, skal du stoppe med at tage LIPITOR 40 mg og kontakte din læge med det samme.
- ammer. LIPITOR 20mg kan passere over i din modermælk og kan skade din baby.
- har leverproblemer.
- er allergiske over for LIPITOR eller nogen af dets ingredienser. Den aktive ingrediens er atorvastatin. Se slutningen af denne indlægsseddel for en komplet liste over ingredienser i LIPITOR.
LIPITOR 20 mg dosering er ikke blevet fastlagt til børn under 10 år.
Før du starter LIPITOR
Fortæl det til din læge, hvis du:
- har muskelsmerter eller svaghed
- drik mere end 2 glas alkohol dagligt
- har diabetes
- har et skjoldbruskkirtelproblem
- har nyreproblemer
Nogle lægemidler bør ikke tages sammen med LIPITOR. Fortæl din læge om al den medicin, du tager, inklusive receptpligtig og ikke-receptpligtig medicin, vitaminer og naturlægemidler. LIPITOR og visse andre lægemidler kan interagere og forårsage alvorlige bivirkninger. Fortæl det især til din læge, hvis du tager medicin mod:
- dit immunsystem
- kolesterol
- infektioner
- prævention
- hjertefejl
- HIV eller AIDS
- hepatitis C-virus
- antivirale midler
Kend al den medicin, du tager. Hav en liste over dem med dig for at vise din læge og apotek.
Hvordan skal jeg tage LIPITOR 40mg?
- Tag LIPITOR 20mg nøjagtigt som foreskrevet af din læge. Du må ikke ændre din dosis eller stoppe med LIPITOR uden at tale med din læge. Din læge kan tage blodprøver for at kontrollere dit kolesteroltal under din behandling med LIPITOR. Din dosis af LIPITOR kan blive ændret baseret på disse blodprøveresultater.
- Tag LIPITOR hver dag på et hvilket som helst tidspunkt af dagen på omtrent samme tidspunkt hver dag. LIPITOR 10 mg kan tages med eller uden mad. Bryd ikke LIPITOR-tabletter, før du tager dem.
- Din læge bør starte dig på en fedtfattig diæt, før du giver dig LIPITOR. Bliv på denne fedtfattige diæt, når du tager LIPITOR.
- Hvis du glemmer en dosis LIPITOR, skal du tage den, så snart du husker det. Tag ikke LIPITOR 10 mg, hvis der er gået mere end 12 timer, siden du glemte din sidste dosis. Vent og tag den næste dosis på dit normale tidspunkt. Tag ikke 2 doser LIPITOR 10mg på samme tid.
- Hvis du tager for meget LIPITOR eller overdosis, skal du straks kontakte din læge eller Giftinformationscentralen. Eller gå til nærmeste skadestue.
Hvad skal jeg undgå, mens jeg tager LIPITOR 10mg?
- Tal med din læge, før du begynder på ny medicin. Dette omfatter receptpligtig og ikke-receptpligtig medicin, vitaminer og naturlægemidler. LIPITOR og visse andre lægemidler kan interagere og forårsage alvorlige bivirkninger.
- Bliv ikke gravid. Hvis du bliver gravid, skal du stoppe med at tage LIPITOR med det samme og ringe til din læge.
Hvad er de mulige bivirkninger af LIPITOR 10mg?
LIPITOR kan forårsage alvorlige bivirkninger. Disse bivirkninger er kun sket for et lille antal mennesker. Din læge kan overvåge dig for dem. Disse bivirkninger forsvinder normalt, hvis din dosis sænkes eller LIPITOR stoppes. Disse alvorlige bivirkninger omfatter:
- Muskelproblemer. LIPITOR 40mg kan forårsage alvorlige muskelproblemer, der kan føre til nyreproblemer, herunder nyresvigt. Du har en større chance for muskelproblemer, hvis du tager visse andre lægemidler sammen med LIPITOR.
- Leverproblemer. Din læge bør tage blodprøver for at kontrollere din lever, før du begynder at tage LIPITOR 20 mg, og hvis du har symptomer på leverproblemer, mens du tager LIPITOR. Ring til din læge med det samme, hvis du har følgende symptomer på leverproblemer:
- føler sig træt eller svag
- mistet appetiten
- smerter i øvre mave
- mørk ravfarvet urin
- gulfarvning af din hud eller det hvide i dine øjne
Ring til din læge med det samme, hvis du har:
- muskelproblemer som svaghed, ømhed eller smerte, der sker uden en god grund, især hvis du også har feber eller føler dig mere træt end normalt. Dette kan være et tidligt tegn på et sjældent muskelproblem.
- muskelproblemer, der ikke forsvinder, selv efter din læge har rådet dig til at stoppe med at tage LIPITOR. Din læge kan lave yderligere test for at diagnosticere årsagen til dine muskelproblemer.
- allergiske reaktioner, herunder hævelse af ansigt, læber, tunge og/eller svælg, der kan forårsage vejrtræknings- eller synkebesvær, som kan kræve behandling med det samme.
- kvalme og opkast.
- udledning af brun eller mørkfarvet urin.
- du føler dig mere træt end normalt
- din hud og det hvide i dine øjne bliver gule.
- mavesmerter.
- allergiske hudreaktioner.
I kliniske undersøgelser rapporterede patienterne følgende almindelige bivirkninger, mens de tog LIPITOR: diarré, mavebesvær, muskel- og ledsmerter og ændringer i nogle laboratorieblodprøver.
Følgende yderligere bivirkninger er blevet rapporteret med LIPITOR:
træthed, seneproblemer, hukommelsestab og forvirring.
Tal med din læge eller apoteket, hvis du har bivirkninger, som generer dig, eller som ikke vil forsvinde.
Disse er ikke alle bivirkningerne af LIPITOR. Spørg din læge eller apoteket om en komplet liste.
Hvordan opbevarer jeg LIPITOR
- Opbevar LIPITOR ved stuetemperatur, 68 til 77°F (20 til 25°C).
- Opbevar ikke medicin, der er forældet, eller som du ikke længere har brug for.
- Opbevar LIPITOR og al medicin utilgængeligt for børn. Vær sikker på, at hvis du smider medicin ud, er det uden for børns rækkevidde.
Generel information om LIPITOR
Lægemidler ordineres nogle gange til tilstande, der ikke er nævnt i indlægssedler. Brug ikke LIPITOR 10mg til en tilstand, som den ikke er ordineret til. Giv ikke LIPITOR til andre mennesker, selvom de har det samme problem, som du har. Det kan skade dem.
Denne folder opsummerer de vigtigste oplysninger om LIPITOR. Hvis du vil have mere information, så tal med din læge. Du kan bede din læge eller apotek om information om LIPITOR, der er skrevet til sundhedspersonale. Eller du kan gå til LIPITORs hjemmeside på www.lipitor.com.
Hvad er ingredienserne i LIPITOR?
Aktiv ingrediens: atorvastatin calcium
Inaktive ingredienser: calciumcarbonat, USP; candelilla voks, FCC; croscarmellosenatrium, NF; hydroxypropylcellulose, NF; lactosemonohydrat, NF; magnesiumstearat, NF; mikrokrystallinsk cellulose, NF; Opadry White YS-1-7040 (hypromellose, polyethylenglycol, talkum, titaniumdioxid); polysorbat 80, NF; simeticonemulsion.
