Medicin mod diarré: Furosemide 40mg, 100mg Anvendelse, bivirkninger og dosering. Pris i onlineapotek. Generisk medicin uden recept.
Hvad er furosemid, og hvordan bruges det?
Furosemid 40mg er et diuretikum, som er et anthranilsyrederivat, der bruges til at behandle ødem forbundet med kongestiv hjertesvigt, levercirrhose og nyresygdom, herunder nefrotisk syndrom. Furosemid 40 mg er særligt nyttigt, når der ønskes et middel med større vanddrivende potentiale. Furosemid 40 mg er også indiceret som supplerende behandling ved akut lungeødem.
Hvad er de mulige bivirkninger af Furosemid?
Furosemid 100mg kan forårsage alvorlige bivirkninger, herunder:
- øget vandladning,
- tørst,
- muskelkramper,
- kløe,
- udslæt,
- svaghed,
- svimmelhed,
- snurrende fornemmelse (vertigo),
- diarré,
- mavesmerter, og
- forstoppelse
ADVARSEL
Furosemid 100mg tabletter er et potent vanddrivende middel, som, hvis det gives i store mængder, kan føre til en dyb diurese med vand- og elektrolytudtømning. Derfor er omhyggelig medicinsk overvågning påkrævet, og dosis og dosisplan skal tilpasses den enkelte patients behov. (Se DOSERING OG ADMINISTRATION.)
BESKRIVELSE
Furosemid-tabletter er et diuretikum, som er et anthranilsyrederivat. Furosemid-tabletter til oral administration indeholder furosemid som den aktive ingrediens og følgende inaktive ingredienser: majsstivelse, vandfri laktose, magnesiumstearat, prægelatineret stivelse, mikrokrystallinsk cellulose, natriumstivelsesglykolat og kolloid siliciumdioxid. Kemisk er det 4-chlor-N-furfuryl-5-sulfamoylantranilsyre. Furosemid-tabletter fås som hvide tabletter til oral administration i doseringsstyrker på 20, 40 og 80 mg. Furosemid 40mg er et hvidt til råhvidt lugtfrit krystallinsk pulver. Det er praktisk talt uopløseligt i vand, tungtopløseligt i alkohol, frit opløseligt i fortyndede alkaliopløsninger og uopløseligt i fortyndede syrer.
CAS-registreringsnummeret er 54-31-9.
Strukturformlen er som følger:
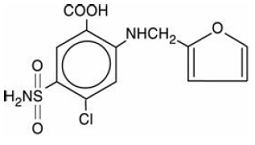
INDIKATIONER
Ødem
Furosemid 40 mg tabletter er indiceret til voksne og pædiatriske patienter til behandling af ødem forbundet med kongestiv hjerteinsufficiens, levercirrhose og nyresygdom, herunder nefrotisk syndrom. Furosemid 40 mg tabletter er særligt nyttige, når et middel med større vanddrivende potentiale ønskes.
Forhøjet blodtryk
Orale Furosemid 40 mg tabletter kan anvendes til voksne til behandling af hypertension alene eller i kombination med andre antihypertensiva. Hypertensive patienter, som ikke kan kontrolleres tilstrækkeligt med thiazider, vil sandsynligvis heller ikke blive tilstrækkeligt kontrolleret med Furosemid-tabletter alene.
DOSERING OG ADMINISTRATION
Ødem
Behandlingen bør individualiseres i henhold til patientens respons for at opnå maksimal terapeutisk respons og for at bestemme den minimale dosis, der er nødvendig for at opretholde dette respons.
Voksne
Den sædvanlige startdosis af Furosemid 100 mg tabletter er 20 til 80 mg givet som en enkelt dosis. Normalt følger en hurtig diurese. Om nødvendigt kan den samme dosis administreres 6 til 8 timer senere, eller dosis kan øges. Dosis kan øges med 20 eller 40 mg og gives ikke tidligere end 6 til 8 timer efter den foregående dosis, indtil den ønskede vanddrivende effekt er opnået. Den individuelt bestemte enkeltdosis bør derefter gives en eller to gange dagligt (f.eks. kl. 8 og 14). Dosen af Furosemid 100 mg tabletter kan titreres omhyggeligt op til 600 mg/dag hos patienter med klinisk svære ødematøse tilstande.
Ødem kan mobiliseres mest effektivt og sikkert ved at give Furosemid 40 mg tabletter 2 til 4 på hinanden følgende dage hver uge.
Når doser over 80 mg/dag gives i længere perioder, er omhyggelig klinisk observation og laboratoriemonitorering særligt tilrådeligt. (Se FORHOLDSREGLER : Laboratorieprøver .)
Geriatriske patienter
Generelt bør dosisvalg til den ældre patient være forsigtigt, sædvanligvis begyndende i den lave ende af doseringsområdet (se FORHOLDSREGLER : Geriatrisk brug ).
Pædiatriske patienter
Den sædvanlige startdosis af orale Furosemid 40 mg tabletter til pædiatriske patienter er 2 mg/kg legemsvægt givet som en enkelt dosis. Hvis det diuretiske respons ikke er tilfredsstillende efter den indledende dosis, kan dosis øges med 1 eller 2 mg/kg tidligst 6 til 8 timer efter den foregående dosis. Doser på mere end 6 mg/kg legemsvægt anbefales ikke. Til vedligeholdelsesbehandling hos pædiatriske patienter bør dosis justeres til det mindste effektive niveau.
Forhøjet blodtryk
Terapi bør individualiseres i henhold til patientens respons for at opnå maksimal terapeutisk respons og for at bestemme den minimale dosis, der er nødvendig for at opretholde den terapeutiske respons.
Voksne
Den sædvanlige startdosis af Furosemid 40 mg tabletter til hypertension er 80 mg, normalt opdelt i 40 mg to gange dagligt. Dosis skal derefter justeres i henhold til respons. Hvis responsen ikke er tilfredsstillende, tilsættes andre antihypertensiva.
Ændringer i blodtrykket skal overvåges nøje, når Furosemid 40 mg tabletter anvendes sammen med andre antihypertensiva, især under den indledende behandling. For at forhindre for stort blodtryksfald bør dosis af andre midler reduceres med mindst 50 procent, når Furosemid 100 mg tabletter føjes til kuren. Da blodtrykket falder under den forstærkende virkning af Furosemid-tabletter, kan en yderligere reduktion i dosis eller endda seponering af andre antihypertensiva være nødvendig.
Geriatriske patienter
Generelt bør dosisvalg og dosisjustering for den ældre patient være forsigtig, sædvanligvis begyndende i den lave ende af dosisområdet (se FORHOLDSREGLER : Geriatrisk brug ).
HVORDAN LEVERET
Furosemid 40 mg tabletter 20 mg leveres som hvide til råhvide, runde, flade, skrå kant, komprimerede tabletter, præget "EP" og "116" på den ene side og almindelige på den anden side i flasker med 100 stk. NDC 69315-116-01) og 1000 ( NDC 69315-116-10).
Furosemid tabeller 40 mg leveres som hvide til råhvide, runde, flad, skrå kant, halverede komprimerede tabletter, præget "EP" over halveret og "117" forneden halveret på den ene side og "40" på den anden side i flasker med 100 stk. NDC 69315-117-01) og 1000 ( NDC 69315-117-10).
Furosemid 40 mg tabletter 80 mg leveres som hvide til råhvide, runde, flad, skrå kant, halverede komprimerede tabletter, præget "EP" over halveret og "118" forneden halveret på den ene side og "80" på den anden side i flasker med 100 stk. NDC 69315-118-01) og 500 ( NDC 69315-118-05).
Bemærk: Dispenser i godt lukkede, lysbestandige beholdere. Udsættelse for lys kan forårsage en let misfarvning. Misfarvede tabletter bør ikke dispenseres.
Opfylder USP Dissolution Test 2
Opbevares ved 20° -25° C (68° -77° F) [ Se USP kontrolleret rumtemperatur ].
Fremstillet af: Leading Pharma, LLC, Fairfield, NJ 07004. Revideret: Okt 2018
BIVIRKNINGER
Bivirkninger er kategoriseret nedenfor efter organsystem og listet efter faldende sværhedsgrad.
Gastrointestinale systemreaktioner
Systemiske overfølsomhedsreaktioner
Centralnervesystemets reaktioner
Hæmatologiske reaktioner
Dermatologiske-overfølsomhedsreaktioner
Kardiovaskulær reaktion
- Ortostatisk hypotension kan forekomme og forværres af alkohol, barbiturater eller narkotika.
- Forøgelse af kolesterol og triglycerid serumniveauer
Andre reaktioner
- hyperglykæmi
- glykosuri
- hyperukæmi
- muskelspasme
- svaghed
- rastløshed
- urinblære spasmer
- tromboflebitis
- feber
Når bivirkningerne er moderate eller alvorlige, bør doseringen af Furosemid tabletter reduceres, eller behandlingen seponeres.
RING DIN LÆGE FOR LÆGE RÅDGIVNING OM BIVIRKNINGER. DU KAN RAPPORTERE BIVIRKNINGER TIL FDA PÅ 1-800-FDA-1088 ELLER LEADING PHARMA, LLC PÅ 1-844-740-7500.
DRUGSINTERAKTIONER
Furosemid-tabletter kan øge det ototoksiske potentiale af aminoglykosid-antibiotika, især i tilfælde af nedsat nyrefunktion. Undgå denne kombination undtagen i livstruende situationer.
Furosemid-tabletter bør ikke anvendes samtidig med ethacrynsyre på grund af muligheden for ototoksicitet. Patienter, der får høje doser salicylater samtidig med furosemid 100 mg tabletter, som ved reumatisk sygdom, kan opleve salicylattoksicitet ved lavere doser på grund af konkurrerende nyreudskillelsessteder.
Der er risiko for ototoksiske virkninger, hvis cisplatin og furosemid-tabletter gives samtidig. Desuden kan nefrotoksiciteten af nefrotoksiske lægemidler såsom cisplatin blive forstærket, hvis Furosemid 40 mg tabletter ikke gives i lavere doser og med positiv væskebalance, når det bruges til at opnå forceret diurese under cisplatinbehandling.
Furosemid 100 mg tabletter har en tendens til at modvirke den skeletmuskelafslappende effekt af tubocurarin og kan forstærke virkningen af succinylcholin.
Lithium bør generelt ikke gives sammen med diuretika, fordi de reducerer lithiums renale clearance og tilføjer en høj risiko for lithiumtoksicitet.
Furosemid 100 mg tabletter kombineret med angiotensinkonverterende enzymhæmmere eller angiotensin II-receptorblokkere kan føre til alvorlig hypotension og forringelse af nyrefunktionen, herunder nyresvigt. En afbrydelse eller reduktion i doseringen af Furosemid-tabletter, angiotensinkonverterende enzymhæmmere eller angiotensinreceptorblokkere kan være nødvendig.
Potentiation forekommer med ganglioniske eller perifere adrenerge blokerende lægemidler.
Furosemid 40 mg tabletter kan nedsætte arteriel reaktion på noradrenalin. Dog kan noradrenalin stadig bruges effektivt.
Samtidig administration af sucralfat og furosemid-tabletter kan reducere de natriuretiske og antihypertensive virkninger af furosemid 40 mg tabletter. Patienter, der får begge lægemidler, bør observeres nøje for at afgøre, om den ønskede diuretiske og/eller antihypertensive effekt af Furosemid 100 mg tabletter opnås. Indtagelsen af Furosemid 100 mg tabletter og sucralfat bør adskilles med mindst to timer.
I isolerede tilfælde kan intravenøs administration af Furosemid-tabletter inden for 24 timer efter indtagelse af chloralhydrat føre til rødmen, svedeanfald, rastløshed, kvalme, stigning i blodtryk og takykardi. Brug af Furosemid 40 mg tabletter samtidig med chloralhydrat anbefales derfor ikke.
Phenytoin interfererer direkte med furosemid-tabletternes nyrevirkning. Der er evidens for, at behandling med phenytoin fører til nedsat intestinal absorption af Furosemid 100 mg tabletter og som følge heraf til lavere maksimale serum furosemid 40 mg koncentrationer.
Methotrexat og andre lægemidler, der ligesom Furosemid-tabletter gennemgår betydelig renal tubulær sekretion, kan reducere effekten af Furosemid-tabletter. Omvendt kan Furosemid 100 mg tabletter nedsætte renal elimination af andre lægemidler, der gennemgår tubulær sekretion. Højdosisbehandling af både Furosemid 100 mg tabletter og disse andre lægemidler kan resultere i forhøjede serumniveauer af disse lægemidler og kan forstærke deres toksicitet såvel som toksiciteten af Furosemid 40 mg tabletter.
Furosemid 100 mg tabletter kan øge risikoen for cephalosporin-induceret nefrotoksicitet selv i tilfælde af mindre eller forbigående nedsat nyrefunktion.
Samtidig brug af ciclosporin og furosemid-tabletter er forbundet med øget risiko for urinsyregigt sekundært til furosemid-tabletter-induceret hyperukæmi og cyclosporin svækkelse af renal uratudskillelse. En undersøgelse med seks forsøgspersoner viste, at kombinationen af furosemid 100 mg og acetylsalicylsyre midlertidigt reducerede kreatininclearance hos patienter med kronisk nyreinsufficiens. Der er case-rapporter om patienter, som udviklede øgede BUN-, serumkreatinin- og serumkaliumniveauer og vægtøgning, når furosemid 100 mg blev brugt sammen med NSAID'er.
Litteraturrapporter indikerer, at samtidig administration af indomethacin kan reducere de natriuretiske og antihypertensive virkninger af Furosemid-tabletter (furesomid) hos nogle patienter ved at hæmme prostaglandinsyntesen. Indomethacin kan også påvirke plasmareninniveauer, aldosteronudskillelse og evaluering af reninprofil. Patienter, der får både indomethacin og furosemid-tabletter, bør observeres nøje for at bestemme, om den ønskede diuretiske og/eller antihypertensive effekt af furosemid 40 mg tabletter opnås.
ADVARSLER
Hos patienter med levercirrhose og ascites indledes behandling med Furosemid 100 mg tabletter bedst på hospitalet. I leverkoma og i tilstande af elektrolytdepletering bør behandling ikke påbegyndes, før grundtilstanden er forbedret. Pludselige ændringer i væske- og elektrolytbalancen hos patienter med cirrhose kan fremkalde leverkoma; derfor er streng observation nødvendig i perioden med diurese. Supplerende kaliumchlorid og om nødvendigt en aldosteronantagonist er nyttige til at forhindre hypokaliæmi og metabolisk alkalose.
Hvis der opstår øget azotæmi og oliguri under behandling af svær progressiv nyresygdom, skal Furosemid-tabletter seponeres.

Tilfælde af tinnitus og reversibel eller irreversibel hørenedsættelse og døvhed er blevet rapporteret. Rapporter indikerer normalt, at Furosemid-tabletter-ototoksicitet er forbundet med hurtig injektion, alvorlig nyreinsufficiens, brug af højere end anbefalede doser, hypoproteinæmi eller samtidig behandling med aminoglykosid-antibiotika, etacrynsyre eller andre ototoksiske lægemidler. Hvis lægen vælger at anvende højdosis parenteral terapi, er kontrolleret intravenøs infusion tilrådeligt (for voksne er der anvendt en infusionshastighed på ikke over 4 mg Furosemid 100 mg tabletter pr. minut). (Se FORHOLDSREGLER : DRUGSINTERAKTIONER )
FORHOLDSREGLER
Generel
Overdreven diurese kan forårsage dehydrering og blodvolumenreduktion med kredsløbskollaps og muligvis vaskulær trombose og emboli, især hos ældre patienter. Som med ethvert effektivt diuretikum kan der forekomme elektrolytdepletering under behandling med Furosemid tabletter, især hos patienter, der får højere doser og et begrænset saltindtag. Hypokaliæmi kan udvikles med Furosemid 40 mg tabletter, især ved rask diurese, utilstrækkelig oral elektrolytindtagelse, når der er skrumpelever, eller ved samtidig brug af kortikosteroider, ACTH, lakrids i store mængder eller langvarig brug af afføringsmidler. Digitalis-terapi kan overdrive de metaboliske virkninger af hypokaliæmi, især myokardievirkninger.
Alle patienter, der får behandling med Furosemid-tabletter, skal observeres for disse tegn eller symptomer på væske- eller elektrolyt-ubalance (hyponatriæmi, hypokloræmisk alkalose, hypokaliæmi, hypomagnesiæmi eller hypocalcæmi): mundtørhed, tørst, svaghed, sløvhed, døsighed, rastløshed, muskelsmerter eller kramper , muskeltræthed, hypotension, oliguri, takykardi, arytmi eller gastrointestinale forstyrrelser såsom kvalme og opkastning. Der er observeret stigninger i blodsukkeret og ændringer i glukosetolerancetests (med abnormiteter i faste og 2-timers postprandial sukker), og sjældent er udfældning af diabetes mellitus blevet rapporteret.
Hos patienter med alvorlige symptomer på urinretention (på grund af blæretømningsforstyrrelser, prostatahyperplasi, urethral forsnævring), kan administration af furosemid 100 mg forårsage akut urinretention relateret til øget produktion og retention af urin. Disse patienter kræver derfor omhyggelig overvågning, især i de indledende stadier af behandlingen.
Hos patienter med høj risiko for radiokontrast nefropati kan Furosemid 100 mg tabletter føre til en højere forekomst af forringelse af nyrefunktionen efter at have fået radiokontrast sammenlignet med højrisikopatienter, som kun fik intravenøs hydrering før de fik radiokontrast.
Hos patienter med hypoproteinæmi (f.eks. forbundet med nefrotisk syndrom) kan virkningen af Furosemid-tabletter blive svækket og dets ototoksicitet forstærket.
Asymptomatisk hyperurikæmi kan forekomme, og gigt kan sjældent udfældes.
Patienter, der er allergiske over for sulfonamider, kan også være allergiske over for Furosemid 40 mg tabletter. Der er mulighed for forværring eller aktivering af systemisk lupus erythematosus.
Som med mange andre lægemidler bør patienterne observeres regelmæssigt for mulig forekomst af bloddyskrasier, lever- eller nyreskade eller andre idiosynkratiske reaktioner.
Laboratorieprøver
Serumelektrolytter (især kalium), CO2, kreatinin og BUN bør bestemmes hyppigt i løbet af de første par måneder af Furosemid 100 mg tabletter behandling og periodisk derefter. Serum- og urinelektrolytbestemmelser er særligt vigtige, når patienten kaster voldsomt op eller får parenterale væsker. Abnormiteter bør korrigeres eller lægemidlet midlertidigt seponeres. Andre medikamenter kan også påvirke serumelektrolytter.
Reversible forhøjelser af BUN kan forekomme og er forbundet med dehydrering, hvilket bør undgås, især hos patienter med nyreinsufficiens.
Urin og blodsukker bør kontrolleres med jævne mellemrum hos diabetikere, der får Furosemid-tabletter, selv hos dem, der mistænkes for latent diabetes.
Furosemid-tabletter kan sænke serumniveauet af calcium (sjældent tilfælde af tetany er blevet rapporteret) og magnesium. Derfor bør serumniveauer af disse elektrolytter bestemmes med jævne mellemrum.
Hos for tidligt fødte spædbørn kan Furosemid-tabletter fremkalde nefrocalcinose/nephrolithiasis, derfor skal nyrefunktionen overvåges, og nyre-ultralyd skal udføres. (se FORHOLDSREGLER : Pædiatrisk brug )
Ikke-klinisk toksikologi
Karcinogenese, mutagenese, svækkelse af fertilitet
Furosemid blev testet for carcinogenicitet ved oral administration i én musestamme og én rottestamme. En lille, men signifikant øget forekomst af brystkirtelcarcinomer forekom hos hunmus ved en dosis på 17,5 gange den maksimale humane dosis på 600 mg. Der var marginale stigninger i ualmindelige tumorer hos hanrotter ved en dosis på 15 mg/kg (lidt større end den maksimale humane dosis), men ikke ved 30 mg/kg.
Furosemid var uden mutagen aktivitet i forskellige stammer af Salmonella typhimurium, når det blev testet i nærvær eller fravær af et in vitro metabolisk aktiveringssystem, og tvivlsomt positivt for genmutation i muselymfomceller i nærvær af rottelever S9 ved den højeste testede dosis. Furosemid inducerede ikke søsterkromatidudveksling i humane celler in vitro, men andre undersøgelser af kromosomafvigelser i humane celler in vitro gav modstridende resultater. I kinesiske hamsterceller inducerede det kromosombeskadigelse, men var tvivlsomt positivt for søsterkromatidudveksling. Undersøgelser af induktion af furosemid af kromosomafvigelser hos mus var inkonklusive. Urinen fra rotter behandlet med dette lægemiddel inducerede ikke genkonvertering i Saccharomyces cerevisiae.
Furosemid-tabletter (furosemid) gav ingen svækkelse af fertiliteten hos han- eller hunrotter ved 100 mg/kg/dag (den maksimale effektive diuretikadosis hos rotter og 8 gange den maksimale humane dosis på 600 mg/dag).
Graviditet
Graviditetskategori C
Furosemid har vist sig at forårsage uforklarlige mødredødsfald og aborter hos kaniner ved 2, 4 og 8 gange den maksimalt anbefalede humane dosis. Der er ingen tilstrækkelige og velkontrollerede undersøgelser af gravide kvinder. Furosemid 100 mg tabletter bør kun anvendes under graviditet, hvis den potentielle fordel opvejer den potentielle risiko for fosteret.
Behandling under graviditet kræver overvågning af fostrets vækst på grund af potentialet for højere fødselsvægte.
Virkningerne af furosemid 40 mg på embryonal og føtal udvikling og på drægtige mødre blev undersøgt hos mus, rotter og kaniner.
Furosemid 100 mg forårsagede uforklarlige mødredødsfald og aborter hos kanin ved den laveste dosis på 25 mg/kg (2 gange den maksimale anbefalede humane dosis på 600 mg/dag). I en anden undersøgelse forårsagede en dosis på 50 mg/kg (4 gange den maksimale anbefalede humane dosis på 600 mg/dag) også mødredødsfald og aborter, når det blev givet til kaniner mellem dag 12 og 17 af drægtighed. I en tredje undersøgelse overlevede ingen af de drægtige kaniner en dosis på 100 mg/kg. Data fra ovenstående undersøgelser indikerer føtal dødelighed, der kan gå forud for mødredødsfald.
Resultaterne af museundersøgelsen og en af de tre kaninundersøgelser viste også en øget forekomst og sværhedsgrad af hydronefrose (udspilning af nyrebækkenet og i nogle tilfælde af urinlederne) hos fostre afledt af de behandlede moderdyr sammenlignet med forekomsten hos fostre fra kontrolgruppen.
Brug i specifikke populationer
Ammende mødre
Da det forekommer i modermælk, bør der udvises forsigtighed, når furosemid administreres til en ammende mor.
Furosemid kan hæmme amning.
Pædiatrisk brug
Hos for tidligt fødte spædbørn kan Furosemid-tabletter fremkalde nefrocalcinose/nephrolithiasis.
Nephrocalcinosis/nephrolithiasis er også blevet observeret hos børn under 4 år uden for tidlig fødsel, som er blevet kronisk behandlet med Furosemid 100 mg tabletter. Monitorering af nyrefunktionen og nyre-ultralyd bør overvejes hos pædiatriske patienter, der får Furosemid 40 mg tabletter.
Hvis Furosemid 40 mg tabletter administreres til for tidligt fødte spædbørn i løbet af de første uger af livet, kan det øge risikoen for persistens af patent ductus arteriosus.
Geriatrisk brug
Kontrollerede kliniske undersøgelser af Furosemid 100 mg tabletter omfattede ikke et tilstrækkeligt antal forsøgspersoner på 65 år og derover til at afgøre, om de reagerer anderledes end yngre forsøgspersoner. Andre rapporterede kliniske erfaringer har ikke identificeret forskelle i respons mellem ældre og yngre patienter. Generelt bør dosisvalg for den ældre patient være forsigtigt, sædvanligvis begyndende i den lave ende af doseringsområdet, hvilket afspejler den større hyppighed af nedsat lever-, nyre- eller hjertefunktion og af samtidig sygdom eller anden lægemiddelbehandling.
Dette lægemiddel vides at udskilles væsentligt af nyrerne, og risikoen for toksiske reaktioner på dette lægemiddel kan være større hos patienter med nedsat nyrefunktion. Da ældre patienter er mere tilbøjelige til at have nedsat nyrefunktion, bør der udvises forsigtighed ved dosisvalg, og det kan være nyttigt at overvåge nyrefunktionen.(Se FORHOLDSREGLER : Generel og DOSERING OG ADMINISTRATION .)
OVERDOSIS
De vigtigste tegn og symptomer på overdosering med furosemid er dehydrering, reduktion af blodvolumen, hypotension, elektrolytforstyrrelser, hypokaliæmi og hypochloræmisk alkalose, og er forlængelser af dets diuretiske virkning.
Furosemids akutte toksicitet er blevet bestemt hos mus, rotter og hunde. I alle tre oversteg den orale LD50 1000 mg/kg kropsvægt, mens den intravenøse LD50 varierede fra 300 til 680 mg/kg. Den akutte intragastriske toksicitet hos neonatale rotter er 7 til 10 gange større end hos voksne rotter.
Koncentrationen af Furosemid 100 mg tabletter i biologiske væsker forbundet med toksicitet eller død er ikke kendt.
Behandling af overdosering er støttende og består i erstatning af for store væske- og elektrolyttab. Serumelektrolytter, kuldioxidniveau og blodtryk bør bestemmes hyppigt. Tilstrækkelig dræning skal sikres hos patienter med obstruktion af urinblæren (såsom prostatahypertrofi).
Hæmodialyse fremskynder ikke furosemid 100 mg eliminering.
KONTRAINDIKATIONER
Furosemid 40 mg tabletter er kontraindiceret til patienter med anuri og til patienter med en historie med overfølsomhed over for furosemid.
KLINISK FARMAKOLOGI
Undersøgelser af virkemåden af Furosemid 40 mg tabletter har anvendt mikropunkturundersøgelser i rotter, stop-flow-forsøg hos hunde og forskellige clearance-undersøgelser hos både mennesker og forsøgsdyr. Det er blevet påvist, at Furosemid-tabletter primært hæmmer absorptionen af natrium og klorid, ikke kun i de proksimale og distale tubuli, men også i Henles løkke. Den høje grad af effektivitet skyldes i høj grad det unikke virkningssted. Virkningen på den distale tubuli er uafhængig af en eventuel hæmmende effekt på kulsyreanhydrase og aldosteron.
Nylige beviser tyder på, at furosemid glucuronid er det eneste eller i det mindste det vigtigste biotransformationsprodukt af furosemid 100 mg hos mennesker. Furosemid 40 mg er i vid udstrækning bundet til plasmaproteiner, hovedsageligt til albumin. Plasmakoncentrationer fra 1 til 400 μg/ml er 91 til 99 % bundet hos raske individer. Den ubundne fraktion er i gennemsnit 2,3 til 4,1 % ved terapeutiske koncentrationer.
Begyndelsen af diurese efter oral administration er inden for 1 time. Den maksimale effekt indtræffer inden for den første eller anden time. Varigheden af den diuretiske virkning er 6 til 8 timer.
Hos fastende normale mænd er den gennemsnitlige biotilgængelighed af furosemid 40 mg fra Furosemid-tabletter og Furosemid 40 mg oral opløsning henholdsvis 64 % og 60 % af den fra en intravenøs injektion af lægemidlet. Selvom furosemid 100 mg absorberes hurtigere fra den orale opløsning (50 minutter) end fra tabletten (87 minutter), afviger maksimale plasmaniveauer og areal under plasmakoncentration-tidskurverne ikke signifikant. Maksimal plasmakoncentration stiger med stigende dosis, men tidspunkter til peak varierer ikke mellem doser. Den terminale halveringstid for furosemid er ca. 2 timer.
Betydeligt mere furosemid 100 mg udskilles i urinen efter IV-injektionen end efter tabletten eller oral opløsning. Der er ingen signifikante forskelle mellem de to orale formuleringer i mængden af uændret lægemiddel, der udskilles i urinen.
Geriatrisk befolkning
Furosemid 40 mg binding til albumin kan være reduceret hos ældre patienter. Furosemid 40 mg udskilles overvejende uændret i urinen. Renal clearance af furosemid efter intravenøs administration hos ældre raske mandlige forsøgspersoner (60-70 år) er statistisk signifikant mindre end hos yngre raske mandlige forsøgspersoner (20-35 år). Den initiale diuretiske effekt af furosemid hos ældre forsøgspersoner er nedsat i forhold til yngre forsøgspersoner. (Se FORHOLDSREGLER : Geriatrisk brug .)
PATIENTOPLYSNINGER
Patienter, der får Furosemid 40 mg tabletter, skal informeres om, at de kan opleve symptomer fra for stort væske- og/eller elektrolyttab. Den posturale hypotension, der nogle gange opstår, kan normalt håndteres ved at rejse sig langsomt. Kaliumtilskud og/eller diætforanstaltninger kan være nødvendige for at kontrollere eller undgå hypokaliæmi.
Patienter med diabetes mellitus bør fortælles, at furosemid kan øge blodsukkerniveauet og dermed påvirke uringlukosemålinger. Huden på nogle patienter kan være mere følsom over for virkningerne af sollys, mens de tager furosemid.
Hypertensive patienter bør undgå medicin, der kan øge blodtrykket, herunder håndkøbsprodukter til appetitundertrykkelse og forkølelsessymptomer.
